2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Метод определения Real-time-PCR.
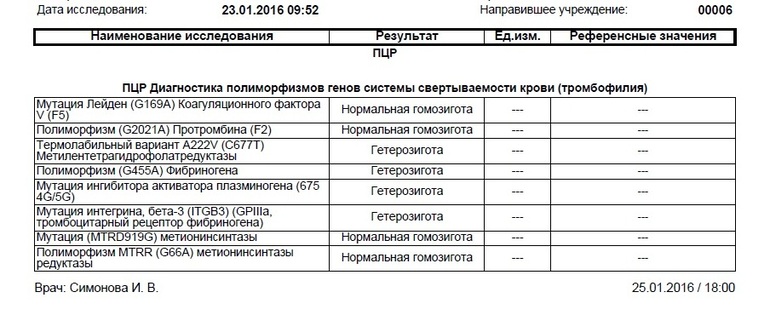
Исследуемый материал Цельная кровь (с ЭДТА)
Доступен выезд на дом
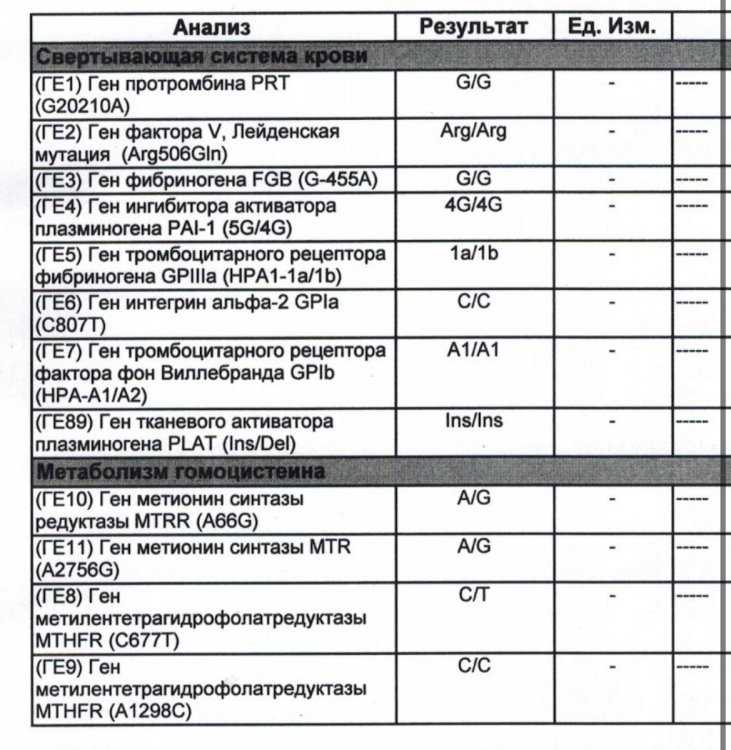
Расширенное исследование генов системы гемостаза: F2, F5, MTHFR, MTR, MTRR, F13, FGB, ITGA2, ITGВ3, F7, PAI-1
Комплексное исследование генетических факторов риска развития нарушений в системе свертывания крови и фолатном цикле (без заключения врача-генетика).
Различные изменения в генах системы гемостаза и цикла обмена фолатов предрасполагают к развитию большого числа патологических состояний: инфаркты, инсульты, тромбоэмболии, кровотечения, патология беременности и родов, осложнения послеоперационного периода и т.д. Профиль включает в себя исследование основных полиморфизмов в генах системы гемостаза и фолатного цикла:
Ген F2 кодирует аминокислотную последовательность белка протромбина. Полиморфизм F2 c.*97G>A приводит к повышенной экспрессии гена. Клинически неблагоприятный вариант полиморфизма (c.*97A) наследуется по аутосомно-доминантному типу. Наличие полиморфизма F2 c.*97G>A в гомозиготной или гетерозиготной форме значительно (в 3 и более раз, а на фоне курения - в 40 и более раз) увеличивает риск возникновения венозных тромбозов, в том числе тромбозов сосудов мозга и сердца, особенно в молодом возрасте. У пациентов-носителей данного полиморфизма повышен риск развития тромбоэмболий после хирургических вмешательств. Приём оральных контрацептивов у данной группы лиц также увеличивает риск тромбозов (относительный риск развития тромбофилии и венозной тромбоэмболии у гетерозиготных носительниц полиморфизма c.*97G>A возрастает в 16 раз).
У пациентов-носителей данного полиморфизма повышен риск развития тромбоэмболий после хирургических вмешательств. Приём оральных контрацептивов у данной группы лиц также увеличивает риск тромбозов (относительный риск развития тромбофилии и венозной тромбоэмболии у гетерозиготных носительниц полиморфизма c.*97G>A возрастает в 16 раз).
Ген F5 кодирует аминокислотную последовательность белка проакцелерина - коагуляционного фактора 5. Нуклеотидная замена c.1601G>A («мутация Лейден») приводит к аминокислотной замене аргинина на глутамин в позиции 534, что придает устойчивость активной форме проакцелерина. Клинически это проявляется рецидивирующими венозными тромбозами и тромбоэмболиями. Наличие полиморфизма в гомозиготной или гетерозиготной форме значительно (в 3 и более раз, а на фоне заместительной гормонотерапии или приема оральных контрацептивов - в 30 и более раз) увеличивает риск венозных тромбозов. Риск инфаркта миокарда увеличивается в 2 и более раз, риск развития патологии беременности (прерывание беременности, преэклампсия, хроническая плацентарная недостаточность и синдром задержки роста плода) увеличивается в 3 и более раз.
Также, пациенты, являющиеся одновременно носителями полиморфизма c.*97G>A гена протромбина и «мутации Лейден», еще в большей степени подвержены риску развития тромбозов и тромбоэмболий.
Ген MTHFR кодирует аминокислотную последовательность фермента метилентетрагидрофолатредуктазы, играющего ключевую роль в метаболизме фолиевой кислоты. Полиморфизм c.665C>T гена MTHFR связан с заменой нуклеотида цитозина (С) на тимин (Т), что приводит к аминокислотной замене аланина на валин в позиции 222. Вариант c.665Т связан с четырьмя группами мультифакториальных заболеваний: сердечно-сосудистыми, дефектами развития плода, колоректальной аденомой и раком молочной железы и яичников. У женщин с генотипом c.665Т/Т дефицит фолиевой кислоты во время беременности может приводить к порокам развития плода, в том числе незаращению нервной трубки. Неблагоприятное воздействие варианта c.665Т- зависит от внешних факторов: низкого содержания в пище фолатов, курения, приема алкоголя.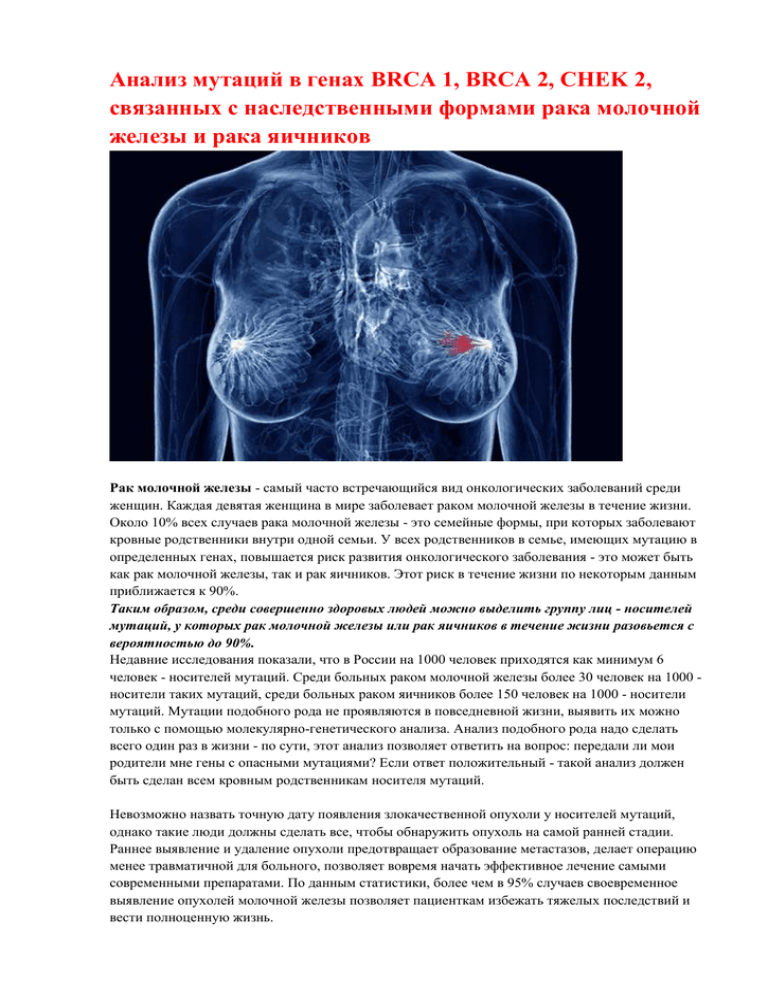 Сочетание генотипа c.665Т/Т и папилломавирусной инфекции увеличивает риск цервикальной дисплазии. Назначение препаратов фолиевой кислоты может значительно снизить негативное влияние данного варианта полиморфизма.
Сочетание генотипа c.665Т/Т и папилломавирусной инфекции увеличивает риск цервикальной дисплазии. Назначение препаратов фолиевой кислоты может значительно снизить негативное влияние данного варианта полиморфизма.
Полиморфизм MTHFR c.1286A>C связан с точечной заменой нуклеотида аденина (А) на цитозин (С), что приводит к замене аминокислотного остатка глутаминовой кислоты на аланин в позиции 429, относящейся к регулирующей области молекулы фермента. При наличии данного полиморфизма отмечается снижение активности фермента MTHFR. Это снижение обычно не сопровождается изменением уровня гомоцистеина в плазме крови у носителей дикого варианта полиморфизма c.665C>T, однако сочетание аллельного варианта* c.1286C с аллелем c.665T приводит к снижению уровня фолиевой кислоты и соответствует по своему эффекту гомозиготному состоянию MTHFR c.665Т/T. При этом риск развития дефектов нервной трубки повышается в 2 раза. Жизнеспособность плодов, имеющих одновременно оба полиморфных варианта, также снижена.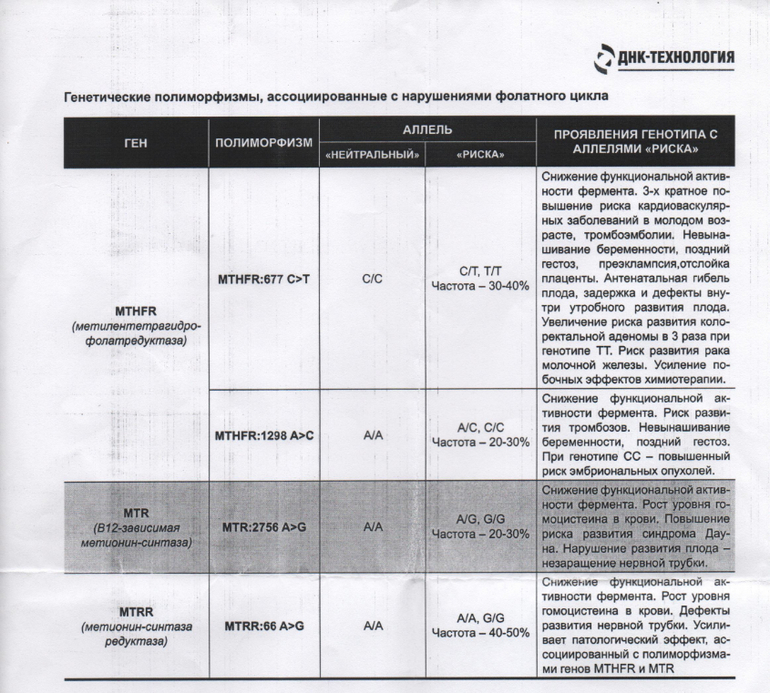
Ген MTR кодирует аминокислотную последовательность фермента метионин синтазы. Полиморфизм c.2756A>G связан с аминокислотной заменой (аспарагиновой кислоты на глицин) в молекуле фермента. В результате этой замены функциональная активность фермента изменяется, что приводит к повышению риска формирования пороков развития у плода. Влияние полиморфизма усугубляется повышенным уровнем гомоцистеина.
Ген MTRR кодирует аминокислотную последовательность фермента редуктазы метионинсинтазы. Полиморфизм c.66A>G связан с аминокислотной заменой в молекуле фермента. В результате этой замены функциональная активность фермента снижается, что приводит к повышению риска развития дефектов нервной трубки у плода. Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма c.66A>G гена MTRR с полиморфизмом c.665C>T в гене MTHFR риск spina bifida увеличивается. Полиморфизм c. 66A>G гена MTRR усиливает гипергомоцистеинемию, вызываемую полиморфизмом c.665C>T в гене MTHFR.
66A>G гена MTRR усиливает гипергомоцистеинемию, вызываемую полиморфизмом c.665C>T в гене MTHFR.
Ген фибриназы (F13) кодирует синтез трансглютаминазы, участвующей в стабилизации фибринового сгустка и в формировании соединительной ткани. Аллельные варианты с.103G/Т и с.103Т/Т приводят к снижению уровня трансглютаминазы с образованием сетчатой структуры фибрина с более тонкими волокнами, меньшими порами, и изменением характеристик проникновения, которое в сочетании с другими факторами риска ассоциируется с возможным риском внутричерепных кровоизлияний и кровотечений из внутренних органов, а также привычным невынашиванием беременности. При этом аллельный вариант с.103Т может выступать в роли протективного фактора в отношении инфаркта миокарда и венозных тромбозов.
Ген FGB кодирует β-цепь фибриногена, являющегося предшественником фибрина. Аллельный вариант c.-467А обусловливает усиленную транскрипцию гена и может приводить к увеличению уровня фибриногена в крови и повышению вероятности образования тромбов при наличии дополнительных факторов риска.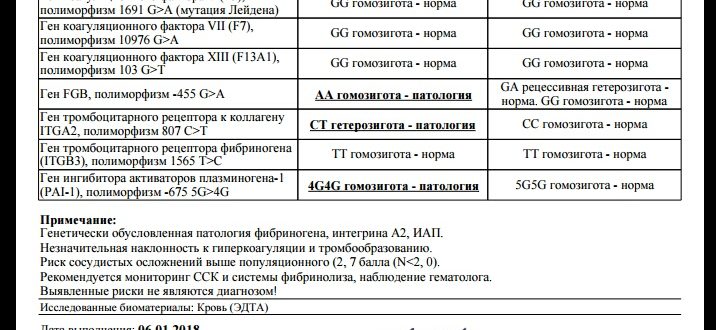 Гетерозиготный вариант c.-467G/А связывают с повышенным риском ишемического инсульта и лакунарными инфарктами церебральных сосудов. Гомозиготный вариант c.-467A/А связывают с повышенным риском инфаркта миокарда.
Гетерозиготный вариант c.-467G/А связывают с повышенным риском ишемического инсульта и лакунарными инфарктами церебральных сосудов. Гомозиготный вариант c.-467A/А связывают с повышенным риском инфаркта миокарда.
Ген гликопротеина Gp1a (ITGA2) кодирует синтез альфа-2-субъединицы интегринов – специализированных рецепторов тромбоцитов. Аллельный вариант c.759Т вызывает изменение первичной структуры субъединицы и свойств рецепторов. При гетерозиготном (c.759C/T) варианте отмечается увеличение скорости адгезии тромбоцитов к коллагену I типа, что может приводить к повышенному риску тромбофилии, инфаркта миокарда и других сердечно-сосудистых заболеваний. Аллельный вариант c.759Т связывают со случаями резистентности к аспирину. Помимо этого, при гомозиготном (c.759Т/T) варианте значительно увеличивается количество рецепторов на поверхности тромбоцитов. В совокупности, при гомозиготном варианте данного полиморфизма значительно повышен риск тромбофилии, инфаркта миокарда и развития других острых эпизодов тромбообразования в возрасте до 50 лет, даже по сравнению с гетерозиготным вариантом.
Ген гликопротеина Gp3a (ITGB3) кодирует синтез бета-3 цепи интегринового комплекса GP2b\3a, участвующего в разнообразных межклеточных взаимодействиях (адгезии и сигнализации). Аллельный вариант c.176С (гетерозигота c.176T/C) обусловливает повышенную адгезию тромбоцитов и может приводить к увеличению риска развития острого коронарного синдрома, а также связан с синдромом привычного невынашивания беременности. Гомозиготный вариант c.176С/C обусловливает повышенную адгезию тромбоцитов и может приводить к значительному увеличению риска развития острого коронарного синдрома в возрасте до 50 лет. У лиц с полиморфными аллельными вариантами часто отмечается пониженная эффективность аспирина.
Аллельный вариант c.1238A (гетерозигота c.1238G/A и гомозигота c.1238А/A) гена F7 приводит к понижению экспрессии гена и снижению уровня фактора 7 в крови, рассматривается как протективный маркёр в отношении развития тромбозов и инфаркта миокарда.
Ген ингибитора активатора плазминогена (PAI-1) кодирует белок-антагонист тканевого и урокиназного активатора плазминогена. Преобладающим в популяции вариантом исследуемого полиморфизма является гетерозиготный вариант -675 5G/4G. В связи с этим данный полиморфизм самостоятельного диагностического значения не имеет, эффект возможно оценить в сочетании с другими факторами предрасполагающими к развитию патологии (например в сочетании с FGB c.-467A). Аллельный вариант -675 4G сопровождается большей активностью гена, чем -675 5G, что обусловливает более высокую концентрацию PAI-1 и уменьшение активности противосвёртывающей системы. Гомозигота -675 4G/4G ассоциирована с повышением риска тромбообразования, преэклампсии, нарушением функции плаценты и самопроизвольного прерывания беременности.
*Примечание: иногда в научной литературе при описании однонуклеотидных замен, характерных для генных полиморфизмов, встречается термин "мутантный аллель". Это терминологическая неточность, так как в классической генетике термин "мутантный аллель" традиционно рассматривается как синоним термина "мутация". При мутациях, как известно, изменение структуры гена приводит к образованию (экспрессии) нефункциональных белков и к неизбежному развитию наследственного заболевания. При полиморфизмах изменение в структуре гена приводит лишь к появлению белков с немного изменёнными физико-химическими свойствами. Такие изменения, как известно, проявляют себя при воздействии на организм различных факторов внешней среды или при изменении функционального состояния организма человека. И только в таких ситуациях функционирование белков со структурными особенностями может, либо способствовать ускорению развития заболевания, либо, напротив, тормозить формирование патологических процессов. Поэтому, на наш взгляд, для разграничения изменений в генах столь очень похожих структурно, но приводящих к несоизмеримо разным последствиям для организма, корректнее в отношении генных полиморфизмов применять понятие "аллельный вариант гена", а не "мутантный аллель".
Это терминологическая неточность, так как в классической генетике термин "мутантный аллель" традиционно рассматривается как синоним термина "мутация". При мутациях, как известно, изменение структуры гена приводит к образованию (экспрессии) нефункциональных белков и к неизбежному развитию наследственного заболевания. При полиморфизмах изменение в структуре гена приводит лишь к появлению белков с немного изменёнными физико-химическими свойствами. Такие изменения, как известно, проявляют себя при воздействии на организм различных факторов внешней среды или при изменении функционального состояния организма человека. И только в таких ситуациях функционирование белков со структурными особенностями может, либо способствовать ускорению развития заболевания, либо, напротив, тормозить формирование патологических процессов. Поэтому, на наш взгляд, для разграничения изменений в генах столь очень похожих структурно, но приводящих к несоизмеримо разным последствиям для организма, корректнее в отношении генных полиморфизмов применять понятие "аллельный вариант гена", а не "мутантный аллель".
Несмотря на множество теорий развития злокачественных опухолей специалисты и сегодня нередко затрудняются ответить на вопрос, почему развивается рак того или иного органа. Однако уже не вызывает сомнений тот факт, что некоторые его разновидности могут быть связаны с наследственной предрасположенностью, выявить которую позволяет специальное генетическое исследование. Анализ BRCA1 и BRCA2. В каких случаях и для чего его проводят? Об этом и многом другом мы беседуем с врачом-акушером-гинекологом «Клиника Эксперт» Курск Татьяной Ивановной Еремеевой.
Несмотря на множество теорий развития злокачественных опухолей специалисты и сегодня нередко затрудняются ответить на вопрос, почему развивается рак того или иного органа. Однако уже не вызывает сомнений тот факт, что некоторые его разновидности могут быть связаны с наследственной предрасположенностью, выявить которую позволяет специальное генетическое исследование.
Анализ BRCA1 и BRCA2. В каких случаях и для чего его проводят? Об этом и многом другом мы беседуем с врачом-акушером-гинекологом «Клиника Эксперт» Курск Татьяной Ивановной Еремеевой.
— Татьяна Ивановна, среди названий исследований, проводимых при подозрении на онкологическое заболевание, упоминаются такие аббревиатуры, как BRCA1 и BRCA2. Что они означают?
— Так называются гены, которые выступают в роли опухолевых супрессоров. Это значит, что они являются своеобразными «контролёрами», препятствующими неконтролируемому и нарушенному процессу деления клетки. Если в этих генах появляются мутации, то гены утрачивают способность отслеживать изменения в геноме клетки, а это, в свою очередь, может привести к атипичным трансформациям в клетках и развитию злокачественных опухолей.
— То есть получается, что можно унаследовать эти гены с такими мутациями и, соответственно, иметь повышенный риск развития опухоли?
— Да, это возможно. Если дети получают повреждённые гены BRCA1 и BRCA2 от родителей, то у них возрастает риск возникновения рака молочной железы, рака яичников и ряда других разновидностей злокачественных новообразований. Однако следует помнить, что ребёнок получает половину генома от матери, а вторую часть от отца, поэтому вероятность передачи генов с дефектами равна 50 % и она не зависит от пола ребёнка (то есть мутировавший ген может получить как девочка, так и мальчик).
Однако следует помнить, что ребёнок получает половину генома от матери, а вторую часть от отца, поэтому вероятность передачи генов с дефектами равна 50 % и она не зависит от пола ребёнка (то есть мутировавший ген может получить как девочка, так и мальчик).
— Может ли мутация встречаться лишь в одном из этих генов?
— Да, может. На сегодняшний день изучено более двух тысяч разновидностей мутаций в генах BRCA1 и BRCA2. На практике можно встретить как сочетанные дефекты обоих генов, так и изолированные повреждения одного из них. Среди населения нашей страны превалируют мутации в гене BRCA1 – они составляют около 80 % от общего количества повреждений в обоих генах. Причём здесь гораздо чаще встречаются повторяющиеся мутации, тогда как большинство дефектов гена BRCA2 уникальны.
— Кому и в каких случаях необходимо сдать анализ на мутации BRCA1 и BRCA2? Судя по тому, что вы сказали ранее, это не всегда только женщины?
— Да, верно. Такую диагностику проводят и мужчинам. Связано это с тем, что повреждение генов BRCA1 и BRCA2 указывает на высокую вероятность развития не только рака молочных желез или яичников, но и злокачественных новообразований других органов, в частности, рака поджелудочной железы, желудка, кишечника и других.
Связано это с тем, что повреждение генов BRCA1 и BRCA2 указывает на высокую вероятность развития не только рака молочных желез или яичников, но и злокачественных новообразований других органов, в частности, рака поджелудочной железы, желудка, кишечника и других.
К примеру, если у мужчины обнаружена мутация гена BRCA1, это может говорить о высоком риске развития рака простаты. Согласно зарубежным исследованиям любые BRCA-мутации повышают вероятность развития нескольких разновидностей опухолей у мужчин в 8 раз. Поэтому такой вид диагностики для них также актуален.
Необходимость в определении мутации генов BRCA1 и BRCA2 возникает тогда, когда пациент (независимо от того, мужчина это или женщина) принадлежит к группе риска. Вероятность наследственной предрасположенности высока, если:
— Татьяна Ивановна, расскажите, пожалуйста, о процедуре проведения исследования на мутации в генах BRCA1 и BRCA2
— Начну с того, что прежде, чем сдать анализ на выявление повреждений в BRCA1 и BRCA2, проводится консультация с врачом-генетиком. Доктор информирует пациента о содержании проводимого исследования, а также о значении положительного и отрицательного результатов. Это делают с целью психологической подготовки пациента к возможному результату.
В качестве материала для генетического анализа служит кровь. Специальной подготовки перед сдачей анализа не предусмотрено. В нашей стране это исследование проводят методом ПЦР (полимеразной цепной реакции).
Подробнее о методе ПЦР читайте в нашей статье: Диагностика инфекций методом ПЦР: что это такое?
— Предположим, что анализ выявил мутацию. Что человеку делать дальше?
— Следует вновь обратиться к врачу-генетику. Если обнаружены мутации в BRCA1 и/или BRCA2, специалист даст пациенту необходимые рекомендации по дальнейшей профилактике онкологических заболеваний.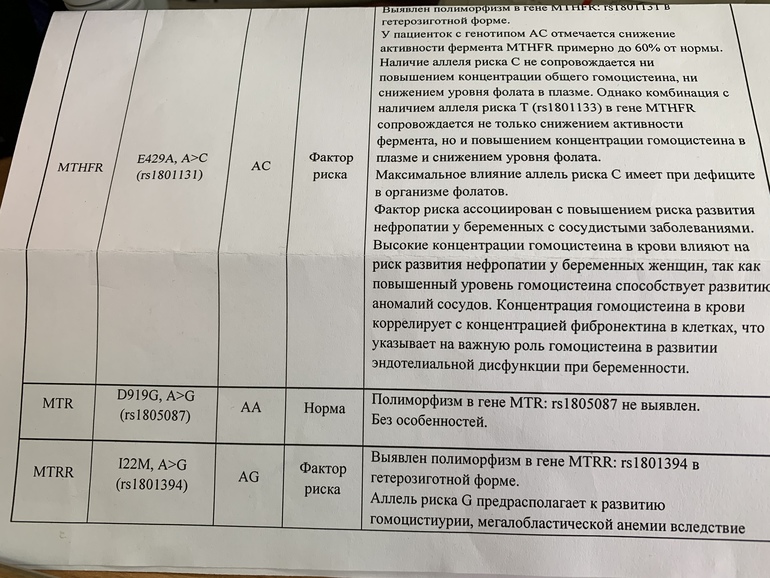
Важно помнить, что выявление подобных генетических дефектов – это не диагноз. Наличие повреждений в этих генах указывает только на возможность развития онкологической патологии в молочных железах или других органах. Хочу также заметить, что положительный анализ не позволяет утверждать, что мутация генов непременно обнаружится у всех близких родственников (мамы, дочери, тёти).
С другой стороны, отрицательный результат не означает, что у пациента никогда не разовьётся опухолевый процесс. В таком случае нет лишь повышенного риска развития злокачественного новообразования вышеуказанных органов.
Подчеркну, что независимо от результатов диагностики на наличие повреждений в генах BRCA1 и BRCA2 не отменяются, в частности, регулярные скрининговые меры профилактики рака молочной железы у женщин – это консультация врача-маммолога и проведение маммографии.
Беседовала Севиля Ибраимова
Редакция рекомендует:
Предрак: бояться или не обращать внимания?
Доктор Карасёв: «Ни одна раковая клетка не пройдёт мимо меня!»
Рак груди – не приговор!
Опасна ли мастопатия? Не паникуем, но лечимся!
Фиброаденома молочной железы: чем может помочь доктор?
Для справки:
Еремеева Татьяна Ивановна
Выпускница лечебного факультета Курского государственного медицинского университета 2007 года
В 2008 году - интернатура по специальности «Акушерство и гинекология».
В 2014 году проходила профессиональную переподготовку по ультразвуковой диагностике
В настоящее время врач – акушер-гинеколог в «Клиника Эксперт» Курск. Принимает по адресу: ул. Карла Либкнехта, д.7
Генетическое тестирование включает в себя исследование вашей ДНК, химической базы данных, содержащей инструкции для функций вашего тела. Генетическое тестирование может выявить изменения (мутации) в ваших генах, которые могут вызвать заболевание или болезнь.
Хотя генетическое тестирование может предоставить важную информацию для диагностики, лечения и профилактики заболеваний, существуют ограничения. Например, если вы здоровый человек, положительный результат генетического тестирования не всегда означает, что у вас разовьется заболевание. С другой стороны, в некоторых ситуациях отрицательный результат не гарантирует отсутствия определенного расстройства.
Обсуждение со своим врачом, медицинским генетиком или консультантом по генетическим вопросам того, что вы будете делать с результатами, является важным шагом в процессе генетического тестирования.
Когда генетическое тестирование не приводит к постановке диагноза, но все же подозревается генетическая причина, некоторые учреждения предлагают секвенирование генома — процесс анализа образца ДНК, взятого из вашей крови.
Каждый человек имеет уникальный геном, состоящий из ДНК всех генов человека. Это комплексное тестирование может помочь выявить генетические варианты, которые могут иметь отношение к вашему здоровью. Это тестирование обычно ограничивается простым изучением кодирующих белок частей ДНК, называемых экзомом.
3 90 играет жизненно важную роль в определении риска развития определенных заболеваний, а также в скрининге, а иногда и в лечении. Различные виды генетического тестирования проводятся по разным причинам:
Различные виды генетического тестирования проводятся по разным причинам:
 Расширенный скрининговый тест на носительство может обнаружить гены, связанные с широким спектром генетических заболеваний и мутаций, и определить, являетесь ли вы и ваш партнер носителями одних и тех же заболеваний.
Расширенный скрининговый тест на носительство может обнаружить гены, связанные с широким спектром генетических заболеваний и мутаций, и определить, являетесь ли вы и ваш партнер носителями одних и тех же заболеваний. 
 2 deletion syndrome )
2 deletion syndrome ) Записаться на прием в клинику Майо
Как правило, генетические тесты имеют небольшой физический риск.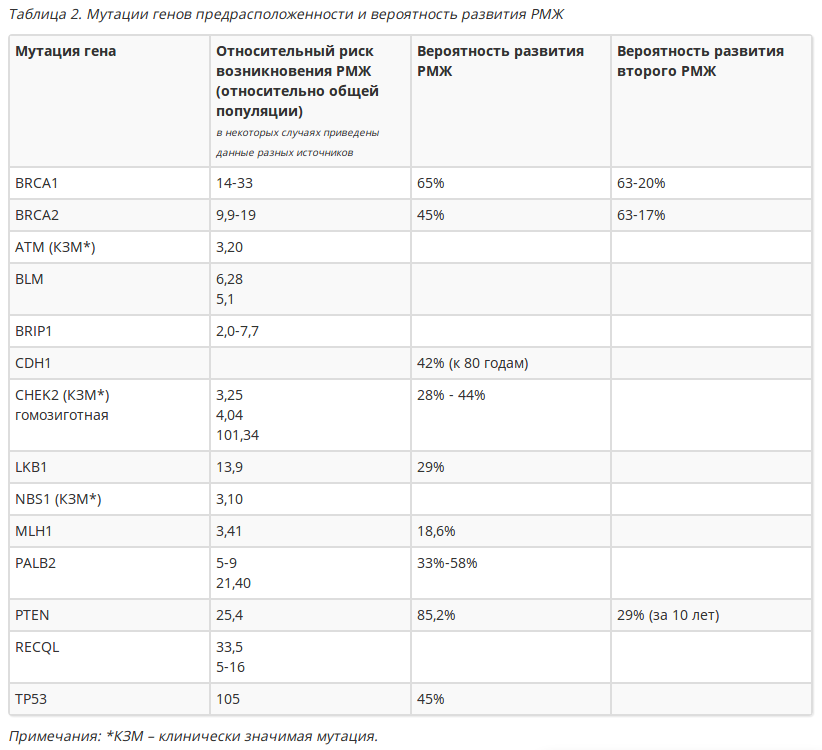 Анализы крови и мазка из щеки практически не представляют риска. Однако пренатальные тесты, такие как амниоцентез или биопсия ворсин хориона, имеют небольшой риск прерывания беременности (выкидыша).
Анализы крови и мазка из щеки практически не представляют риска. Однако пренатальные тесты, такие как амниоцентез или биопсия ворсин хориона, имеют небольшой риск прерывания беременности (выкидыша).
Генетическое тестирование также может иметь эмоциональные, социальные и финансовые риски. Обсудите все риски и преимущества генетического тестирования со своим врачом, медицинским генетиком или консультантом по генетическим вопросам, прежде чем проходить генетический тест.
Прежде чем пройти генетическое тестирование, соберите как можно больше информации об истории болезни вашей семьи. Затем поговорите со своим врачом или консультантом по генетике о своей личной и семейной истории болезни, чтобы лучше понять свой риск. Задавайте вопросы и обсуждайте любые опасения по поводу генетического тестирования на этой встрече. Также расскажите о своих вариантах в зависимости от результатов теста.
Если вы проходите тестирование на генетическое заболевание, передающееся по наследству, вы можете обсудить свое решение пройти генетическое тестирование со своей семьей.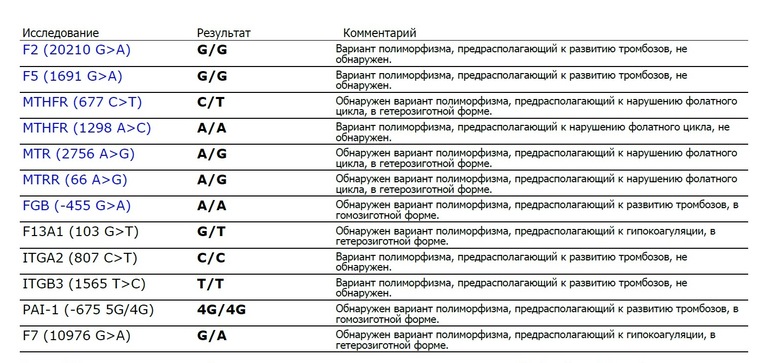 Эти беседы перед тестированием могут дать вам представление о том, как ваша семья может отреагировать на результаты вашего теста и как это может на них повлиять.
Эти беседы перед тестированием могут дать вам представление о том, как ваша семья может отреагировать на результаты вашего теста и как это может на них повлиять.
Не все полисы медицинского страхования оплачивают генетическое тестирование. Поэтому, прежде чем делать генетический тест, узнайте у своей страховой компании, что будет покрываться.
В Соединенных Штатах федеральный закон о недискриминации генетической информации от 2008 г. (GINA) помогает предотвратить дискриминацию вас медицинскими страховыми компаниями или работодателями на основании результатов анализов. В соответствии с GINA дискриминация при приеме на работу, основанная на генетическом риске, также является незаконной. Однако этот закон не распространяется на страхование жизни, долгосрочного ухода или страхования по инвалидности. Большинство штатов предлагают дополнительную защиту.
В зависимости от типа теста, образец вашей крови, кожи, амниотической жидкости или другой ткани будет взят и отправлен в лабораторию для анализа.
Время, необходимое для получения результатов генетического теста, зависит от типа теста и вашего медицинского учреждения. Поговорите со своим врачом, медицинским генетиком или консультантом по генетическим вопросам перед тестом о том, когда можно ожидать результатов, и обсудите их.
Поговорите со своим врачом, медицинским генетиком или консультантом по генетическим вопросам перед тестом о том, когда можно ожидать результатов, и обсудите их.
Если результат генетического теста положительный, это означает, что было обнаружено генетическое изменение, на которое проводилось тестирование. Действия, которые вы предпримете после получения положительного результата, будут зависеть от причины, по которой вы прошли генетическое тестирование.
Если целью является:
 Результаты теста также могут предоставить информацию, которую следует учитывать, когда вы и ваш партнер принимаете решения о планировании семьи.
Результаты теста также могут предоставить информацию, которую следует учитывать, когда вы и ваш партнер принимаете решения о планировании семьи. Поговорите со своим врачом о том, что означает для вас положительный результат. В некоторых случаях вы можете внести изменения в образ жизни, которые могут снизить риск развития заболевания, даже если у вас есть ген, делающий вас более восприимчивым к заболеванию. Результаты также могут помочь вам сделать выбор в отношении лечения, планирования семьи, карьеры и страхового покрытия.
Результаты также могут помочь вам сделать выбор в отношении лечения, планирования семьи, карьеры и страхового покрытия.
Кроме того, вы можете принять участие в исследованиях или регистрах, связанных с вашим генетическим заболеванием или заболеванием. Эти варианты могут помочь вам оставаться в курсе новых разработок в области профилактики или лечения.
Отрицательный результат означает, что мутировавший ген не был обнаружен тестом, что может быть обнадеживающим, но не дает 100-процентной гарантии того, что у вас нет расстройства. Точность генетических тестов для обнаружения мутировавших генов варьируется в зависимости от того, на какое заболевание проводится тестирование, и от того, была ли мутация гена ранее идентифицирована у члена семьи.
Даже если у вас нет мутировавшего гена, это не обязательно означает, что вы никогда не заболеете. Например, у большинства людей, у которых развивается рак молочной железы, нет гена рака молочной железы (9). 0228 BRCA1 или BRCA2 ). Кроме того, генетическое тестирование может не выявить все генетические дефекты.
0228 BRCA1 или BRCA2 ). Кроме того, генетическое тестирование может не выявить все генетические дефекты.
В некоторых случаях генетический тест может не дать полезной информации о рассматриваемом гене. У всех есть вариации в том, как проявляются гены, и часто эти вариации не влияют на ваше здоровье. Но иногда может быть трудно отличить болезнетворный ген от безвредной вариации гена. Эти изменения называются вариантами неопределенного значения. В этих ситуациях может потребоваться последующее тестирование или периодические проверки гена с течением времени.
Независимо от результатов вашего генетического тестирования, поговорите со своим врачом, медицинским генетиком или консультантом по генетическим вопросам, если у вас возникнут вопросы или опасения. Это поможет вам понять, что результаты означают для вас и вашей семьи.
Ознакомьтесь с исследованиями Mayo Clinic, посвященными тестам и процедурам, помогающим предотвращать, выявлять, лечить или управлять состояниями.
Персонал клиники Мэйо
Этот тест ищет мутации (изменения) в гене под названием MTHFR. Гены — это основные единицы наследственности, передаваемые от матери и отца.
У каждого человека есть два гена MTHFR, один из которых унаследован от матери, а другой — от отца. Мутации могут возникать в одном или обоих генах MTHFR. Существуют различные типы мутаций MTHFR. Тест MTHFR ищет две из этих мутаций, также известных как варианты. Варианты MTHFR называются C677T и A129.8С.
Ген MTHFR помогает вашему организму расщеплять вещество под названием гомоцистеин. Гомоцистеин — это тип аминокислоты, химическое вещество, которое ваш организм использует для производства белков. Обычно фолиевая кислота и другие витамины группы В расщепляют гомоцистеин и превращают его в другие вещества, необходимые вашему организму.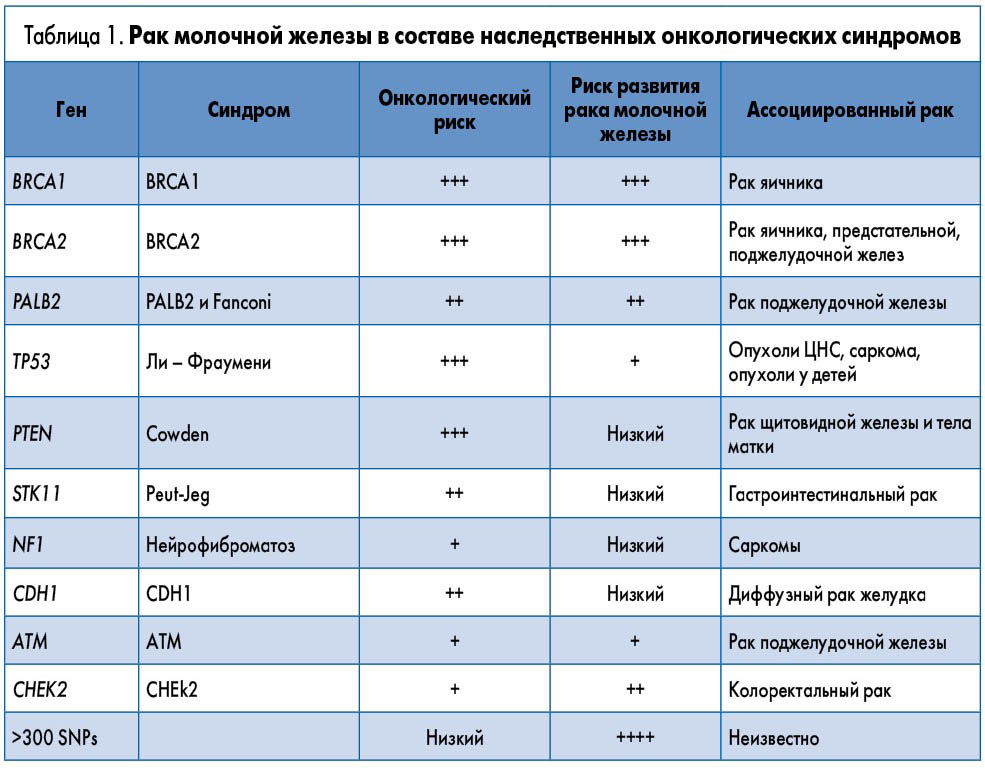 Тогда в кровотоке должно остаться очень мало гомоцистеина.
Тогда в кровотоке должно остаться очень мало гомоцистеина.
Если у вас есть мутация MTHFR, ваш ген MTHFR может работать неправильно. Это может привести к накоплению слишком большого количества гомоцистеина в крови, что приведет к различным проблемам со здоровьем, в том числе:
Кроме того, женщины с мутациями MTHFR имеют более высокий риск рождения ребенка с одним из следующих врожденных дефектов:
Вы можете снизить уровень гомоцистеина, принимая фолиевую кислоту или другие витамины группы В.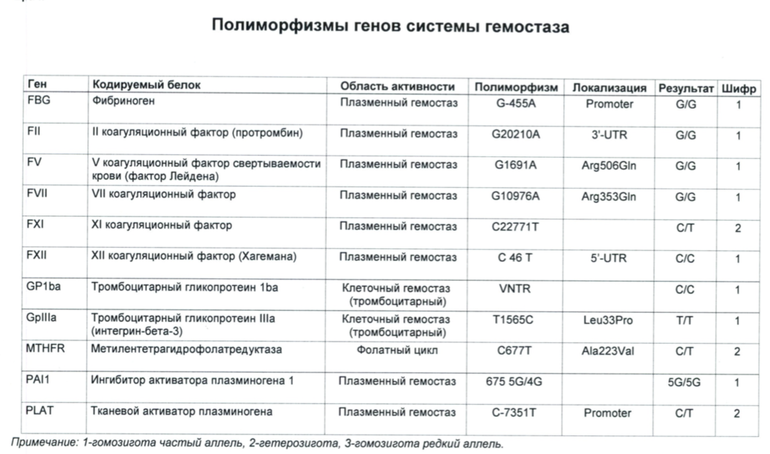 Их можно принимать в виде пищевых добавок или добавлять в рацион путем изменения диеты. Если вам нужно принимать фолиевую кислоту или другие витамины группы В, ваш лечащий врач порекомендует вам лучший вариант.
Их можно принимать в виде пищевых добавок или добавлять в рацион путем изменения диеты. Если вам нужно принимать фолиевую кислоту или другие витамины группы В, ваш лечащий врач порекомендует вам лучший вариант.
Другие названия: общий гомоцистеин плазмы, анализ мутаций ДНК метилентетрагидрофолатредуктазы
Этот тест используется для определения наличия у вас одной из двух мутаций MTHFR: C677T и A1298C. Его часто используют после того, как другие тесты показывают, что у вас уровень гомоцистеина в крови выше нормы. Такие состояния, как высокий уровень холестерина, заболевания щитовидной железы и дефицит рациона, также могут повышать уровень гомоцистеина. Тест MTHFR подтвердит, вызваны ли повышенные уровни генетической мутацией.
Несмотря на то, что мутация MTHFR повышает риск врожденных дефектов, тест обычно не рекомендуется беременным женщинам. Прием добавок фолиевой кислоты во время беременности может значительно снизить риск врожденных дефектов нервной трубки. Таким образом, большинству беременных женщин рекомендуется принимать фолиевую кислоту, независимо от того, есть ли у них мутация MTHFR.
Таким образом, большинству беременных женщин рекомендуется принимать фолиевую кислоту, независимо от того, есть ли у них мутация MTHFR.
Вам может понадобиться этот тест, если:
Медицинский работник возьмет образец крови из вены на вашей руке с помощью маленькой иглы. После введения иглы небольшое количество крови собирается в пробирку или флакон. Вы можете почувствовать легкое жжение, когда игла входит или выходит. Обычно это занимает не более пяти минут.
Для скрининга новорожденных медицинский работник протирает пятку вашего ребенка спиртом и прокалывает пятку маленькой иглой. Он или она возьмет несколько капель крови и наложит на это место повязку.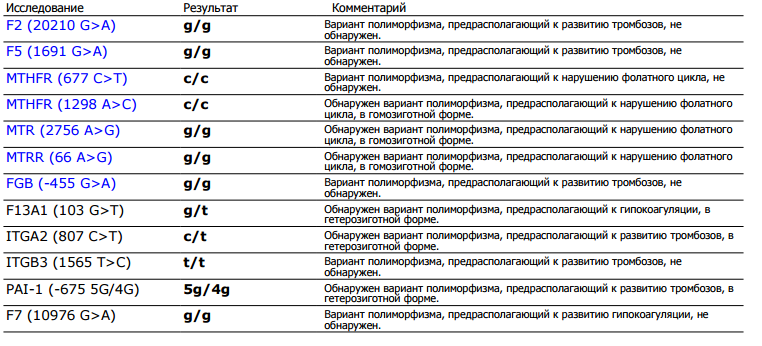
Тестирование чаще всего проводится в возрасте от 1 до 2 дней, обычно в больнице, где он родился. Если ваш ребенок родился не в больнице или если вы выписались из больницы до того, как ребенка можно было сдать на анализ, как можно скорее поговорите со своим лечащим врачом о планировании тестирования.
Для проведения теста на мутацию MTHFR не требуется никакой специальной подготовки.
Существует очень небольшой риск для вас или вашего ребенка при тестировании MTHFR. У вас может быть небольшая боль или синяк в месте введения иглы, но большинство симптомов быстро проходят.
Ваш ребенок может чувствовать легкое пощипывание, когда пятка ткнется, и на этом месте может образоваться небольшой синяк. Это должно быстро уйти.
Ваши результаты покажут, положительная или отрицательная у вас мутация MTHFR. В случае положительного результата результат покажет, какая из двух мутаций у вас есть, и есть ли у вас одна или две копии мутировавшего гена.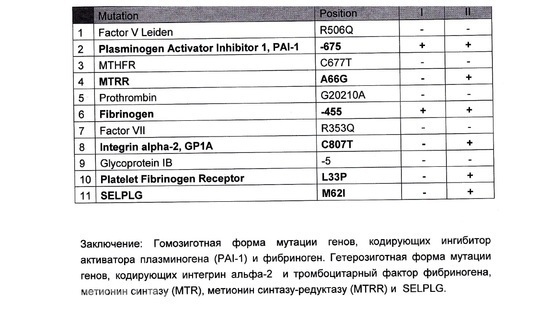 Если ваши результаты были отрицательными, но у вас высокий уровень гомоцистеина, ваш лечащий врач может назначить дополнительные анализы, чтобы выяснить причину.
Если ваши результаты были отрицательными, но у вас высокий уровень гомоцистеина, ваш лечащий врач может назначить дополнительные анализы, чтобы выяснить причину.
Независимо от причины высокого уровня гомоцистеина ваш лечащий врач может порекомендовать принимать фолиевую кислоту и/или другие добавки витамина B и/или изменить свой рацион. Витамины группы В могут помочь вернуть уровень гомоцистеина в норму.
Если у вас есть вопросы по поводу результатов, обратитесь к своему лечащему врачу.
Узнайте больше о лабораторных тестах, референтных диапазонах и понимании результатов.
Некоторые поставщики медицинских услуг предпочитают проводить тест только на уровень гомоцистеина, а не тест на ген MTHFR. Это потому, что лечение часто одинаково, независимо от того, вызван ли высокий уровень гомоцистеина мутацией.
 Генетический тест, который вам не нужен; 2013 г., 27 сентября [цитировано 18 августа 2018 г.]; [около 4 экранов]. Доступно по адресу: https://health.clevelandclinic.org/a-genetic-test-you-dont-need
Генетический тест, который вам не нужен; 2013 г., 27 сентября [цитировано 18 августа 2018 г.]; [около 4 экранов]. Доступно по адресу: https://health.clevelandclinic.org/a-genetic-test-you-dont-need 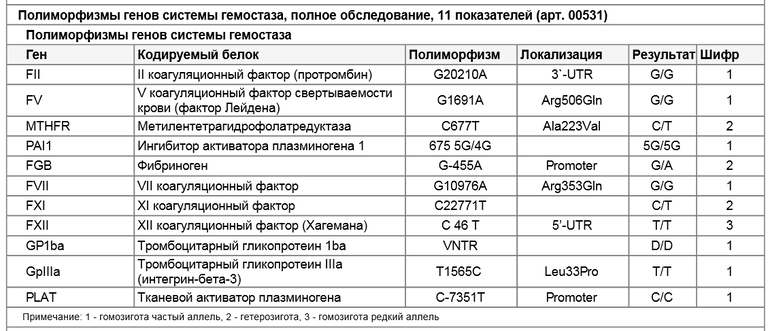 Фонд Немура; с1995–2018. скрининговые тесты новорожденных; [цитировано 18 августа 2018 г.]; [около 3 экранов]. Доступно по адресу: https://kidshealth.org/en/parents/newborn-screening-tests.html?ref=search&WT.ac=msh-p-dtop-en-search-clk
Фонд Немура; с1995–2018. скрининговые тесты новорожденных; [цитировано 18 августа 2018 г.]; [около 3 экранов]. Доступно по адресу: https://kidshealth.org/en/parents/newborn-screening-tests.html?ref=search&WT.ac=msh-p-dtop-en-search-clk  ]; [около 3 экранов]. Доступно по адресу: https://www.marchofdimes.org/baby/newborn-screening-tests-for-your-baby.aspx
]; [около 3 экранов]. Доступно по адресу: https://www.marchofdimes.org/baby/newborn-screening-tests-for-your-baby.aspx 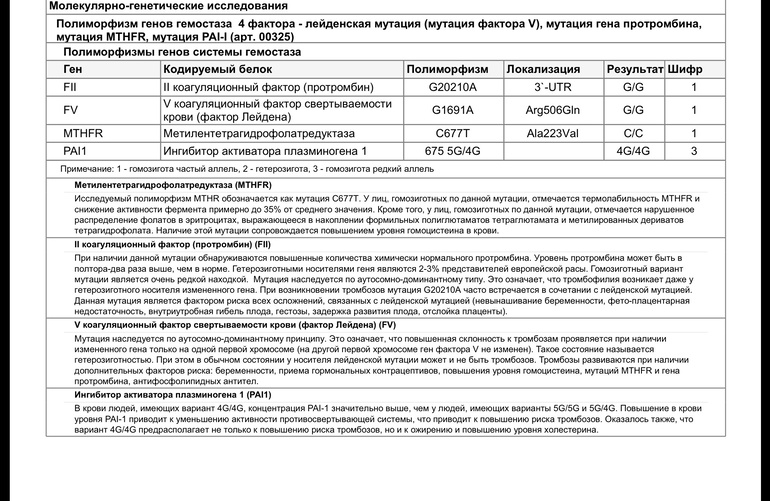 ]; [около 3 экранов]. Доступно по адресу: https://www.cancer.gov/publications/dictionaries/cancer-terms/search?contains=false&q=gene
]; [около 3 экранов]. Доступно по адресу: https://www.cancer.gov/publications/dictionaries/cancer-terms/search?contains=false&q=gene  [цитировано 18 августа 2018 г.]; [около 3 экранов]. Доступно по адресу: https://ghr.nlm.nih.gov/gene/MTHFR
[цитировано 18 августа 2018 г.]; [около 3 экранов]. Доступно по адресу: https://ghr.nlm.nih.gov/gene/MTHFR