2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Описание
Метод определения Иммунофенотипирование (проточная цитофлюориметрия)
Исследуемый материал Цельная кровь (с ЭДТА)
Доступен выезд на дом
Онлайн-регистрация
Исследование содержания активированных лимфоцитов может быть назначено дополнительно к профилю № 191 Иммунологическое исследование скрининговое или тесту № 4192 Фенотипирование лимфоцитов, основные субпопуляций для оценки уровня активации или дисфункции соответствующих клеточных популяций.
Тест входит в состав профиля №192 Иммунологическое исследование расширенное. Отдельно от исследования содержания основных субпопуляций лимфоцитов тест № 1311 «Активированные лимфоциты» не проводится в связи с отсутствием информативности такого исследования.
CD3 – поверхностный маркёр, специфичный для всех клеток субпопуляции Т-лимфоцитов. По функциям относится к семейству белков, формирующих комплекс мембранной передачи сигнала, связанный с Т-клеточным рецептором.
HLA-DR – один из антигенов MHC класса II (major histocompatibility complex - главный комплекс гистосовместимости), участвующих в презентации потенциально чужеродных антигенов, что необходимо для формирования адекватного иммунного ответа. При иммунофенотипировании может быть использован в качестве маркёра активированных клеток.
CD3+HLA-DR+ - клетки, представляющие собой зрелые активированные Т-лимфоциты человека.
CD3-HLA-DR+ - В-лимфоциты и активированные ЕК- лимфоциты.
Подготовка
Строго натощак (в период с 7.00 до 11.00) после ночного периода голодания от 8 до 14 часов.
Накануне исследования необходимо исключить повышенные психоэмоциональные и физические нагрузки (спортивные тренировки), приём алкоголя, за час до исследования – курение.
Показания к назначению
Важно! Исследование №1311 «Активированные лимфоциты (CD3+HLA-DR+, CD3-HLA-DR+)» рекомендуется назначать только в дополнение к скрининговому иммунологическому исследованию (№191) или тесту №4192 «Основные субпопуляции лимфоцитов».
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения.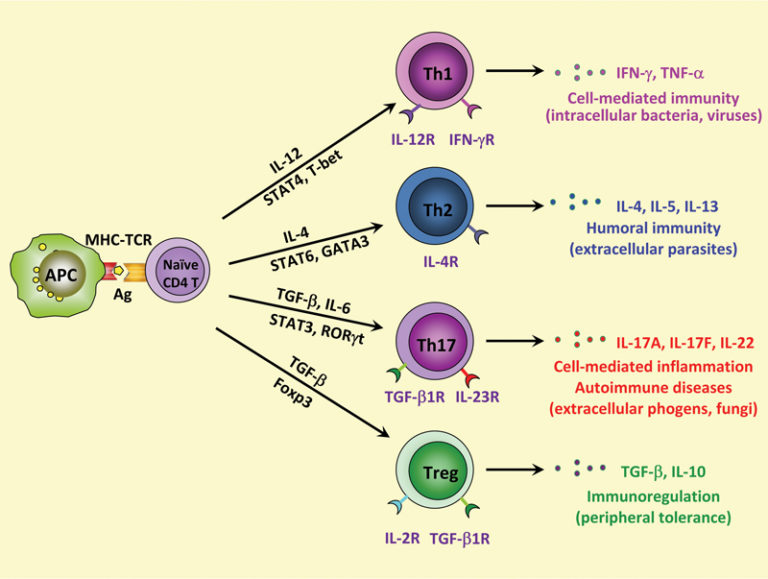 Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения в Независимой лаборатории ИНВИТРО:
|
CD3+HLA-DR+ (Активированные Т-лимфоциты) |
|
|
CD3-HLA-DR+ (Активированные не-Т-лимфоциты) |
|
Референсные значения субпопуляций лимфоцитов:
| CD3+HLA-DR+ (зрелые активированные T-лимфоциты) |
| Возраст | % от общего количества лимфоцитов |
1 мес.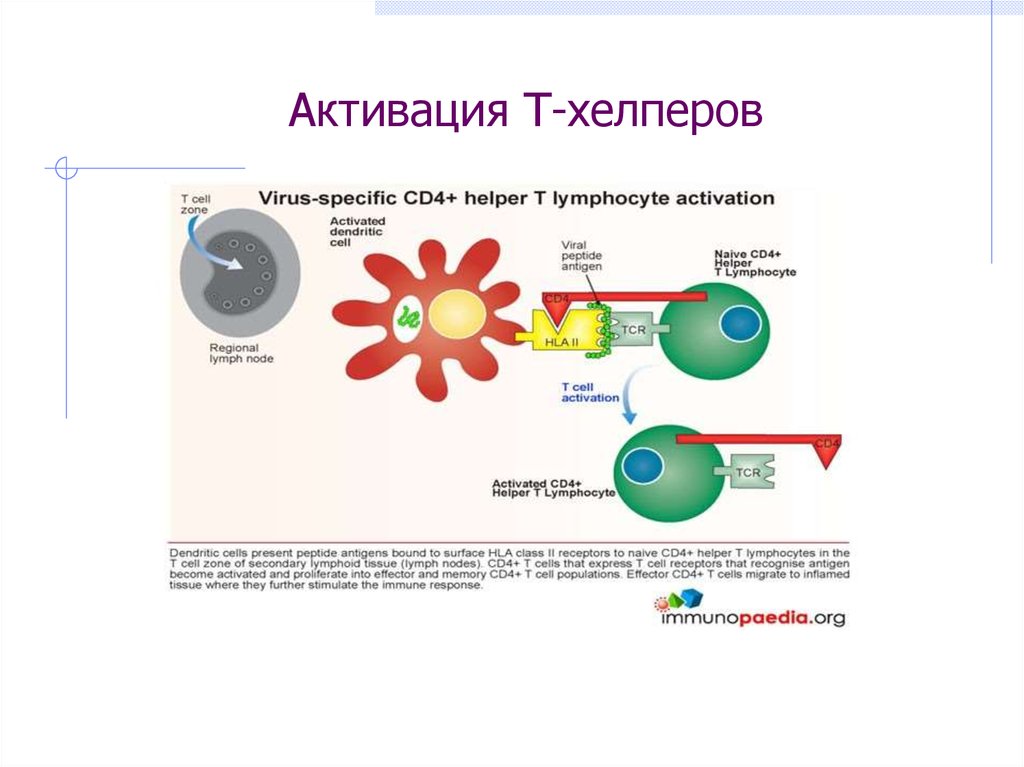 - 4 мес.
- 4 мес. | 1-9 |
| 4 мес. - 1 год | 1-7 |
| 1 - 2 года | 3-12 |
| 2 - 6 лет | 3-13 |
| 6 - 12 лет | 3-14 |
| 12 - 16 лет | 1-8 |
| > 16 лет | 2-20 |
| CD3-HLA-DR+ (В-лимфоциты и активированные ЕК- лимфоциты) |
| Возраст | % от общего количества лимфоцитов | Абсолютное количество клеток х 106/л |
| 1 мес. - 16 лет | 5-20 | 60 - 600 |
| >16 лет | 7-21 | 100-640 |
Интерпретация:
Повышение показателей – генерализованный острый или активный хронический воспалительный процесс.
Снижение показателей - не имеет самостоятельного диагностического значения.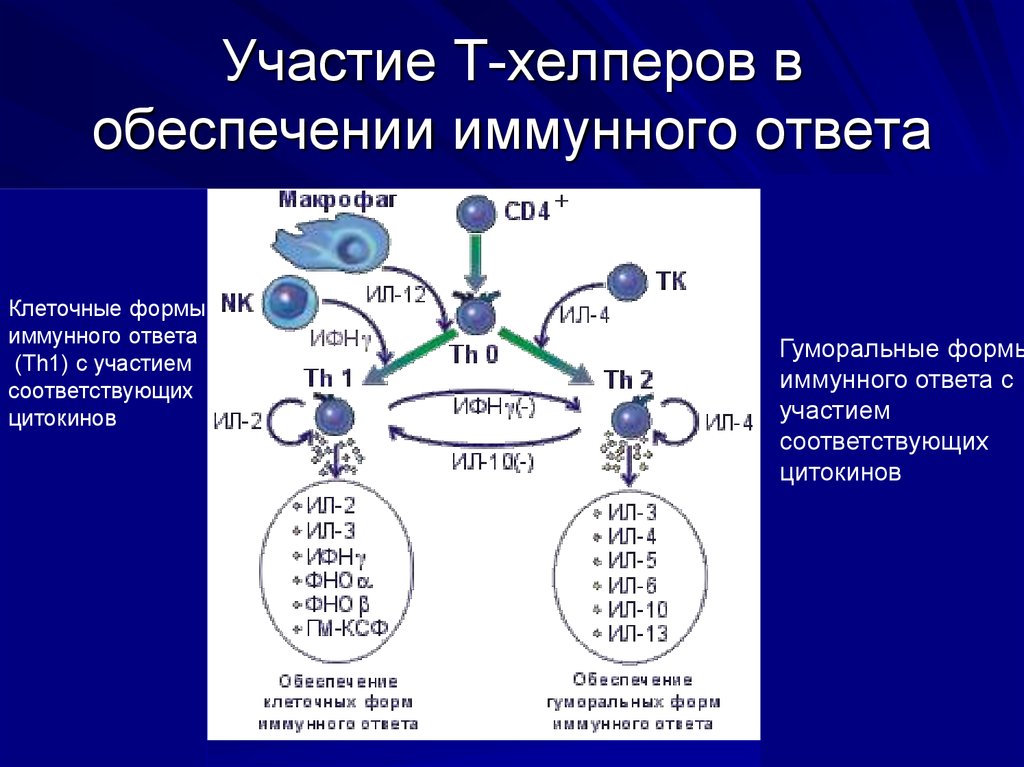
Первым исследованием всегда является подсчет лейкоцитарной формулы (см. главу «Гематологические исследования»). Оцениваются как относительные, так и абсолютные значения количества клеток периферической крови.
Определение основных популяций (Т-клетки, В-клетки, натуральные киллеры) и субпопуляций Т-лимфоцитов (Т-хелперы, Т-ЦТЛ). Для первичного исследования иммунного статуса и выявления выраженных нарушений иммунной системы ВОЗ рекомендовано определение CD3, CD4, CD8, CD19, CD16+56, соотношение CD4/CD8. Исследование позволяет определить относительное и абсолютное количество основных популяций лимфоцитов: Т-клетки – CD3, В-клетки – CD19, натуральные киллеры (NK) – CD3- CD16++56+, субпопуляции Т лимфоцитов (Т-хелперы CD3+ CD4+, Т-цитотоксические CD3+ CD8+ и их соотношение).
Метод исследования
Иммунофенотипирование лимфоцитов проводится c использованием моноклональных антител к поверхностным дифференцировочным ангинам на клетках иммунной системы, методом проточной лазерной цитофлуорометрии на проточных цитофлуориметрах.
Выбор зоны анализа лимфоцитов производится по дополнительному маркеру CD45, который представлен на поверхности всех лейкоцитов.
Условия взятия и хранения образцов
Венозная кровь, взятая из локтевой вены, утром, строго натощак, в вакуумную систему до указанной на пробирке метки. В качестве антикоагулянта используется К2ЭДТА. После взятия пробирку с образцом медленно переворачивают 8-10 раз для перемешивония крови с антикоагулянтом. Хранение и транспортировка строго при 18–23°С в вертикальном положении не более 24 ч.
Невыполнение этих условий приводит к некорректным результатам.
Интерпретация результатов
Т-лимфоциты (CD3+ клетки). Повышенное количество свидетельствует о гиперактивности иммунитета, наблюдается при острых и хронических лимфолейкозах. Увеличение относительного показателя встречается при некоторых вырусных и бактериальных инфекциях в начале заболевания, обострениях хронических заболеваний.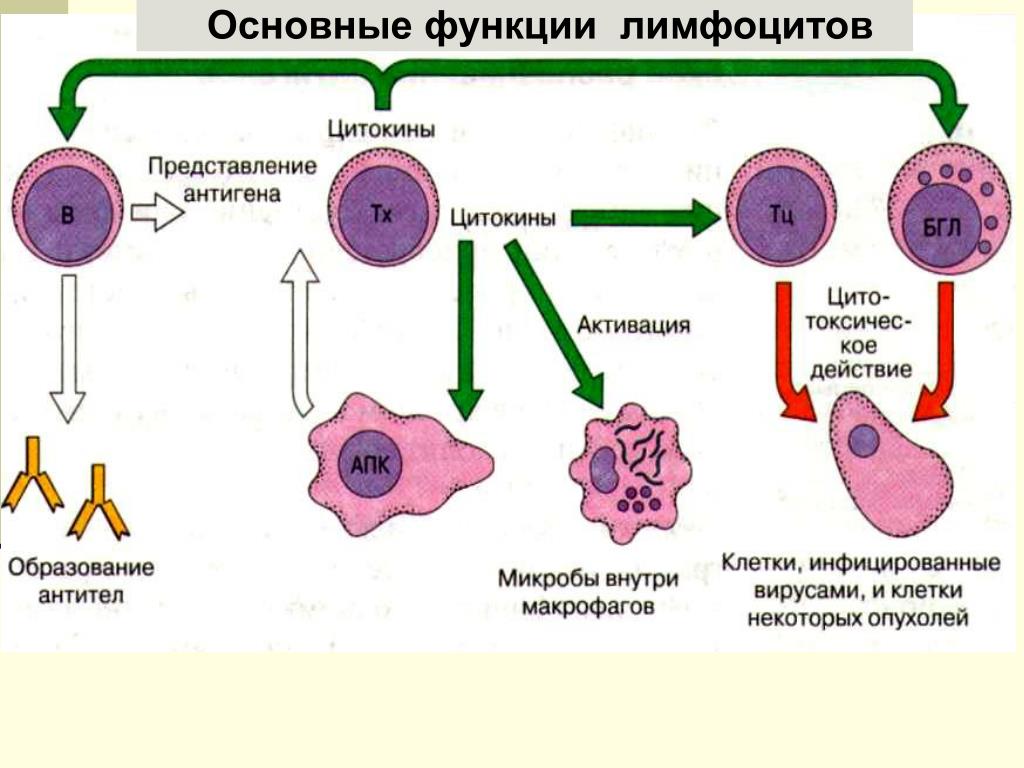
Снижение абсолютного количества Т-лимфоцитов свидетельствует о недостаточности клеточного иммунитета, а именно о недостаточности клеточно-эффекторного звена иммунитета. Выявляется при воспалениях разнообразной этиологии, злокачественных новообразованиях, после травмы, операций, инфаркта, при курении, приеме цитостатиков. Повышение их числа в динамике заболевания – клинически благоприятный признак.
В-лимфоциты (CD19+ клетки) Снижение наблюдается при физиологических и врожденных гипогаммаглобулинемиях и агаммаглобулинемиях, при новообразованиях иммунной системы, лечении иммунодепрессантами, острой вирусной и хронической бактериальной инфекциях, состоянии после удаления селезенки.
Увеличение отмечается при аутоиммунных заболеваниях, хронических заболеваниях печени, циррозе, муковисцедозе, бронхиальной астме, паразитарных и грибковых инфекциях. Характерно в период реконвалесценции после перенесенных острых и хронических вирусных и бактериальных инфекций. Выраженное увеличение наблюдается при хроническом В-лимфолейкозе.
Выраженное увеличение наблюдается при хроническом В-лимфолейкозе.
NK-лимфоциты с фенотипом CD3-CD16++56+ Натуральные киллеры (NK-клетки) – популяция больших гранулярных лимфоцитов. Они способны лизировать клетки-мишени, инфицированные вирусами и другими внутриклеточными антигенами, опухолевые клетки, а также другие клетки аллогенного и ксеногенного происхождения.
Увеличение количества NK-клеток связано с активацией антитрансплантационного иммунитета, в некоторых случаях отмечается при бронхиальной астме, встречается при вирусных заболеваниях, повышается при злокачественных новообразованиях и лейкозах, в периоде реконвалесценции.
Снижение наблюдается при врожденных иммунодефицитах, паразитарных инфекциях, аутоиммунных заболеваниях, облучении, лечении цитостатиками и кортикостероидами, стрессе, дефиците цинка.
Т-лимфоциты хелперы с фенотипом CD3+CD4+ Увеличение абсолютного и относительного количества наблюдается при аутоиммунных заболеваниях, может быть при аллергических реакциях, некоторых инфекционных заболеваниях.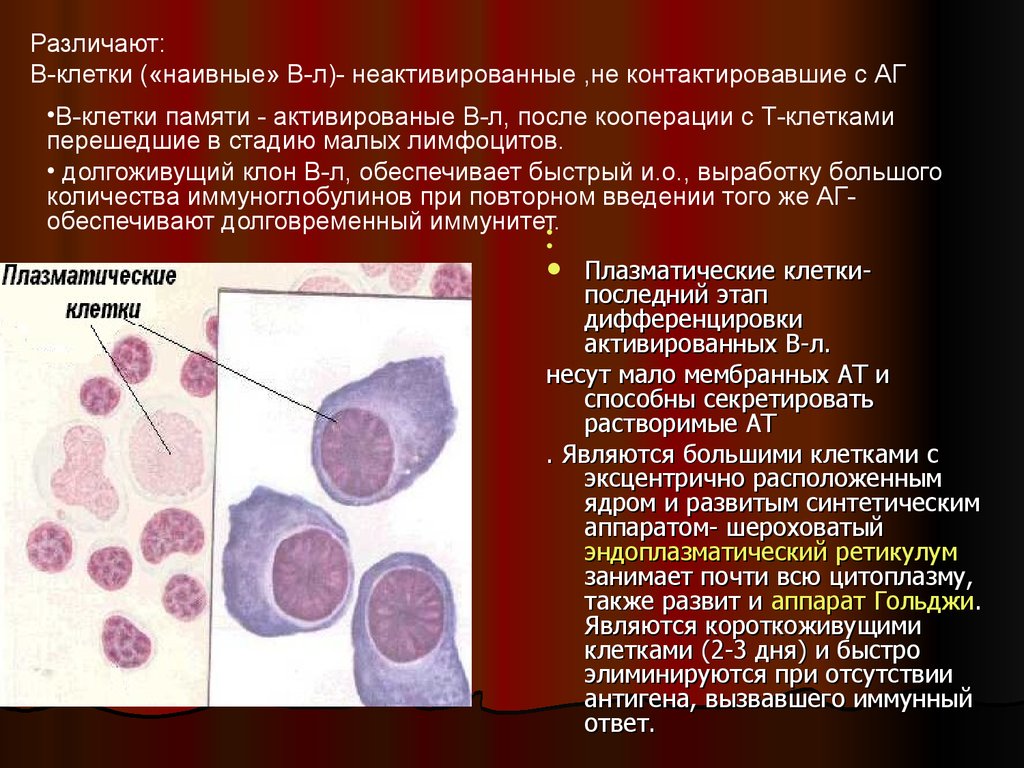 Это увеличение свидетельствует о стимуляции иммунной системы на антиген и служит подтверждением гиперреактивных синдромов.
Это увеличение свидетельствует о стимуляции иммунной системы на антиген и служит подтверждением гиперреактивных синдромов.
Снижение абсолютного и относительного количества Т-клеток свидетельствует о гипореактивном синдроме с нарушением регуляторного звена иммунитета, является патогномичным признаком для ВИЧ-инфекции; встречается при хронических заболеваниях (бронхитах, пневмониях и т.д.), солидных опухолях.
Т-цитотоксические лимфоциты с фенотипом CD3+ CD8+ Повышение выявляется практически при всех хронических инфекциях, вирусных, бактериальных, протозойных инфекциях. Является характерным для ВИЧ-инфекции. Снижение наблюдается при вирусных гепатитах, герпесе, аутоиммунных заболеваниях.
Соотношение CD4+/CD8+ Исследование соотношения CD4+/CD8+ (CD3, CD4, CD8, CD4/CD8) рекомендовано только для мониторинга ВИЧ-инфекции и контроля эффективности АРВ терапии. Позволяет определить абсолютное и относительное количество Т-лимфоцитов, субпопуляций Т-хелперов, ЦТЛ и их соотношение.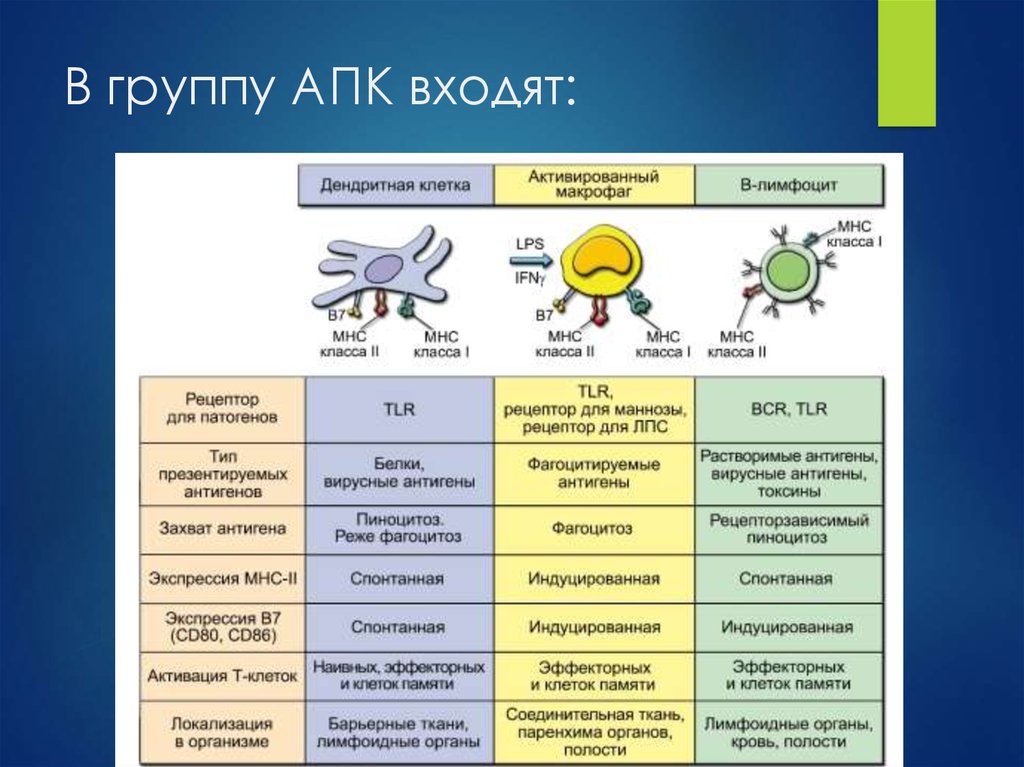
Диапазон значений – 1,2–2,6. Снижение наблюдается при врожденных иммунодефицитах (синдром Ди-Джоржи, Незелофа, Вискотта-Олдрича), при вирусных и бактериальных инфекциях, хронических процессах, воздействии радиации и токсических химических веществ, множественной миеломе, стрессе, снижается с возрастом, при эндокринных заболеваниях, солидных опухолях. Является патогномичным признаком для ВИЧ-инфекции (менее 0,7).
Увеличение значения более 3 – при аутоиммунных заболеваниях, остром Т-лимфобластном лейкозе, тимоме, хроническом Т-лейкозе.
Изменение соотношения может быть связано с количеством хелперов и ЦТЛ у данного пациента. Например, снижение количества CD4+ Т-клеток при острой пневмонии в начале заболевания ведет к снижению индекса, а ЦТЛ при этом могут не измениться.
Для дополнительного исследования и выявления изменений иммунной системы при патологиях требующих оценки наличия острого или хронического воспалительного процесса и степени его активности, рекомендуется включать подсчет количества активированных Т-лимфоцитов с фенотипом CD3+HLA-DR+ и ТNK–клеток с фенотипом CD3+CD16++56+.
Т-активированные лимфоциты с фенотипом CD3+HLA-DR+ Маркер поздней активации, показатель гиперреактивности иммунитета. По экспрессии данного маркера можно судить о выраженности и силе иммунного ответа. Появляется на Т-лимфоцитах после 3-го дня острого заболевания. При благоприятном течении заболевания снижается до нормы. Увеличение экспрессии на Т-лимфоцитах может быть при многих заболеваниях, связанных с хроническим воспалением. Отмечено его повышение у пациентов с гепатитом С, пневмониями, ВИЧ-инфекцией, солидными опухолями, аутоиммунными заболеваниями.
ТNK-лимфоциты с фенотипом CD3+CD16++CD56+ Т-лимфоциты, несущие на своей поверхности маркеры CD16++ CD 56+. Эти клетки имеют свойства как Т-, так и NK-клеток. Исследование рекомендовано как дополнительный маркер при острых и хронических заболеваниях.
Снижение их в периферической крови может наблюдаться при различных органоспецифических заболеваниях и системных аутоиммунных процессах. Увеличение отмечено при воспалительных заболеваниях разной этиологии, опухолевых процессах.
Увеличение отмечено при воспалительных заболеваниях разной этиологии, опухолевых процессах.
Исследование ранних и поздних маркеров активации Т-лимфоцитов (CD3+CD25+, CD3-CD56+, CD95, CD8+CD38+) дополнительно назначают для оценки изменений ИС при острых и хронических заболеваниях, для диагностики, прогноза, мониторинга течения заболевания и проводимой терапии.
Т-активированные лимфоциты с фенотипом CD3+CD25+, рецeптор к ИЛ2 CD25+ – маркер ранней активации. О функциональном состоянии Т-лимфоцитов (CD3+) свидетельствует количество экспрессирующих рецепторов к ИЛ2 (CD25+). При гиперактивных синдромах количество этих клеток возрастает (острые и хронические лимфолейкозы, тимома, отторжение трансплантата), кроме того, повышение их может свидетельствовать о ранней стадии воспалительного процесса. В периферической крови их можно выявить в первые три дня болезни. Снижение числа этих клеток может наблюдаться при врожденных иммунодефицитах, аутоиммунных процессах, ВИЧ-инфекции, грибковых и бактериальных инфекциях, ионизирующей радиации, старении, отравлении тяжелыми металлами.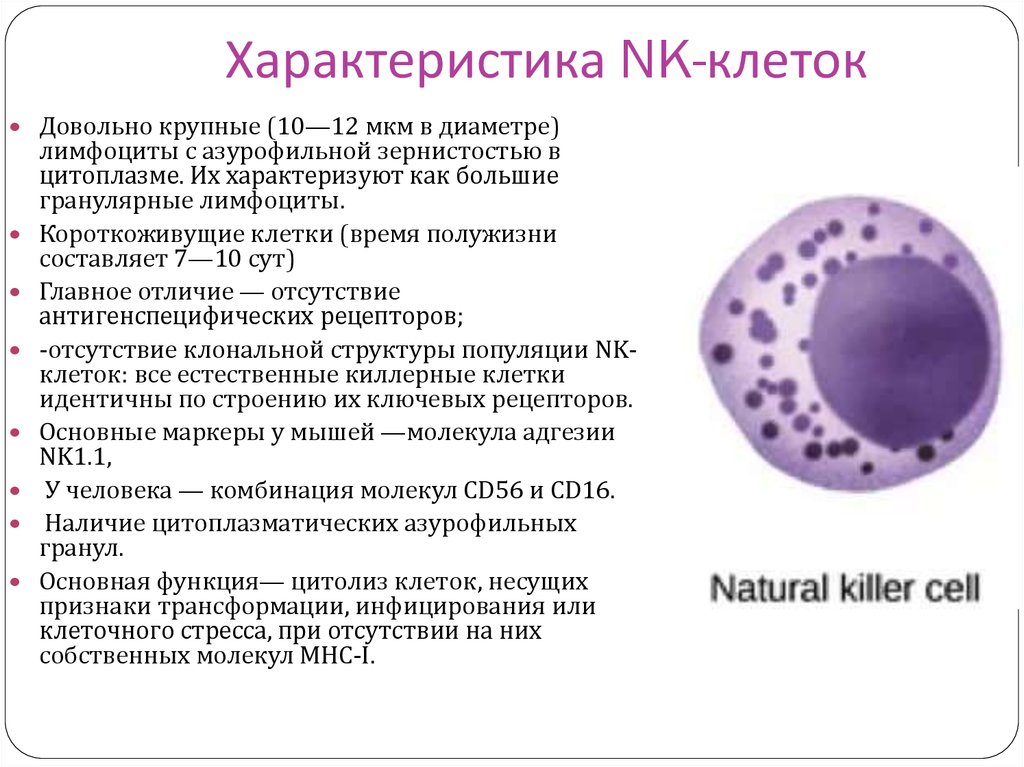
Т-цитотоксические лимфоциты с фенотипом CD8+CD38+ Присутствие CD38+ на ЦТЛ лимфоцитах отмечено у пациентов с разными заболеваниями. Информативный показатель при ВИЧ-инфекции, ожоговой болезни. Увеличение числа ЦТЛ с фенотипом CD8+CD38+ наблюдается при хронических воспалительных процессах, онкологических и некоторых эндокринных заболеваниях. При проведении терапии показатель снижается.
Субпопуляция натуральных киллеров с фенотипом CD3- CD56+ Молекула CD56 – адгезивная молекула, широко представленная в нервной ткани. Кроме натуральных киллеров, экспрессируется на многих типах клеток, в том число на Т-лимфоцитах.
Увеличение данного показателя свидетельствуют о расширении активности специфического клона клеток киллеров, которые имеют меньшую цитолитическую активность, чем NK-клетки с фенотипом CD3- CD16+. Количество этой популяции возрастает при гематологических опухолях (ЕК-клеточная или Т-клеточная лимфома, плазмоклеточная миелома, апластическая крупноклеточная лимфома), хронических заболеваниях, некоторых вырусных инфекциях.
Снижение отмечается при первичных иммунодефицитах, вирусных инфекциях, системных хронических заболеваниях, стрессе, лечении цитостатиками и кортикостероидами.
Рецептор CD95+ – один из рецепторов апоптоза. Апоптоз – сложный биологический процесс, необходимый для удаления из организма поврежденных, старых и инфицированных клеток. Рецептор CD95 экспрессируется на всех клетках иммунной системы. Он играет важную роль в контроле функционирования иммунной системы, так как является одним из рецепторов апоптоза. Его экспрессия на клетках определяет готовность клеток к апоптозу.
Снижение доли CD95+-лимфоцитов в крови пациентов свидетельствует о нарушении эффективности последнего этапа выбраковки дефектных и инфицированных собственных клеток, что может привести к рецидиву заболевания, хронизации патологического процесса, развитию аутоиммунных заболеваний и повышению вероятности опухолевой трансформации (к примеру, рака шейки матки при папилломотозной инфекции).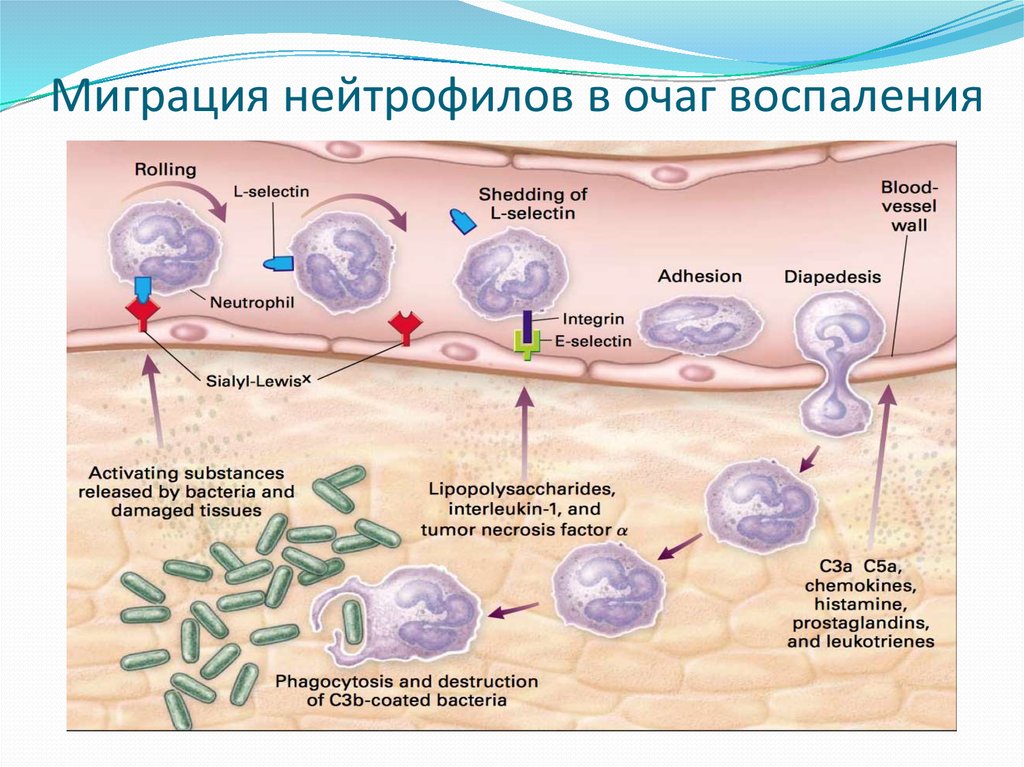 Определение экспрессии CD95 имеет прогностическое значение при миело- и лимфопролифератиных заболеваниях.
Определение экспрессии CD95 имеет прогностическое значение при миело- и лимфопролифератиных заболеваниях.
Повышение интенсивности апоптоза наблюдается при вирусных заболеваниях, септических состояниях, при употреблении наркотических средств.
Активированные лимфоциты CD3+CDHLA-DR+, CD8+CD38+, CD3+CD25+, CD95. Тест отражает функциональное состояние Т-лимфоцитов и рекомендован для контроля за течением заболевания и контроля иммунотерапии при воспалительных заболеваниях разной этиологии.
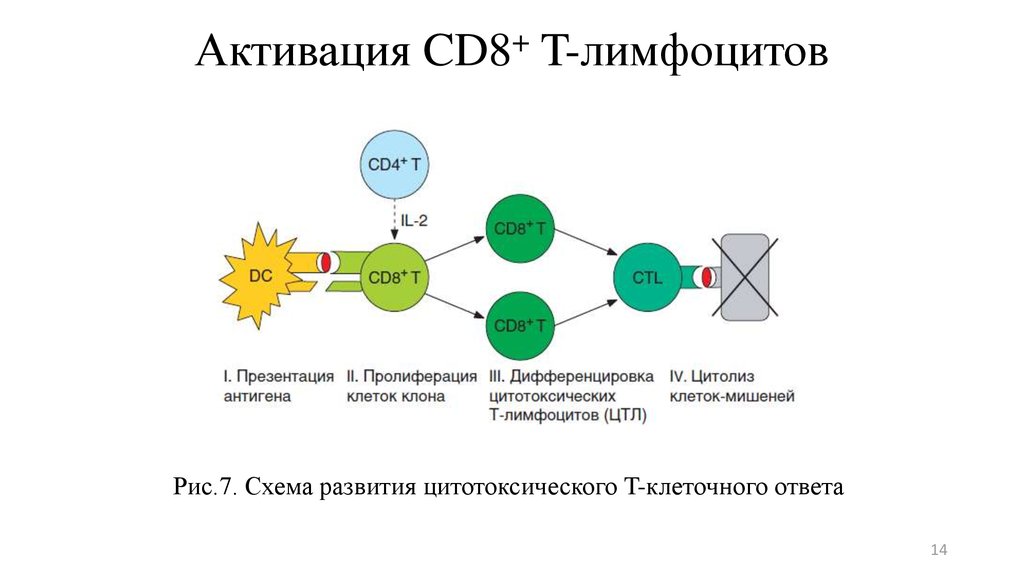
Активация лимфоцитов происходит, когда лимфоциты (В-клетки или Т-клетки) запускаются через антиген-специфические рецепторы на их клеточной поверхности. Это заставляет клетки пролиферировать и дифференцироваться в специализированные эффекторные лимфоциты. Например, активированные В-клетки могут давать начало клеткам, продуцирующим антитела, а некоторые активированные Т-клетки становятся цитотоксическими Т-клетками.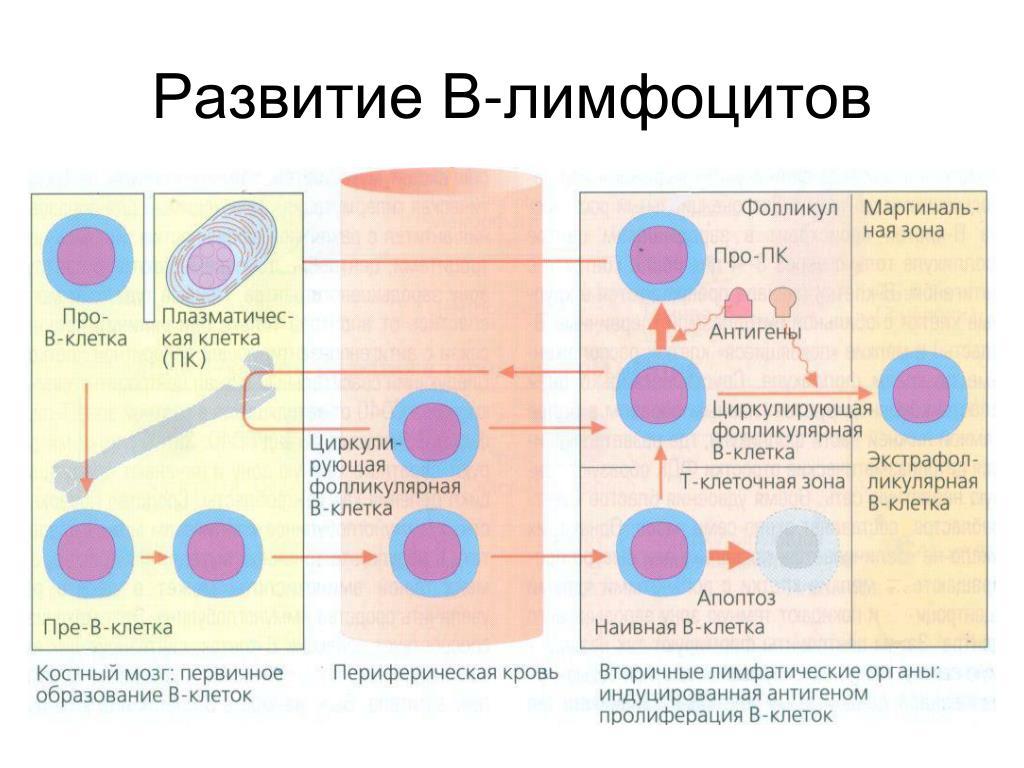
Исследовательская работа
| Открытый доступ
Научные отчеты 12, 21056
Исследовательская работа
| Открытый доступ
Белок линкер для активации Т-клеток (LAT) участвует в активации Т-клеток. Здесь авторы обнаруживают события конденсации LAT в микронном масштабе ниже по течению от одиночно связанных рецепторов Т-клеток во время активации Т-клеток и характеризуют, как время конденсации LAT влияет на передачу сигналов Т-клеток ниже по течению.
Nature Communications 13, 7446
Исследовательская работа
| Открытый доступ
Известно, что корецептор Т-клеток CD4 значительно увеличивает способность передачи сигналов Т-клеточного рецептора (TCR), запускаемую молекулой MHC, связанной с пептидом. Здесь авторы показывают, что механистической основой усиления является совместное связывание TCR и CD4 с комплексом MHC-пептид.
Nature Communications 13, 7055
Исследовательская работа
| Открытый доступ
MR1 функционирует как антигенпрезентирующий белок на клетках в дополнение к клеткам MAIT. Здесь авторы используют раннюю специфичную к Т-клеткам мышь с дефицитом Bcl11b, у которой развивается аутоиммунитет через популяцию нетрадиционных MR1-рестриктированных Т-клеток, и характеризуют их функцию.
Nature Communications 13, 6948
Исследовательская работа
| Открытый доступ
Научные отчеты 12, 19487
Исследовательская работа
| Открытый доступ
Боковой амиотрофический склероз (БАС) является первичным нейродегенеративным заболеванием, которое характеризуется повышенной инфильтрацией иммунными клетками центральной нервной системы. Здесь авторы показывают, что фенотипический профиль Т-клеток в крови и спинномозговой жидкости пациентов с недавно диагностированным БАС может предсказать прогрессирование заболевания, тем самым предоставляя доказательства того, что Т-клетки вносят вклад в патологию заболевания.
Здесь авторы показывают, что фенотипический профиль Т-клеток в крови и спинномозговой жидкости пациентов с недавно диагностированным БАС может предсказать прогрессирование заболевания, тем самым предоставляя доказательства того, что Т-клетки вносят вклад в патологию заболевания.
Nature Communications 13, 6733
Все исследования и обзоры
Основные результаты исследований |
Природа Иммунология 23, 1399
Новости и просмотры |
Текущие реципиенты вакцины против SARS-CoV-2 различаются по анамнезу инфекции и степени выраженности вызванного ими ответа антител. Большую когорту людей, отличающихся этими параметрами, опрашивают на наличие субпопуляций эффекторных Т-клеток, В-клеток памяти и способности распознавать эпитопы из вызывающих беспокойство вариантов SARS-CoV-2.
Природа Иммунология 23, 1403-1404
Новости и просмотры |
m1A58 — это распространенная модификация тРНК, которая может влиять на эффективность трансляции белка. Здесь Лю и соавт. показывают, что метилирование тРНК контролирует активацию Т-клеток in vivo путем усиления трансляции ключевого фактора транскрипции Myc.
Природа Иммунология 23, 1401-1402
Все новости и комментарии
Содержание
Вы больше визуал? Посмотрите наши онлайн-видеолекции и начните свой курс иммунологии прямо сейчас бесплатно!
Изображение: «Т-вспомогательная клетка» от
allinonemovie. Лицензия: CC 0
Лицензия: CC 0
Когда воздействие антигена происходит впервые ( первичная доза ), наш организм дает первичный иммунный ответ. Существует латентный период, когда сразу после примирующей дозы антитела в сыворотке не обнаруживаются. Далее следует логарифмическая фаза , в которой происходит активный биосинтез антител.
Во время плато или стационарного состояния концентрация антител в сыворотке остается постоянной. Наконец, наблюдается фаза упадка , во время которой катаболизм преобладает над синтезом. Таким образом, первичная реакция медленная, вялая и кратковременная. Он имеет длительную лаг-фазу от 5 до 7 дней. Низкие титры антител (IgM) сохраняются кратковременно. Первичный ответ может занять 14 дней, чтобы решить и создать ячейки памяти.
Вторичный иммунный ответ наблюдается, когда один и тот же антиген попадает в организм во второй раз (т. е. бустерная доза ). Это может произойти через несколько недель, месяцев или даже лет. После бустерной дозы наблюдается заметно усиленный ответ, характеризующийся ускоренным появлением иммунокомпетентных клеток и антител.
е. бустерная доза ). Это может произойти через несколько недель, месяцев или даже лет. После бустерной дозы наблюдается заметно усиленный ответ, характеризующийся ускоренным появлением иммунокомпетентных клеток и антител.
Он имеет очень короткую и незначительную латентную фазу от 2 до 3 дней и высокие уровни антител (IgG), сохраняющиеся в течение длительного периода. Таким образом, вторичная реакция является быстрой, мощной и с длительной анамнестической реакцией или реакцией на припоминание.
Изображение: «Т-клеточный рецептор в комплексе с MHC I и II». Дэвид Гудселл – Молекула месяца RCSB doi: 10.2210/rcsb_pdb/mom_2005_3. Лицензия: CC BY 3.0
Лимфоидные органы в зависимости от их функций делятся на первичные и вторичные. Первичные лимфоидные органы включают вилочковую железу, фабрициальную сумку, костный мозг и кишечный эпителий, в которых имеется антигеннезависимая пролиферация и дифференцировка лимфоцитов .
Вторичные лимфоидные органы включают лимфатические узлы, селезенку и ассоциированную со слизистой оболочкой лимфоидную ткань, где антигенные стимулы инициируют иммунный ответ в лимфоцитах. Они тактически расположены таким образом, чтобы чужеродные антигены, проникающие через кровоток, периферические ткани и участки слизистой оболочки, умело улавливались.
Структура вторичной лимфоидной ткани такова, что она способствует инициации адаптационных реакций. Это из-за лучшего взаимодействия между дендритные клетки , несущие антиген, В-клетки и Т-клетки .
Однако пути транспорта антигена, транспортировка лимфоцитов и отличительные клеточные популяции решают задачу вторичной специфичной лимфоидной ткани при иммунных ответах на различные чужеродные антигены (в том числе трансплантированные органы).
Изображение: «Вилочковая железа находится над сердцем. На световой микрофотографии тимуса новорожденного отчетливо видны трабекулы и дольки, включая темноокрашенную кору и более светлую окраску мозгового вещества каждой дольки. LM × 100. (Микрофотография предоставлена Регентами Медицинской школы Мичиганского университета © 2012 г.)», Колледжем OpenStax по анатомии лимфатической и иммунной систем, https://legacy.cnx.org/content/m46563/1.4/, Лицензия: CC BY 3.0
LM × 100. (Микрофотография предоставлена Регентами Медицинской школы Мичиганского университета © 2012 г.)», Колледжем OpenStax по анатомии лимфатической и иммунной систем, https://legacy.cnx.org/content/m46563/1.4/, Лицензия: CC BY 3.0
Эта лимфоэпителиальная двудольная структура расположена за верхней частью грудины. Она приобретает характерный лимфоидный вид к 390–260– месяцам беременности и увеличивается в размерах в процессе внутриутробного развития. Он достигает максимальных размеров при рождении, с возрастом постепенно уменьшается в размерах и, наконец, атрофируется.
Он состоит из долек , которые дифференцируются на наружную кору и внутреннюю мозговую оболочку . Незрелые лимфоциты из желточного мешка, печени плода и костного мозга попадают в тимус. В коре тимуса они претерпевают такие изменения, как созревание и достижение удельных характеристик поверхности . Кроме того, они перемещаются в мозговое вещество тимуса, где лимфоциты завершают процесс своего созревания и выходят в кровь .
Кроме того, они перемещаются в мозговое вещество тимуса, где лимфоциты завершают процесс своего созревания и выходят в кровь .
Зрелые Т-клетки далее высевают во вторичные лимфоидные органы. Это основное место пролиферации лимфоцитов и продуцирования Т-лимфоцитов, где лимфоциты приобретают новые поверхностные антигены.
Вилочковая железа придает иммунологическую компетентность лимфоцитам с помощью гормоноподобных гуморальных факторов тимозина, тимопоэтина, и т. д. (которые секретируются эпителием тимуса), так что лимфоциты становятся способными к установлению CMI.
Изображение: «Красная и белая пульпа в селезенке». по ДуФай. Лицензия: Public Domain
Селезенка является крупнейшим лимфососудистым органом; состоит из красной и белой пульпы, разделенных краевой зоной. Белая целлюлоза богат лимфоидной тканью, в то время как красная пульпа богата пазухами и содержит большое количество эритроцитов.
Белая пульпа состоит в основном из Т-лимфоцитов. Внешняя лимфоидная область представляет собой область, зависимую от В-клеток, т.е. зародышевый центр/мантийный слой . Приблизительно 30–40 % клеток селезенки составляют Т-клетки, а 50 % — В-клетки.
Периартериальные лимфоидные скопления в белой пульпе известны как Мальпигиевы тельца или фолликулы . После антигенной стимуляции в белой пульпе образуются зародышевые центры; они состоят из большого количества быстро делящихся клеток. Селезенка — единственный лимфатический орган, специализирующийся на фильтрации крови (в виде дендритных клеток 90–208 и макрофагов 90–209). Это основное место синтеза антител против передающихся через кровь патогенов .
MALT представляет собой потенциально важную совокупность лимфоцитов (как В-, так и Т-лимфоцитов) в виде изолированных клеток или небольших скоплений клеток.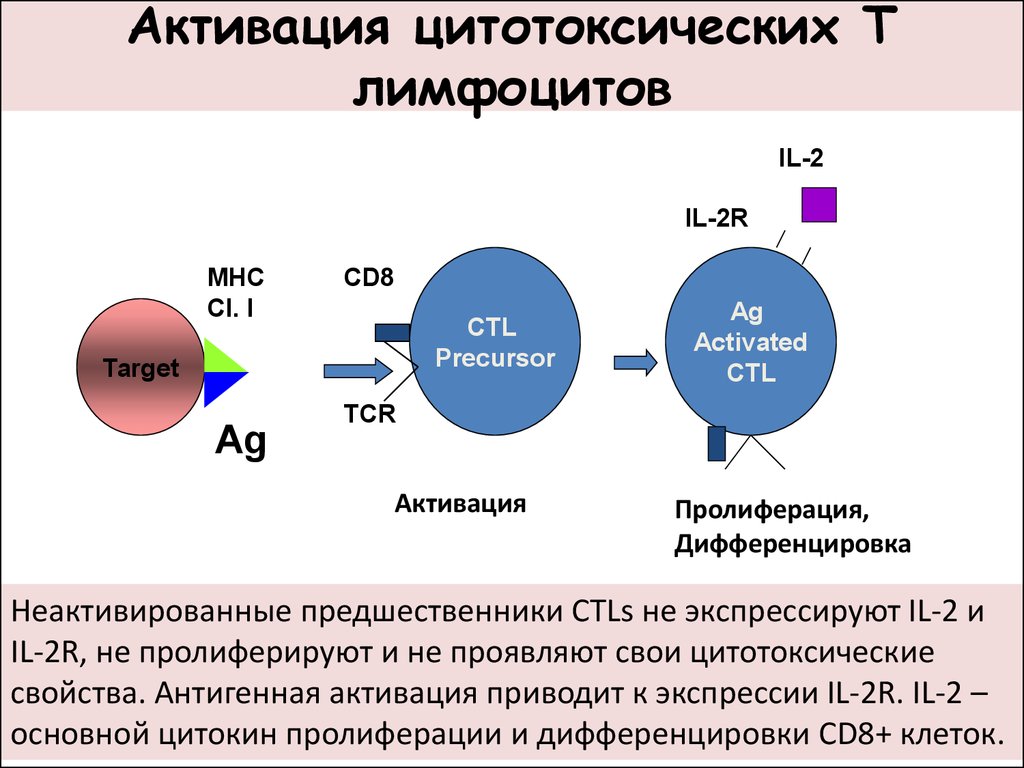 Они в основном продуцируют IgA, присутствующие на слизистой оболочке пищеварительной, дыхательной, мочеполовой и других поверхностей.
Они в основном продуцируют IgA, присутствующие на слизистой оболочке пищеварительной, дыхательной, мочеполовой и других поверхностей.
Такие лимфоидные ткани кишечника называются лимфоидной тканью, ассоциированной с кишечником (GALT) ; те, которые находятся в дыхательных путях, называются бронхоассоциированной лимфоидной тканью (BALT) . Основными структурами GALT у человека являются миндалины, аппендикс, пейеровы бляшки и собственная пластинка кишечника.
MALT содержит смесь В-клеток, Т-клеток, фагоцитирующих клеток, плазматических клеток и АПК . Секреторный IgA является основным Ig, продуцируемым MALT. IgG, IgM и IgE также производятся локально. В основном он обеспечивает иммунитет против патогенов, внедряющихся в местные ткани.
Память В-клетки и плазматические клетки являются строительными блоками иммунологической памяти. Обе эти клетки являются частью гуморальной иммунной системы и в основном продуцируются в герминативных центрах (ГЦ).
Высокоаффинные антитела продуцируются в ГК в результате объединения следующих процессов – клональной экспансии В-клеток, соматической гипермутации и селекции на основе аффинности. Цитокиновый интерлейкиновый фактор (IL-21) недавно был признан ключевым фактором, который может напрямую влиять на судьбу В-клеток, модулируя эти процессы в GCs. Существуют различные типы иммунных клеток, участвующих в В-клеточных реакциях ГХ.
GC возникают через 7–10 дней после предварительного воздействия тимусзависимого антигена. Активированные В-клетки претерпевают интенсивную пролиферацию на протяжении всей первой стадии формирования ГК. Хорошо выраженная темная зона формируется пролиферирующими В-клетками (центробластами) в ГЖ.
Со временем центробластов созревают в центроцитов , которые мигрируют в область, содержащую фолликулярных дендритных клеток, , т.е. в светлую зону ГК. В светлой зоне присутствуют комплексы Ag-Ab, и таким образом центроциты вступают в контакт с Ag.
Изображение: «Путь активации Т-лимфоцитов запускается, когда Т-клетка встречает родственный антиген, связанный с молекулой MHC, на поверхности инфицированной клетки или фагоцита». Производная работа Hazmat2. Лицензия: Public Domain
Ig, присутствующие на поверхности В-клеток, ведут себя как специфические рецепторы антигенов . Когда антиген попадает в наш организм, он реагирует с В-клетками соответствующей специфичности. Это взаимодействие стимулирует В-клетки к трансформация бластоидов , превращение их в плазмобласты ( образование клона ) и, наконец, в плазматические клетки .
Каждая В-клетка обладает генетическими инструкциями для производства антитела с уникальной антигенной специфичностью в виде мембранного рецептора . После получения сигнала В-клетки дифференцируются в плазматических клеток , которые продуцируют и секретируют антитела.
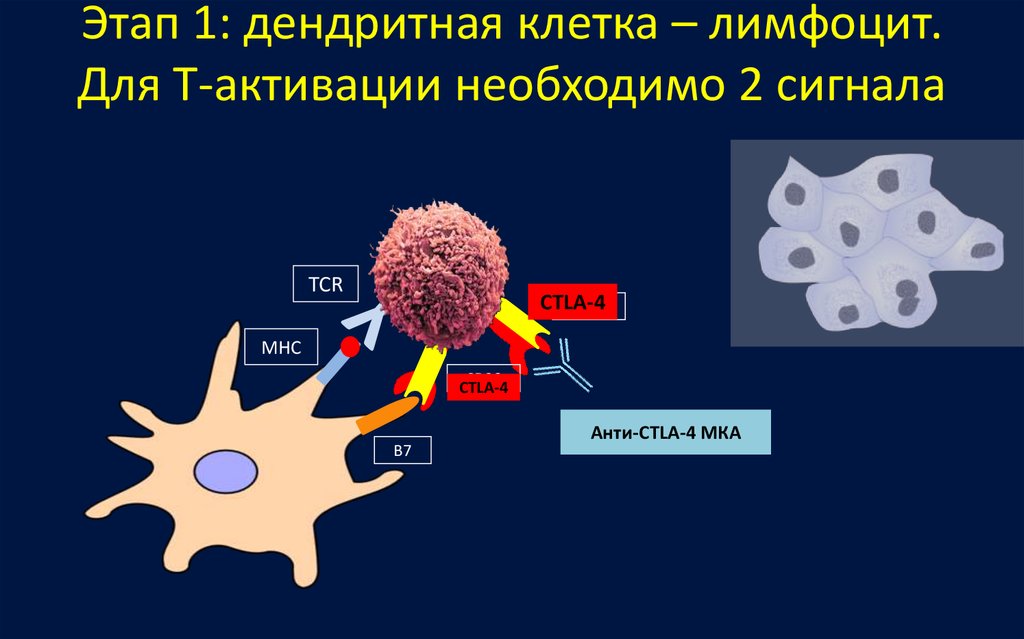
Антиген, присутствующий в более чем молекулах МНС , приводит к Активация Т-лимфоцитов. Роль различных костимулирующих молекул заключается в обеспечении пролиферации и дифференцировки Т-лимфоцитов . APC помогают костимулирующим молекулам в этой задаче. Только белковые антигены, нагруженные на молекулы MHC, распознаются Т-клетками.
Реакции контактной чувствительности — это реакции, при которых происходит индукция Т-лимфоцитов химическими веществами, попадающими в наш организм через кожу. После сенсибилизация антигеном , эффективный иммунный ответ продуцируется дифференцированными эффекторными Т-клетками.
костимулирующие молекулы образуются из наивных Т-клеток путем их пролиферации и дифференцировки в эффекторные клетки . БТРы помогают им в этом переходе. Костимуляция жизненно важна для эффективного иммунного ответа, представленного Т-лимфоцитами, сенсибилизированными антигеном.
Изображение: «Тимоциты попадают в тимус и проходят ряд стадий развития, которые обеспечивают как функцию, так и толерантность, прежде чем они покинут и станут функциональными компонентами адаптивного иммунного ответа». Хизер Кетчум, Эрик Брайт на cnx.org (бесплатно скачать на http://cnx.org/contents/a7fa09d4-b7d6-4ae8-a6fa-71037b392af9@1.), Лицензия: CC BY 4.0
Хорошо известны костимулирующие молекулы B7-1(CD80) и B7-2(CD86) . Существует экспрессия костимулирующих молекул на активированных АПК. Их лиганды, известные как CD28 , присутствуют на поверхности Т-клеток.
Активированные Т-клетки также экспрессируют лиганды CD40, которые связываются с CD40 на АПК. Каскад следует во время активации Т-клеток. Связывание CD40L и CD40 приводит к экспрессии костимулирующих молекул (B7-1 и B7-2), которые далее связываются с TCR (CD28). Кроме того, цитокины (IL-12), секретируемые АПК стимулируют пролиферацию и дифференцировку Т-лимфоцитов .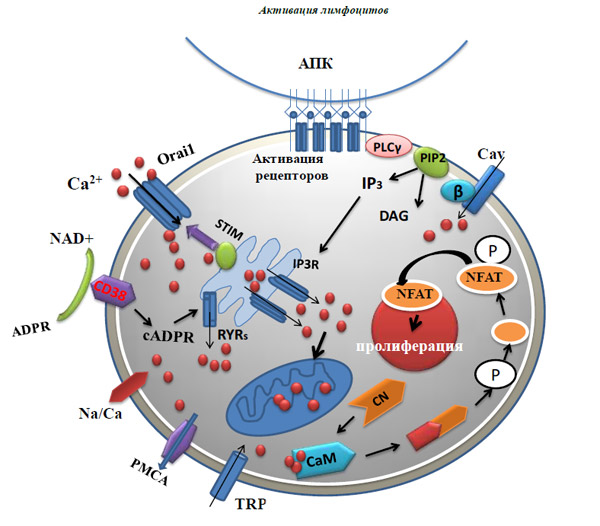
Активация митоген-активируемого белка (MAP) необходима для активации Т-клеток, вызванной CD28. Экспрессия антиапоптотических Bcl-x и Bcl-2 стимулируется киназой MAP , которая вызывает пролонгированное выживание клеток. CTLA-4 (цитотоксический антиген Т-лимфоцитов-4) и PD1 (запрограммированная смерть 1) являются ингибиторами CD28, вызывающими модуляцию активации Т-лимфоцитов. Доступ к костимулирующим молекулам полностью подавляется при активации CTLA-4, поскольку он имеет высокое сродство к этим молекулам.
В-лимфоциты , вновь образованные в костном мозге, мигрируют на периферию для стимуляции или исключения из иммунной системы. При активации В-клетки будут пролиферировать в клоны клеток, некоторые из которых образуют эффекторных клеток, секретирующих Ig с более высокой скоростью, в то время как другие образуют клетки долговременной памяти.
Таким образом, часть иммунной системы представляет собой односторонний путь дифференцировки , конечной точкой которого является плазматическая клетка.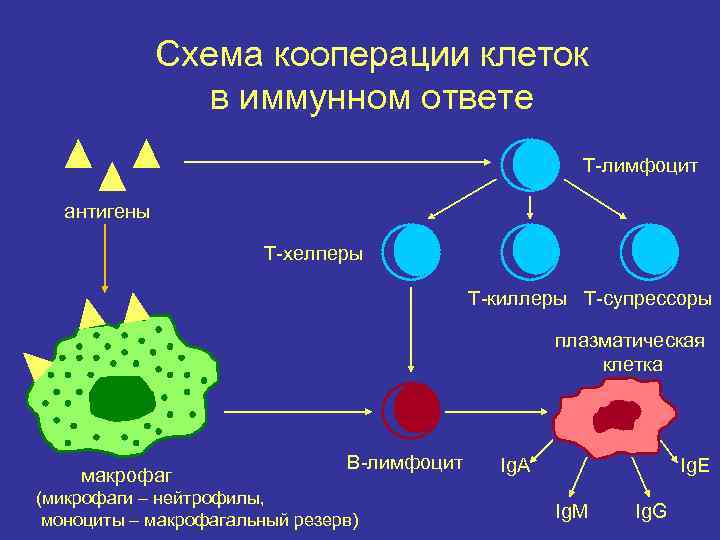 Это уникально в том смысле, что клональная специфичность, относящаяся к данному антигенному эпитопу, регулирует амплификацию данного клона В-клеток. Это основа Теория клональной селекции , предложенная Jerne в 1955 г. и Burnet в 1957 г.
Это уникально в том смысле, что клональная специфичность, относящаяся к данному антигенному эпитопу, регулирует амплификацию данного клона В-клеток. Это основа Теория клональной селекции , предложенная Jerne в 1955 г. и Burnet в 1957 г.
Согласно этой теории, молекулы Ig присутствуют на поверхности В-клеток и работают как специфические рецепторы для специфических антигенов. Когда Ag вводится, он соединяется с той молекулой Ig на поверхности, которая подходит для него. Это взаимодействие приводит к пролиферации этого лимфоцита с образованием клона клеток, продуцирующих антитело той же специфичности, что и на поверхности родительского лимфоцита. Некоторые из дочерних клеток преобразуются в ячеек памяти . Следовательно, АГ выбирает специфическую В-клетку и стимулирует ее пролиферацию в клон клеток, продуцирующих специфическое антитело.
Изображение: «Функция клеток TFH: подмножество наивных Т-клеток в зоне Т-клеток активируется антигеном.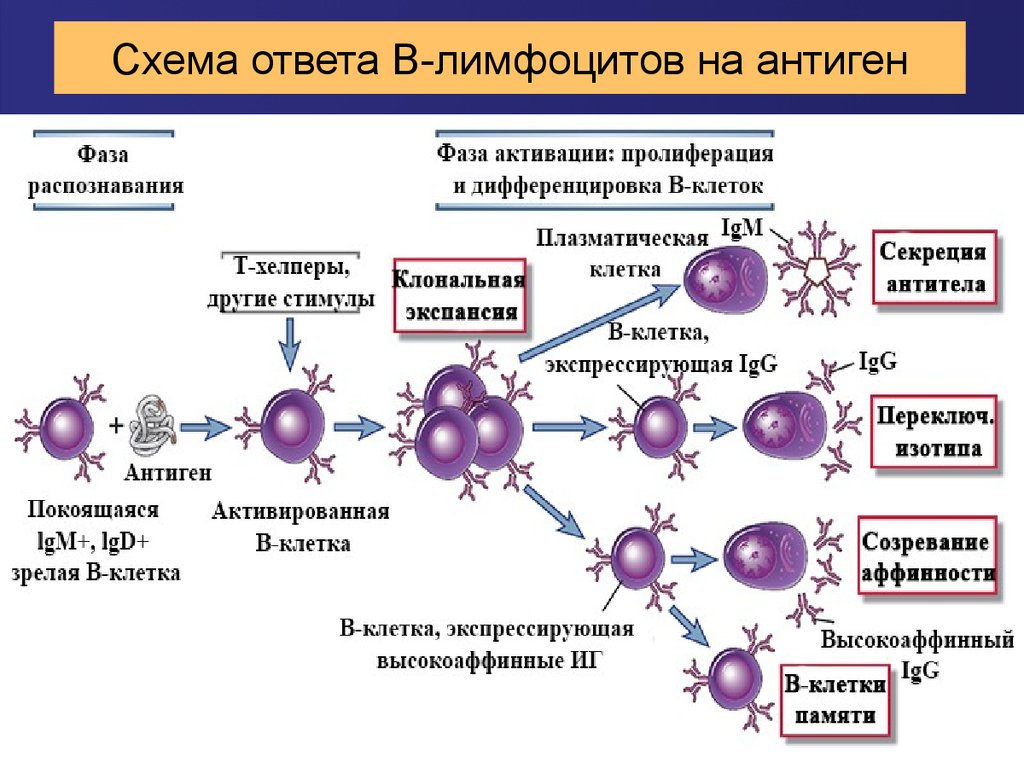 Они мигрируют в фолликулы, где дифференцируются в клетки TFH, которые взаимодействуют с фолликулярными клетками B (Fo B) и инструктируют их. Таким образом, они подвергаются переключению изотипа, соматической гипермутации и быстрому клеточному делению в семенные зародышевые центры (GC). В этих зародышевых центрах клетки TFH продолжают оказывать помощь В-клеткам GC, чтобы облегчить их производство высокоаффинных антителопродуцирующих плазматических клеток (ПК) и В-клеток долгоживущей памяти (Mem)». по науке мальчик83. Лицензия: CC BY-SA 3.0
Они мигрируют в фолликулы, где дифференцируются в клетки TFH, которые взаимодействуют с фолликулярными клетками B (Fo B) и инструктируют их. Таким образом, они подвергаются переключению изотипа, соматической гипермутации и быстрому клеточному делению в семенные зародышевые центры (GC). В этих зародышевых центрах клетки TFH продолжают оказывать помощь В-клеткам GC, чтобы облегчить их производство высокоаффинных антителопродуцирующих плазматических клеток (ПК) и В-клеток долгоживущей памяти (Mem)». по науке мальчик83. Лицензия: CC BY-SA 3.0
Зародышевые центры (GC) – это места, где происходят важные этапы дифференцировки В-клеток. Эти этапы включают в себя созревание аффинности , переключение классов , плазменные В-клетки и формирование клеток памяти . GC важны для первых двух из этих шагов, а остальные происходят вне GC.
E2A , EBF, и Pax5 представляют собой факторы транскрипции , влияющие на дифференцировку В-клеток из плеврипотентные гемопоэтические клетки .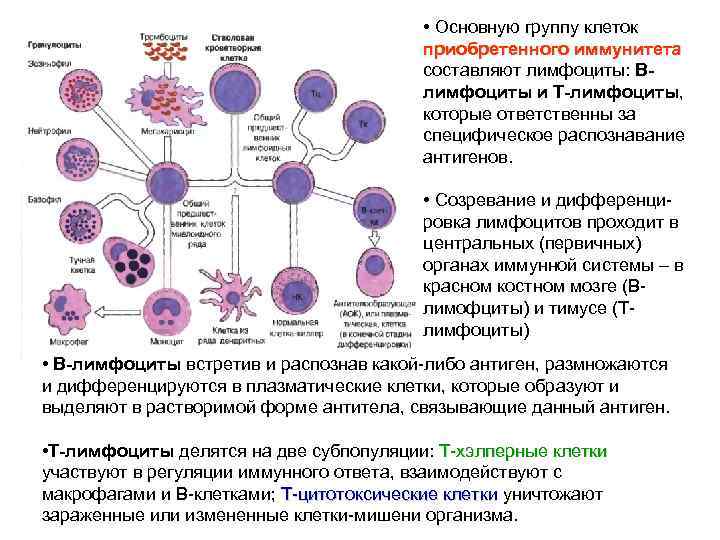 Они помогают в развитии В-клеток, транскрибируя определенные гены и вызывая их рекомбинацию. В-клетки развиваются в следующем порядке: плеврипотентных гемопоэтических стволовых клеток к Pro B-клеткам, к фолликулярным B-клеткам, к маргинальным B-клеткам, к B1 B-клеткам.
Они помогают в развитии В-клеток, транскрибируя определенные гены и вызывая их рекомбинацию. В-клетки развиваются в следующем порядке: плеврипотентных гемопоэтических стволовых клеток к Pro B-клеткам, к фолликулярным B-клеткам, к маргинальным B-клеткам, к B1 B-клеткам.
После отбора В-клеток происходит дифференцировка в плазматические клетки и клетки памяти. Обычно в плазматических клетках отсутствует определяемый мембраносвязанный иммуноглобулин. Из-за отсутствия мембраносвязанных Ig в плазматических клетках происходит синтез секретируемых антител.
Плазматические клетки, продуцирующие Ig, синтезируют иммуноглобулины с очень высокой скоростью, около 1000 молекул Ig на клетку в секунду. Плазматические клетки образованы из зрелых В-клеток из-за изменения процессинга РНК. Ячейки памяти образованы из В-клеток, не отобранных в светлую зону ГК. В результате переключения класса наивные В-клетки коэкспрессируют только IgM и IgD, в то время как все Ig экспрессируются клетками памяти.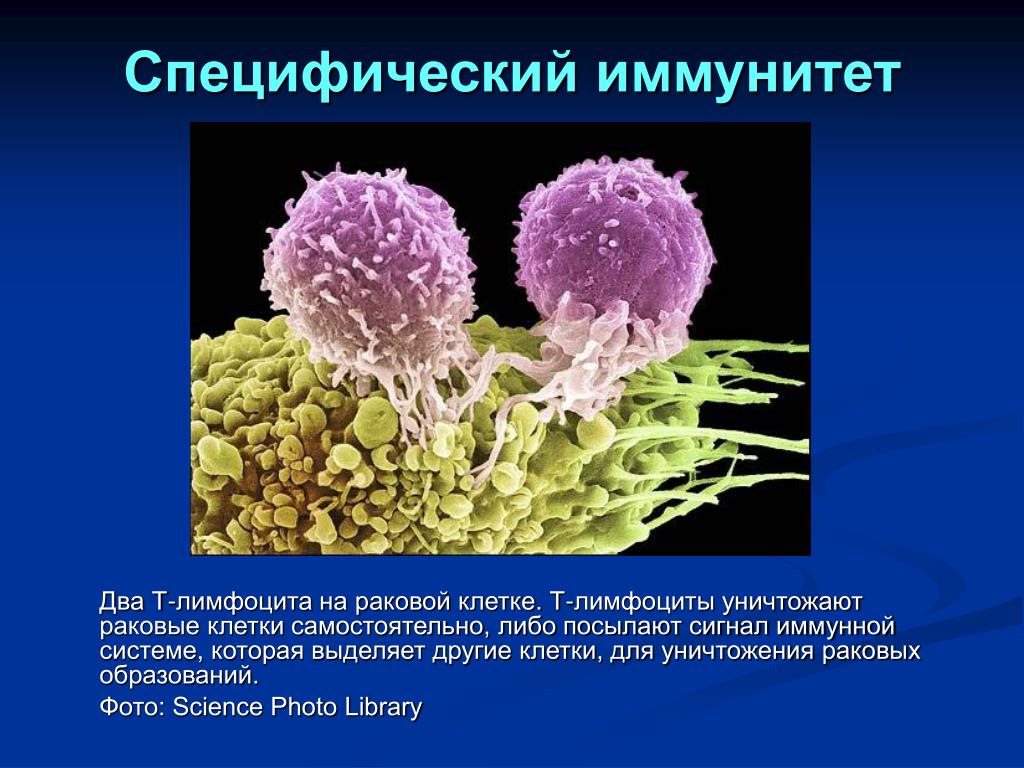 Разные Ig имеют разные характеристики. Например, IgG усиливает фагоцитоз, а IgA препятствует всасыванию Ag. IgM — первое антитело, вырабатываемое в результате первичного иммунного ответа.
Разные Ig имеют разные характеристики. Например, IgG усиливает фагоцитоз, а IgA препятствует всасыванию Ag. IgM — первое антитело, вырабатываемое в результате первичного иммунного ответа.
Дендритные клетки (ДК) представляют собой тип АПК. Они способны первичных ответов Т-лимфоцитов . Они должны пройти весь путь до вторичных лимфоидных органов для презентации чужеродных АГ наивным Т-клеткам.
Эта миграция контроллеров домена представляет собой многоэтапный процесс, который строго регулируется. Хемокины играют важную роль в этом процессе. Родственные хемокиновые рецепторы экспрессируются после их продукции.
TLR (Toll-подобный рецептор) представляет собой хемокин, экспрессируемый на эффекторных клетках и стимулирующий миграцию DC. В процессе миграции экспрессируются специфические молекулы селектина на клапанах с высоким эндотелием, и стимулированные лимфатические узлы также претерпевают физические изменения. Всякий раз, когда ДК активируются, реакция хемокинов уменьшается, что способствует их миграции к дренирующим лимфатическим узлам.
Всякий раз, когда ДК активируются, реакция хемокинов уменьшается, что способствует их миграции к дренирующим лимфатическим узлам.
DC способны не только перерабатывать Ag, но и приобретать Ag. Они косвенно приводят к первичной активации Т-лимфоцитов за счет экспрессии костимулирующих молекул. ДК могут передавать определенную информацию Т-клеткам. В зависимости от переданной информации результатом может быть формирование эффекторов Th2, Th3, Th27 и клеток памяти .
Общие лимфоидные клетки-предшественники образуются из плеврипотентных гемопоэтических клеток . Транскрипционные факторы играют важную роль в формировании NKC или Pro-T-клеток из общих лимфоидных клеток-предшественников.
Существует рецептор выреза , который активируется лимфоидными клетками-предшественниками. При дроблении рецептор вырезки перемещается в ядро. Это приводит к активации GATA 3 , который представляет собой фактор транскрипции, генерирующий про-Т-клетки.