2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
В последние годы в мире неуклонно растет интерес к диссекции артерий, кровоснабжающих головной мозг, – относительно новой и недостаточно изученной проблеме цереброваскулярных заболеваний. Ее основное клиническое проявление – ишемический инсульт (ИИ), чаще развивающийся в молодом возрасте. Изучение и прижизненная диагностика диссекции церебральных артерий стала возможной благодаря широкому внедрению в клинику магнитно-резонансной томографии (МРТ). МРТ позволяет безопасно для больного проводить повторное ангиографическое исследование, что важно для диагностики диссекции, поскольку она представляет собой динамическую патологию, а также с помощью режима Т1 с подавлением сигнала от жировой ткани (Т1 f-s) визуализировать непосредственно интрамуральную (внутристеночную) гематому (ИМГ) – прямой признак диссекции. Применение МРТ показало, что диссекция является весьма распространенной патологией, а не редкостью, как считалось ранее.
Кроме того, стало очевидным, что диссекция церебральных артерий лишь в небольшом числе случаев приводит к летальному исходу, тогда как первоначально она рассматривалась как фатальное заболевание.
В России целенаправленное изучение диссекции церебральных артерий начали проводить с конца 90-х годов прошлого столетия в Научном центре неврологии РАМН (до 2007 г. – Научно-исследовательский институт неврологии РАМН) практически одновременно с исследованиями, выполняемыми за рубежом. Но первые морфологические описания отдельных случаев церебральной диссекции, клинически, однако, нераспознанной, были сделаны в 80-е годы XX в. в нашей стране Д. Е. Мацко, А. А. Никоновым и Л. В. Шишкиной и соавт. В настоящее время исследование данной проблемы ведут в Научном центре неврологии РАМН, где обследовано более 200 больных с прижизненно верифицированной диссекцией церебральных артерий, из которых более половины – больные с диссекцией внутренней сонной (ВСА) и позвоночной (ПА) артерий.
Диссекция церебральных артерий представляет собой проникновение крови из просвета артерии в ее стенку через разрыв интимы.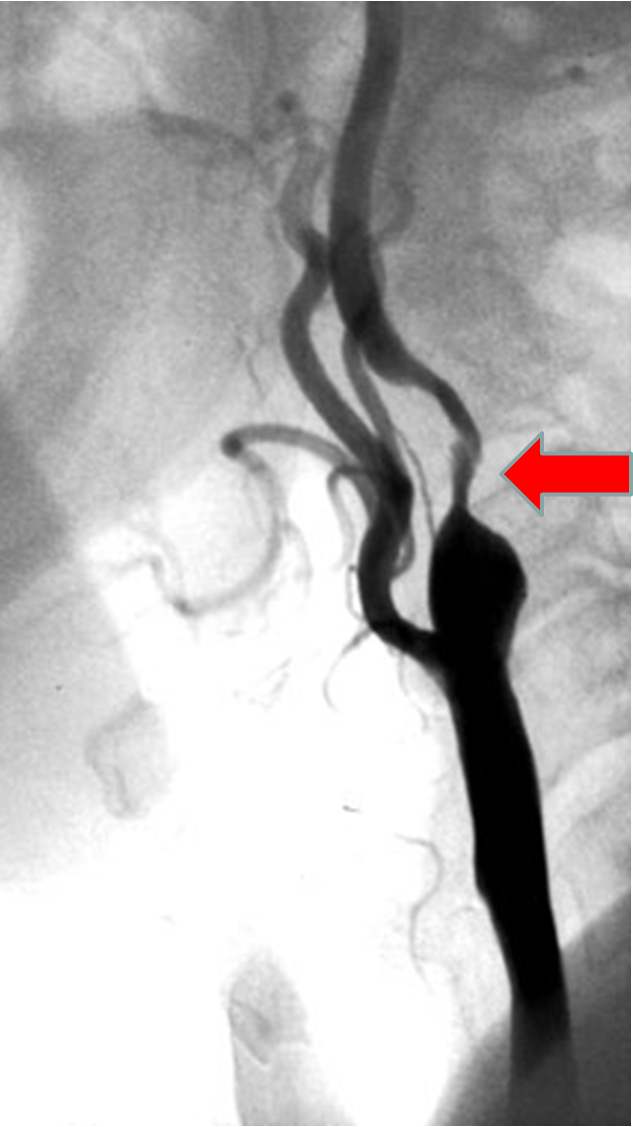 Формирующаяся при этом ИМГ, разделяя слои артериальной стенки, распространяется по длине артерии на различное расстояние, чаще всего в сторону интимы, приводя к сужению или даже окклюзии просвета артерии, что служит причиной ишемии головного мозга. Стеноз незначительной степени, обусловленный ИМГ, клинически может протекать бессимптомно. Распространение ИМГ в сторону наружной оболочки (адвентиции) приводит к развитию псевдоаневризмы, которая может стать причиной изолированной шейно-головной боли, или к истинной расслаивающей аневризме. Тромбы, образующиеся в расслаивающей аневризме, являются источником артерио-артериальной эмболии и ИИ. Диссекция развивается как в магистральных артериях головы (ВСА и ПА), так и в их ветвях (средняя, задняя, передняя мозговые артерии, основная артерия). При этом большинство исследователей полагают, что диссекция чаще возникает в ВСА и ПА, чем в их ветвях. Вместе с тем нельзя исключить, что диссекция в ветвях ВСА и ПА часто недоучитывается из-за трудности визуализации в них ИМГ и ошибочно расценивается как тромбоз.
Формирующаяся при этом ИМГ, разделяя слои артериальной стенки, распространяется по длине артерии на различное расстояние, чаще всего в сторону интимы, приводя к сужению или даже окклюзии просвета артерии, что служит причиной ишемии головного мозга. Стеноз незначительной степени, обусловленный ИМГ, клинически может протекать бессимптомно. Распространение ИМГ в сторону наружной оболочки (адвентиции) приводит к развитию псевдоаневризмы, которая может стать причиной изолированной шейно-головной боли, или к истинной расслаивающей аневризме. Тромбы, образующиеся в расслаивающей аневризме, являются источником артерио-артериальной эмболии и ИИ. Диссекция развивается как в магистральных артериях головы (ВСА и ПА), так и в их ветвях (средняя, задняя, передняя мозговые артерии, основная артерия). При этом большинство исследователей полагают, что диссекция чаще возникает в ВСА и ПА, чем в их ветвях. Вместе с тем нельзя исключить, что диссекция в ветвях ВСА и ПА часто недоучитывается из-за трудности визуализации в них ИМГ и ошибочно расценивается как тромбоз.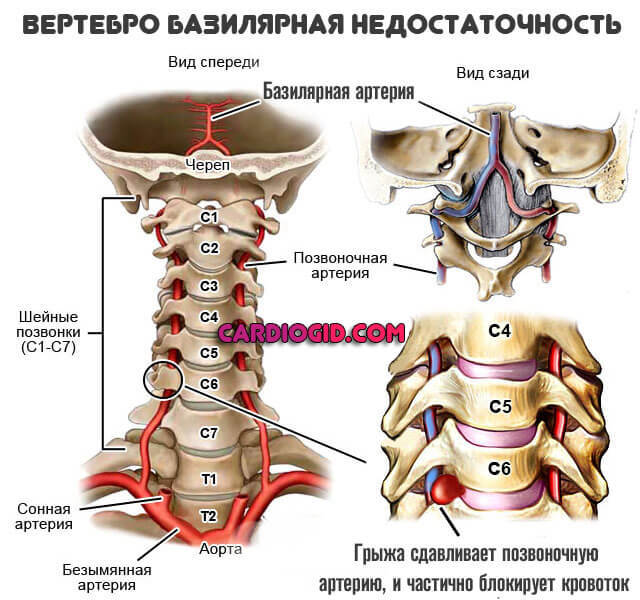 Диссекция может развиваться в любом возрасте – от младенческого до пожилого, однако в большинстве случаев (по данным НЦ Неврологии РАМН – 75%) она наблюдается у лиц молодого возраста (до 45 лет). Отмечено, что при интракраниальном поражении возраст больных, как правило, меньше, чем при экстракраниальном, а при вовлечении ПА – меньше, чем при поражении сонных артерий. Распределение больных по полу также зависит от локализации диссекции: ВСА чаще поражается у мужчин, а ПА – у женщин. Диссекция обычно развивается у лиц, считающих себя здоровыми, не страдающих атеросклерозом, тромбофилией, сахарным диабетом и редко имеющих умеренную артериальную гипертонию.
Диссекция может развиваться в любом возрасте – от младенческого до пожилого, однако в большинстве случаев (по данным НЦ Неврологии РАМН – 75%) она наблюдается у лиц молодого возраста (до 45 лет). Отмечено, что при интракраниальном поражении возраст больных, как правило, меньше, чем при экстракраниальном, а при вовлечении ПА – меньше, чем при поражении сонных артерий. Распределение больных по полу также зависит от локализации диссекции: ВСА чаще поражается у мужчин, а ПА – у женщин. Диссекция обычно развивается у лиц, считающих себя здоровыми, не страдающих атеросклерозом, тромбофилией, сахарным диабетом и редко имеющих умеренную артериальную гипертонию.
Диссекция внутренней сонной артерии.
Основными провоцирующими факторами диссекции ВСА являются травма головы или шеи, как правило, легкая; физическая нагрузка с напряжением мышц плечевого пояса и шеи; наклоны, запрокидывание, повороты головы; прием алкоголя; текущая или предшествующая инфекция; прием контрацептивов или послеродовый период у женщин. В условиях предшествующей слабости артериальной стенки указанные факторы и состояния играют провоцирующую, а не каузальную роль, приводя к разрыву интимы и развитию диссекции, которая в этих случаях рассматривается как спонтанная.
В условиях предшествующей слабости артериальной стенки указанные факторы и состояния играют провоцирующую, а не каузальную роль, приводя к разрыву интимы и развитию диссекции, которая в этих случаях рассматривается как спонтанная.
Клинически диссекция ВСА чаще всего проявляется ИИ, реже – преходящим нарушением мозгового кровообращения (НМК). К более редким (менее 5%) ее проявлениям относятся изолированная шейная/головная боль, локализующаяся в большинстве случаев на стороне диссекции; изолированное одностороннее поражение черепных нервов вследствие их ишемии, когда питающие нерв артерии отходят от расслоенной ВСА; изолированный синдром Горнера, обусловленный воздействием ИМГ на периартериальное симпатическое сплетение, когда гематома в основном распространяется в сторону адвентиции и существенно не сужает просвет ВСА. Небольшие ИМГ могут протекать бессимптомно и случайно выявляются при МРТ. Характерный признак НМК при диссекции ВСА – головная/шейная боль. Боль, обычно тупая, давящая, реже пульсирующая, стреляющая, появляется за несколько часов или дней до ИИ на стороне диссекции. Ее причиной служит раздражение чувствительных рецепторов сосудистой стенки развивающейся в ней гематомой. Примерно у трети больных ИИ предшествует преходящее НМК в церебральном бассейне ВСА или глазничной артерии в виде кратковременного снижения зрения на стороне диссекции. НМК, как правило, развивается в бассейне средней мозговой артерии (СМА) и проявляется двигательными, чувствительными и афатическими нарушениями, которые в половине случаев выявляются утром при пробуждении, в другой половине случаев – во время активного бодрствования.
Ее причиной служит раздражение чувствительных рецепторов сосудистой стенки развивающейся в ней гематомой. Примерно у трети больных ИИ предшествует преходящее НМК в церебральном бассейне ВСА или глазничной артерии в виде кратковременного снижения зрения на стороне диссекции. НМК, как правило, развивается в бассейне средней мозговой артерии (СМА) и проявляется двигательными, чувствительными и афатическими нарушениями, которые в половине случаев выявляются утром при пробуждении, в другой половине случаев – во время активного бодрствования.
Прогноз для жизни в большинстве случаев благоприятный, летальный исход наблюдается примерно в 5% случаев. Обычно он наступает при обширных инфарктах мозга, обусловленных диссекцией интракраниального отдела ВСА с переходом на СМА и переднюю мозговую артерию. У большинства же больных, особенно при поражении экстракраниального отдела ВСА, прогноз для жизни благоприятный и наблюдается хорошее восстановление нарушенных функций. При вовлечении интракраниального отдела ВСА и распространении диссекции на СМА либо при эмболии последней восстановление нарушенных функций значительно хуже.
Рецидивы диссекции возникают нечасто и обычно отмечаются в 1-й месяц после дебюта заболевания. Они могут появляться как в интактной, так и в уже подвергавшейся диссекции артерии.
Основной механизм развития ИИ – гемодинамический в условиях нарастающего стенозирующе-окклюзирующего процесса в ВСА, обусловленного ИМГ. Реже НМК развивается по механизму артериоартериальной эмболии. Ее источником служат тромбы, образующиеся в расслаивающей аневризме, тромбированные фрагменты ИМГ, попадающие в кровоток при вторичном прорыве интимы, или тромботические наслоения в месте разрыва интимы.
Диссекция позвоночной артерии.
Диссекция ПА, по данным большинства авторов, наблюдается несколько реже, чем диссекция ВСА. Однако нельзя исключить, что ПА вовлекается чаще, чем указано в литературе, так как многие случаи диссекции ПА, проявляющейся изолированной цервикоцефалгией, клинически не распознаются и статистически не учитываются.
Основные клинические признаки диссекции ПА – ишемические НМК и изолированная шейная/головная боль. Такая боль возникает примерно в трети случаев. К редким проявлениям относятся нарушения кровообращения в шейном отделе спинного мозга, изолированная радикулопатия, нарушение слуха. Более чем у трети больных диссекция обнаруживается в обеих ПА, причем диссекция одной ПА может быть причиной НМК, а второй ПА – причиной изолированной шейной/головной боли, либо клинически протекать бессимптомно и выявляется только при нейровизуализации. Характерной особенностью НМК при диссекции ПА, как и при диссекции ВСА, является ее ассоциация с шейной/головной болью на стороне расслоенной ПА. Обычно боль локализуется по задней поверхности шеи и в затылке, появляясь за несколько дней или 2–3 недель до очаговых неврологических симптомов. Боль часто возникает после повторных наклонов, поворотов головы, длительного нахождения головы в неудобном положении, реже – после травмы головы/шеи, как правило, легкой. Наблюдаемое при этом натяжение ПА при слабости сосудистой стенки вызывает разрыв интимы и инициирует диссекцию.
Такая боль возникает примерно в трети случаев. К редким проявлениям относятся нарушения кровообращения в шейном отделе спинного мозга, изолированная радикулопатия, нарушение слуха. Более чем у трети больных диссекция обнаруживается в обеих ПА, причем диссекция одной ПА может быть причиной НМК, а второй ПА – причиной изолированной шейной/головной боли, либо клинически протекать бессимптомно и выявляется только при нейровизуализации. Характерной особенностью НМК при диссекции ПА, как и при диссекции ВСА, является ее ассоциация с шейной/головной болью на стороне расслоенной ПА. Обычно боль локализуется по задней поверхности шеи и в затылке, появляясь за несколько дней или 2–3 недель до очаговых неврологических симптомов. Боль часто возникает после повторных наклонов, поворотов головы, длительного нахождения головы в неудобном положении, реже – после травмы головы/шеи, как правило, легкой. Наблюдаемое при этом натяжение ПА при слабости сосудистой стенки вызывает разрыв интимы и инициирует диссекцию. Причинами шейной/головной боли при диссекции ПА служат раздражение болевых рецепторов артериальной стенки формирующейся в ней гематомой, а также ишемия мышц шеи, в кровоснабжении которых участвуют ветви ПА. Еще одна особенность НМК состоит в том, что часто (около 80%) она развивается в момент поворота или наклона головы. Очаговые неврологические симптомы – атаксия, вестибулярные нарушения, реже – расстройство чувствительности, дизартрия, дисфагия, дисфония, парезы.
Причинами шейной/головной боли при диссекции ПА служат раздражение болевых рецепторов артериальной стенки формирующейся в ней гематомой, а также ишемия мышц шеи, в кровоснабжении которых участвуют ветви ПА. Еще одна особенность НМК состоит в том, что часто (около 80%) она развивается в момент поворота или наклона головы. Очаговые неврологические симптомы – атаксия, вестибулярные нарушения, реже – расстройство чувствительности, дизартрия, дисфагия, дисфония, парезы.
Наиболее частым механизмом развития НМК при диссекции ПА является артерио-артериальная эмболия. На это указывают клинические проявления (острое развитие симптомов ишемии головного мозга, обычно во время активного бодрствования, часто при повороте/наклоне головы) и результаты ангиографии (наличие у большинства больных гемодинамически незначимых стенозов, которые существенно не нарушают церебральную гемодинамику и обеспечивают дистальное продвижение эмболов). Источником эмболии многие исследователи считают фрагменты ИМГ, попадающие в кровоток при вторичном прорыве интимы.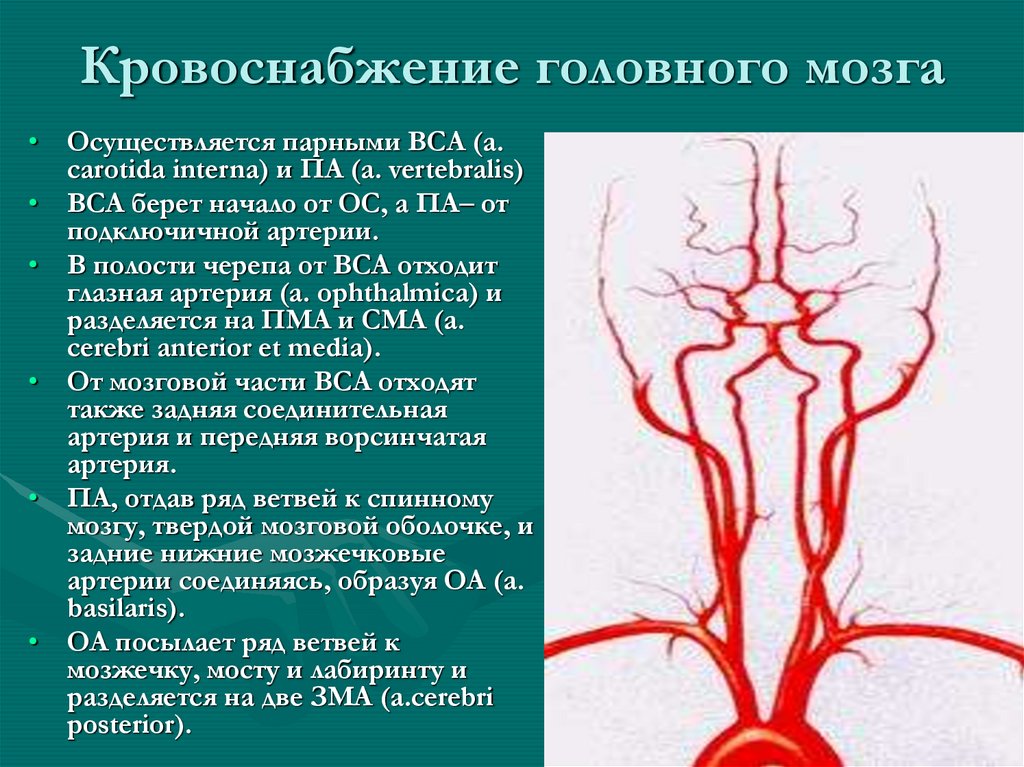 По мнению других исследователей, это внутрисосудистые пристеночные тромбы, сформировавшиеся в месте разрыва интимы. Решающее значение в верификации диссекции ВСА и ПА имеет нейровизуализационное исследование, в первую очередь МРТ в режиме ангиографии (МРА) и МРТ в режиме Т1 f-s, позволяющие выявить ИМГ. Наиболее частым характерным ангиографическим признаком диссекции ВСА/ПА является неравномерный, реже – равномерный пролонгированный стеноз («симптом четок», или «нитки бус», «симптом струны»), предокклюзионное конусообразное сужение просвета ВСА («симптом пламени свечи»). Такие характерные ангиографические признаки диссекции, как расслаивающая аневризма и двойной просвет, встречаются значительно реже. Диссекция представляет собой динамическую патологию: стенозы ВСА/ПА, обусловленные ИМГ, во всех случаях полностью или частично разрешаются через 2–3 месяца. Реканализация исходной окклюзии, вызванной диссекцией, наблюдается только в половине случаев. Характерными МРТ-признаками диссекции служат ИМГ, которая визуализируется в режиме Т1 f-s на протяжении ≥2 месяцев, и увеличение наружного диаметра артерии.
По мнению других исследователей, это внутрисосудистые пристеночные тромбы, сформировавшиеся в месте разрыва интимы. Решающее значение в верификации диссекции ВСА и ПА имеет нейровизуализационное исследование, в первую очередь МРТ в режиме ангиографии (МРА) и МРТ в режиме Т1 f-s, позволяющие выявить ИМГ. Наиболее частым характерным ангиографическим признаком диссекции ВСА/ПА является неравномерный, реже – равномерный пролонгированный стеноз («симптом четок», или «нитки бус», «симптом струны»), предокклюзионное конусообразное сужение просвета ВСА («симптом пламени свечи»). Такие характерные ангиографические признаки диссекции, как расслаивающая аневризма и двойной просвет, встречаются значительно реже. Диссекция представляет собой динамическую патологию: стенозы ВСА/ПА, обусловленные ИМГ, во всех случаях полностью или частично разрешаются через 2–3 месяца. Реканализация исходной окклюзии, вызванной диссекцией, наблюдается только в половине случаев. Характерными МРТ-признаками диссекции служат ИМГ, которая визуализируется в режиме Т1 f-s на протяжении ≥2 месяцев, и увеличение наружного диаметра артерии.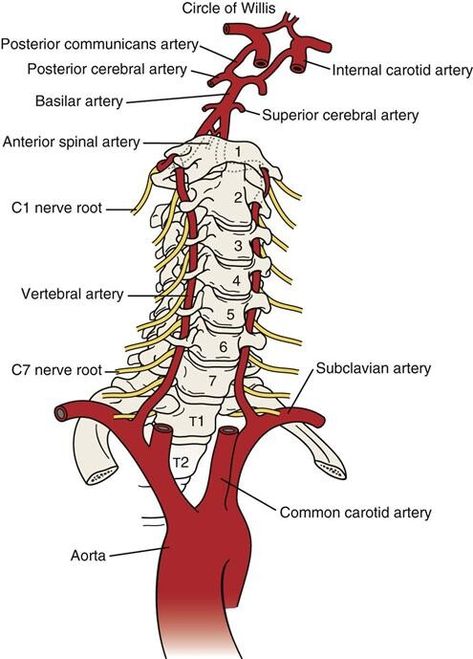 Следует иметь в виду, что в течение 1-й недели заболевания ИМГ при МРТ в режиме Т1 f-s не выявляется, поэтому диагностическое значение приобретают компьютерная томография (КТ) и МРТ в режиме Т2 f-s.
Следует иметь в виду, что в течение 1-й недели заболевания ИМГ при МРТ в режиме Т1 f-s не выявляется, поэтому диагностическое значение приобретают компьютерная томография (КТ) и МРТ в режиме Т2 f-s.
В большинстве случаев с течением времени происходит хорошее или полное восстановление нарушенных функций. Диссекция ПА может рецидивировать. Через 4–15 месяцев рецидив отмечен у 10% пациентов.
Морфологическое исследование артерий мозга при диссекции играет основополагающую роль в выяснении причин слабости артериальной стенки, приводящей к диссекции. Оно позволяет выявить расслоение, истончение, а иногда и отсутствие внутренней эластической мембраны, участки фиброза в интиме, неправильную ориентировку миоцитов в медии. Предполагается, что изменение сосудистой стенки обусловлено генетически детерминированной слабостью соединительной ткани, в первую очередь патологией коллагена. Однако мутации в гене коллагена не обнаружены. Впервые в мире сотрудниками НЦ неврологии РАМН высказано предположение, что причиной слабости артериальной стенки является митохондриальная цитопатия. Это подтвердило исследование биоптатов мышц и кожи. При гистологическом и гистохимическом исследовании мышц обнаружены красные рваные волокна, изменение реакции на сукцинатдегидрогеназу и цитохромоксидазу, субсарколеммальный тип окрашивания в волокнах с сохранной реакцией. Электронно-микроскопическое исследование артерий кожи выявило изменения митохондрий, вакуолизацию, отложение жира, липофусцина и гликогена в клетках с измененными митохондриями, отложения кальция в экстраклеточном матриксе. Комплекс выявленных изменений, характерных для митохондриальной цитопатии, позволил российским исследователям предложить термин «митохондриальная артериопатия» для обозначения патологии артерий, предрасполагающей к диссекции.
Это подтвердило исследование биоптатов мышц и кожи. При гистологическом и гистохимическом исследовании мышц обнаружены красные рваные волокна, изменение реакции на сукцинатдегидрогеназу и цитохромоксидазу, субсарколеммальный тип окрашивания в волокнах с сохранной реакцией. Электронно-микроскопическое исследование артерий кожи выявило изменения митохондрий, вакуолизацию, отложение жира, липофусцина и гликогена в клетках с измененными митохондриями, отложения кальция в экстраклеточном матриксе. Комплекс выявленных изменений, характерных для митохондриальной цитопатии, позволил российским исследователям предложить термин «митохондриальная артериопатия» для обозначения патологии артерий, предрасполагающей к диссекции.
Лечение ИИ, обусловленного диссекцией, окончательно не определено, так как отсутствуют рандомизированные плацебоконтролируемые исследования с включением большого количества больных. В связи с этим нет четко установленных методов лечения в остром периоде инсульта. Чаще всего рекомендуется введение прямых антикоагулянтов с последующим переходом на непрямые антикоагулянты, которые применяют в течение 3–6 месяцев. Цель их назначения – предотвращение артерио-артериальной эмболии и поддержание ИМГ в разжиженном состоянии, что способствует ее разрешению. Следует иметь в виду, что назначение больших доз антикоагулянтов может привести к нарастанию ИМГ и ухудшению кровоснабжения головного мозга. В качестве альтернативы этим препаратам в остром периоде инсульта рекомендуется применение антиагрегантов, при этом различия в исходах инсульта, по предварительным данным, отсутствуют. С целью оценки безопасности лечения низкомолекулярным гепарином и аспирином в остром периоде диссекции французские исследователи провели измерение объема и протяженности ИМГ в течение 1-й недели лечения. Небольшое увеличение этих параметров наблюдалось у трети больных, однако ни в одном случае не отмечено нарастания степени стеноза или развития повторной диссекции. Применение антикоагулянтов и антиагрегантов ограничивается 2–3 месяцами, в течение которых происходит развитие ИМГ.
Чаще всего рекомендуется введение прямых антикоагулянтов с последующим переходом на непрямые антикоагулянты, которые применяют в течение 3–6 месяцев. Цель их назначения – предотвращение артерио-артериальной эмболии и поддержание ИМГ в разжиженном состоянии, что способствует ее разрешению. Следует иметь в виду, что назначение больших доз антикоагулянтов может привести к нарастанию ИМГ и ухудшению кровоснабжения головного мозга. В качестве альтернативы этим препаратам в остром периоде инсульта рекомендуется применение антиагрегантов, при этом различия в исходах инсульта, по предварительным данным, отсутствуют. С целью оценки безопасности лечения низкомолекулярным гепарином и аспирином в остром периоде диссекции французские исследователи провели измерение объема и протяженности ИМГ в течение 1-й недели лечения. Небольшое увеличение этих параметров наблюдалось у трети больных, однако ни в одном случае не отмечено нарастания степени стеноза или развития повторной диссекции. Применение антикоагулянтов и антиагрегантов ограничивается 2–3 месяцами, в течение которых происходит развитие ИМГ. Дальнейший профилактический прием этих препаратов нецелесообразен, так как причиной ИИ при диссекции является не гиперкоагуляция, а слабость артериальной стенки. Поскольку основная причина, предрасполагающая к развитию диссекции – слабость артериальной стенки, лечебные мероприятия как в остром, так и в отдаленном периоде инсульта должны быть направлены на ее укрепление. Если учесть данные о митохондриальной цитопатии, приводящей к энергетической недостаточности клеток артериальной стенки и ее дисплазии, способствующей возникновению диссекции, можно считать обоснованным применение препаратов с «трофическим» и энерготропным действием. Одним из таких препаратов является актовегин, который используется как в остром, так и в отдаленном периоде инсульта, обусловленного диссекцией. Он представляет собой биологически активное вещество естественного происхождения – депротеинизированный дериват телячьей крови. Основное действие актовегина заключается в активизации клеточного метаболизма за счет облегчения поступления кислорода и глюкозы в клетку, что обеспечивает дополнительный приток энергетических субстратов и увеличивает в 18 раз продукцию АТФ – универсального донатора энергии, необходимой для жизнедеятельности и функционирования клетки.
Дальнейший профилактический прием этих препаратов нецелесообразен, так как причиной ИИ при диссекции является не гиперкоагуляция, а слабость артериальной стенки. Поскольку основная причина, предрасполагающая к развитию диссекции – слабость артериальной стенки, лечебные мероприятия как в остром, так и в отдаленном периоде инсульта должны быть направлены на ее укрепление. Если учесть данные о митохондриальной цитопатии, приводящей к энергетической недостаточности клеток артериальной стенки и ее дисплазии, способствующей возникновению диссекции, можно считать обоснованным применение препаратов с «трофическим» и энерготропным действием. Одним из таких препаратов является актовегин, который используется как в остром, так и в отдаленном периоде инсульта, обусловленного диссекцией. Он представляет собой биологически активное вещество естественного происхождения – депротеинизированный дериват телячьей крови. Основное действие актовегина заключается в активизации клеточного метаболизма за счет облегчения поступления кислорода и глюкозы в клетку, что обеспечивает дополнительный приток энергетических субстратов и увеличивает в 18 раз продукцию АТФ – универсального донатора энергии, необходимой для жизнедеятельности и функционирования клетки. Используются и другие препараты с нейрометаболическим действием для восстановления нарушенных вследствие инсульта функций: церебролизин, пирацетам, глиатилин, цераксон.
Используются и другие препараты с нейрометаболическим действием для восстановления нарушенных вследствие инсульта функций: церебролизин, пирацетам, глиатилин, цераксон.
В остром периоде диссекции, помимо медикаментозного лечения, большое значение имеет соблюдение следующих правил: необходимо избегать резких движений головой, травм, физического напряжения, натуживания, которые могут привести к нарастанию диссекции.
Диссекция ВСА и ПА является частой причиной ИИ в молодом возрасте, реже – причиной изолированной шейной/головной боли.
Знание клинических и ангиографических особенностей данного вида сосудистой патологии головного мозга позволяет провести правильное ее лечение и вторичную профилактику.
Резюме.В статье приведены два клинических случая диагностики и эффективного лечения диссекции позвоночной артерии, осложнившейся ишемическим инсультом в вертебрально-базилярном бассейне.
Одной из причин ишемических инсультов в молодом возрасте, наряду с тромбофилией, употреблением наркотиков, аномалией развития церебральных сосудов, в 25% случаев является диссекция артерий, кровоснабжающих головной мозг (1). Впервые данная патология была описана в середине ХХ века, а ее возникновение практически всегда считали следствием перенесенной травмы (6). Более детальное изучение диссекции экстра и интракраниальных артерий началось с середины 70-х годов ХХ века в связи с широким применением метода церебральной ангиографии (3).
Как правило, данная патология развивается вследствие продольного надрыва сосудистой стенки с образованием интрамуральной гематомы в зоне интима-медиа. По литературным данным, диссекция чаще наблюдается в экстракраниальных сосудах — 88% (каротидная — 58%, вертебральная –30%), и только в 12% она происходит в интракраниальном бассейне (5). Нередко при диссекции экстракраниальных артерий встречаются указания на травму, предшествовавшую развитию клинической картины инсульта. Травматическое расслоение стенки артерии возникает после тупой закрытой или проникающей травмы шеи, общего сотрясения (например, при падении) и чаще всего локализуется экстракраниально (4).
Травматическое расслоение стенки артерии возникает после тупой закрытой или проникающей травмы шеи, общего сотрясения (например, при падении) и чаще всего локализуется экстракраниально (4).
Иногда диссекция носит ятрогенный характер. Так, в некоторых клинических наблюдениях встречаются указания на отчетливую связь двусторонней диссекции позвоночных артерий с мануальной терапией на шейном отделе позвоночника (8). Спонтанной диссекции, как правило, предшествует резкое движение головой (ее повороты, наклоны, разгибание), во время которых может возникать компрессия или резкое растяжение сосудистой стенки расположенным рядом костносвязочным аппаратом (4).
Возникновению спонтанной диссекции иногда предшествует бессимптомная системная патология сосудистой стенки, обусловленная фибромускулярной дисплазией, наследственным поражением соединительной ткани (синдромы Элерса—Данлоса и Марфана), артериитом, ангиолипоматозом, костной патологией в шейном отделе позвоночника (синдром Клиппеля—Фейля) (2), (3).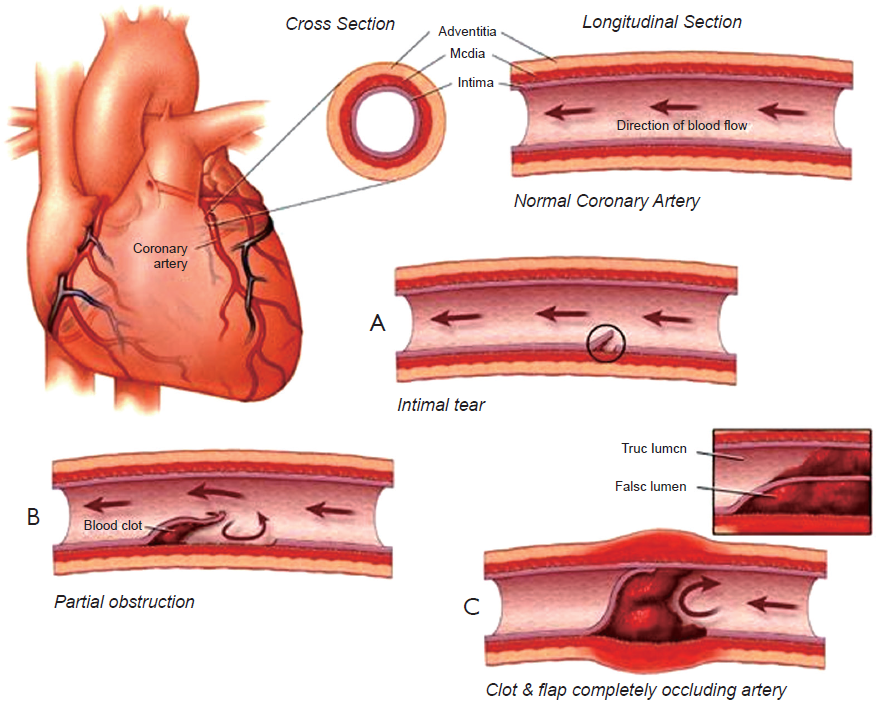 Доказана также связь спонтанной множественной диссекции с перенесенной незадолго острой инфекцией (9). Как правило, клинические проявления цервикальной диссекции складываются из повторяющихся транзиторных ишемических атак, инфарктов мозга, субарахноидальных кровоизлияний. Наиболее часто, (в 62-84%) при диссекции диагностируется инфаркт мозга (7), причиной развития которого является артериальная эмболия из области повреждения сосуда. Значительно реже имеет место гемодинамический вариант ишемического инсульта.
Доказана также связь спонтанной множественной диссекции с перенесенной незадолго острой инфекцией (9). Как правило, клинические проявления цервикальной диссекции складываются из повторяющихся транзиторных ишемических атак, инфарктов мозга, субарахноидальных кровоизлияний. Наиболее часто, (в 62-84%) при диссекции диагностируется инфаркт мозга (7), причиной развития которого является артериальная эмболия из области повреждения сосуда. Значительно реже имеет место гемодинамический вариант ишемического инсульта.
В 2015 году в сосудистом неврологическом отделении ГКБСМП им.Н.С.Карповича г.Красноярска наблюдались двое больных.
Клинический пример №1: больная Л., 21 год, поступила в отделение нейрореанимации с жалобами на слабость в правых конечностях, онемение в правой половине тела, головокружение, боль в области шеи слева. При детальном опросе выяснилось, что 19 дней назад, в период новогодних праздников, пациентка, катаясь с ледяной горки, получила «незначительную», по ее оценке, травму. Она описала падение, сопровождающееся запрокидыванием головы «назад». Ухудшение наступило без видимых причин, в связи с чем на догоспитальном этапе верификация диагноза была затруднена.
Она описала падение, сопровождающееся запрокидыванием головы «назад». Ухудшение наступило без видимых причин, в связи с чем на догоспитальном этапе верификация диагноза была затруднена.
При неврологическом осмотре: сознание ясное, критична, инструкции выполняет. Отмечается резкая болезненность в области задней поверхности шеи слева. Выявляется сглаженность правой носогубной складки, центральный правосторонний гемипарез со снижением мышечной силы до 3 баллов, правосторонняя гемигипестезия по проводниковому типу, признаки динамической мозжечковой атаксии (интенция при пальце-носовой и коленно-пяточных пробах) с обеих сторон. Правосторонняя гомонимная гемианопсия.
Рис.1. Больная Л. МРТ головного мозга.
На МРТ головного мозга : в медиобазальных отделах левой затылочной доли (в области язычковой извилины с распространением в гиппокамп) определяются мономорфные зоны цитотоксического отека неправильной формы, локализованные преимущественно в сером веществе мозга, размерами 2,3х7,6х2,3 см.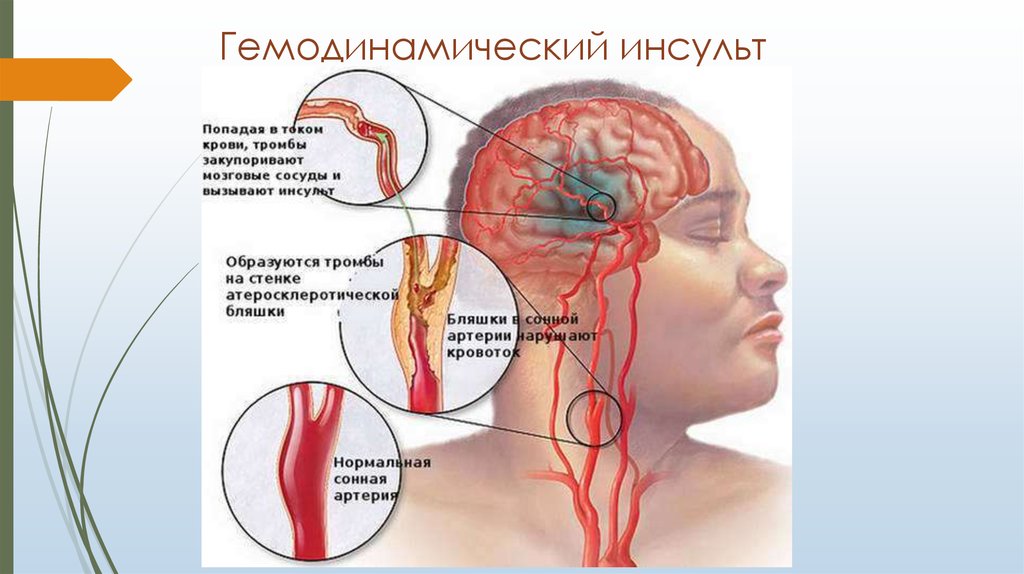 Масс-эффект незначительный в виде сужения субарахноидальных борозд на уровне выявленных изменений. В области таламусов с двух сторон определяются очаги измененного МР сигнала. При внутривенном усилении определяется выраженное однородное накопление контраста (рис.1).
Масс-эффект незначительный в виде сужения субарахноидальных борозд на уровне выявленных изменений. В области таламусов с двух сторон определяются очаги измененного МР сигнала. При внутривенном усилении определяется выраженное однородное накопление контраста (рис.1).
На МРА головного мозга определяется значительное сужение просвета и снижение кровотока (снижение интенсивности МР-сигнала) V4 сегмента правой позвоночной артерии на всем видимом протяжении. Вариант соединения позвоночных артерий – неслияние (правая позвоночная артерия не соединяется с аналогичным сегментом слева, продолжается в заднюю нижнюю мозжечковую артерию; слева – продолжается в основную артерию, равную по диаметру.
Рис.2.Больная Л. МРА артерий шеи.
На МРА артерий шеи: определяется выраженное расширение левой позвоночной артерии на уровне V2 верхнего края тела С3 позвонка до 0,7 см и последующее сужение менее 0,1-0,2 см на уровне тела С2 позвонка протяженностью 0,7 см. После сужения сохраняется расширение левой позвоночной артерии до V3 сегмента и на уровне сегмента (картина выраженного стеноза левой позвоночной артерии, выраженной престенотической дилатации в сегменте V2 левой позвоночной артерии (рис.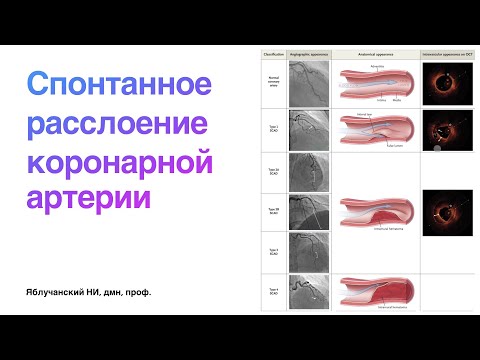 2).
2).
Данные нейровизуализации позволили установить диагноз: ишемический инсульт по типу артериальной тромбоэмболии в бассейне левой задней мозговой артерии с синдромом правостороннего центрального гемипареза, гемигипестезии, правосторонней гомонимной гемианопсии на фоне травматической диссекции левой позвоночной артерии с формированием критического стеноза этой артерии. Вариант развития сосудов Виллизиева круга (гипоплазия V3 сегмента и неслияние правой позвоночной артерии).
Немаловажное значение в развитии инсульта у данной больной играет выявленная на МРА аномалия развития сосудов Виллизиева круга. Так, «пострадавшая» артерия является практически единственным сосудом, из которого формируется весь вертебрально-базилярный бассейн. После консультации сосудистого хирурга было предложено проведение церебральной ангиографии с последующим решением вопроса об эндоваскулярном лечении стеноза левой позвоночной артерии.
Проведенное эндоваскулярное контрастное исследование, подтвердило стеноз V2 сегмента левой позвоночной артерии 70% с постаневризматическим расширением (диссекция) и постаневризматическим критическим стенозом V3 сегмента (рис.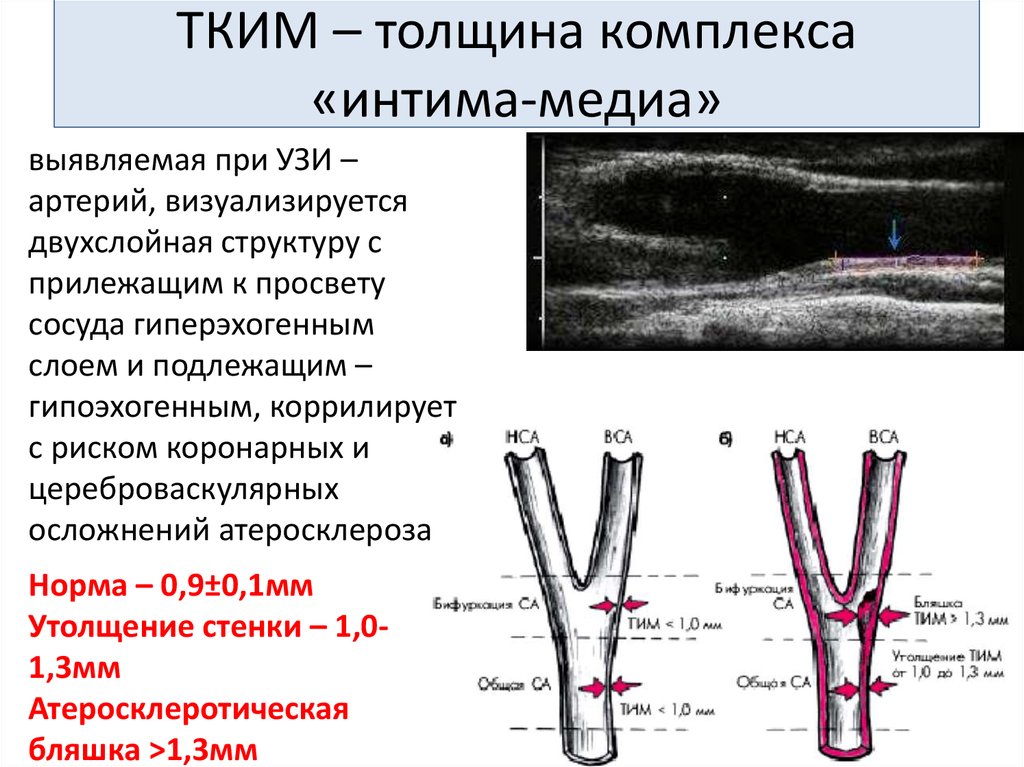 3). Ангиографическими признаками диссекции левой позвоночной артерии у данной больной являются: неравномерность просвета сосуда, стеноз по типу «крысиного хвоста».
3). Ангиографическими признаками диссекции левой позвоночной артерии у данной больной являются: неравномерность просвета сосуда, стеноз по типу «крысиного хвоста».
Рис.3.Больная Л. Ангиография левой позвоночной артерии (исходная).
Выполнено оперативное вмешательство: Эндопротезирование левой позвоночной артерии: РЭД (рентгенэндоваскулярная дилатация) в зоне стенозов баллонным катетером диаметром 2,0 мм, установлено 2 стента( BioMime 4,5х 16мм ), просвет артерии восстановлен. Рентгенконтраст: Визипак 320-160мл.
Рис.4.Больная Л. Ангиография левой позвоночной артерии (после операции).
На представленном снимке видно, что стеноза в сегментах V2 и V3 не выявляется, кровоток в левой позвоночной артерии восстановлен (рис.4).
После проведенного лечения: состояние больной удовлетворительное, мышечная сила восстановилась до 5 баллов в правой ноге и 4 баллов в правой руке, в которой также остается ощущение «онемения». Гомонимная гемианопсия регрессировала. С рекомендацией не прерывать прием дезагрегантов (плавикс, аспирин), а также продолжить нейропротективную, сосудистую терапию, пациентка была выписана под наблюдение невролога по месту жительства.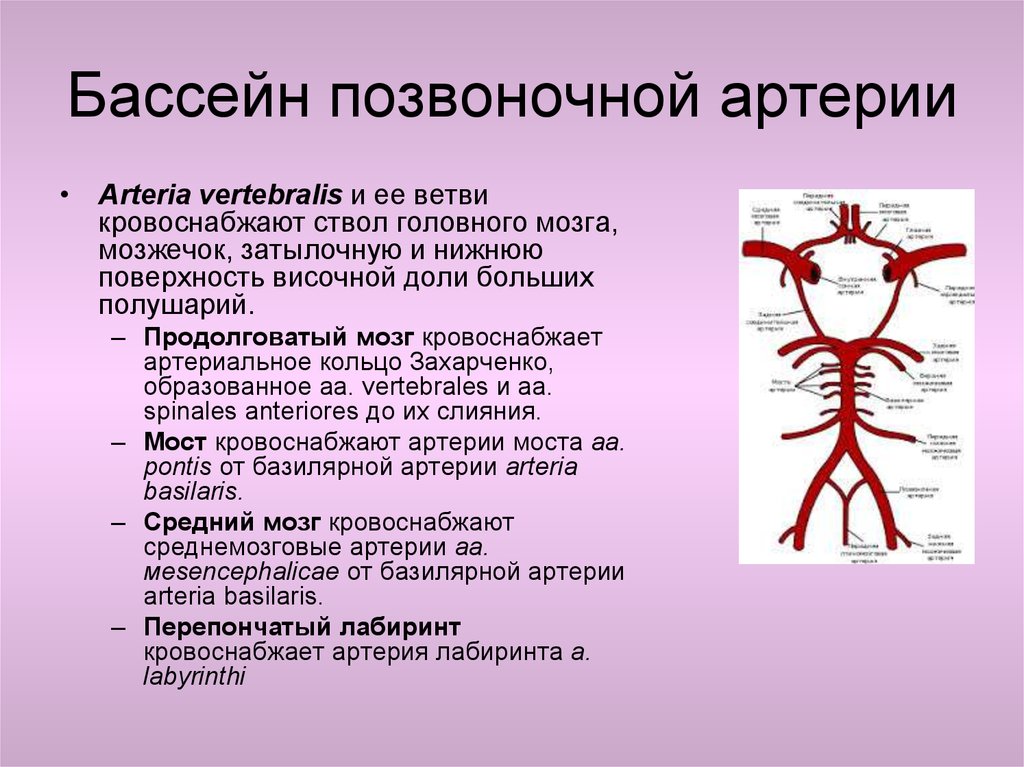
Клинический пример №2:
Больной Т., 31 год, поступил в стационар с жалобами на онемение и неловкость в левых конечностях, зрительные нарушения, головокружение. В неврологическом статусе при поступлении выявлялся: центральный парез VII,XII слева, центральный левосторонний гемипарез со снижением мышечной силы до 3б в руке и 4б в ноге, левосторонняя гомонимная гемианопсия, левосторонняя гемигипестезия.
На основании данных дообследования был выставлен диагноз: Повторный ишемический инсульт по типу артериальной тромбоэмболии в бассейне правой задней мозговой артерии с синдромом левостороннего центрального гемипареза, гемигипестезии, левосторонней гомонимной гемианопсии, на фоне диссекции правой позвоночной артерии с формированием аневризмы на уровне СI-CII.
Из анамнеза известно, что впервые был доставлен бригадой «скорой помощи» в неврологическое отделение ГКБСМП три месяца назад с жалобами на остро возникшую слабость в левых конечностях, нарушение зрения. После дообследования был установлен диагноз: ишемический инсульт в вертебрально-базилярном бассейне с синдромом левосторонней гомонимной гемианопсии, левостороннего центрального гемипареза. Выявленная на МСКТА мешотчатая аневризма на уровне С1-2 правой позвоночной артерии не была расценена как возможная причина ишемического инсульта.
Выявленная на МСКТА мешотчатая аневризма на уровне С1-2 правой позвоночной артерии не была расценена как возможная причина ишемического инсульта.
Пациент выписан из стационара со значительным улучшением. Повторный инсульт в бассейне правой задней мозговой артерии развился через три месяца. Углубленный сбор анамнеза позволил установить, что в 2013 году больной перенес спинальную травму с компрессионным переломом L2-3 позвонков. Отмечался нижний парапарез, симптомы которого регрессировали на фоне лечения. В 2014 году — повторный эпизод падения с высоты, после чего появились боли в шейном отделе позвоночника.
Рис.5. Больной Т.МРТ головного мозга.
На МРТ головного мозга: супратенториально, на медиальной поверхности правой затылочной доли обширная зона кистозно-ликворной трансформации размерами 56х20х18 мм. В таламусе справа — «застарелый» ишемический инсульт 14х8 мм с кистозно-ликворной трансформацией (рис.5).
На МРА головного мозга картина гипоплазии интракраниального сегмента позвоночной артерии справа.
Рис.6. Больной Т. Ангиография правой позвоночной артерии (исходная).
На МСКТА и церебральной ангиографии: справа, на уровне СI-СII в позвоночной артерии определяется мешотчатая аневризма (рис.6) с широким основанием, размерами 3х1,5 мм в экстракраниальной части правой позвоночной артерии.
Проведено эндоваскулярное вмешательство на сосудах шеи, позволившее выявить стеноз позвоночной артерии в V3-V4, с аневризматическим мешком 2,4 на 1,9 мм; шейка аневризмы- 3,4мм. Выполнена РЭО аневризмы (спиралью CompassComplex 2,5х3,5см) со стент ассистенцией (LVIS 5х23мм). Просвет артерии восстановлен.Аневризматический мешок не контрастируется (рис.7). Рентгенконтраст: Визипак 320-160мл.
Рис.7. Больной Т. Ангиография правой позвоночной артерии (после операции).
Пациент выписан из стационара в удовлетворительном состоянии с рекомендациями принимать плавикс 75 мг в течение 2 месяцев, аспирин кардио 100 мг — пожизненно.
Таким образом, очевидно, что инсульт, развившийся в молодом возрасте, требует пристального внимания клиницистов.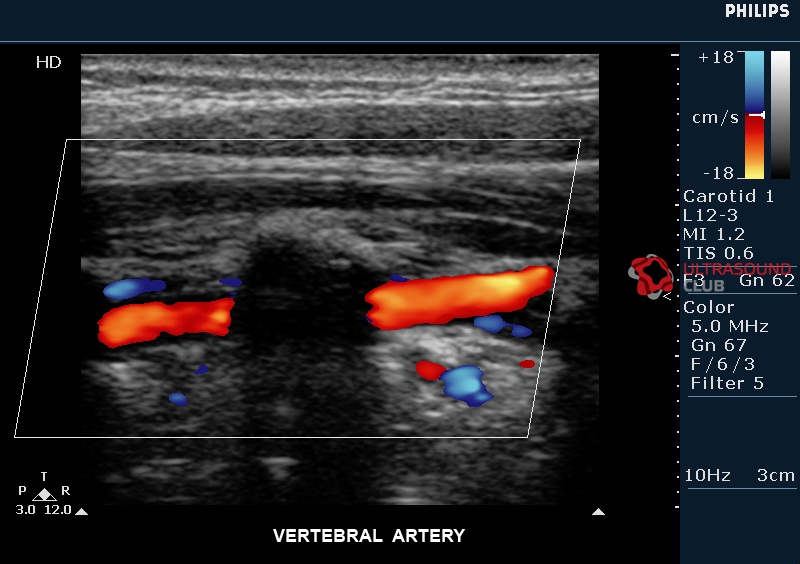 Для уточнения причины сосудистой катастрофы, помимо рутинных методов, необходимо проводить целенаправленное исследование брахиоцефальных артерий (МРА сосудов шеи, МСКТА сосудов шеи, а при необходимости — ангиографическое исследование по Сельдингеру).
Для уточнения причины сосудистой катастрофы, помимо рутинных методов, необходимо проводить целенаправленное исследование брахиоцефальных артерий (МРА сосудов шеи, МСКТА сосудов шеи, а при необходимости — ангиографическое исследование по Сельдингеру).
Приведенные в данной статье клинические наблюдения показывают, что улучшение оснащенности сосудистого центра, привлечение технологий эндоваскулярной хирургии, способствует значительному повышению качества диагностики и лечения данного заболевания.
1. Kristensen B, Malm J, Carlberg B, et al. Эпидемиология и этиология ишемического инсульта у молодых людей в возрасте от 18 до 44 лет в Северной Швеции. Инсульт. 1997; 28: 1702–1709. [PubMed] [Google Scholar]
2. Schievink WI. Спонтанный диссекция сонных и позвоночных артерий. N Engl J Med. 2001; 344: 898–906. [PubMed] [Google Scholar]
3. Белецкий В., Надареишвили З. , Линч Дж., Шуайб А., Вулфенден А., Норрис Дж. В. Расслоение шейной артерии: время для терапевтических испытаний? Инсульт. 2003; 34: 2856–2860. [PubMed] [Академия Google]
, Линч Дж., Шуайб А., Вулфенден А., Норрис Дж. В. Расслоение шейной артерии: время для терапевтических испытаний? Инсульт. 2003; 34: 2856–2860. [PubMed] [Академия Google]
4. Бьюссе В., Д'Англежан-Шатийон Дж., Тубул П.Дж., Амаренко П., Буссер М.Г. Динамика симптомов экстракраниальной диссекции сонной артерии. Серия из 80 пациентов. Инсульт. 1995; 26: 235–239. [PubMed] [Google Scholar]
5. Savitz SI, Caplan LR, Edlow JA. Подводные камни в диагностике инфаркта мозжечка. Академия скорой медицинской помощи. 2007; 14:63–68. [PubMed] [Google Scholar]
6. Bossuyt PM, Reitsma JB, Bruns DE, et al. На пути к полному и точному отчету об исследованиях диагностической точности: инициатива STARD. Клиническая химия. 2003;49: 1–6. [PubMed] [Google Scholar]
7. Simel DL, Rennie D, Bossuyt PM. Заявление STARD для отчетов об исследованиях диагностической точности: применение к анамнезу и физикальному обследованию. J Gen Intern Med. 2008; 23: 768–774. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Ganesan V, Chong WK, Cox TC, Chawda SJ, Prengler M, Kirkham FJ. Инсульт заднего кровообращения в детском возрасте: факторы риска и рецидивы. Неврология. 2002; 59: 1552–1556. [PubMed] [Google Scholar]
Ganesan V, Chong WK, Cox TC, Chawda SJ, Prengler M, Kirkham FJ. Инсульт заднего кровообращения в детском возрасте: факторы риска и рецидивы. Неврология. 2002; 59: 1552–1556. [PubMed] [Google Scholar]
9. Yamaura A, Watanabe Y, Saeki N. Расслаивающие аневризмы внутричерепной позвоночной артерии. Дж Нейрохирург. 1990;72:183–188. [PubMed] [Google Scholar]
10. Zhao WY, Krings T, Alvarez H, Ozanne A, Holmin S, Lasjaunias P. Лечение спонтанной геморрагической внутричерепной вертебробазилярной диссекции: обзор 21 последовательного случая. Acta Neurochir (Вена) 2007; 149: 585–596. обсуждение 596. [PubMed] [Google Scholar]
11. Arnold M, Bousser MG, Fahrni G, et al. Расслоение позвоночной артерии: представление результатов и предикторы исхода. Инсульт. 2006; 37: 2499–2503. [PubMed] [Академия Google]
12. Dziewas R, Konrad C, Drager B, et al. Расслоение шейной артерии - клинические особенности, факторы риска, терапия и исход у 126 пациентов. Дж Нейрол. 2003; 250:1179–1184. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
13. Boet R, Wong HT, Yu SC, Poon WS. Диссекции вертебробазилярных артерий: современная практика. Hong Kong Med J. 2002; 8: 33–38. [PubMed] [Google Scholar]
14. Shin JH, Suh DC, Choi CG, Leei HK. Расслоение позвоночной артерии: спектр результатов визуализации с акцентом на ангиографию и корреляцию с клиническими проявлениями. Рентгенография. 2000; 20:1687–169.6. [PubMed] [Google Scholar]
15. Saeed AB, Shuaib A, Al-Sulaiti G, Emery D. Расслоение позвоночной артерии: предупреждающие симптомы, клинические особенности и прогноз у 26 пациентов. Может J Neurol Sci. 2000; 27: 292–296. [PubMed] [Google Scholar]
16. de Bray JM, Penisson-Besnier I, Dubas F, Emile J. Экстракраниальные и внутричерепные вертебробазилярные диссекции: диагностика и прогноз. J Neurol Нейрохирург Психиатрия. 1997; 63:46–51. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Provenzale JM, Morgenlander JC, Gress D. Спонтанное расслоение позвонков: клинические, обычные ангиографические, КТ и МРТ результаты.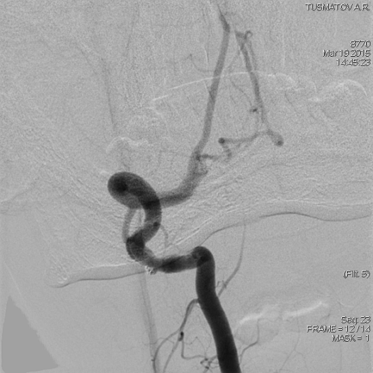 J Comput Assist Томогр. 1996;20:185–193. [PubMed] [Google Scholar]
J Comput Assist Томогр. 1996;20:185–193. [PubMed] [Google Scholar]
18. Хикс П.А., Ливитт Дж.А., Мокри Б. Офтальмологические проявления расслоения позвоночной артерии. Пациенты наблюдались в клинике Майо с 1976 по 1992 год. Офтальмология. 1994; 101:1786–1792. [PubMed] [Google Scholar]
19. Josien E. Расслоение экстракраниальной позвоночной артерии: девять случаев. Дж Нейрол. 1992; 239:327–330. [PubMed] [Google Scholar]
20. Мокри Б., Хаузер О.В., Сандок Б.А., Пьепграс Д.Г. Спонтанные расслоения позвоночных артерий. Неврология. 1988;38:880–885. [PubMed] [Google Scholar]
21. Chiras J, Marciano S, Vega Molina J, Touboul J, Poirier B, Bories J. Спонтанная расслаивающая аневризма экстракраниальной позвоночной артерии (20 случаев) Нейрорадиология. 1985; 27: 327–333. [PubMed] [Google Scholar]
22. Wolf PA, D’Agostino RB, Belanger AJ, Kannel WB. Вероятность инсульта: профиль риска Фрамингемского исследования. Инсульт. 1991; 22: 312–318. [PubMed] [Google Scholar]
23. Manabe H, Yonezawa K, Kato T, Toyama K, Haraguchi K, Ito T. Частота расслоения внутричерепных артерий у неэкстренных амбулаторных пациентов с жалобами на головную боль: предварительное исследование с МРТ/МРА исследованиями . Acta Neurochir Suppl. 2010; 107:41–44. [PubMed] [Академия Google]
Manabe H, Yonezawa K, Kato T, Toyama K, Haraguchi K, Ito T. Частота расслоения внутричерепных артерий у неэкстренных амбулаторных пациентов с жалобами на головную боль: предварительное исследование с МРТ/МРА исследованиями . Acta Neurochir Suppl. 2010; 107:41–44. [PubMed] [Академия Google]
24. Krespi Y, Gurol ME, Coban O, Tuncay R, Bahar S. Расслоение позвоночной артерии с изолированной болью в шее. J Нейровизуализация. 2002; 12: 179–182. [PubMed] [Google Scholar]
25. Rane NJ, McAuley D. Расслоение позвоночной артерии в виде изолированного головокружения. Emerg Med J. 2007; 24:732. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Adams HPJ, del Zoppo G, Alberts MJ, et al. Руководство по раннему лечению взрослых с ишемическим инсультом: руководство Американской кардиологической ассоциации/Американской ассоциации инсульта, Совета по инсульту, Совета по клинической кардиологии, Совета по сердечно-сосудистой радиологии и интервенционным вмешательствам, а также результатов исследований атеросклеротического заболевания периферических сосудов и качества медицинской помощи в междисциплинарной исследовательской работе. Группы: Американская академия неврологии подтверждает ценность этого руководства как учебного пособия для неврологов. Инсульт. 2007; 38: 1655–1711. [PubMed] [Академия Google]
Группы: Американская академия неврологии подтверждает ценность этого руководства как учебного пособия для неврологов. Инсульт. 2007; 38: 1655–1711. [PubMed] [Академия Google]
27. Шиевинк В.И. Лечение спонтанных расслоений сонных и позвоночных артерий. Карр Опин Кардиол. 2000;15:316–321. [PubMed] [Google Scholar]
28. Hausser I, Muller U, Engelter S, et al. Различные типы изменений соединительной ткани, связанные с расслоением шейных артерий. Акта Нейропатол. 2004; 107: 509–514. [PubMed] [Google Scholar]
29. Dittrich R, Heidbreder A, Rohsbach D, et al. Соединительнотканный и сосудистый фенотип у пациентов с диссекцией шейных артерий. Неврология. 2007;68:2120–2124. [PubMed] [Академия Google]
30. Ransohoff DF, Feinstein AR. Проблемы спектра и смещения в оценке эффективности диагностических тестов. Медицинский журнал Новой Англии. 1978; 299: 926–930. [PubMed] [Google Scholar]
1. Ахмад Х.А., Геррати Р.П., Дэвис С.М., Кэмерон П.А. Расслоения шейно-мозговых артерий. J Accid Emerg Med. 1999; 16: 422–424. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Accid Emerg Med. 1999; 16: 422–424. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Ahn JY, Han IB, Kim TG, Yoon PH, Lee YJ, Lee BH, Seo SH, Kim DI, Hong CK, Joo JY. Эндоваскулярное лечение диссекции внутричерепных позвоночных артерий с установкой стента или свертыванием стента. AJNR Am J Нейрорадиол. 2006; 27:1514–1520. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Anxionnat R, Roy D, Bracard S, Marchal JC, Auque J, Ducrocq X, Roland J, Picard L. Диссекция внутричерепных позвоночных артерий, выявленная субарахноидальным кровоизлиянием. Отчет о семи случаях. J Нейрорадиол. 1994; 21:1–16. [PubMed] [Google Scholar]
4. Arnold M, Cumurciuc R, Stapf C, Favrole P, Berthet K, Bousser MG. Боль как единственный симптом расслоения шейных артерий. J Neurol Нейрохирург Психиатрия. 2006; 77: 1021–1024. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Арнольд М., Буссер М.Г., Фарни Г., Фишер У., Георгиадис Д., Ганджур Дж., Беннингер Д., Стурценеггер М. , Маттл Х.П., Баумгартнер Р.В. Расслоение позвоночной артерии: Представление результатов и предикторы исхода. Инсульт. 2006; 37: 2499–2503. [PubMed] [Google Scholar]
, Маттл Х.П., Баумгартнер Р.В. Расслоение позвоночной артерии: Представление результатов и предикторы исхода. Инсульт. 2006; 37: 2499–2503. [PubMed] [Google Scholar]
6. Auer A, Felber S, Schmidauer C, Waldenberger P, Aichner F. Магнитно-резонансная ангиография и клинические особенности расслоения экстракраниальной позвоночной артерии. J Neurol Нейрохирург Психиатрия. 1998; 64: 474–481. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Бартельс Э., Флюгель К.А. Оценка экстракраниальной диссекции позвоночной артерии с помощью дуплексной визуализации цветового потока. Инсульт. 1996; 27: 290–295. [PubMed] [Google Scholar]
8. Bartels E. Диссекция экстракраниальной позвоночной артерии: клинические данные и ранняя неинвазивная диагностика у 24 пациентов. J Нейровизуализация. 2006; 16: 24–33. [PubMed] [Google Scholar]
9. Белецкий В., Надареишвили З., Линч Дж., Шуайб А., Вулфенден А., Норрис Дж. В. Расслоение шейной артерии: время для терапевтических испытаний? Инсульт. 2003; 34: 2856–2860. [PubMed] [Академия Google]
2003; 34: 2856–2860. [PubMed] [Академия Google]
10. Бергер М.С., Уилсон С.Б. Внутричерепные расслаивающие аневризмы заднего отдела кровообращения. Отчет о шести случаях и обзор литературы. Дж Нейрохирург. 1984; 61: 882–894. [PubMed] [Google Scholar]
11. Boet R, Wong HT, Yu SC, Poon WS. Диссекции вертебробазилярных артерий: Современная практика. Hong Kong Med J. 2002; 8: 33–38. [PubMed] [Google Scholar]
12. Campos CR, Calderaro M, Scaff M, Conforto AB. Первичные головные боли и болезненная спонтанная диссекция шейных артерий. J Головная боль. 2007; 8: 180–184. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Chen CJ, Tseng YC, Lee TH, Hsu HL, см. LC. Мультисекционная КТ-ангиография в сравнении с катетерной ангиографией в диагностике расслоения позвоночной артерии. AJNR Am J Нейрорадиол. 2004; 25: 769–774. [PMC free article] [PubMed] [Google Scholar]
14. Chiche L, Praquin B, Koskas F, Kieffer E. Спонтанный диссекция экстракраниальной позвоночной артерии: показания и отдаленные результаты хирургического лечения. Энн Васк Сург. 2005; 19: 5–10. [PubMed] [Google Scholar]
Энн Васк Сург. 2005; 19: 5–10. [PubMed] [Google Scholar]
15. Chiras J, Marciano S, Vega Molina J, Touboul J, Poirier B, Bories J. Спонтанная расслаивающая аневризма экстракраниальной позвоночной артерии (20 случаев) Нейрорадиология. 1985;27:327–333. [PubMed] [Google Scholar]
16. Chung YS, Han DH. Вертебробазилярная диссекция: возможная роль хлыстовой травмы в ее патогенезе. Нейрол Рез. 2002; 24:129–138. [PubMed] [Google Scholar]
17. Клеверт Д.А., Юнг Э.М., Джонсон Т., Кубале Р., Рупп Н., Шенберг С.О., Райзер М. Расслоение шейной артерии: улучшенная диагностика с помощью ультразвукового исследования b-потока. Clin Hemorheol Microcirc. 2007; 36: 141–153. [PubMed] [Google Scholar]
18. Клеверт Д.А., Рупп Н., Рейзер М., Юнг Э.М. Улучшенная диагностика расслоения сосудов с помощью ультразвукового b-потока: сравнение с цветовой допплерографией и энергетической допплерографией. Евро Радиол. 2005; 15: 342–347. [PubMed] [Академия Google]
19. Dae Hee H, Kwon OK, Chang Wan O. Клинические характеристики диссекции вертебробазилярной артерии. Медико-хирургическая неврология: Neurol. Мед.-Чир. 1998; 38: 107–113. [PubMed] [Google Scholar]
Клинические характеристики диссекции вертебробазилярной артерии. Медико-хирургическая неврология: Neurol. Мед.-Чир. 1998; 38: 107–113. [PubMed] [Google Scholar]
20. de Bray JM, Pasco A, Dubas F, Emile J. Расслоения сонных и позвоночных артерий: предполагаемые ультразвуковые аспекты. Acta Neurologica Taiwanica: Acta Neurol. Тайвань. 2000;9:9–12. [Google Scholar]
21. de Bray JM, Penisson-Besnier I, Dubas F, Emile J. Экстракраниальные и внутричерепные вертебробазилярные диссекции: диагностика и прогноз. J Neurol Нейрохирург Психиатрия. 1997;63:46–51. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. de Sousa JE, Halfon MJ, Bonardo P, Reisin RC, Fernandez Pardal MM. Различные болевые паттерны у пациентов с расслоением позвоночных артерий. Неврология. 2005; 64: 925–926. [PubMed] [Google Scholar]
23. Дитрих Р., Дзиевас Р., Риттер М.А., Клоска С.П., Бахманн Р., Нассенштейн И., Куленбаумер Г., Хайндель В., Рингельштейн Э.Б., Набави Д.Г. Отрицательные результаты УЗИ у больных с расслоением шейных артерий. Отрицательное УЗИ при кадке. Дж Нейрол. 2006; 253:424–433. [PubMed] [Академия Google]
Отрицательное УЗИ при кадке. Дж Нейрол. 2006; 253:424–433. [PubMed] [Академия Google]
24. Дзиевас Р., Конрад С., Драгер Б., Эверс С., Бессельманн М., Людеманн П., Куленбаумер Г., Стогбауэр Ф., Рингельштейн Э.Б. Расслоение шейной артерии - клинические особенности, факторы риска, терапия и исход у 126 пациентов. Дж Нейрол. 2003; 250:1179–1184. [PubMed] [Google Scholar]
25. Ganesan V, Chong WK, Cox TC, Chawda SJ, Prengler M, Kirkham FJ. Инсульт заднего кровообращения в детском возрасте: факторы риска и рецидивы. Неврология. 2002; 59: 1552–1556. [PubMed] [Google Scholar]
26. Gelbert F, Assouline E, Hodes JE, Reizine D, Woimant F, George B, Hagueneau M, Merland JJ. МРТ при спонтанной диссекции позвоночных и сонных артерий. 15 случаев изучались при 0,5 тесла. Нейрорадиология. 1991;33:111–113. [PubMed] [Google Scholar]
27. Greselle JF, Zenteno M, Kien P, Castel JP, Caille JM. Спонтанный диссекция вертебро-базилярной системы. Исследование 18 случаев (15 пациентов) J Neuroradiol. 1987; 14: 115–123. [PubMed] [Google Scholar]
28. Хан Д.Х., Квон ОК, О К.В. Клиническая характеристика диссекции вертебробазилярной артерии. Neurol Med Chir (Токио) 1998; 38 (Приложение): 107–113. [PubMed] [Google Scholar]
29. Хашимото М., Джохкура К., Итикава Т., Кодзима А., Нисимура С., Шинонага М. Консервативное лечение разрыва вертебробазилярной расслаивающей аневризмы. Неврология наук. 2008;29: 241–244. [PubMed] [Google Scholar]
30. Хикс П.А., Ливитт Дж.А., Мокри Б. Офтальмологические проявления расслоения позвоночной артерии. Пациенты наблюдались в клинике Майо с 1976 по 1992 год. Офтальмология. 1994; 101:1786–1792. [PubMed] [Google Scholar]
31. Хоффманн М., Сакко Р.Л., Чан С., Мор Дж.П. Неинвазивное выявление расслоения позвоночной артерии. Инсульт. 1993; 24:815–819. [PubMed] [Google Scholar]
32. Хосоя Т., Адачи М., Ямагути К., Хаку Т., Каяма Т., Като Т. Клинические и нейрорадиологические особенности диссекции внутричерепной вертебробазилярной артерии. Инсульт. 1999;30:1083–1090. [PubMed] [Google Scholar]
33. Hosoya T, Watanabe N, Yamaguchi K, Kubota H, Onodera Y. Расслоение внутричерепной позвоночной артерии при синдроме Валленберга. AJNR Am J Нейрорадиол. 1994; 15:1161–1165. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Hufnagel A, Hammers A, Leonhardt G, Schonle PW, Bohm KD. Инсульт после мануальной терапии шейного отдела позвоночника. Журнал неврологии: J. Neurol. 1999; 246: 683–688. [PubMed] [Google Scholar]
35. Josien E. Расслоение экстракраниальной позвоночной артерии: девять случаев. Дж Нейрол. 1992;239:327–330. [PubMed] [Google Scholar]
36. Kim CH, Son YJ, Paek SH, Han MH, Kim JE, Chung YS, Kwon BJ, Oh CW, Han DH. Клинический анализ вертебробазилярной диссекции. Acta Neurochir (Вена) 2006; 148: 395–404. [PubMed] [Google Scholar]
37. Китанака С., Сасаки Т., Эгучи Т., Тераока А., Накане М., Хойя К. Расслоение внутричерепных позвоночных артерий: клинические, радиологические особенности и хирургические соображения. Нейрохирургия. 1994; 34: 620–626. обсуждение 626-627. [PubMed] [Академия Google]
38. Леклерк Х, Лукас С, Годфруа О, Никол Л, Моретти А, Лейс Д, Пруво Дж.П. Предварительный опыт использования МР-ангиографии с контрастным усилением для оценки структуры позвоночной артерии при подозрении на диссекцию. AJNR Am J Нейрорадиол. 1999; 20:1482–1490. [Бесплатная статья PMC] [PubMed] [Google Scholar]
39. Lee JS, Yong SW, Bang OY, Shin YS, Kim BM, Kim SY. Сравнение спонтанной диссекции внутричерепной позвоночной артерии с поражением крупных артерий. Арх Нейрол. 2006; 63: 1738–1744. [PubMed] [Академия Google]
40. Lee JW, Jung JY, Kim YB, Huh SK, Kim DI, Lee KC. Спонтанная расслаивающая аневризма внутричерепной позвоночной артерии: стратегии лечения. Yonsei Med J. 2007; 48: 425–432. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Lee VH, Brown RD, Jr., Mandrekar JN, Mokri B. Частота и исход расслоения шейной артерии: популяционное исследование. Неврология. 2006; 67: 1809–1812. [PubMed] [Google Scholar]
42. Lu CJ, Sun Y, Jeng JS, Huang KM, Hwang BS, Lin WH, Chen RC, Yip PK. Визуализация в диагностике и последующей оценке расслоения позвоночной артерии. J УЗИ Мед. 2000;19: 263–270. [PubMed] [Google Scholar]
43. Mas JL, Bousser MG, Hasboun D, Laplan D. Расслоение экстракраниальных позвоночных артерий: обзор 13 случаев. Инсульт. 1987; 18: 1037–1047. [PubMed] [Google Scholar]
44. Metso TM, Metso AJ, Helenius J, Haapaniemi E, Salonen O, Porras M, Hernesniemi J, Kaste M, Tatlisumak T. Прогноз и безопасность антикоагулянтной терапии при расслоении внутричерепных артерий у взрослых. Инсульт. 2007; 38: 1837–1842. [PubMed] [Google Scholar]
45. Мокри Б., Хаузер О.В., Сандок Б.А., Пьепграс Д.Г. Спонтанные расслоения позвоночных артерий. Неврология. 1988;38:880–885. [PubMed] [Google Scholar]
46. Naito I, Iwai T, Sasaki T. Лечение расслоений внутричерепных позвоночных артерий, первоначально проявляющихся без субарахноидального кровоизлияния. Нейрохирургия. 2002; 51: 930–937. обсуждение 937-938. [PubMed] [Google Scholar]
47. Накагава К., Тохо Х., Морисако Т., Осака Ю., Тацузава К., Накаэ Х., Овада К., Мацуда К., Карасава Дж. Долгосрочное последующее исследование неразорвавшейся диссекции позвоночной артерии : Клинические результаты и серийные ангиографические данные. Дж Нейрохирург. 2000;93:19–25. [PubMed] [Google Scholar]
48. Nebelsieck J, Sengelhoff C, Nassenstein I, Maintz D, Kuhlenbaumer G, Nabavi DG, Ringelstein EB, Dittrich R. Чувствительность нейроваскулярного ультразвука для обнаружения спонтанного расслоения шейной артерии. Дж. Клин Нейроски. 2009; 16:79–82. [PubMed] [Google Scholar]
49. Пелконен О., Тиккакоски Т., Пыхтинен Дж., Сотаниеми К. Результаты КТ и МРТ головного мозга при диссекции шейно-головной артерии. Акта Радиол. 2004; 45: 259–265. [PubMed] [Академия Google]
50. Пелузо Дж. П., ван Рой В. Дж., Служевски М., Беуте Г. Н., Майуа С. Б. Эндоваскулярное лечение симптоматических интрадуральных расслаивающих аневризм позвонков. AJNR Am J Нейрорадиол. 2008; 29: 102–106. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Pozzati E, Andreoli A, Limoni P, Casmiro M. Расслаивающие аневризмы вертебробазилярной системы: исследование 16 случаев. Сур Нейрол. 1994; 41: 119–124. [PubMed] [Google Scholar]
52. Provenzale JM, Morgenlander JC, Gress D. Спонтанное расслоение позвонков: клинические, обычные ангиографические, КТ и МРТ результаты. J Comput Assist Томогр. 1996;20:185–193. [PubMed] [Google Scholar]
53. Pugliese F, Crusco F, Cardaioli G, Tambasco N, Boranga B, Scaroni R, Maselli A, Lupattelli L. КТ-ангиография по сравнению с цветовой допплерографией при остром расслоении позвоночной артерии. Radiol Med (Турин) 2007; 112: 435–443. [PubMed] [Google Scholar]
54. Рамгрен Б., Кронквист М., Ромнер Б., Брандт Л., Холтас С., Ларссон Э.М. Вертебробазилярная диссекция с субарахноидальным кровоизлиянием: ретроспективное исследование 29 пациентов. Нейрорадиология. 2005;47:97–104. [PubMed] [Google Scholar]
55. Reuter U, Hamling M, Kavuk I, Einhaupl KM, Schielke E. Расслоение позвоночной артерии после хиропрактики на шее в Германии в течение трех лет. Дж Нейрол. 2006; 253:724–730. [PubMed] [Google Scholar]
56. Ротер Дж., Шварц А., Раутенберг В., Хеннеричи М. Магнитно-резонансная ангиография спонтанного расслоения позвоночной артерии, подозреваемого при допплерографии. Дж Нейрол. 1995; 242:430–436. [PubMed] [Google Scholar]
57. Саид А.Б., Шуайб А., Аль-Сулайти Г., Эмери Д. Расслоение позвоночной артерии: предупреждающие симптомы, клинические особенности и прогноз у 26 пациентов. Может J Neurol Sci. 2000;27:292–296. [PubMed] [Google Scholar]
58. Саката Н., Такебаяси С., Кодзима М., Масава Н., Судзуки К., Такатама М. Патология расслаивающей внутричерепной аневризмы. Невропатология. 2000; 20:104–108. [PubMed] [Google Scholar]
59. Sheah K, Lim W, Chan C. Эндоваскулярное и хирургическое лечение расслаивающих аневризм позвоночной артерии с субарахноидальным кровоизлиянием: среднесрочный опыт. Энн Академ Мед Сингапур. 2005; 34: 262–270. [PubMed] [Google Scholar]
60. Shibata T, Kubo M, Kuwayama N, Hirashima Y, Endo S. Предупреждение о субарахноидальном кровоизлиянии и инфаркте вследствие расслоения вертебробазилярной артерии. Клин Джей Пейн. 2006;22:193–196. [PubMed] [Google Scholar]
61. Симодзи Т., Бандо К., Накадзима К., Ито К. Расслаивающая аневризма позвоночной артерии. Отчет о семи случаях и результатах ангиографии. Дж Нейрохирург. 1984; 61: 1038–1046. [PubMed] [Google Scholar]
62. Shin JH, Suh DC, Choi CG, Leei HK. Расслоение позвоночной артерии: спектр результатов визуализации с акцентом на ангиографию и корреляцию с клиническими проявлениями. Рентгенография. 2000; 20:1687–1696. [PubMed] [Google Scholar]
63. Шин Ю.С., Ким Х.С., Ким С.Ю. Стентирование при вертебробазилярной диссекции: возможный вариант лечения негеморрагической вертебробазилярной диссекции. Нейрорадиология. 2007;49: 149–156. [PubMed] [Google Scholar]
64. Зильберт П. Л., Мокри Б., Шиевинк В.И. Головная боль и боль в шее при спонтанных расслоениях внутренних сонных и позвоночных артерий. Неврология. 1995; 45: 1517–1522. [PubMed] [Google Scholar]
65. Sturzenegger M. Головная боль и боль в шее: предупреждающие симптомы расслоения позвоночной артерии. Головная боль. 1994; 34: 187–193. [PubMed] [Google Scholar]
66. Sturzenegger M, Mattle HP, Rivoir A, Rihs F, Schmid C. Ультразвуковые данные при спонтанной экстракраниальной диссекции позвоночной артерии. Инсульт. 1993;24:1910–1921. [PubMed] [Google Scholar]
67. Takagi T, Takayasu M, Suzuki Y, Yoshida J. Прогнозирование повторного кровотечения по ангиографическим признакам при расслаивающих аневризмах позвоночной артерии. Нейрохирург Ред. 2007; 30:32–38. обсуждение 38-39. [PubMed] [Google Scholar]
68. Вертинский А.Т., Шварц Н.Е., Фишбейн Н.Дж., Розенберг Дж., Альберс Г.В., Захарчук Г. Сравнение мультидетекторной КТ-ангиографии и МРТ диссекции шейной артерии. AJNR Am J Нейрорадиол. 2008; 29: 1753–1760. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Весселс Т., Моссо М., Крингс Т., Клотч С., Харрер Ю.Ю. Экстракраниальная и внутричерепная диссекция позвоночной артерии: долгосрочное клиническое и дуплексное сонографическое наблюдение. Дж. Клин Ультразвук. 2008; 36: 472–479. [PubMed] [Google Scholar]
70. Yamada M, Kitahara T, Kurata A, Fujii K, Miyasaka Y. Расслоение внутричерепной позвоночной артерии с субарахноидальным кровоизлиянием: клинические характеристики и исходы у консервативно леченных пациентов. Дж Нейрохирург. 2004; 101: 25–30. [PubMed] [Академия Google]
71. Ямаура А., Оно Дж., Хираи С. Клиническая картина внутричерепной нетравматической расслаивающей аневризмы. Невропатология. 2000; 20:85–90. [PubMed] [Google Scholar]
72. Yamaura A, Watanabe Y, Saeki N. Расслаивающие аневризмы внутричерепной позвоночной артерии. Дж Нейрохирург. 1990; 72: 183–188. [PubMed] [Google Scholar]
73. Yoshimoto Y, Wakai S. Диссекция неразорвавшейся внутричерепной позвоночной артерии. Клиническое течение и серия рентгенологических изображений. Инсульт. 1997; 28: 370–374. [PubMed] [Академия Google]
74. Zhao WY, Krings T, Alvarez H, Ozanne A, Holmin S, Lasjaunias P. Лечение спонтанной геморрагической внутричерепной вертебробазилярной диссекции: обзор 21 последовательного случая. Acta Neurochir (Вена) 2007; 149: 585–596. обсуждение 596. [PubMed] [Google Scholar]
75. Zuber M, Meary E, Meder JF, Mas JL. Магнитно-резонансная томография и динамическая КТ при диссекциях шейных артерий. Инсульт. 1994; 25: 576–581. [PubMed] [Google Scholar]
Расслоение позвоночной артерии (ДПА) является редкой причиной инсульта среди населения в целом, но одной из наиболее частых причин инсульта у пациентов моложе 45 лет. Его признаки и симптомы могут быть расплывчатыми, что затрудняет диагностику. Сообщалось о спонтанных расслоениях, но случайная незначительная травма обычно ускоряет это потенциально опасное состояние. Часто искривление шеи, вызванное манипуляциями хиропрактики, изгибом шеи или тупой травмой, вызывает расслоение. Расслоение артерии может в конечном итоге привести к инсульту, который часто откладывается на несколько дней после острого расслоения. В этом упражнении рассматривается оценка и ведение пациентов с расслоением позвоночной артерии и подчеркивается роль членов межпрофессиональной команды в сотрудничестве для обеспечения хорошо скоординированного ухода и улучшения результатов для пострадавших пациентов.
Цели:
Опишите этиологию расслоения позвоночной артерии.
Опишите клиническую картину пациента с расслоением позвоночной артерии.
Обобщите варианты лечения расслоения позвоночной артерии.
Объясните важность улучшения координации помощи между членами межпрофессиональной бригады для улучшения исходов у пациентов с расслоением позвоночной артерии.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Расслоение позвоночной артерии (ДПН) является редкой причиной инсульта в общей популяции; однако представляет собой одну из наиболее частых причин инсульта у пациентов моложе 45 лет. Его признаки и симптомы могут быть расплывчатыми, а диагноз может быть неуловимым. [1][2][3] Сообщалось о спонтанных расслоениях. Однако случайная незначительная травма часто провоцирует это потенциально опасное состояние. Часто некоторые деформации шеи, такие как манипуляции хиропрактики, сгибание шеи или тупая травма, вызывают расслоение. Расслоение артерии может в конечном итоге привести к инсульту, который часто может быть отсрочен на несколько дней после острого расслоения.
Большинство расслоений внутричерепные. Подсчитано, что расслоение позвоночной артерии может быть причиной не менее 20% ишемических инсультов у молодых людей.
Пациенты обычно сообщают о незначительных, довольно безобидных провоцирующих явлениях до появления симптомов. Кашель, рвота, процедуры хиропрактики и тупая травма, вероятно, являются инициирующими событиями. Подсчитано, что 1 из 20 000 манипуляций на шейном отделе позвоночника приводит к инсульту. [4][5][6] Тупая травма шеи является наиболее частым провоцирующим фактором. Пациенты с заболеваниями соединительной ткани также подвержены повышенному риску. Синдром Элерса-Данлоса является наиболее распространенным заболеванием соединительной ткани, которое может привести к расслоению позвоночной артерии. Когда пациенты с серьезным повреждением шейного отдела спинного мозга или переломами позвоночника проходят скрининг на предмет повреждения позвоночной артерии, примерно у 20–40% выявляется травматическая окклюзия. Интересно, что эта окклюзия имеет тенденцию быть бессимптомной, в отличие от расслоения, и ее лечение является спорным.
Other risk factors for vertebral artery dissection include:
Yoga
Nose blowing
Painting the ceiling
Judo, wrestling
Hypertension
Fibromuscular dysplasia
Женский пол
Использование противозачаточных таблеток
Кистозный медиальный некроз
Васкулит
Послеродовой период[7]
По оценкам, расслоение позвоночной артерии является причиной примерно 2 % всех ишемических инсультов. Однако считается, что у пациентов среднего и молодого возраста (от 30 до 45 лет) он достигает 10–25%, что составляет значительную часть населения, страдающего этим заболеванием. Общая частота расслоения позвоночной артерии и сонной артерии оценивается в 2,6 на 100 000 человек. Расслоения сонных артерий встречаются в 3-5 раз чаще, чем расслоения позвоночных артерий. Следует отметить, что хиропрактики отвергают связь между манипуляциями и расслоением позвоночной артерии на том основании, что расслоение является причиной боли в шее и причиной, по которой пациенты обращаются за помощью к хиропрактике. Нет никаких убедительных доказательств, связывающих эти две ведущие некоторые медицинские ассоциации только для того, чтобы предположить причинно-следственную связь.
Анатомия позвоночной артерии
Сегмент 1 начинается от первой ветви подключичной артерии и достигает отверстий С5-С6.
Сегмент 2 проходит в пределах поперечных отверстий от С5/С6 до С2.
Сегмент 3 представляет собой извилистый сегмент, который начинается у поперечных отверстий С2 и проходит в заднелатеральной части, огибает С1 и затем проходит между атлантом и затылком. Этот сегмент артерии окружен нервами, мышцами и атланто-затылочной мембраной.
Сегмент 4 — внутричерепной; он прободает твердую мозговую оболочку в области большого затылочного отверстия и проходит до места соединения мозгового вещества и моста; здесь она сливается с основной артерией.
Большинство спонтанных расслоений происходит в сегменте 3, который может распространяться и вовлекать сегмент 4.
Артериальная анатомия состоит из трех слоев, называемых ). Расслоение происходит при нарушении структурной целостности артериальной стенки. Разрывы интимы приводят к расслаиванию артериальной крови между слоями артериальной стенки. Кровь в артериальной стенке провоцирует образование гематом и тромбов.[8] Последующее нарушение артериального кровотока, вторичное по отношению к стенозу, приводит к симптомам расслоения позвоночной артерии и, в конечном итоге, к инсульту. Расслоение позвоночной артерии может быть как экстракраниальным, так и внутричерепным. Экстракраниальная диссекция обычно затрагивает дистальный экстракраниальный сегмент около атланта и аксиса. Внутричерепные расслоения часто связаны с субарахноидальным кровоизлиянием и имеют гораздо худший прогноз. Неврологические последствия как экстракраниальной, так и внутричерепной диссекции могут быть результатом церебральной ишемии вследствие тромбоэмболии, гипоперфузии или их комбинации. Однако тромбоэмболия, а не гипоперфузия, считается основной причиной ишемических симптомов.
История
Клиническая картина обычно представляет собой острую и сильную одностороннюю боль в шее и/или головную боль. Незначительная травма шеи часто провоцирует боль. Боль обычно локализуется в затылочно-шейной области шеи или головы. Часто травма носит незначительный характер.
Неврологические симптомы часто проявляются с задержкой и могут вообще отсутствовать. Однако у 70% пациентов будет некоторый тип неврологического дефицита, который может проявляться поздно.0003
Боковые мозговые синдромы (синдром Валленберга) и инфаркты мозжечка являются наиболее частой локализацией инсульта. Синдром Валленберга определяется сенсорным дефицитом, затрагивающим туловище и конечности на противоположной стороне инфаркта, и сенсорным дефицитом, затрагивающим лицо и черепные нервы на той же стороне, что и инфаркт. При наличии неврологических симптомов преобладающими симптомами являются головокружение, атаксия, дисфагия (черепные нервы 9 и 10), нарушение равновесия, односторонняя потеря слуха, дизартрия, диплопия и головокружение.
При экстракраниальных расслоениях часто присутствует шум. Сообщалось даже о шуме на противоположной стороне, вторичном по отношению к увеличению коллатерального кровотока. Что часто отличает этот тип пациентов от пациентов с инфарктом мозжечка, вторичным по отношению к атеросклеротическому заболеванию, так это возраст пациента и наличие боли. При внутричерепном расслоении субарахноидальное кровоизлияние присутствует в 50% случаев. Эта группа больных имеет выраженную неврологическую симптоматику, прогноз значительно хуже, чем у больных с экстракраниальными расслоениями.
Медицинский осмотр
NYSTAGMUS
Тункал Атаксия
Ипсилатеральная потеря вкуса (гипогея), синдром Хорнера, нарушение проприографии и тонкое прикосновение
9022 2 400223 9. 010101010101010 годы. Отклонение языка в сторону пораженияМежъядерная офтальмоплегия
МРТ конкурирует с ангиографией для установления диагноза, но не всегда доступна для большинства. КТ и КТА часто являются первыми полученными исследованиями. КТ может выявить ишемию задней черепной ямки или субарахноидальное кровоизлияние. Он также может выявить закупорку позвоночной артерии или пристеночный тромб. Однако КТА превосходит КТ и должна выполняться. КТА легче выявляет неравномерность просвета сосудов или утолщение стенки артерий. CTA является начальным тестом выбора. Сосудистое дуплексное сканирование демонстрирует аномальный кровоток в 95% больных. Тем не менее, он показывает признаки, характерные для диссекции, только у 20% пациентов.[9]
МРТ может выявить лоскут интимы и тромбоз просвета. Иногда гиперинтенсивность сосудистой стенки визуализируется на Т1-взвешенных изображениях и считается патогномоничной.
Если МРТ и КТ не выявили какой-либо патологии, может потребоваться церебральная ангиограмма.
Если КТ показывает отсутствие кровотечения, можно начинать антикоагулянтную терапию.
Для тех пациентов, которые выжили после первоначальной диссекции, прогноз обычно благоприятный. Примерно 10% больных умирают первоначально.
Целью лечения является предотвращение инсульта, который является осложнением расслоения позвоночной артерии. Лечение проводится антикоагулянтами, обычно гепарином. Если нет противопоказаний, то тромболитическую терапию можно начинать, пока время находится в пределах 4,5 часов от появления симптомов.
В одном последующем клиническом исследовании 80% пациентов достигли полного выздоровления. Смерть обычно наступает после обширной внутричерепной диссекции, инфаркта ствола мозга или субарахноидального кровоизлияния. Большинство расслоений со временем проходят без неврологического дефицита. Однако имейте в виду, что, когда диссекция является внутричерепной или распространяется внутричерепно, риск субарахноидального кровоизлияния значительно возрастает, и антикоагуляция противопоказана. [10][11][12] Эндоваскулярное или хирургическое лечение предназначено для пациентов с сопутствующими осложнениями или тех, чья максимальная медикаментозная терапия оказалась безуспешной.
Госпитализация необходима для всех пациентов с расслоением позвоночной артерии. Тщательный мониторинг неврологического дефицита имеет жизненно важное значение.
Сегодня технологические достижения позволили использовать эндоваскулярные методы лечения диссекции позвоночной артерии. Тем не менее, роль этой терапии остается спорной, поскольку большинство пациентов можно лечить с помощью антикоагулянтной терапии. Кроме того, большинство вскрытий ремонтируют самостоятельно. Таким образом, эндоваскулярная терапия лучше всего подходит для пациентов, которым не показаны тромболитики и/или у которых имеется субарахноидальное кровоизлияние.
Хирургическое вмешательство в виде шунтирования проводится редко и не всегда успешно.
Стратегии вторичной профилактики включают снижение риска путем воздействия на сосудистые факторы риска и их модификации. Аспирин используется в качестве профилактической терапии при большинстве этиологий. При мерцательной аритмии рекомендуется антикоагулянтная терапия. Большинству пациентов с инсультом, в том числе молодым людям, следует проводить терапию статинами.[13]
Растяжение шейки матки
Migraine headache
Stroke, hemorrhage
Stroke, ischemia
Tension headache
For patients who do survive the initial acute extracranial диссекция, прогноз благоприятный с полным выздоровлением почти у 80-90% пациентов. Однако, по крайней мере, у 10% разовьются повторные приступы, большой инсульт или смерть. Пациенты с тяжелым неврологическим дефицитом на момент поступления обычно имеют неблагоприятный прогноз. Последующие ангиографические исследования показали заживление примерно у 60% пациентов.
Пациенты, у которых развивается внутричерепная диссекция, имеют плохой прогноз. Те, кто поступает с измененным сознанием и неврологическим дефицитом, чувствуют себя плохо. Внутричерепные расслоения позвонков часто связаны с инфарктами ствола головного мозга, субарахноидальными кровоизлияниями и летальным исходом.
Прогноз для молодых пациентов без сопутствующих заболеваний, таких как гипертония, диабет и курение, может сильно отличаться от прогноза для тех, у кого они есть.
Инфаркт мозжечка и ствола мозга
Субарахноидальное кровоизлияние
Псевдоаневризма позвоночной артерии, приводящая к компрессионной нейропатии черепных нервов.
Пациенты должны наблюдаться каждые 3–6 месяцев при наличии симптомов или до тех пор, пока визуализация не покажет полное разрешение. Как долго проводить антикоагулянтную терапию, пока неизвестно, но не менее 6 месяцев.
Головная боль или боль в шее, связанные с расслоением позвоночной артерии, могут предшествовать развитию неврологических симптомов на срок до 14 дней. Пациенты могут сообщать о неясных неврологических симптомах, связанных с болью, которая может быть преходящей. Проблема для врача отделения неотложной помощи заключается в том, что, когда обследование начинается с сильной головной боли или боли в шее, компьютерная томография и люмбальная пункция могут быть отрицательными. У этих пациентов часто диагностируют головную боль или даже транзиторную ишемическую атаку (ТИА), что откладывает диагностику и лечение. Сильная боль остается отличительной чертой и не может быть проигнорирована. Дальнейшая неврологическая визуализация с помощью КТА или МРТ должна быть выполнена, если клинические подозрения высоки. Пациенты с расслоением позвоночной артерии должны быть госпитализированы для тщательного неврологического наблюдения и, по показаниям, антикоагулянтной терапии. Хирургическое вмешательство показано очень редко.
Диагностика и лечение расслоения позвоночной артерии непросты и лучше всего выполняются межпрофессиональной командой, в которую входят рентгенолог, врач отделения неотложной помощи, практикующая медсестра, невролог и сосудистый хирург. После того, как визуализация поставила диагноз, лечение зависит от симптомов пациента.
Для тех пациентов, которые пережили первичную диссекцию, прогноз обычно благоприятный. Примерно 10% больных умирают первоначально. В одном последующем клиническом исследовании 80% достигли полного выздоровления. Смерть обычно наступает после обширной внутричерепной диссекции, инфаркта ствола мозга или субарахноидального кровоизлияния. Целью лечения является предотвращение инсульта, который является осложнением расслоения позвоночной артерии. Лечение проводится антикоагулянтами, обычно гепарином. Для тех, у кого есть неврологический дефицит, необходима соответствующая реабилитационная терапия. Фармацевт должен информировать пациента о соблюдении режима приема лекарств, контроле артериального давления и прекращении курения. Фармацевт также должен контролировать МНО, чтобы убедиться, что оно находится в терапевтическом диапазоне.
Эндоваскулярные или хирургические методы лечения предназначены для пациентов с сопутствующими осложнениями или тех, чья максимальная медикаментозная терапия оказалась безуспешной. Большинство расслоений со временем проходят без неврологического дефицита. Тесное общение с членами команды жизненно важно, если кто-то хочет улучшить результаты.
Восстановление может быть длительным, а полное восстановление часто невозможно.[3][14]
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Прокомментируйте эту статью.
Zhou Y, Wang L, Zhang JR, Zhou K, Shuai J, Gong ZL, Liu Y, Wei F, Han YF, Shen L, Yang QW. Ангиопластика и стентирование при тяжелом симптомном атеросклеротическом стенозе интракраниальной вертебробазилярной артерии. Дж. Клин Нейроски. 2019 Май; 63:17-21. [PubMed: 30850180]
Ким М.К., Лим Ю.К. Консервативное лечение неразорвавшейся спонтанной внутричерепной позвоночной артерии. Мировой нейрохирург. 2019Июнь;126:e402-e409. [PubMed: 30822585]
Маркус Х.С., Леви С., Кинг А., Мэдиган Дж., Норрис Дж., Расслоение шейной артерии при исследовании инсульта (CADISS) Исследователи. Антитромбоцитарная терапия против антикоагулянтной терапии при диссекции шейной артерии: исследование диссекции шейной артерии при инсульте (CADISS), окончательные результаты рандомизированного клинического испытания. ДЖАМА Нейрол. 2019 01 июня; 76 (6): 657-664. [Бесплатная статья PMC: PMC6563567] [PubMed: 30801621]
Пила А.Е., Макинтош А.С., Контурис А., Ньюман П., Гайда Дж.Е. Диссекция позвоночной артерии в спорте: систематический обзор. Спорт Мед. 2019 Апрель; 49 (4): 553-564. [PubMed: 30758815]
Уолш Б.А., Грегори В.Д., Уиттл Дж.С. Деконструкция рассечения: отчет о болезни и обзор тупой цереброваскулярной травмы шеи. Представитель Emerg Med. 2018;2018:6120781. [Бесплатная статья PMC: PMC6106916] [PubMed: 30174964]
Hu Y, Du J, Liu Z, Wu H, Ding J, Jian F. Расслоение позвоночной артерии, вызванное атлантоаксиальной дислокацией: клинический случай и обзор литературы. Чайлдс Нерв Сист. 201935 января (1): 187–190. [PubMed: 30109422]
Финли А., Роджерс Б., Ричардс Т., Фогель Х. Послеродовая диссекция позвоночной артерии. BMJ Case Rep. 2015 24 ноября 2015 г. [бесплатная статья PMC: PMC4680301] [PubMed: 26604230]
Yun SY, Heo YJ, Jeong HW, Baek JW, Choo HJ, Seo JH, Kim ST, Ли JY, Джин SC. Спонтанный диссекция внутричерепной позвоночной артерии при остром ишемическом инсульте: результаты магнитно-резонансной томографии высокого разрешения. Neuroradiol J. 2018 Jun;31(3):262-269. [Бесплатная статья PMC: PMC5958508] [PubMed: 29565222]
McNally JS, Hinckley PJ, Sakata A, Eisenmenger LB, Kim SE, De Havenon AH, Quigley EP, Iacob E, Treiman DL, Parker DL . Магнитно-резонансная томография и клинические факторы, ассоциированные с ишемическим инсультом у пациентов с подозрением на диссекцию шейной артерии. Инсульт. 2018 Октябрь;49(10):2337-2344. [Бесплатная статья PMC: PMC6208137] [PubMed: 30355108]
Turner RC, Lucke-Wold BP, Boo S, Rosen CL, Sedney CL. Потенциальные опасности манипуляций на шее и риск расслоения и разрушительного инсульта: иллюстративный случай и обзор литературы. Biomed Res Rev. 2018; 2(1) [бесплатная статья PMC: PMC6016850] [PubMed: 29951644]