2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Кардиомиопатия - это изменение мышцы сердца часто невыясненной причины.
Условием постановки диагноза «кардиомиопатия» является отсутствие (или исключение после обследования) врожденных аномалий развития, клапанных пороков сердца, поражения, обусловленного системными заболеваниями сосудов, артериальной гипертонии, перикардита, а также некоторых редких вариантов поражения проводящей системы сердца.
Существует три группы основных причин развития первичной кардиомиопатии: врожденная, смешанная, и приобретенная. К вторичным относятся кардиомиопатии вследствие какого-либо заболевания.
Врождённая патология сердца развивается вследствие нарушения закладки тканей миокарда во время эмбриогенеза. Причин очень много, начиная от вредных привычек будущей матери и заканчивая стрессами и неправильным питанием. Так же известны кардиомиопатии беременных и воспалительные кардиомиопатии, которые по существу можно назвать миокардитом.
К вторичным формам относятся следующие виды:
Проявления ГКМП многообразны и зависят от ряда факторов: степени гипертрофии миокарда, наличия и величины градиента давления, недостаточности митрального клапана, нередко встречающейся у больных, степени уменьшения полости левого желудочка и тяжести нарушения насосной и диастолической функций сердца и др. Жалобы часто отсутствуют.
Различают 3 группы КМП:
Гипертрофическую.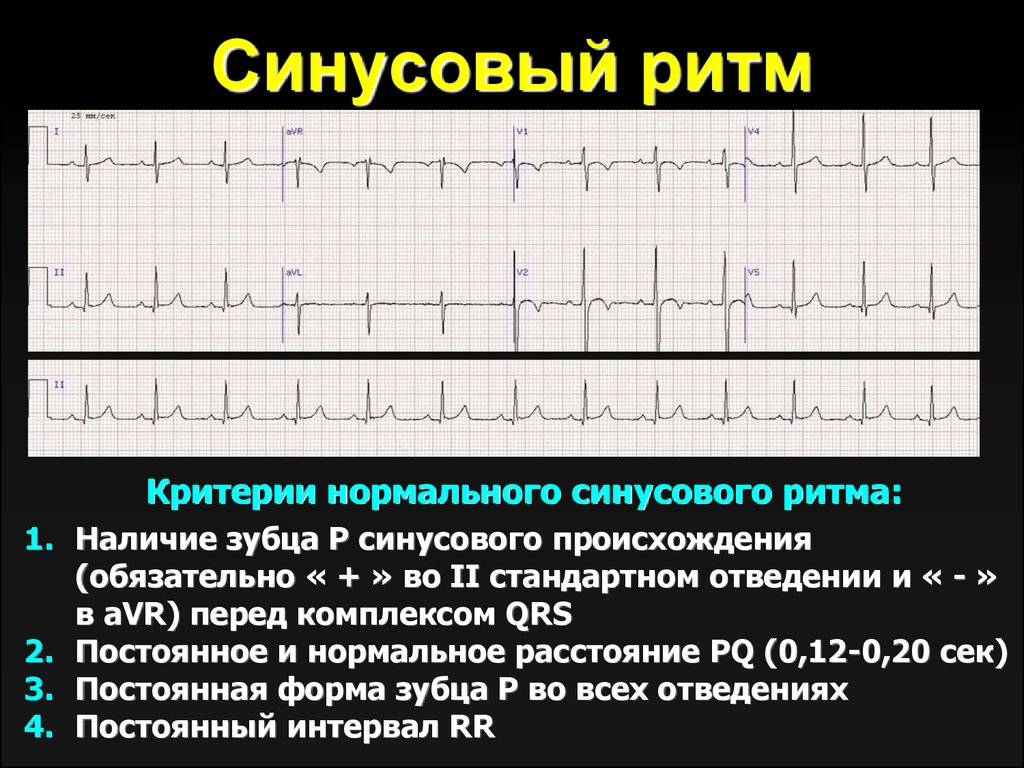
Дилатационную (застойную).
Рестриктивную.
Симптомы дилатационной кардиомиопатии:
Симптомы гипертрофической кардиомиопатии:
Симптомы рестриктивной кардиомиопатии:
Основным инструментальным методом диагностики всех видов кардиомиопатий является УЗИ сердца.
Суточное холтеровское мониторирование электрокардиограммы позволяет оценить частоту и выраженность нарушений ритма сердца и внутрисердечных блокад, а так же эффективность проводимого лечения.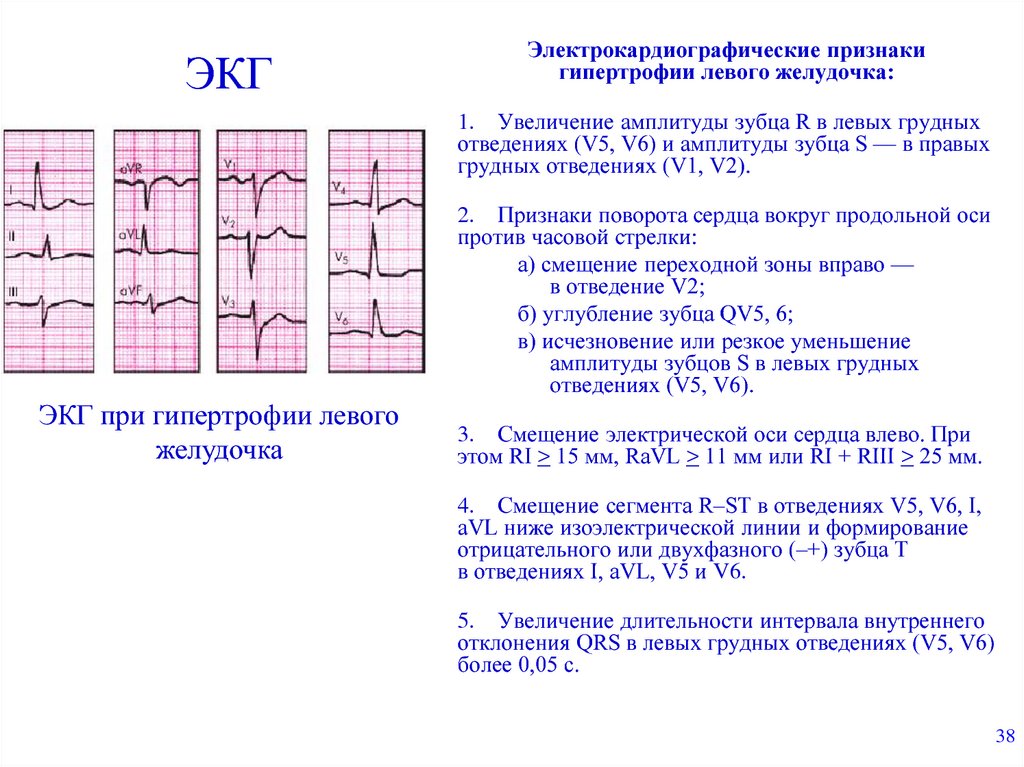 Лабораторная диагностика важна для контроля эффективности проводимой терапии в оценке состояния водно-солевого баланса, для исключения некоторых побочных эффектов препаратов, а также для выявления вторичных причин поражения сердца.
Лабораторная диагностика важна для контроля эффективности проводимой терапии в оценке состояния водно-солевого баланса, для исключения некоторых побочных эффектов препаратов, а также для выявления вторичных причин поражения сердца.
Так как причины кардиомиопатии не до конца известны, специальной профилактики на данный момент не существует. Необходимо своевременно лечить заболевания сердца.
Подробнее о детской кардиологии в клинике «ЮгМед»
Оставляя свои персональные данные, Вы даете добровольное согласие на обработку своих персональных данных. Под персональными данными понимается любая информация, относящаяся к Вам, как субъекту персональных данных (ФИО, дата рождения, город проживания, адрес, контактный номер телефона, адрес электронной почты, род занятости и пр). Ваше согласие распространяется на осуществление Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» любых действий в отношении ваших персональных данных, которые могут понадобиться для сбора, систематизации, хранения, уточнения (обновление, изменение), обработки (например, отправки писем или совершения звонков) и т. п. с учетом действующего законодательства. Согласие на обработку персональных данных даётся без ограничения срока, но может быть отозвано Вами (достаточно сообщить об этом в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед»). Пересылая в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» свои персональные данные, Вы подтверждаете, что с правами и обязанностями в соответствии с Федеральным законом «О персональных данных» ознакомлены.
п. с учетом действующего законодательства. Согласие на обработку персональных данных даётся без ограничения срока, но может быть отозвано Вами (достаточно сообщить об этом в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед»). Пересылая в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» свои персональные данные, Вы подтверждаете, что с правами и обязанностями в соответствии с Федеральным законом «О персональных данных» ознакомлены.
Кардиолог
Соколов
Денис Владимирович
Стаж 17 лет
Врач кардиолог первой категории, кандидат медицинских наук, член Asute Cardiovascular Care Association (ASSA)
Записаться на прием
Брадикардия – патологическое снижение частоты сердечных сокращений, наблюдаемое у пациентов различных возрастов.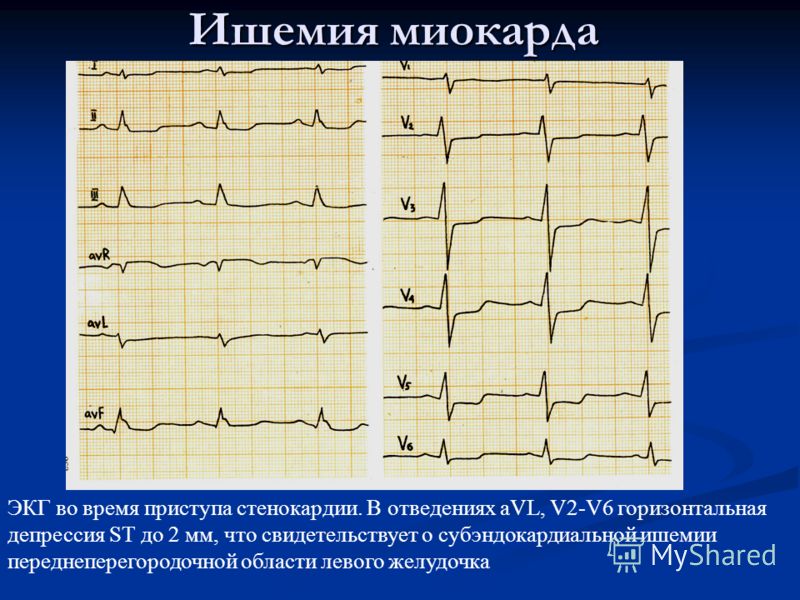 Развивается на фоне острых или хронических заболеваний сердца. Пороговым значением при постановке диагноза становятся 60 сокращений сердечной мышцы в минуту. Пациенты страдают от слабости, систематической потери сознания, головокружений и перепадов артериального давления. Выраженная синусовая брадикардия (40 ЧСС/мин) может привести к развитию сердечной недостаточности. Для ее предотвращения пациенту имплантируется кардиостимулятор.
Развивается на фоне острых или хронических заболеваний сердца. Пороговым значением при постановке диагноза становятся 60 сокращений сердечной мышцы в минуту. Пациенты страдают от слабости, систематической потери сознания, головокружений и перепадов артериального давления. Выраженная синусовая брадикардия (40 ЧСС/мин) может привести к развитию сердечной недостаточности. Для ее предотвращения пациенту имплантируется кардиостимулятор.
Патология развивается на фоне неспособности синусового узла к выработке необходимого для нормальной частоты сердечных сокращений количества электрических импульсов. Умеренная синусовая брадикардия может не приводить к расстройству гемодинамики. Выраженная форма патологии провоцирует недостаточное кровоснабжение тканей. Развивается кислородное голодание органов.
Профессиональные спортсмены могут столкнуться с физиологической брадикардией, которая рассматривается кардиологами как норма. В состоянии покоя у тренированных людей фиксируются 50-60 сердечных сокращений в минуту. Во сне это значение падает на 25-30%.
Во сне это значение падает на 25-30%.
Кардиологи выделяют пять форм по этиологическому основанию:
Экстракардиальный тип развивается под действием нейрогенных факторов, органический – на фоне патологических поражений сердца. Лекарственная и токсическая формы заболевания возникают при попадании в организм пациент токсинов или лекарственных препаратов в избыточных дозировках. Синусовая брадикардия спортсменов становится результатом многолетних тренировок, направленных на достижение максимальной ЧСС при физических нагрузках.
Патологические типы могут протекать в острой или хронической формах. В первом случае причиной нарушения ЧСС становятся инфаркты, миокардиты, интоксикации. Хроническая брадикардия становится результатом возрастных склеротических поражений сердечной мышцы.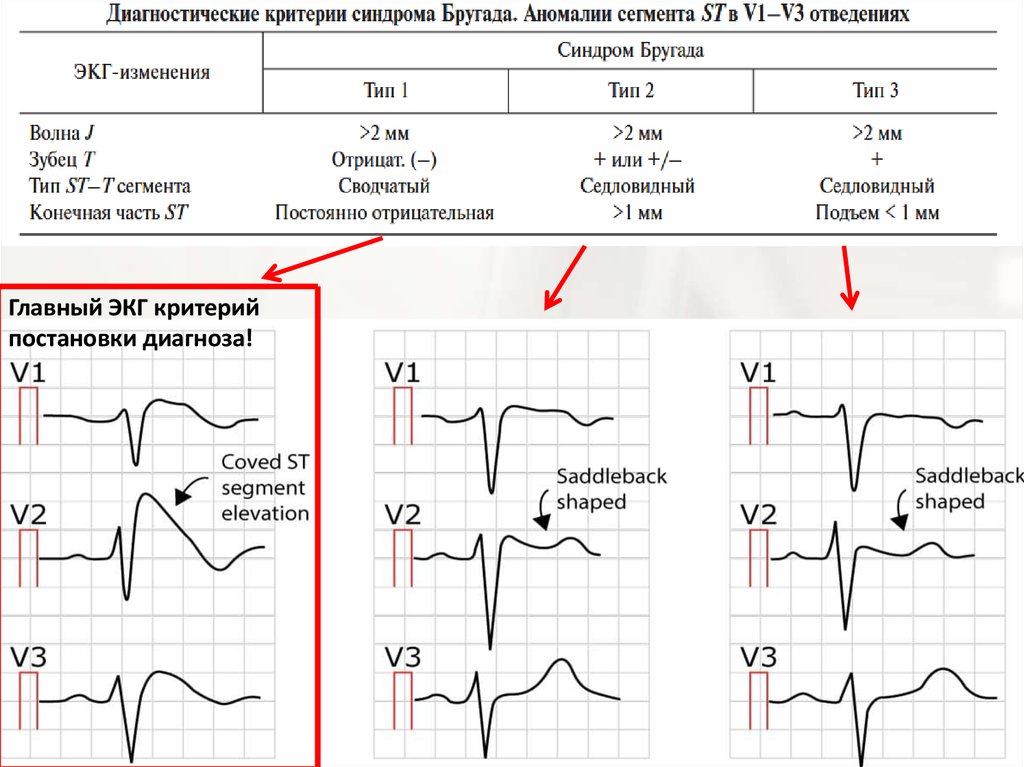
Органический тип проявляется на фоне нескольких патологий:
Перечисленные заболевания провоцируют дегенеративные изменения в синусовом узле и нарушение проводимости в миокарде.
Экстракардиальная форма брадикардии – результат неврозов, повышенного внутричерепного давления или сдавления каротидного синуса одеждой.
Токсические поражения развиваются при контакте человека с опасными химическими веществами. Брадикардии этого типа часто развиваются на фоне профессиональной деятельности пациента.
Лекарственные брадикардии проявляются при нарушении человеком предписанной дозировки препарата или длительном приеме медикаментов с выраженным воздействием на частоту сокращения сердца.
Умеренное течение редко сопровождается явными клиническими симптомами. Выраженная форма патологии провоцирует:
Выраженная форма патологии провоцирует:
Пациенты могут испытывать сложности с дыханием, ощущать выраженную боль в грудной клетке. Представители старшей возрастной группы сталкиваются с нарушением концентрации, кратковременной потерей памяти, эпизодическими расстройствами зрения.
Нарушение сократительной функции миокарда приводит к гипоксии головного мозга. На фоне могут развиваться приступы судорог продолжительностью до 60 секунд. Данное состояние рассматривается кардиологами как наиболее опасное при подтвержденной брадикардии. Пациент нуждается в неотложной помощи, поскольку затянувшиеся приступы судорог провоцируют остановку дыхательной деятельности.
Диагностика и лечение брадикардии выполняются кардиологом. Врач осматривает ребенка или взрослого и собирает данные для анамнеза. Пристальное внимание уделяется пульсу пациента, звучности сердечных тонов и частоте дыхательных движений. При наличии соответствующих показаний кардиолог может направить пациента к неврологу, нейрохирургу, инфекционисту.
Врач осматривает ребенка или взрослого и собирает данные для анамнеза. Пристальное внимание уделяется пульсу пациента, звучности сердечных тонов и частоте дыхательных движений. При наличии соответствующих показаний кардиолог может направить пациента к неврологу, нейрохирургу, инфекционисту.
Органическая форма требует проведения УЗИ сердца. Ультразвуковое исследование позволяет оценить изменения размеров сердечной мышцы, выявить очаги дегенеративных поражений. Нагрузочная велоэргометрия направлена на определение прироста частоты сердечных сокращений при различных объемах физических нагрузок.
Умеренное течение заболевания без выраженных клинических проявлений не требует терапии. Органическая, токсическая и экстракардиальная формы брадикардии предполагают обязательное лечение основной патологии. Пациентам с лекарственным типом заболевания назначаются сниженные дозировки препаратов, замедляющих сердечный ритм.
При выраженной брадикардии с приступами судорог проводится хирургическое вмешательство. Пациенту имплантируется электрокардиостимулятор, служащий заменой водителя ритма. Частота вырабатываемых имплантатом импульсов соответствует возрастной норме пациента. Стабильный сердечный ритм приводит к нормализации гемодинамики и устранению кислородного голодания органов.
Пациенту имплантируется электрокардиостимулятор, служащий заменой водителя ритма. Частота вырабатываемых имплантатом импульсов соответствует возрастной норме пациента. Стабильный сердечный ритм приводит к нормализации гемодинамики и устранению кислородного голодания органов.
Прогноз осложняется при наличии у пациента органических поражений сердца. Устойчивое снижение сердечного ритма может привести к присвоению человеку инвалидности. Умеренный характер брадикардии позволяет добиться полного восстановления работоспособности пациента вне зависимости от причин нарушения сердечного ритма. Наличие у ребенка или взрослого хронических системных патологий ведет к формированию удовлетворительного прогноза.
Какие профилактические меры позволяют предотвратить развитие брадикардии?
Избежать устойчивого нарушения сердечного ритма можно при своевременном обращении за медицинской помощью из-за интоксикаций или ухудшения самочувствия при приеме лекарств. Пациентам с отягощенным семейным анамнезом рекомендуется ежегодно проходить осмотры у кардиолога.
Пациентам с отягощенным семейным анамнезом рекомендуется ежегодно проходить осмотры у кардиолога.
В каком возрасте человек может столкнуться с симптомами брадикардии?
Нарушения в работе водителя сердечного ритма возможны в любом возрасте. Вероятность развития устойчивой формы значительно возрастает при достижении человеком 65 лет.
Наши специалисты готовы проконсультировать вас по телефону:
+7 (495) 775-73-60
1. Schellong G, Riepenhausen M, Bruch C, Kotthoff S, Vogt J, Bolling T, et al. Поздние заболевания клапанов и другие пороки сердца после различных доз лучевой терапии средостения при болезни Ходжкина у детей и подростков: отчет по продольному проекту последующего наблюдения GPOH немецко-австрийских исследований DAL-HD. Детский рак крови. 2010;55(6):1145–52. doi: 10.1002/pbc.22664. [PubMed] [CrossRef] [Академия Google]
Детский рак крови. 2010;55(6):1145–52. doi: 10.1002/pbc.22664. [PubMed] [CrossRef] [Академия Google]
2. Алеман Б.М., ван ден Белт-Дусебаут А.В., Де Брюин М.Л., Веер М.Б. в 'т, Баайенс М.Х., Де Бур Дж.П. и др. Поздняя кардиотоксичность после лечения лимфомы Ходжкина. Кровь. 2007; 109 (5): 1878–86. doi: 10.1182/blood-2006-07-034405. [PubMed] [CrossRef] [Google Scholar]
3. McGale P, Darby SC, Hall P, Adolfsson J, Bengtsson NO, Bennet AM, et al. Частота сердечно-сосудистых заболеваний у 35 000 женщин, получавших лучевую терапию по поводу рака молочной железы в Дании и Швеции. Радиотер Онкол. 2011;100(2):167–75. doi: 10.1016/j.radonc.2011.06.016. [PubMed] [CrossRef] [Академия Google]
4. Harris EE, Correa C, Hwang WT, Liao J, Litt HI, Ferrari VA, et al. Поздняя сердечная смертность и заболеваемость у больных раком молочной железы на ранней стадии после органосохраняющего лечения. Дж. Клин Онкол. 2006;24(25):4100–6. doi: 10.1200/JCO.2005.05.1037. [PubMed] [CrossRef] [Google Scholar]
5. Ishikura S, Nihei K, Ohtsu A, Boku N, Hironaka S, Mera K, et al. Долговременная токсичность после радикальной химиолучевой терапии плоскоклеточного рака грудного отдела пищевода. Дж. Клин Онкол. 2003;21(14):2697–702. doi: 10.1200/JCO.2003.03.055. [PubMed] [CrossRef] [Google Scholar]
Ishikura S, Nihei K, Ohtsu A, Boku N, Hironaka S, Mera K, et al. Долговременная токсичность после радикальной химиолучевой терапии плоскоклеточного рака грудного отдела пищевода. Дж. Клин Онкол. 2003;21(14):2697–702. doi: 10.1200/JCO.2003.03.055. [PubMed] [CrossRef] [Google Scholar]
6. Darby SC, Cutter DJ, Boerma M, Constine LS, Fajardo LF, Kodama K, et al. Радиационно-обусловленные болезни сердца: современные знания и перспективы на будущее. Int J Radiat Oncol Biol Phys. 2010;76(3):656–65. doi: 10.1016/j.ijrobp.2009.09.064. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Lauk S, Kiszel Z, Buschmann J, Trott KR. Радиационно-индуцированная болезнь сердца у крыс. Int J Radiat Oncol Biol Phys. 1985;11(4):801–8. doi: 10.1016/0360-3016(85)-1. [PubMed] [CrossRef] [Google Scholar]
8. Marks LB, Yu X, Prosnitz RG, Zhou SM, Hardenbergh PH, Blazing M, et al. Частота и функциональные последствия дефектов сердечной перфузии, связанных с лучевой терапией. Int J Radiat Oncol Biol Phys. 2005;63(1):214–23. doi: 10.1016/j.ijrobp.2005.01.029. [PubMed] [CrossRef] [Google Scholar]
Int J Radiat Oncol Biol Phys. 2005;63(1):214–23. doi: 10.1016/j.ijrobp.2005.01.029. [PubMed] [CrossRef] [Google Scholar]
9. Gayed IW, Liu HH, Yusuf SW, Komaki R, Wei X, Wang X, et al. Распространенность ишемии миокарда после сопутствующей химиолучевой терапии, обнаруженная с помощью визуализации перфузии миокарда с гейтированием у пациентов с раком пищевода. Дж Нукл Мед. 2006;47(11):1756–62. [PubMed] [Академия Google]
10. Несто Р.В., Ковальчук Г.Ю. Ишемический каскад: временная последовательность гемодинамических, электрокардиографических и симптоматических проявлений ишемии. Ам Джей Кардиол. 1987;59(7):23C–30. doi: 10.1016/0002-9149(87)-5. [PubMed] [CrossRef] [Google Scholar]
11. Neely JR, Rovetto MJ, Oram JF. Утилизация миокардом углеводов и липидов. Prog Cardiovasc Dis. 1972;15(3):289–329. doi: 10.1016/0033-0620(72)
-1. [PubMed] [CrossRef] [Google Scholar] 12. Umezawa R, Takase K, Jingu K, Takanami K, Ota H, Kaneta T, et al. Оценка радиационно-индуцированного повреждения миокарда с помощью сцинтиграфии с йод-123-бета-метил-йодофенилпентадекановой кислотой.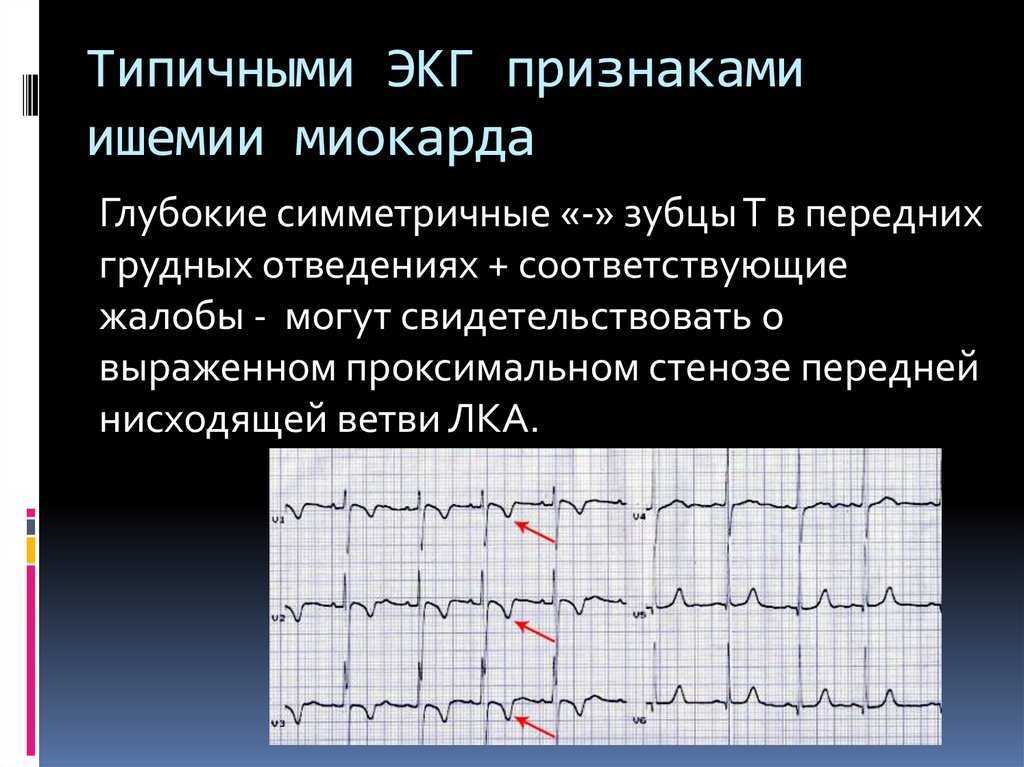 J Радиат Рез. 2013;54(5):880–9. doi: 10.1093/jrr/rrt011. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
J Радиат Рез. 2013;54(5):880–9. doi: 10.1093/jrr/rrt011. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Feng M, Moran JM, Koelling T, Chughtai A, Chan JL, Freedman L, et al. Разработка и проверка атласа сердца для изучения облучения сердца после лечения рака молочной железы. Int J Radiat Oncol Biol Phys. 2011;79(1):10–8. doi: 10.1016/j.ijrobp.2009.10.058. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Yeo UJ, Taylor ML, Supple JR, Smith RL, Dunn L, Kron T, et al. Имеет ли смысл «деформировать» дозу? Трехмерное экспериментальное подтверждение искажения дозы. мед. физ. 2012;39(8): 5065–72. doi: 10.1118/1.4736534. [PubMed] [CrossRef] [Google Scholar]
15. Janssens G, de Xivry JO, Fekkes S, Dekker A, Macq B, Lambin P, et al. Оценка нежестких моделей регистрации межфракционного накопления дозы при лучевой терапии. мед. физ. 2009;36(9):4268–76. doi: 10.1118/1.3194750. [PubMed] [CrossRef] [Google Scholar]
16. Murphy MJ, Salguero FJ, Siebers JV, Staub D, Vaman C. Метод оценки влияния деформируемых неопределенностей регистрации изображений на картирование суточной дозы. мед. физ. 2012;39(2): 573–80. doi: 10.1118/1.3673772. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Метод оценки влияния деформируемых неопределенностей регистрации изображений на картирование суточной дозы. мед. физ. 2012;39(2): 573–80. doi: 10.1118/1.3673772. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Fedorov A, Beichel R, Kalpathy-Cramer J, Finet J, Fillion-Robin JC, Pujol S, et al. 3D Slicer как платформа обработки изображений для Quantitative Imaging Network. Магнитно-резонансная томография. 2012;30(9):1323–41. doi: 10.1016/j.mri.2012.05.001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Murphy K, van Ginneken B, Reinhardt JM, Kabus S, Ding K, Deng X, et al. Оценка методов регистрации на КТ грудной клетки: задача EMPIRE10. IEEE Trans Med Imaging. 2011;30(11):1901–20. doi: 10.1109/TMI.2011.2158349. [PubMed] [CrossRef] [Google Scholar]
19. Seppenwoolde Y, Muller SH, Theuws JC, Baas P, Belderbos JS, Boersma LJ, et al. Зависимость доза-эффект облучения и локальное восстановление перфузии у больных немелкоклеточным раком легкого. Int J Radiat Oncol Biol Phys. 2000;47(3):681–90. doi: 10.1016/S0360-3016(00)00454-5. [PubMed] [CrossRef] [Google Scholar]
Int J Radiat Oncol Biol Phys. 2000;47(3):681–90. doi: 10.1016/S0360-3016(00)00454-5. [PubMed] [CrossRef] [Google Scholar]
20. Tateno M, Tamaki N, Yukihiro M, Kudoh T, Hattori N, Tadamura E, et al. Оценка поглощения жирных кислот при ишемической болезни сердца без инфаркта миокарда. Дж Нукл Мед. 1996;37(12):1981-5. [PubMed] [Google Scholar]
21. Mochizuki T, Murase K, Higashino H, Miyagawa M, Sugawara Y, Kikuchi T, et al. Ишемический «образ памяти» при остром инфаркте миокарда 123I-BMIPP после реперфузионной терапии: сравнение с 99mTc-пирофосфатом и двухизотопной ОФЭКТ 201Tl. Энн Нукл Мед. 2002;16(8):563–8. doi: 10.1007/BF02988634. [PubMed] [CrossRef] [Google Scholar]
22. Jingu K, Nemoto K, Kaneta T, Oikawa M, Ogawa Y, Ariga H, et al. Временное изменение натрийуретического пептида головного мозга после лучевой терапии рака грудной клетки пищевода. Int J Radiat Oncol Biol Phys. 2007;69(5): 1417–23. doi: 10.1016/j.ijrobp.2007.05.054. [PubMed] [CrossRef] [Google Scholar]
23. Hardenbergh PH, Munley MT, Bentel GC, Kedem R, Borges-Neto S, Hollis D, et al. Изменения перфузии сердца у больных раком молочной железы, получавших лучевую терапию и доксорубицин: предварительные результаты. Int J Radiat Oncol Biol Phys. 2001;49(4):1023–8. doi: 10.1016/S0360-3016(00)01531-5. [PubMed] [CrossRef] [Google Scholar]
Hardenbergh PH, Munley MT, Bentel GC, Kedem R, Borges-Neto S, Hollis D, et al. Изменения перфузии сердца у больных раком молочной железы, получавших лучевую терапию и доксорубицин: предварительные результаты. Int J Radiat Oncol Biol Phys. 2001;49(4):1023–8. doi: 10.1016/S0360-3016(00)01531-5. [PubMed] [CrossRef] [Google Scholar]
24. Seemann I, Gabriels K, Visser NL, Hoving S, te Poele JA, Pol JF, et al. Облучение вызывало умеренные изменения сердечной функции мышей, несмотря на прогрессирующее структурное повреждение миокарда и микроциркуляторного русла. Радиотер Онкол. 2012;103(2):143–50. doi: 10.1016/j.radonc.2011.10.011. [PubMed] [CrossRef] [Академия Google]
25. Mulrooney DA, Yeazel MW, Kawashima T, Mertens AC, Mitby P, Stovall M, et al. Сердечные исходы в когорте взрослых, перенесших рак в детстве и подростковом возрасте: ретроспективный анализ когорты, изучавшей выживших после рака у детей. БМЖ. 2009;339:b4606. doi: 10.1136/bmj.b4606. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Lancellotti P, Nkomo VT, Badano LP, Bergler-Klein J, Bogaert J, Davin L, et al. Консенсус экспертов по мультимодальной визуализации сердечно-сосудистых осложнений лучевой терапии у взрослых: отчет Европейской ассоциации сердечно-сосудистой визуализации и Американского общества эхокардиографии. J Am Soc Эхокардиогр. 2013;26(9): 1013–32. doi: 10.1016/j.echo.2013.07.005. [PubMed] [CrossRef] [Google Scholar]
Lancellotti P, Nkomo VT, Badano LP, Bergler-Klein J, Bogaert J, Davin L, et al. Консенсус экспертов по мультимодальной визуализации сердечно-сосудистых осложнений лучевой терапии у взрослых: отчет Европейской ассоциации сердечно-сосудистой визуализации и Американского общества эхокардиографии. J Am Soc Эхокардиогр. 2013;26(9): 1013–32. doi: 10.1016/j.echo.2013.07.005. [PubMed] [CrossRef] [Google Scholar]
27. Tukenova M, Guibout C, Oberlin O, Doyon F, Mousannif A, Haddy N, et al. Роль лечения рака в долгосрочной общей и сердечно-сосудистой смертности после рака у детей. Дж. Клин Онкол. 2010;28(8):1308–15. doi: 10.1200/JCO.2008.20.2267. [PubMed] [CrossRef] [Google Scholar]
28. Demkow U, Stelmaszczyk-Emmel A. Кардиотоксичность химиотерапии на основе цисплатина у пациентов с запущенным немелкоклеточным раком легкого. Респир Физиол Нейробиол. 2013;187(1):64–7. doi: 10.1016/j.resp.2013.03.013. [PubMed] [CrossRef] [Академия Google]
29. Meinardi MT, Gietema JA, van der Graaf WT, van Veldhuisen DJ, Runne MA, Sluiter WJ, et al.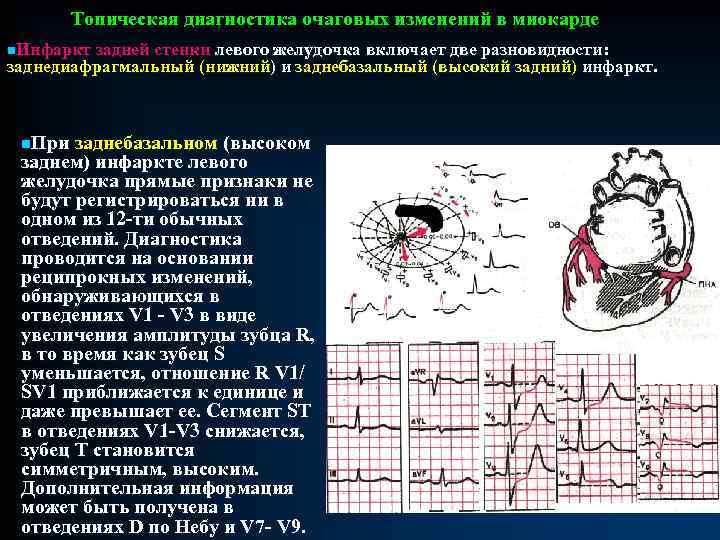 Сердечно-сосудистые заболевания у выживших в течение длительного времени после метастатического рака яичка. Дж. Клин Онкол. 2000;18(8):1725–32. [PubMed] [Google Scholar]
Сердечно-сосудистые заболевания у выживших в течение длительного времени после метастатического рака яичка. Дж. Клин Онкол. 2000;18(8):1725–32. [PubMed] [Google Scholar]
30. Barjaktarovic Z, Schmaltz D, Shyla A, Azimzadeh O, Schulz S, Haagen J, et al. Индуцированная радиацией передача сигналов приводит к нарушению митохондрий в сердце мыши через 4 недели после воздействия рентгеновских лучей. ПЛОС Один. 2011;6(12):e27811. doi: 10.1371/journal.pone.0027811. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Острый инфаркт миокарда является одной из основных причин смерти в развитых странах, с распространенностью около трех миллионов человек во всем мире, при этом ежегодно в Соединенных Штатах умирает более одного миллиона человек. В этом упражнении рассматривается представление, оценка и ведение пациентов с острым инфарктом миокарда и подчеркивается роль межпрофессиональной команды в уходе за этими пациентами.
Цели:
Опишите разницу во времени до пика и продолжительности между тропонином, креатинкиназой МВ и ЛДГ.
Опишите, как обследовать пациента с потливостью и болью в груди, иррадиирующей в двусторонние руки.
Опишите разницу в лечении инфаркта миокарда с подъемом сегмента ST, инфаркта миокарда без подъема сегмента ST и нестабильной стенокардии.
Узнайте, как стратегии межпрофессиональной бригады улучшают координацию межпрофессиональной бригады при оказании помощи пациентам с острым инфарктом миокарда.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Острый инфаркт миокарда является одной из ведущих причин смерти в развитых странах. Распространенность этого заболевания приближается к трем миллионам человек во всем мире, при этом в Соединенных Штатах ежегодно умирает более одного миллиона человек. Острый инфаркт миокарда можно разделить на две категории: ИМ без подъема сегмента ST (NSTEMI) и ИМ с подъемом сегмента ST (ИМпST). Нестабильная стенокардия похожа на NSTEMI. Однако сердечные маркеры не повышены.[1][2][3]
Острый инфаркт миокарда можно разделить на две категории: ИМ без подъема сегмента ST (NSTEMI) и ИМ с подъемом сегмента ST (ИМпST). Нестабильная стенокардия похожа на NSTEMI. Однако сердечные маркеры не повышены.[1][2][3]
ИМ приводит к необратимому повреждению сердечной мышцы из-за недостатка кислорода. ИМ может привести к нарушению диастолической и систолической функции и сделать пациента склонным к аритмиям. Кроме того, ИМ может привести к ряду серьезных осложнений. Суть в том, чтобы реперфузировать сердце и восстановить кровоток. Чем раньше начато лечение (менее 6 часов с момента появления симптомов), тем лучше прогноз.
ИМ диагностируется при наличии двух из следующих критериев:
Симптомы ишемии
Новые изменения сегмента ST или блокада левой ножки пучка Гиса (БЛНПГ)
Наличие патологических зубцов Q на ЭКГ
Наличие внутрикоронарного тромба при вскрытии или ангиографии
Этиологией острого инфаркта миокарда является снижение коронарного кровотока.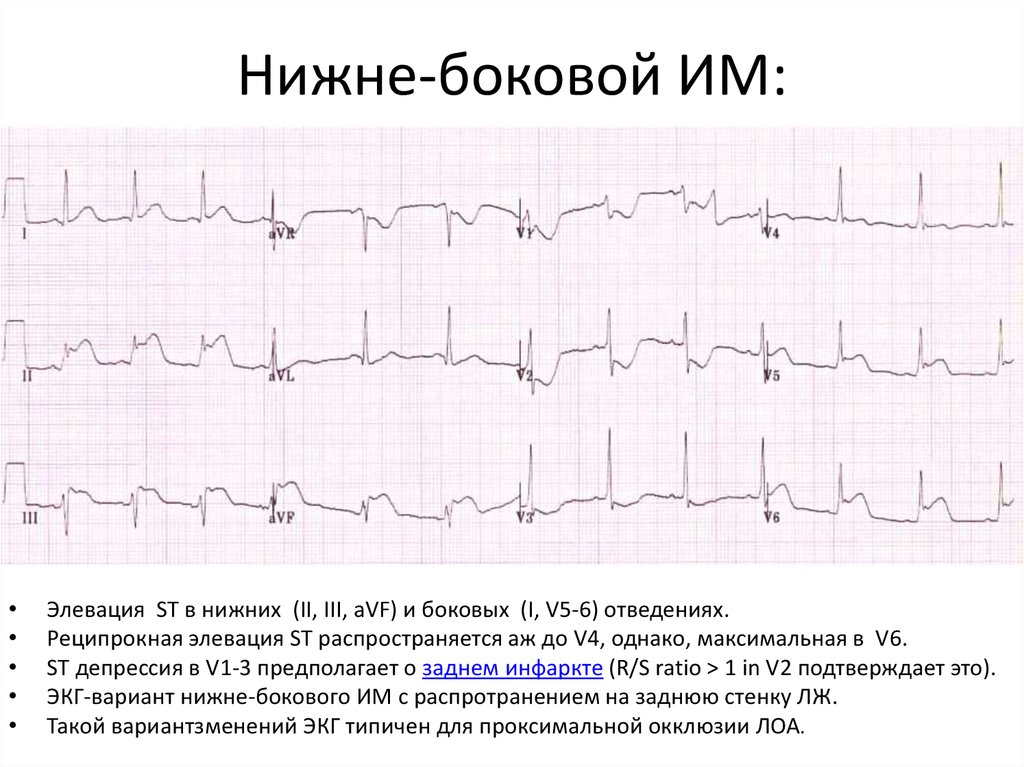 Доступный запас кислорода не может удовлетворить потребность в кислороде, что приводит к ишемии сердца. Снижение коронарного кровотока является многофакторным. Атеросклеротические бляшки классически разрываются и приводят к тромбозу, способствуя резкому снижению кровотока в коронарных артериях. Другие причины снижения оксигенации/ишемии миокарда включают эмболию коронарных артерий, на долю которой приходится 2,9% пациентов, кокаин-индуцированная ишемия, расслоение коронарных артерий и коронарный вазоспазм.[4][5]
Доступный запас кислорода не может удовлетворить потребность в кислороде, что приводит к ишемии сердца. Снижение коронарного кровотока является многофакторным. Атеросклеротические бляшки классически разрываются и приводят к тромбозу, способствуя резкому снижению кровотока в коронарных артериях. Другие причины снижения оксигенации/ишемии миокарда включают эмболию коронарных артерий, на долю которой приходится 2,9% пациентов, кокаин-индуцированная ишемия, расслоение коронарных артерий и коронарный вазоспазм.[4][5]
Немодифицируемые факторы риска
Модифицируемые факторы риска
Smoking
Dyslipidemia
Diabetes mellitus
Hypertension
Obesity
Sedentary lifestyle
Poor oral hygiene
Наличие заболевания периферических сосудов
Повышенный уровень гомоцистеина
Другие причины ИМ
Trauma
Vasculitis
Drug use (cocaine)
Coronary artery anomalies
Coronary artery emboli
Aortic dissection
Excess demand on the heart (hyperthyroidism , анемия)
Среди пациентов, страдающих острым инфарктом миокарда, 70% летальных исходов связаны с окклюзией атеросклеротическими бляшками. Поскольку атеросклероз является преобладающей причиной острого инфаркта миокарда, факторы риска атеросклеротического заболевания часто снижаются при профилактике заболевания. На модифицируемые факторы риска приходится 90% (мужчины) и 94% (женщины) инфарктов миокарда. Модифицируемые факторы риска включают курение сигарет, физические упражнения, гипертонию, ожирение, уровни холестерина, ЛПНП и триглицеридов. Напротив, возраст, пол и семейный анамнез являются неизменяемыми факторами риска развития атеросклероза.[6][7]
Поскольку атеросклероз является преобладающей причиной острого инфаркта миокарда, факторы риска атеросклеротического заболевания часто снижаются при профилактике заболевания. На модифицируемые факторы риска приходится 90% (мужчины) и 94% (женщины) инфарктов миокарда. Модифицируемые факторы риска включают курение сигарет, физические упражнения, гипертонию, ожирение, уровни холестерина, ЛПНП и триглицеридов. Напротив, возраст, пол и семейный анамнез являются неизменяемыми факторами риска развития атеросклероза.[6][7]
Атеросклеротический разрыв приводит к воспалительному каскаду моноцитов и макрофагов, образованию тромбов и агрегации тромбоцитов. Это приводит к снижению доставки кислорода через коронарную артерию, что приводит к снижению оксигенации миокарда. Неспособность продуцировать АТФ в митохондриях приводит к ишемическому каскаду и, следовательно, к апоптозу (гибели клеток) эндокарда или инфаркту миокарда.
За некоторыми исключениями из-за генетической изменчивости коронарные артерии имеют уникальное и диагностическое территориальное распределение. Например, левая передняя нисходящая коронарная артерия снабжает кровью межжелудочковую перегородку, переднебоковую стенку и верхушку желудочка. Левая огибающая артерия кровоснабжает нижнелатеральную стенку. Правая коронарная артерия кровоснабжает правый желудочек. Нижняя стенка кровоснабжается либо левой огибающей, либо правой коронарной артерией.[8]
Например, левая передняя нисходящая коронарная артерия снабжает кровью межжелудочковую перегородку, переднебоковую стенку и верхушку желудочка. Левая огибающая артерия кровоснабжает нижнелатеральную стенку. Правая коронарная артерия кровоснабжает правый желудочек. Нижняя стенка кровоснабжается либо левой огибающей, либо правой коронарной артерией.[8]
Гистология инфаркта миокарда меняется в зависимости от течения болезни. В момент времени 0 микроскопических гистологических изменений нет. При световой микроскопии через 0,5-4 часа выявляется волнистость волокон по периферии ткани. Гликоген истощается. От 4 до 12 часов в миокарде происходит коагуляционный некроз и отек. Через 12–24 часа крупный образец становится темным и пятнистым. При гистологическом исследовании выявляют некроз полос сокращения и преобладание нейтрофилов. На 1-3 сутки происходит потеря ядер, а на 3-7 сутки появляются макрофаги для удаления апоптозных клеток. На 7-10 сутки появляется грануляционная ткань.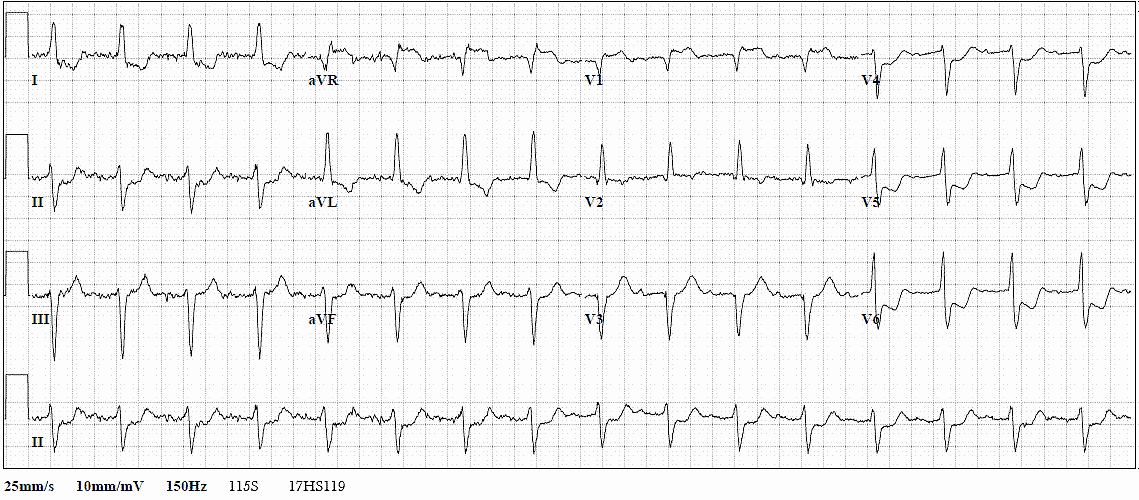 На 10-й день и далее наблюдается отложение коллагена. Через 2 месяца миокард рубцуется.
На 10-й день и далее наблюдается отложение коллагена. Через 2 месяца миокард рубцуется.
Сердечные биомаркеры полезны в диагностике острого инфаркта миокарда, особенно ИМ без подъема сегмента ST. Тропонин является наиболее специфичным лабораторным тестом и имеет две изоформы, I и T. Пик тропонинов приходится на 12 часов и сохраняется в течение семи дней. Креатининкиназа МВ также специфична для миокарда. Он достигает пика в десять часов; однако он нормализуется в течение двух-трех дней. ЛДГ достигает пика через 72 часа и нормализуется через 10-14 часов. В клинической практике ЛДГ не используется для диагностики острого ИМ. Наконец, МБ имеет очень низкую специфичность в отношении миокарда и не используется в клинической практике; быстро поднимается и нормализуется. Высокочувствительный тропонин недавно был одобрен для использования в Соединенных Штатах после тщательного изучения и использования в Европе. Хотя он более чувствителен, чем обычный тропонин, он также менее специфичен. Таким образом, потенциальные проблемы включают многочисленные ложноположительные интерпретации.[3]
Таким образом, потенциальные проблемы включают многочисленные ложноположительные интерпретации.[3]
Анамнез и физикальное обследование часто противоречивы при оценке острого инфаркта миокарда. В анамнезе следует сосредоточить внимание на начале, качестве и сопутствующих симптомах. Недавние исследования показали, что потливость и двусторонняя иррадиирующая боль в руку чаще всего связаны с инфарктом миокарда у мужчин. Сопутствующие симптомы включают:
При физикальном осмотре, что наиболее важно, должны быть отмечены жизненные показатели и внешний вид пациента, включая потоотделение, а также изменения в легких и аускультация сердца.
Частота сердечных сокращений может выявить тахикардию, фибрилляцию предсердий или желудочковую аритмию
Неравные импульсы, если у пациента есть аортальное расслоение
Гровавый давление обычно высоки, но гипотенция, если пациент находится в шоке
Гровавый давление обычно высока, но гипотенция, если пациент находится в шоке
Кровь, обычно высокое, но гипотенция, если пациент находится в шоке
. Обычно высокое, но гипотенция, если у пациента в шоке
Обычно высокое, но гипотенция, если у пациента в шоке
7007777 3
70002 70002 70002 70002 70002
.
Тахипноэ и лихорадка не являются редкостью.
Шейные вены могут быть набухшими, что указывает на правожелудочковую недостаточность
Сердце: латеральное смещение верхушечного толчка, мягкий S1, пальпируемый S4, новый шум митральной регургитации. Громкий голосистолический шум, иррадиирующий на грудину, может свидетельствовать о разрыве межжелудочковой перегородки.
Хрипы и свистящие хрипы часты, если у пациента развился отек легких боль в груди. Женщины часто имеют нетипичные симптомы, такие как боль в животе или головокружение, и могут вообще не ощущать боли в груди. У пожилых пациентов чаще одышка является симптомом инфаркта миокарда. Все эти проявления также должны побуждать к выполнению ЭКГ [9].][10][11]
ЭКГ высокоспецифична для ИМ (от 95% до 97%), но не чувствительна (примерно 30%). Правостороннее, заднее расположение электродов и повторное тестирование ЭКГ могут повысить чувствительность ЭКГ. Например, остроконечные зубцы T на ЭКГ, известные как «сверхострые зубцы T», часто указывают на раннюю ишемию и прогрессируют до подъема сегмента ST. При наличии элевации ST более 2 мм в двух смежных отведениях на ЭКГ (нижние: отведения II, III, aVF; перегородки равны V1, V2; передние: V3, V4; боковые: I, aVL, V5, V6) свидетельствуют об инфаркте миокарда с подъемом сегмента ST. Нередко наблюдаются депрессии сегмента ST, которые визуализируются в противоположных анатомических областях миокарда.
Правостороннее, заднее расположение электродов и повторное тестирование ЭКГ могут повысить чувствительность ЭКГ. Например, остроконечные зубцы T на ЭКГ, известные как «сверхострые зубцы T», часто указывают на раннюю ишемию и прогрессируют до подъема сегмента ST. При наличии элевации ST более 2 мм в двух смежных отведениях на ЭКГ (нижние: отведения II, III, aVF; перегородки равны V1, V2; передние: V3, V4; боковые: I, aVL, V5, V6) свидетельствуют об инфаркте миокарда с подъемом сегмента ST. Нередко наблюдаются депрессии сегмента ST, которые визуализируются в противоположных анатомических областях миокарда.
ЭКГ-диагностика ИМпST может быть затруднена, особенно у пациентов с блокадой левой ножки пучка Гиса и кардиостимуляторами. Sgarbosa описал критерии, которые могут помочь врачу или практикующему врачу в диагностике ИМпST у этих пациентов. Изолированные подъемы сегмента ST в aVR указывают на окклюзию ствола левой коронарной артерии в соответствующих клинических условиях. Wellens отметил глубокие двухфазные зубцы T в V2, V3 и обнаружил, что они часто предсказывают надвигающуюся окклюзию проксимальной левой передней нисходящей артерии, которая может привести к разрушительному инфаркту миокарда передней стенки.
У пациентов с инфарктом миокарда может отсутствовать диагностическая ЭКГ с подъемом сегмента ST. Пациентов с типичной болью в груди следует обследовать на предмет ИМбпST с едва уловимыми отклонениями на ЭКГ, включая депрессию сегмента ST и изменения зубца Т. Здесь также могут быть полезны серийные ЭКГ для поиска динамических изменений. ЭКГ без острых изменений или каких-либо аномалий часто встречается при NSTEMI.
Существуют диагностические руководства, которые могут помочь практикующему врачу определить, полезно ли дальнейшее тестирование для выявления пациентов с NSTEMI. Учитывая низкую чувствительность ЭКГ к ИМпST, тропонины почти повсеместно используются у пациентов с подозрительной историей болезни. Шкала HEART была утверждена и популяризирована. Он использует подозрения клинициста, факторы риска пациента, диагностику ЭКГ и уровень тропонина для определения «уровня риска».
Лабораторные принадлежности
Натрийуретический пептид типа В (BNP) не следует назначать в качестве маркера ИМ, но его лучше использовать для стратификации риска, особенно у пациентов с ИМ, у которых развилась сердечная недостаточность.
Визуализация сердца
Кардиоангиография используется для выполнения чрескожного коронарного вмешательства (ЧКВ) или определения препятствий в коронарных сосудах.
Эхокардиограмма используется для оценки движения стенок, степени аномалии клапана, ишемической митральной недостаточности (МР) и наличия тампонады сердца.
Всем пациентам с ИМпST и NSTEMI требуется немедленно жевать аспирин от 160 мг до 325 мг. Кроме того, пациент должен иметь внутривенный доступ и кислородную поддержку, если насыщение кислородом составляет менее 91%. Опиоиды могут использоваться для контроля боли в дополнение к сублингвальному нитроглицерину, если артериальное давление адекватно.
Лечение ИМпST включает немедленную реперфузию. Предпочтение отдается экстренному чрескожному коронарному вмешательству (ЧКВ). Перед ЧКВ пациенты должны получить двойные антиагреганты, включая внутривенную инфузию гепарина, а также ингибитор рецептора аденозиндифосфата (ингибитор P2Y2), чаще всего тикагрелор. Кроме того, во время чрескожного вмешательства можно вводить ингибитор гликопротеина IIb/IIIa или прямой ингибитор тромбина.
Кроме того, во время чрескожного вмешательства можно вводить ингибитор гликопротеина IIb/IIIa или прямой ингибитор тромбина.
Если чрескожное вмешательство невозможно в течение 90 минут после постановки диагноза ИМпST, следует попытаться провести реперфузию с помощью внутривенного тромболитического агента.
ИМ без подъема сегмента ST у стабильного бессимптомного пациента может оказаться неэффективным при неотложном чрескожном коронарном вмешательстве, и его следует лечить с помощью антитромбоцитарных препаратов. Чрескожное коронарное вмешательство может быть выполнено в течение 48 часов после госпитализации и может привести к снижению госпитальной летальности и сокращению продолжительности пребывания в стационаре. У пациентов с ИМбпST с рефрактерной ишемией или ишемией с гемодинамической или электрической нестабильностью ЧКВ следует выполнять в экстренном порядке.
Перед выпиской по поводу острого инфаркта миокарда пациентам обычно назначают аспирин, высокие дозы статинов, бета-блокаторы и/или ингибиторы АПФ.
Если планируется ЧКВ, оно должно быть выполнено в течение 12 часов. Если предполагается фибринолитическая терапия, ее следует проводить в течение 120 минут. Всем больным рекомендуется парентеральная антикоагулянтная терапия в дополнение к антитромбоцитарной терапии.
Расслоение аорты
Перикардит
Acute gastritis
Acute cholecystitis
Asthma
Esophagitis
Myocarditis
Pneumothorax
Pulmonary embolism
Acute MI still carries a высокий уровень смертности, причем большинство смертей происходит до прибытия в больницу. По меньшей мере 5-10% выживших умирают в течение первых 12 месяцев после ИМ, и около 50% нуждаются в госпитализации в течение того же года. Общий прогноз зависит от степени повреждения мышц. Хорошие результаты наблюдаются у пациентов, которым проводится ранняя перфузионно-тромболитическая терапия в течение 30 минут после прибытия или ЧКВ в течение 9 минут.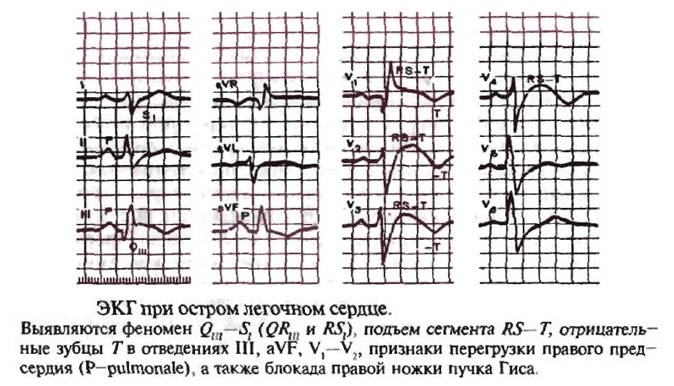 0 минут). Кроме того, исходы хорошие, если фракция выброса сохранена и пациенту начато лечение аспирином, бета-блокаторами и ингибиторами АПФ.
0 минут). Кроме того, исходы хорошие, если фракция выброса сохранена и пациенту начато лечение аспирином, бета-блокаторами и ингибиторами АПФ.
Факторы, которые отрицательно влияют на прогноз:
Диабет
Расширенный возраст
Предыдущий ИМ, Периферийная сосудистая заболевания (PVD), или инсульт
. Demported Repercected
67676767676767676767676 700767676 700767676 700767676 700767676 700767676 700767676 700767676 700767676 700767676 700767676 700767676767676 гг. самый сильный предсказатель)Присутствие застойной сердечной недостаточности (CHF)
Повышенный С-реактивный белок и уровни BNP
депрессия

Аневризма левого желудочка
Аритмии
Эмболы
Пациент должен быть доставлен в отделение неотложной помощи как можно скорее после появления симптомов солевая диета
Записаться на кардиологический реабилитационный центр
Прекратить курить
Соблюдать режим приема лекарств
Лечением острого инфаркта миокарда занимается межпрофессиональная бригада, специализирующаяся исключительно на заболеваниях сердца. Помимо кардиолога, команда обычно состоит из кардиохирурга, интервенционного кардиолога, реаниматолога, специалиста по кардиореабилитации, медсестер интенсивной терапии или кардиологии и физиотерапевтов. Поскольку многие пациенты умирают еще до того, как попадут в больницу, ключевым моментом является информирование пациента о симптомах и своевременное обращение в отделение неотложной помощи.
Фармацевт, практикующая медсестра и поставщики первичной медико-санитарной помощи должны обучать пациентов тому, как принимать нитроглицерин, и если после трех доз облегчения не наступает, то 911 надо звать.
При сортировке медсестра должна немедленно связаться с межпрофессиональной бригадой, поскольку время до реперфузии ограничено. Кардиолог может рассмотреть возможность проведения тромболизиса или ЧКВ в зависимости от продолжительности симптомов и противопоказаний. Все пациенты нуждаются в наблюдении в отделении интенсивной терапии. Медсестры должны быть бдительны в отношении потенциально опасных для жизни осложнений и сообщать бригаде в случае обнаружения отклонений от нормы клинических признаков или лабораторных показателей. Ни один пациент не должен быть преждевременно выписан, поскольку осложнения ИМ могут возникнуть в течение недели после ИМ. После стабилизации больные нуждаются в тщательном обучении медсестрой по снижению факторов риска ишемической болезни сердца. Помимо практикующей медсестры, социальный работник должен быть привлечен для облегчения ухода на дому, кардиореабилитации и необходимости любых вспомогательных услуг, находясь дома. Фармацевт должен обратиться и предоставить информацию о надлежащей дозировке лекарств и обсудить возможные побочные эффекты.
Помимо практикующей медсестры, социальный работник должен быть привлечен для облегчения ухода на дому, кардиореабилитации и необходимости любых вспомогательных услуг, находясь дома. Фармацевт должен обратиться и предоставить информацию о надлежащей дозировке лекарств и обсудить возможные побочные эффекты.
После выписки пациенту необходимо пройти программу кардиореабилитации, соблюдать здоровую диету, бросить курить, воздержаться от употребления алкоголя, снизить массу тела, снизить уровень холестерина и глюкозы в крови. Пациент должен быть информирован о важности соблюдения режима приема лекарств для снижения артериального давления и уровня холестерина в крови. [15][16][17][Уровень 2] Фармацевты просматривают назначенные лекарства, проверяют взаимодействие и обучают пациентов важности соблюдения режима. [Уровень 5]
Исходы
Острый инфаркт миокарда по-прежнему имеет высокую смертность вне стационара. Данные показывают, что не менее трети пациентов умирают до поступления в больницу, а еще 40-50% умирают по прибытии. Еще 5-10% больных умирают в течение первых 12 месяцев после перенесенного инфаркта миокарда. Повторная госпитализация встречается примерно у 50% пациентов в течение первых 12 месяцев после первого ИМ. Общий прогноз зависит от фракции выброса, возраста и других сопутствующих заболеваний. Те, кто не подвергается реваскуляризации, будут иметь худший результат по сравнению с пациентами, которым проводится реваскуляризация. Наилучший прогноз у пациентов с ранней и успешной реперфузией и сохраненной функцией левого желудочка [18, 19].][20] [Уровень 2]
Еще 5-10% больных умирают в течение первых 12 месяцев после перенесенного инфаркта миокарда. Повторная госпитализация встречается примерно у 50% пациентов в течение первых 12 месяцев после первого ИМ. Общий прогноз зависит от фракции выброса, возраста и других сопутствующих заболеваний. Те, кто не подвергается реваскуляризации, будут иметь худший результат по сравнению с пациентами, которым проводится реваскуляризация. Наилучший прогноз у пациентов с ранней и успешной реперфузией и сохраненной функцией левого желудочка [18, 19].][20] [Уровень 2]
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Образец, показывающий инфаркт миокарда в левом желудочке и межжелудочковой перегородке. Звездочка (*) также указывает на гипертрофию левого желудочка. Предоставлено Wikimedia Commons (CC by 4.0) https://creativecommons.org/licenses/by/4. 0/
0/
Предупреждающие признаки сердечного приступа (инфаркта миокарда) у женщин. Предоставлено Министерством здравоохранения США и Управлением социальных служб по вопросам женского здоровья
ЭКГ, показывающая волны Парди, указывающие на острый инфаркт миокарда в нижних отведениях II, III и aVF с реципрокными изменениями в переднебоковых отведениях. Предоставлено Wikimedia Commons, Glenlarson (Public Domain-Self)
Чреспищеводная эхокардиография, тромбоэмболия, легочная артерия, легочная эмболия, тромбоэмболия, правая легочная артерия, TE, RPA, острое повышение сегмента ЭКГ, имитирующее инфаркт миокарда у пациента с легочная эмболия. Внесите свой вклад (подробнее...)
Nascimento BR, Brant LCC, Marino BCA, Passaglia LG, Ribeiro ALP. Внедрение систем лечения инфаркта миокарда в странах с низким/средним уровнем дохода. Сердце. 2019 янв; 105(1):20-26. [PubMed: 30269080]
Барбери С., ван ден Хондел К.Е. Использование сердечного тропонина Т (cTnT) в посмертной диагностике острого инфаркта миокарда и внезапной сердечной смерти: систематический обзор. Междунар. криминалистики. 2018 ноябрь;292:27-38. [PubMed: 30269044]
Алаур Б., Лью Ф., Кайер Т.Е. Сердечный тропонин - проблемы диагностики и влияние на сердечно-сосудистые заболевания. Энн Мед. 2018 декабрь; 50 (8): 655-665. [PubMed: 30265127]
Массберг С., Ползин А. [Обновление рекомендаций ESC 2017: Двойная антитромбоцитарная терапия]. Dtsch Med Wochenschr. 2018 авг; 143(15):1090-1093. [PubMed: 30060279]
Шин А.Дж. «От атеросклероза к атеротромбозу: от немой хронической патологии к острому критическому событию». Преподобный Мед Льеж. 2018 май; 73(5-6):224-228. [В паблике: 29926559]. , Ньюби Л.К., Сабатин М.С., Джульяно Р.П. Способы и сроки смерти у 66 252 пациентов с острым коронарным синдромом без подъема сегмента ST, включенных в 14 исследований TIMI. Eur Heart J. 07 ноября 2018 г.; 39 (42): 3810-3820. [Статья бесплатно PMC: PMC6220126] [PubMed: 30239711]
Eur Heart J. 07 ноября 2018 г.; 39 (42): 3810-3820. [Статья бесплатно PMC: PMC6220126] [PubMed: 30239711]
Deng D, Liu L, Xu G, Gan J, Shen Y, Shi Y, Zhu R, Lin Y. Эпидемиология и сывороточные метаболические характеристики Пациенты с острым инфарктом миокарда в центрах боли в груди. Иран J Общественное здравоохранение. 2018 июль; 47 (7): 1017-1029. [Бесплатная статья PMC: PMC6119561] [PubMed: 30182001]
Haig C, Carrick D, Carberry J, Mangion K, Maznyczka A, Wetherall K, McEntegart M, Petrie MC, Eteiba H, Lindsay M, Худ С., Уоткинс С., Дэви А., Махрус А., Морди И., Ахмед Н., Тенг Юэ Мэй В., Форд И., Радженович А., Уэлш П., Саттар Н., Олдройд К.Г., Берри С. Текущее курение и прогноз после острого сегмента ST Подъемный инфаркт миокарда: новые патофизиологические данные. JACC Cardiovasc Imaging. 2019 Июн;12(6):993-1003. [Бесплатная статья PMC: PMC6547246] [PubMed: 30031700]
Алькесар-Арбе А., Санчис Дж. , Гильен Э., Бардахи А., Миро Т., Ордоньес-Льянос Дж. Сердечный тропонин в диагностике, измерение и интерпретация острого инфаркта миокарда в отделении неотложной помощи: консенсусное заявление. Чрезвычайные ситуации. 2018 окт; 30 (5): 336-349. [PubMed: 30260119]
, Гильен Э., Бардахи А., Миро Т., Ордоньес-Льянос Дж. Сердечный тропонин в диагностике, измерение и интерпретация острого инфаркта миокарда в отделении неотложной помощи: консенсусное заявление. Чрезвычайные ситуации. 2018 окт; 30 (5): 336-349. [PubMed: 30260119]
Перера М., Аггарвал Л., Скотт И.А., Логан Б. Полученный уход по сравнению с уходом за пациентами, госпитализированными с болью в груди, возможного сердечного происхождения, под руководством ADP. Int J Gen Med. 2018;11:345-351. [Бесплатная статья PMC: PMC6128279] [PubMed: 30214268]
Райли Р.Ф., Миллер К.Д., Рассел Г.Б., Солиман Э.З., Хистанд Б.К., Херрингтон Д.М., Малер С.А. Полезность серийных электрокардиограмм в 12 отведениях для прогнозирования 30-дневных исходов у пациентов с недифференцированной болью в груди (исследование ASAP CATH). Ам Джей Кардиол. 01 августа 2018 г .; 122 (3): 374–380. [PubMed: 30196932]
Ларсон Э.А., Герман Д. М., Шатцель Дж., ДеЛогери Т.Г. Антикоагулянтная терапия у кардиологических больных: краткий обзор. Евр Дж Гематол. 2019Январь; 102(1):3-19. [PubMed: 30203452]
М., Шатцель Дж., ДеЛогери Т.Г. Антикоагулянтная терапия у кардиологических больных: краткий обзор. Евр Дж Гематол. 2019Январь; 102(1):3-19. [PubMed: 30203452]
Bath PM, Woodhouse LJ, Appleton JP, Beridze M, Christensen H, Dineen RA, Flaherty K, Duley L, England TJ, Havard D, Heptinstall S, James M, Kasonde C, Кришнан К., Маркус Х.С., Монтгомери А.А., Покок С., Рэндалл М., Ранта А., Робинсон Т.Г., Скатт П., Венейблс Г.С., Спригг Н. Тройная антитромбоцитарная терапия по сравнению с рекомендациями для предотвращения рецидива после острого ишемического инсульта или транзиторной ишемической атаки: ТАРДИС РКИ. Оценка медицинских технологий. 2018 авг; 22 (48): 1-76. [Бесплатная статья PMC: PMC6139477] [PubMed: 30179153]
Adamski P, Adamska U, Ostrowska M, Navarese EP, Kubica J. Оценка текущей и появляющейся антитромботической терапии, доступной в настоящее время для лечения острого коронарного синдрома у пожилых людей. Эксперт Опин Фармаколог. 2018 сен;19(13):1415-1425. [PubMed: 30132731]
2018 сен;19(13):1415-1425. [PubMed: 30132731]
Aeyels D, Seys D, Sinnaeve PR, Claeys MJ, Gevaert S, Schoors D, Sermeus W, Panella M, Bruyneel L, Vanhaecht K. Управление улучшением качества в больнице: Анализ важности и эффективности для определения приоритетов лечения инфаркта миокарда с подъемом сегмента ST. Eur J Cardiovasc Nurs. 2018 авг; 17 (6): 535-542. [В паблике: 29448818]
Швааб Б. [Кардиореабилитация]. Реабилитация (Штутг). 2018 Апрель; 57 (2): 117-126. [PubMed: 29216666]
El Hajj MS, Jaam MJ, Awaisu A. Влияние фармацевта на приверженность лечению и сердечно-сосудистые исходы у пациентов после острого коронарного синдрома: систематический обзор. Рез Социал Адм Фарм. 2018 июнь; 14 (6): 507-520. [PubMed: 28641999]
Stone GW, Ellis SG, Gori T, Metzger DC, Stein B, Erickson M, Torzewski J, Williams J, Lawson W, Broderick TM, Kabour A, Piegari G, Cavendish J, Bertolet B, Choi JW, Marx SO, Généreux P, Kereiakes DJ.