2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Температура при инсульте
После инсульта у некоторых пациентов меняется температура тела. Если после ишемического кровоизлияния она опускается ниже нормальных показателей 36,6°С, это считается положительным признаком. Жар после геморрагического удара — опасное состояние, которое требует неотложной помощи врача. Дальше мы расскажем подробнее о нормальных и критических показателях температуры после мозгового кровоизлияния, перечислим причины жара, возможные осложнения и методы первой помощи пациенту.
Бывает температура центрального генеза, то есть нарушение регуляции на фоне огромного стресса в мозге, мозговой катастрофы — инсульта. При этом нарушается нейромедиаторный баланс и возникает лихорадка центрального генеза.
Второй вариант — присоединение какой-то вторичной тематики: инфекционное осложнение, пневмония, мочевая инфекция. Бывает, что в первые сутки что-то прицепляется к пациенту, если он ослаблен.
Поделиться:
Нормальная температура после инсульта зависят от его формы. После ишемического удара нормой считается показатель 36,6°С или немного ниже. Незначительное понижение — благоприятный показатель, это говорит о выздоровлении пациента.
После геморрагического инсульта нормальная температура колеблется от 36,6°С до 37,5°С. Показатели выше считаются патологией. Дальнейший подъем температуры указывает на степень инсульта:
40°С — критическая температура. Когда жар усиливается, сворачивается белок в тканях и крови, наступают необратимые изменения. С большой вероятностью пациент может впасть в кому или умереть.
Бортневский А. Е. Рентгенолог • стаж 17 лет
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 28 Ноября 2022 года
Москалева В. В. Редактор • Журналист • Опыт 10 лет
В. Редактор • Журналист • Опыт 10 лет
Размещенные на сайте материалы написаны авторами с медицинским образованием и специалистами компании ЦМРТ
Подробнее
Понравилась статья?
Подпишитесь, чтобы не пропустить следующую и получить уникальный подарок от ЦМРТ.
Нажимая на кнопку, я принимаю соглашение на обработку моих данных.
круглосуточная запись по тел.
+7 (812) 748-59-05
Нужна предварительная консультация? Оставьте свои данные, мы вам перезвоним и ответим на все вопросы
Информация на сайте является ознакомительной, проконсультируйтесь с лечащим врачом
Вашa заявка была отправлена,
наш оператор перезвонит Вам
Мы вам перезвоним и ответим на все вопросы
ВАше имя
телефон
Нажимая на кнопку, я принимаю соглашение на обработку моих данныхЗапишем на услугу или на приём к врачу. Оператор свяжется с вами в течение двух минут.
Оператор свяжется с вами в течение двух минут.
ВАше имя
телефон
ВАше имя
телефон
Ваш вопрос
Прислать ответ на e-mail
Публиковать анонимно
Нажимая на кнопку, я принимаю соглашение на обработку моих данных. Ваш вопрос может быть опубликован на сайте.
Вашa заявка была отправлена,
наш оператор перезвонит Вам
Главная » Все конференции » Архив конференций / Conferences' Archive » III Всероссийская неделя медицинской науки с международным участием » 75-я студенческая межрегиональная научно-практическая конференция «Молодые ученые — здравоохранению» » Скорая неотложная и анестезиолого-реанимационная помощь » Гипертермия у выживших больных при инсульте
ID: 2014-05-4-A-3663
Оригинальная статья
Калинина Ю. С.
С.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава России
Научный руководитель: к.м.н., доцент Котов С.Н.
гипертермия, инфаркт мозга, внутримозговое кровоизлияние
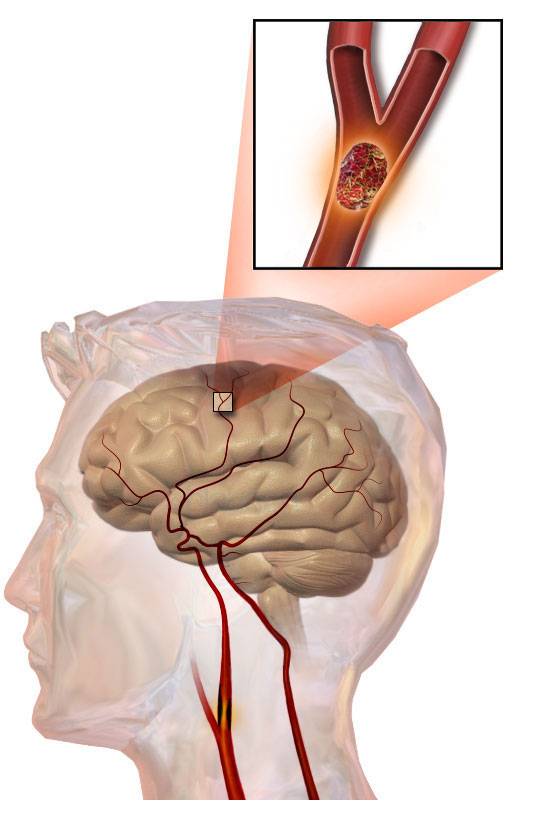
Острое нарушение мозгового кровообращения является актуальной и прогрессирующей медико-социальной проблемой и остается одной из ведущих причин смертности и заболеваемости [1, 2, 3].
Одной из причин, влияющих на прогноз и исход инсульта, продолжительность пребывания в стационаре и отделении реанимации и интенсивной терапии (ОРИТ), является гипертермия. В отделениях интенсивной терапии у больных с мозговым повреждением различной этиологии гипертермия регистрируется в 40-70% случаев [4, 5, 6]. При инфаркте мозга гипертермия встречается в 18-61% случаев [4, 7].
Отягощающее влияние гипертермии у больных с инсультом на исход и прогноз заболевания, а также на увеличение сроков пребывания в стационаре рассматривается как в обзорных статьях, так и в мета-анализах [4, 5, 8]. Большинство авторов высказывают мысль о повреждающем воздействии гипертермии при любом повреждении головного мозга через механизмы нарушения целостности гематоэнцефалического барьера, снижения стабильности клеточных мембран, нарушения работы ферментов и др. [4, 8, 9]. Однако до настоящего времени недостаточно изучены причинно следственные отношения развития гипертермии у больных с инсультом [8].
Большинство авторов высказывают мысль о повреждающем воздействии гипертермии при любом повреждении головного мозга через механизмы нарушения целостности гематоэнцефалического барьера, снижения стабильности клеточных мембран, нарушения работы ферментов и др. [4, 8, 9]. Однако до настоящего времени недостаточно изучены причинно следственные отношения развития гипертермии у больных с инсультом [8].
Цель работы – уточнить причины и динамику температуры тела в зависимости от вида инсульта и наличия или отсутствия гнойно-воспалительных осложнений (ГВО) у выживших больных.
Проведен ретроспективный анализ историй болезни 89 пациентов с инсультом в возрасте 50-86 лет (табл. 1). Деление пациентов на группы и подгруппы отражено на таб. 3.
В исследование включались больные только в остром периоде инсульта. Пациенты поступившие с острым нарушением мозгового кровообращения из других стационаров, тем более, с имеющимися гнойно-воспалительными осложнениями, не включались в исследование, так как у данных больных отсутствовали данные о температурной реакции на начальном периоде заболевания.
Верификация инсульта проводилась на основе Приказа Минздравсоцразвития РФ от 01.08.2007 N 513 «Об утверждении стандарта медицинской помощи больным с инсультом (при оказании специализированной помощи)». Компьютерная томография и/или магнитно-резонансная томография выполнялись в 1-3 сутки при поступлении в стационар однократно и, по показаниям, повторно.
Для обозначения повышения температуры тела использовали термин гипертермия. В МБК-10 термины гипертермия, лихорадка и пирексия сведены вместе и представлены в одной рубрике – R50.9. С целью удобства сравнения групп больных с инфарктом мозга и внутримозговым кровоизлиянием за гипертермию принимали значение аксиллярной температуры за 37,2°С [3, 7]. Для оценки гипертермии использовали общеизвестную для врачей классификацию повышения температуры тела из пропедевтики внутренних болезней [10].
Измерение аксиллярной температуры проводилось 4-8 раз в сутки. Из полученных показателей температуры выбирали максимальное значение, которое и использовали для составления температурных кривых за все время пребывания пациентов в стационаре. Регистрация температуры проводилась с помощью прикроватного мониторы МПР 6-03 «Тритон» с использованием температурных датчиков.
Регистрация температуры проводилась с помощью прикроватного мониторы МПР 6-03 «Тритон» с использованием температурных датчиков.
Дифференциальную диагностику инфекционной гипертермии от центральной проводили по следующим критериям: абсолютной величины гипертермии, цикличности температурной реакции, эффективности антипиретической терапии, взаимосвязи температурной реакции с гнойно-воспалительными осложнениями, динамикой температурной реакции в зависимости от появления или стихания ГВО.
Коррекцию гипертермии проводили согласно общепринятым рекомендациям ведущих учреждений НИИ нейрохирургии им. Н.Н. Бурденко, НИИ скорой помощи им. Н.В. Склифосовского, Военно-медицинской Академии и НИИ им. А.Л.Поленова [11]. Использовали физические и фармакологические методы купирования гипертермии. Однако, несмотря на проводимую терапию, в ряде случаев у пациентов сохранялась стойкая гипертермия. В иных случаях эффект от проводимой терапии регистрировался отсрочено. В связи с этим оценивали такие показатели как продолжительность гипертермии (час), продолжительность некупируемой гипертермии (час). Дополнительно фиксировали начало гипертермии (час), продолжительность гипертермии (сутки).
Дополнительно фиксировали начало гипертермии (час), продолжительность гипертермии (сутки).
Для оценки влияния инфекционного компонента в гипертермическом синдроме вели учет структуры и количества ГВО. Гнойно-воспалительные осложнения делили на интракраниальные и экстракраниальные. Обязательным условием включения данных пациентов в подгруппы больных с гнойно-воспалительными осложнениями была регистрация SIRS (Bone R.C., 1992).
Статистический анализ и построение графиков проводили с помощью программы Microsoft Office Excel 2007.
При сличении графиков динамики температуры выживших больных с внутримозговым кровоизлиянием и инфарктом мозга прослеживается различие в сторону более высокой суточной температуры у больных с кровоизлиянием (рис. 1). Из графика следует, что повышение температуры тела сохраняется у большинства больных в течение первых 6 дней, причем у больных с кровоизлиянием за данный отрезок времени фиксируется более крутая температурная кривая. Крутизна подъема кривой обусловлена не только высокими абсолютными цифрами гипертермии у больных в группе с кровоизлиянием, но и большим процентом температурящих больных по сравнению с пациентами с инфарктом мозга (табл. 1). Графическая кривая также наглядно демонстрирует значимое увеличение продолжительности пребывания больных с ВК в стационаре (на 3,8 дней, р<0,05) по сравнению с больными с ИМ.
Крутизна подъема кривой обусловлена не только высокими абсолютными цифрами гипертермии у больных в группе с кровоизлиянием, но и большим процентом температурящих больных по сравнению с пациентами с инфарктом мозга (табл. 1). Графическая кривая также наглядно демонстрирует значимое увеличение продолжительности пребывания больных с ВК в стационаре (на 3,8 дней, р<0,05) по сравнению с больными с ИМ.
Температурная кривая больных с инфарктом мозга в подгруппе с ГВО указывает на постепенное повышение аксиллярной температуры тела, начиная с 4 суток, с максимумом подъема на 12-14 сутки (рис. 2). При этом гипертермия начинает фиксироваться с седьмых суток, что совпадает со сроками выявления гнойно-воспалительных осложнений у больных с инфарктом мозга (табл. 2) и достоверно (р<0,05) позже развития гипертермии у больных без ГВО (табл. 1). Пациенты с гнойно-воспалительными осложнениями достоверно дольше (на 3,6 сут, р<0,05) находились в отделении реанимации и значимо позже (на 5,3 сут, р<0,05) выписывались из больницы (табл. 1).
1).
Динамика температуры у выживших больных с внутримозговым кровоизлиянием наглядно демонстрирует начальное повышение аксиллярной температуры в обеих подгруппах и повторное повышение только у больных в подгруппе с ГВО (рис. 3). Табличный материал в данном случае не отражает всей полноты картины, так как показывает лишь суммарные сроки начала и продолжительности гипертермии (табл. 1).
У больных с внутримозговым кровоизлиянием с гнойно-воспалительными осложнениями отмечается достоверное (р<0,05) увеличение продолжительности сроков гипертермии (табл. 1), так как у пациентов данной подгруппы повышение температуры регистрировалось в связи с мозговым повреждением, а также, повторно, при возникновении гнойно-воспалительных осложнений. Также в данной подгруппе увеличивались сроки пребывания в стационаре (на 4,5 сут, р>0,05) и в отделении реанимации (на 5,2 сут, р<0,05) (табл. 1). При этом корреляционный анализ показал связь гипертермии с продолжительностью пребывания больных в отделении реанимации (r=0,62) и стационаре (r=0,58).
На продолжительность пребывания в отделении реанимации и стационаре влияют не только вид инсульта, но и развитие ГВО. Полученные данные показывают влияние гнойно-воспалительных осложнений на увеличение сроков пребывания пациентов в отделении реанимации и стационаре как у больных с инфарктом мозга, так и у пациентов с ВК.
Гипертермия у больных с ВК имеет более высокие абсолютные значения по сравнению с пациентами с инфарктом мозга. Данный факт объясняет большее значение гипертермии в увеличении сроков пребывания больных с ВК в стационаре и отделении реанимации.
У выживших больных с ИМ и ВК гипертермия преимущественно детерминирована развитием ГВО. Гипертермия достоверно увеличивает сроки пребывания выживших больных в отделении реанимации и стационаре независимо от вида инсульта.
1. Гусев Е.И., Скворцова В.И., Стаховская Л.В. Проблема инсульта в Российской Федерации: время активных действий. Журнал неврологии и психиатрии 2007; 6: 4–10.
Журнал неврологии и психиатрии 2007; 6: 4–10.
2. Суслина, З.А., Варакин Ю.Я., Верещагин Н.В. Сосудистые заболевания головного мозга: Эпидемиология. Основы профилактики. М: МЕДпресс-информ; 2009.
3. Saini M., Saqqur M., Kamruzzaman A., et al. VISTA Investigators. Effect of hyperthermia on prognosis after acute ischemic stroke. Stroke 2009; 40(9): 3051-3059.
4. Hajat C., Hajat S., Sharma P. Effect of poststroke pyrexia on stroke outcome: a meta-analysis of studies in patients. Stroke 2000; 31: 410-414.
5. Wartenberg K.E., Schmidt J.M., et al. Impact of medial complication on outcome after subarachnoid hemorrhage. Crit. Care Med. 2006; 34: 617-613.
6. Seo W.K., Yu S.W., et al. The impact of hyperthermia and infection on acute ischemic stroke patients in the intensive care unit. Neurocrit. Care 2008; 9: 183-188.
7. Phipps M.S., Desai R.A., Wira C., Bravata D.M. Epidemiology and Outcomes of Fever Burden Among Patients With Acute Ischemic Stroke. Stroke 2011; 42: 3357-3362.
Stroke 2011; 42: 3357-3362.
8. Greer D.M., Funk N.L., Reaven N.L., et al. Impact of fever on outcome in patients with stroke and neurologic injury. A comprehensive meta-analysis. Stroke 2008; 39(11): 3029-3035.
9. Stocchetti N., Protti A., Impact of pyrexia on neurochemistry and cerebral oxygenation after acute brain injury. J. Neurol. Neursurg. Psychiatry 2005; 76: 1135-1139.
10. Мухин Н.А., Моисеев В.С. Пропедевтика внутренних болезней: Учебник. М.: ГЭОТАР-МЕД; 2004.
11. http://icjcorp.ru/2008-02-08.html
Таблица 1.
Сравнение основных параметров гипертермического синдрома и показателей
связанных с гипертермией у выживших больных с ИМ и ВК
| Инфаркт мозга | ВК | |||
| Количество больных, абс. | 50 | 39 | ||
| Возраст больных, годы | 67,6±8,9 | 58,2±11,3 | ||
| Доля температурящих больных, абс. (%) | 20 (40) | 21 (54) | ||
| Больные без ГВО | Больные с ГВО | Больные без ГВО | Больные с ГВО | |
| 1 | 2 | 3 | 4 | |
| Количество больных, абс. | 42 (84) | 8 (16) | 30 (77) | 9 (23) |
| Возраст больных, годы | 67,1±8,2 | 70±13,7 | 57,7±12,6 | 60±6,5 |
| Критерий Стьюдента | p1-2>0,05 | p3-4>0,05 | ||
| Сроки пребывания в стационаре, дни | 16,4±3,0 | 21,7±3,0 | 20,2±2,8 | 24,7±4,5 |
| Критерий Стьюдента | p1-2<0,05 | p3-4>0,05 | ||
| Сроки пребывания в реанимации, дни | 1,4±0,8 | 5±2,6 | 2,1±1,1 | 7,3±3,1 |
| Критерий Стьюдента | p1-2<0,05 | p3-4<0,05 | ||
| Размеры очага поражения, см3 | 32,5±38,4 | 39,9±52,9 | 11,8±6,3 | 9,9±4,4 |
| Критерий Стьюдента | p1-2>0,05 | p3-4>0,05 | ||
| Количество больных с дислокацией срединных структур, абс. | 0 (0) | 2 (25) | 15 (50) | 6 (66) |
| Доля температурящих больных, абс. (%) | 12 (28) | 8 (100) | 12 (40) | 9 (100) |
| Начало гипертермии, сутки | 2,4±0,9 | 7,7±2,7 | 2,6±1,5 | 7±5,5 |
| p1-2<0,05 | p3-4<0,05 | |||
| Продолжительность гипертермии, сутки | 2,1±1,5 | 6,2±2,6 | 2,5±1,3 | 8±3,5 |
| p1-2<0,05 | p3-4<0,05 | |||
Таблица 2.
Структура гнойно-воспалительных осложнений и сроки их выявления у
выживших больных с ИМ и ВК
| Группы больных | Инфаркт мозга | ВК |
| Количество больных, абс. (%) | 8 (16) | 9 (23) |
| Количество ГВО на больного | 1,2±0,5 | 1,3±0,5 |
| Сроки регистрации, сутки | 9,7±2,9 | 11,7±4,6 |
| Структура ГВО | Частота встречаемости, % | |
| 1. | ||
| Менингит | ||
| 2. Экстракраниальные ГВО | ||
| Пневмония | 11 | |
| Гнойный трахеобронхит | 62,5 | 33 |
| Инфекция мочевыводящих путей | 75 | 22 |
| Пролежни | 50 | 22 |
<p>
Рисунок 1.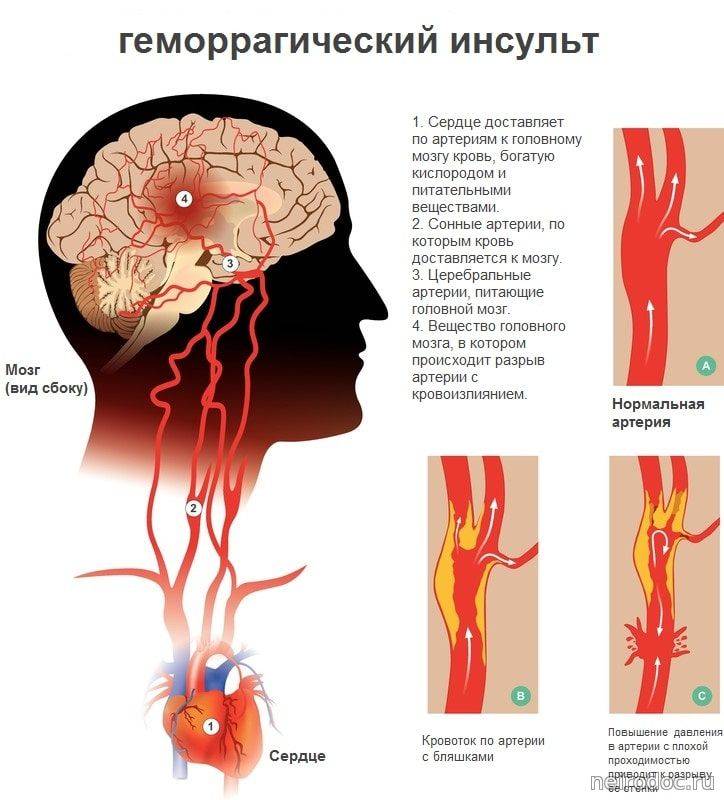 Сравнение динамики температуры тела у выживших больных с ИМ и ВК без ГВО</p>
Сравнение динамики температуры тела у выживших больных с ИМ и ВК без ГВО</p>
<p> Рисунок 2. Сравнение динамики температуры тела у выживших больных с ИМ в зависимости от наличия или отсутствия ГВО</p>
<p> Рисунок 3. Сравнение динамики температуры тела у выживших больных с ВК в зависимости от наличия или отсутствия ГВО</p>
2014-05-4-A-3663.pdf
1. Sessler DI. Терморегуляторные защитные механизмы. Крит Уход Мед. 2009;37(7 доп.):S203–10. [PubMed] [Google Scholar]
2. Azzimondi G, Bassein L, Nonino F, et al. Лихорадка при остром инсульте ухудшает прогноз. Перспективное исследование. Инсульт. 1995;26:2040–3. [PubMed] [Google Scholar]
3. Castillo J, Davalos A, Marrugat J, Noya M. Сроки лихорадочного поражения головного мозга при остром ишемическом инсульте. Инсульт. 1998; 29: 2455–60. [PubMed] [Академия Google]
[PubMed] [Академия Google]
4. Хиндфельт Б. Прогностическое значение субфебрилитета и лихорадки при ишемическом инфаркте мозга. Акта Нейрол Сканд. 1976; 53: 72–79. [PubMed] [Google Scholar]
5. Кумрал Э., Тарлачи С., Акарер А. Влияние этиологии и топографии поражения на температуру тела в начале инсульта. J Инсульт Цереброваскулярная дис. 2001; 10: 150–6. [PubMed] [Google Scholar]
6. Castillo J, Martinez F, Leira R, et al. Смертность и заболеваемость острым инфарктом мозга, связанные с температурой и базальными аналитическими параметрами. Цереброваскулярная дис. 1994;4:66–71. [Google Scholar]
7. Reith J, Jorgensen HS, Pedersen PM, et al. Температура тела при остром инсульте: связь с тяжестью инсульта, размером инфаркта, смертностью и исходом. Ланцет. 1996; 347: 422–5. [PubMed] [Google Scholar]
8. Хаджат С., Хаджат С., Шарма П. Влияние постинсультной лихорадки на исход инсульта: метаанализ исследований у пациентов. Инсульт. 2000;31:410–4. [PubMed] [Google Scholar]
9. Greer DM, Funk SE, Reaven NL, et al. Влияние лихорадки на исход у пациентов с инсультом и неврологическими повреждениями: всесторонний метаанализ. Инсульт. 2008;39: 3029–35. [PubMed] [Google Scholar]
Greer DM, Funk SE, Reaven NL, et al. Влияние лихорадки на исход у пациентов с инсультом и неврологическими повреждениями: всесторонний метаанализ. Инсульт. 2008;39: 3029–35. [PubMed] [Google Scholar]
10. Мерсер Дж. Глоссарий терминов по тепловой физиологии, третье издание. Jpn J Physiol. 2001; 51: 245–80. [Google Scholar]
11. Клюгер М.Дж. Лихорадка снова. Педиатрия. 1992; 90: 846–50. [PubMed] [Google Scholar]
12. Kluger MJ. Лихорадка: актуальная тема. Новости физиол. 1986; 1: 25–27. [Google Scholar]
13. Kozak W, Kluger MJ, Tesfaigzi J, et al. Молекулярные механизмы лихорадки и эндогенного антипиреза. Анналы НЯ акад. 2000;917:121–34. [PubMed] [Google Scholar]
14. Ким Дж.С. Цитокины и молекулы адгезии при инсульте и связанных с ним заболеваниях. J Neurol Sci. 1996; 137: 69–78. [PubMed] [Google Scholar]
15. Baena RC, Busto R, Dietrich WD, et al. Гипертермия, отсроченная на 24 часа, усугубляет повреждение нейронов в гиппокампе крыс после глобальной ишемии. Неврология. 1997; 48: 768–73. [PubMed] [Google Scholar]
Неврология. 1997; 48: 768–73. [PubMed] [Google Scholar]
16. Dietrich WD, Busto R, Valdes I, Loor Y. Эффекты нормотермической и легкой гипертермической ишемии переднего мозга у крыс. Инсульт. 1990;21:1318–25. [PubMed] [Google Scholar]
17. Dietrich WD, Halley M, Valdes I, Busto R. Взаимосвязь между повышенной проницаемостью сосудов и острым повреждением нейронов после температурно-контролируемой ишемии головного мозга у крыс. Акта Нейропатол. 1991; 81: 615–25. [PubMed] [Google Scholar]
18. Maier CM, Ahern K, Cheng ML, et al. Оптимальная глубина и продолжительность легкой гипотермии в фокальной модели преходящей церебральной ишемии: влияние на неврологический исход, размер инфаркта, апоптоз и воспаление. Инсульт. 1998;29:2171–80. [PubMed] [Google Scholar]
19. Hanstock CC, Boisvert DP, Bendall MR, Allen PS. In vivo оценка очаговых изменений лактата в головном мозге с помощью протонной спектроскопии ЯМР. J Cereb Blood Flow Metab. 1988; 8: 208–14. [PubMed] [Google Scholar]
20. Oddo M, Frangos S, Milby A, et al. Индуцированная нормотермия ослабляет церебральный метаболический дистресс у пациентов с аневризматическим субарахноидальным кровоизлиянием и рефрактерной лихорадкой. Инсульт. 2009;40:1913–6. [PubMed] [Академия Google]
Oddo M, Frangos S, Milby A, et al. Индуцированная нормотермия ослабляет церебральный метаболический дистресс у пациентов с аневризматическим субарахноидальным кровоизлиянием и рефрактерной лихорадкой. Инсульт. 2009;40:1913–6. [PubMed] [Академия Google]
21. Ротондо Д., Абул Х.Т., Милтон А.С., Дэвидсон Дж. Пирогенные иммуномодуляторы повышают уровень простагландина Е2 в крови одновременно с началом лихорадки. Евр Дж Фармакол. 1988; 154: 145–52. [PubMed] [Google Scholar]
22. Blatteis CM, Li S, Li Z, et al. Цитокины, PGE2 и эндотоксическая лихорадка: переоценка. Простагландины Другие липиды Медиат. 2005; 76: 1–18. [PubMed] [Google Scholar]
23. Grau AJ, Buggle F, Schnitzler P, et al. Лихорадка и инфекция в ранние сроки после ишемического инсульта. J Neurol Sci. 1999;171:115–20. [PubMed] [Google Scholar]
24. Langer M, Cigada M, Mandelli M, et al. Пневмония с ранним началом: многоцентровое исследование в отделениях интенсивной терапии. Интенсивная терапия Мед. 1987; 13: 342–6. [PubMed] [Google Scholar]
1987; 13: 342–6. [PubMed] [Google Scholar]
25. Кеннеди Г.А., Кантер Р.К., Вайнер Л.Б., Томпкинс Дж.М. Можно ли прогнозировать ранние бактериальные осложнения аспирации с дыхательной недостаточностью? Педиатр Неотложная помощь. 1992; 8: 123–5. [PubMed] [Google Scholar]
26. Wu J, Hua Y, Keep RF, et al. Окислительное повреждение головного мозга экстравазационными эритроцитами после внутримозгового кровоизлияния. Мозг Res. 2002;953:45–52. [PubMed] [Google Scholar]
27. Мац П.Г., Фуджимура М., Чан П.Х. Субарахноидальный гемолиз вызывает фрагментацию ДНК по типу, сходному с апоптозом в мозге мыши. Мозг Res. 2000;858:312–9. [PubMed] [Google Scholar]
28. Штайнер А.А., Бранко Л.Г. Центральный путь СО-гемовой оксигеназы повышает температуру тела простагландин-независимым путем. J Appl Physiol (1985) 2000; 88: 1607–13. [PubMed] [Google Scholar]
29. Walentynowicz K, Szefer M, Wojtal B, et al. Роль простагландинов в гем-индуцированной лихорадке. J Physiol Pharmacol.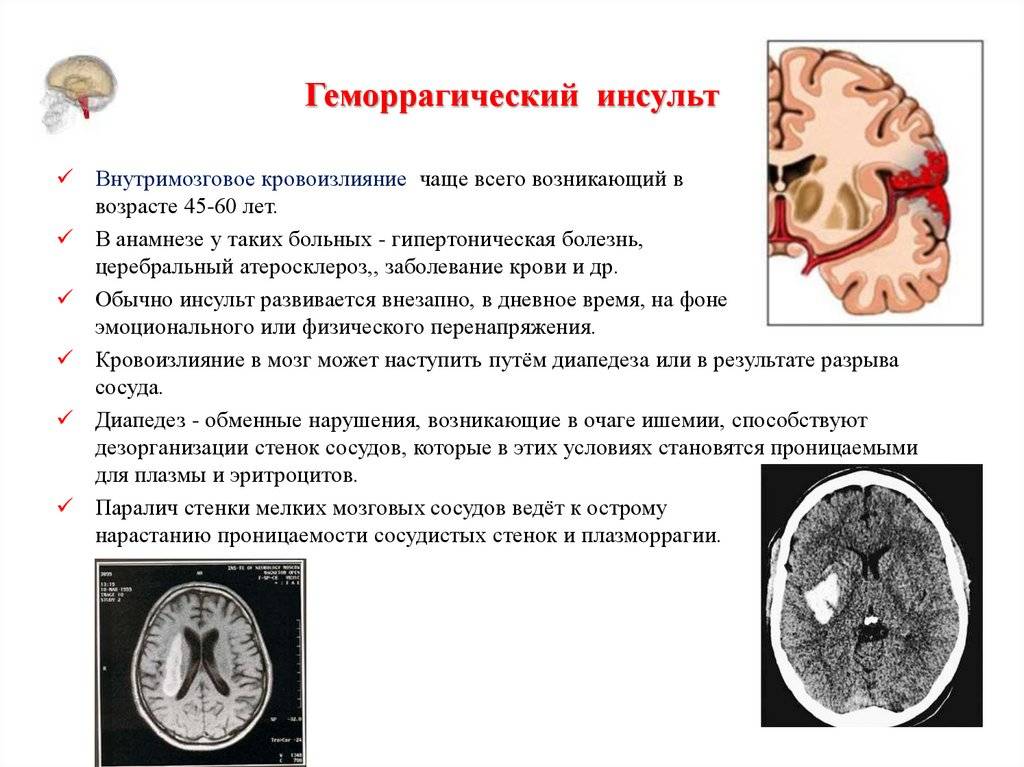 2006; 57 (Приложение 8): 73–82. [PubMed] [Академия Google]
2006; 57 (Приложение 8): 73–82. [PubMed] [Академия Google]
30. Boysen G, Christensen H. Тяжесть инсульта определяет температуру тела при остром инсульте. Инсульт. 2001; 32: 413–7. [PubMed] [Google Scholar]
31. Manian FA. Проспективное исследование ежедневного измерения С-реактивного белка в сыворотке крови взрослых с нейтропенией. Клин Инфекция Дис. 1995; 21: 114–21. [PubMed] [Google Scholar]
32. Smith CJ, Emsley HCA, Vail A, et al. Вариабельность системного острофазового ответа после ишемического инсульта. J Neurol Sci. 2006; 251:77–81. [PubMed] [Академия Google]
33. Накаяма Т., Сонода С., Урано Т. и др. Мониторинг сывороточного амилоидного белка А и С-реактивного белка как маркеров воспаления при инфекционных заболеваниях. Клин Хим. 1993; 39: 293–7. [PubMed] [Google Scholar]
34. Bengzon J, Grubb A, Bune A, et al. Уровни С-реактивного белка после стандартных нейрохирургических процедур. Акта Нейрохир. 2003; 145: 667–70. [PubMed] [Google Scholar]
35. Audebert HJ, Rott MM, Eck T, Haberl RL. Системный воспалительный ответ зависит от исходной тяжести инсульта, но ослабляется успешным тромболизисом. Инсульт. 2004; 35:2128–33. [PubMed] [Академия Google]
Audebert HJ, Rott MM, Eck T, Haberl RL. Системный воспалительный ответ зависит от исходной тяжести инсульта, но ослабляется успешным тромболизисом. Инсульт. 2004; 35:2128–33. [PubMed] [Академия Google]
36. Marquardt L, Ruf A, Mansmann U, et al. Воспалительная реакция после острого ишемического инсульта. J Neurol Sci. 2005; 236: 65–71. [PubMed] [Google Scholar]
37. Leys D, Ringelstein EB, Kaste M, Hacke W для Исполнительного комитета Европейской инициативы по борьбе с инсультом. Основные компоненты ухода за инсультным отделением: результаты европейского экспертного опроса. Цереброваскулярная дис. 2007; 23: 344–52. [PubMed] [Google Scholar]
38. Ringleb PA, Bousser M-G, Ford G, et al. Руководство по ведению ишемического инсульта и транзиторной ишемической атаки 2008 г. Cerebrovasc Dis. 2008; 25: 457–507. [PubMed] [Академия Google]
39. Adams HP, Jr, del Zoppo G, Alberts MJ, et al. Рекомендации по раннему лечению взрослых с ишемическим инсультом: рекомендации Совета по инсульту Американской кардиологической ассоциации/Американской ассоциации инсульта, Совета по клинической кардиологии, Совета по сердечно-сосудистой радиологии и интервенционным вмешательствам, а также Атеросклеротических заболеваний периферических сосудов и результатов качества медицинской помощи в междисциплинарных исследованиях. Группы. Инсульт. 2007; 38: 1655–711. [PubMed] [Google Scholar]
Группы. Инсульт. 2007; 38: 1655–711. [PubMed] [Google Scholar]
40. Broderick J, Connolly S, Feldmann E, et al. Руководство по лечению спонтанного внутримозгового кровоизлияния у взрослых: обновление 2007 г.: руководство Совета по инсульту Американской кардиологической ассоциации/Американской ассоциации инсульта, Исследовательского совета по высокому кровяному давлению и Междисциплинарной рабочей группы по качеству лечения и результатам исследований. Тираж. 2007;116:e391–413. [PubMed] [Google Scholar]
41. Mayer S, Commichau C, Scarmeas N, et al. Клинические испытания охлаждающего одеяла с циркуляцией воздуха для контроля лихорадки у неврологических пациентов в критическом состоянии. Неврология. 2001; 56: 292–8. [PubMed] [Google Scholar]
42. О’Доннелл Дж., Аксельрод П., Фишер С., Лорбер Б. Использование и эффективность гипотермических одеял для лихорадящих пациентов в отделении интенсивной терапии. Клин Инфекция Дис. 1997; 24:1208–13. [PubMed] [Google Scholar]
43. Diringer MN. Лечение лихорадки в отделении неврологической реанимации с помощью катетерной системы теплообмена. Крит Уход Мед. 2004;32:559–64. [PubMed] [Google Scholar]
Diringer MN. Лечение лихорадки в отделении неврологической реанимации с помощью катетерной системы теплообмена. Крит Уход Мед. 2004;32:559–64. [PubMed] [Google Scholar]
44. Георгиадис Д., Шварц С., Коллмар Р., Шваб С. Эндоваскулярное охлаждение при умеренной гипотермии у пациентов с острым инсультом: первые результаты нового подхода. Инсульт. 2001;32:2550–3. [PubMed] [Google Scholar]
45. Kammersgaard LP, Rasmussen BH, Jorgensen HS, et al. Осуществимость и безопасность индуцирования умеренной гипотермии у бодрствующих пациентов с острым инсультом посредством поверхностного охлаждения: исследование случай-контроль: Копенгагенское исследование инсульта. Инсульт. 2000;31:2251–6. [PubMed] [Академия Google]
46. Schwab S, Schwarz S, Spranger M, et al. Умеренная гипотермия в лечении больных с тяжелым инфарктом средней мозговой артерии. Инсульт. 1998;29:2461–6. [PubMed] [Google Scholar]
47. Schwab S, Georgiadis D, Berrouschot J, et al. Целесообразность и безопасность умеренной гипотермии после массивного инфаркта полушария. Инсульт. 2001;32:2033–5. [PubMed] [Google Scholar]
Инсульт. 2001;32:2033–5. [PubMed] [Google Scholar]
48. Meisel C, Prass K, Braun J, et al. Профилактическое антибактериальное лечение улучшает общий медицинский и неврологический исход в мышиной модели инсульта. Инсульт. 2004; 35: 2–6. [PubMed] [Академия Google]
49. Schwarz S, Al-Shajlawi F, Sick C, et al. Влияние профилактической антибиотикотерапии мезлоциллином плюс сульбактам на частоту и высоту лихорадки после тяжелого острого ишемического инсульта: исследование инфекции Мангейма при инсульте (MISS) Инсульт. 2008;39:1220–7. [PubMed] [Google Scholar]
50. Chamorro A, Horcajada JP, Obach V, et al. Исследование «Ранняя системная профилактика инфекций после инсульта»: рандомизированное клиническое исследование. Инсульт. 2005; 36: 1495–500. [PubMed] [Академия Google]
51. Harms H, Prass K, Meisel C, et al. Профилактическая антибактериальная терапия при остром ишемическом инсульте: рандомизированное контролируемое исследование. ПЛОС Один. 2008;3:e2158. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52. Fagan SC, Waller JL, Nichols FT, et al. Миноциклин для улучшения неврологического исхода при инсульте (MINOS): исследование по подбору дозы. Инсульт. 2010;41:2283–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Fagan SC, Waller JL, Nichols FT, et al. Миноциклин для улучшения неврологического исхода при инсульте (MINOS): исследование по подбору дозы. Инсульт. 2010;41:2283–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Sulter G, Elting JW, Maurits N, et al. Ацетилсалициловая кислота и ацетаминофен для борьбы с повышенной температурой тела при остром ишемическом инсульте. Цереброваскулярная дис. 2004; 17:118–22. [PubMed] [Академия Google]
54. Dippel DW, van Breda EJ, van der Worp HB, et al. Влияние парацетамола (ацетаминофена) и ибупрофена на температуру тела при остром ишемическом инсульте PISA, двойное слепое рандомизированное плацебо-контролируемое исследование II фазы [ISRCTN98608690] BMC Cardiovasc Disord. 2003;3:2. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Kasner SE, Wein T, Piriyawat P, et al. Ацетаминофен для изменения температуры тела при остром инсульте: рандомизированное клиническое исследование. Инсульт. 2002; 33:130–4. [PubMed] [Академия Google]
56. Koennecke HC, Leistner S. Профилактическое жаропонижающее лечение ацетаминофеном при остром ишемическом инсульте: экспериментальное исследование. Неврология. 2001;57:2301–3. [PubMed] [Google Scholar]
Koennecke HC, Leistner S. Профилактическое жаропонижающее лечение ацетаминофеном при остром ишемическом инсульте: экспериментальное исследование. Неврология. 2001;57:2301–3. [PubMed] [Google Scholar]
57. den Hertog HM, van der Worp HB, van Gemert HM, et al. Парацетамол (ацетаминофен) при инсульте (PAIS): многоцентровое, рандомизированное, плацебо-контролируемое исследование III фазы. Ланцет Нейрол. 2009; 8: 434–40. [PubMed] [Google Scholar]
58. Судано И., Фламмер А.Дж., Периат Д. и соавт. Ацетаминофен повышает артериальное давление у пациентов с ишемической болезнью сердца. Тираж. 2010;122:1789–96. [PubMed] [Google Scholar]
. 1999 г., 15 декабря; 171(2):115-20.
doi: 10.1016/s0022-510x(99)00261-0.
А. Дж. Грау 1 , F Buggle, P Schnitzler, M Spiel, C Lichy, W Hacke
 [email protected]
[email protected] А. Дж. Грау и соавт. J Neurol Sci. .
. 1999 г., 15 декабря; 171(2):115-20.
дои: 10.1016/s0022-510x(99)00261-0.
А. Дж. Грау 1 , Ф. Баггл, П. Шницлер, М. Шпиль, К. Личи, В. Хакке
 [email protected]
[email protected] Предыдущие исследования показали, что повышенная температура тела в ранние сроки после ишемического инсульта связана с выраженным неврологическим дефицитом и неблагоприятным исходом. Цель этого исследования состояла в том, чтобы проанализировать распространенность и предполагаемую этиологию фебрильной температуры тела (>/=38,0°C) в ранние сроки после инсульта и изучить связь между температурой тела, тяжестью инсульта и исходом. Мы исследовали 119последовательных пациентов, которые были госпитализированы в течение 24 часов после ишемического инсульта. Пациенты были обследованы на инфекции до ишемии с использованием стандартизированного опросника и ежедневно проходили клиническое обследование после инсульта. При лихорадке проводились стандартизированные рентгенологические и микробиологические исследования. Лихорадка в течение 48 ч после инсульта наблюдалась у 30 (25,2%) больных. Вероятными причинами лихорадки были инфекционная или химико-аспирационная пневмония (n=12), другие инфекции дыхательных путей (n=7), инфекции мочевыводящих путей (n=4), вирусные инфекции (n=3) или недостаточно определенная (n=5) ). (У одного пациента было две возможные причины лихорадки.) У тринадцати из этих пациентов инфекция, скорее всего, была приобретена до инсульта. Лихорадка вновь появлялась чаще в течение 1-2 дней, чем с 3 по 7 день после инсульта (р = 0,016). Лихорадка ассоциировалась с более тяжелым дефицитом при поступлении независимо от возраста, сосудистых заболеваний и факторов риска (отношение шансов 9.6; 95% доверительный интервал 3.1-29). Лихорадка является частым осложнением в ранние сроки после инсульта и в большинстве случаев может быть объяснена инфекцией или химико-аспирационной пневмонией. Примерно у половины инфицированных пациентов инфекция, скорее всего, была приобретена до инсульта.
При лихорадке проводились стандартизированные рентгенологические и микробиологические исследования. Лихорадка в течение 48 ч после инсульта наблюдалась у 30 (25,2%) больных. Вероятными причинами лихорадки были инфекционная или химико-аспирационная пневмония (n=12), другие инфекции дыхательных путей (n=7), инфекции мочевыводящих путей (n=4), вирусные инфекции (n=3) или недостаточно определенная (n=5) ). (У одного пациента было две возможные причины лихорадки.) У тринадцати из этих пациентов инфекция, скорее всего, была приобретена до инсульта. Лихорадка вновь появлялась чаще в течение 1-2 дней, чем с 3 по 7 день после инсульта (р = 0,016). Лихорадка ассоциировалась с более тяжелым дефицитом при поступлении независимо от возраста, сосудистых заболеваний и факторов риска (отношение шансов 9.6; 95% доверительный интервал 3.1-29). Лихорадка является частым осложнением в ранние сроки после инсульта и в большинстве случаев может быть объяснена инфекцией или химико-аспирационной пневмонией. Примерно у половины инфицированных пациентов инфекция, скорее всего, была приобретена до инсульта. Лихорадка была связана с более выраженным неврологическим дефицитом при поступлении.
Лихорадка была связана с более выраженным неврологическим дефицитом при поступлении.
Предикторы раннего инфицирования при мозговом ишемическом инсульте.
Ашур В., Аль-Анвар А.Д., Камель А.Е., Айдарос М.А. Ашур В. и др. Джей Мед Лайф. 2016 апрель-июнь;9(2):163-9. Джей Мед Лайф. 2016. PMID: 27453748 Бесплатная статья ЧВК.
Инфекции, диагностированные после поступления в инсультное отделение, и их влияние на госпитальную смертность в Польше с 1995 по 2015 год.
Карлински М.А., Бембенек Ю.П., Барановска А., Курковска-Ястржебска И., Члонковска А. Карлински М.А. и соавт. J Инсульт Цереброваскулярная дис. 2018 июль; 27 (7): 1775-1782. doi: 10.1016/j.jstrokecerebrovasdis.2018. 02.005. J Инсульт Цереброваскулярная дис. 2018. PMID: 29526387
02.005. J Инсульт Цереброваскулярная дис. 2018. PMID: 29526387
Инфекции, присутствующие при поступлении, по сравнению с внутрибольничными инфекциями у пациентов с острым ишемическим инсультом.
Беме А.К., Кумар А.Д., Дорси А.М., Зиглер Дж.Е., Асуани М.С., Лиерли М.Дж., Монлезун Д.Дж., Джордж А.Дж., Олбрайт К.С., Бисли Т.М., Мартин-Шилд С. Беме А.К. и соавт. J Инсульт Цереброваскулярная дис. 2013 ноябрь;22(8):e582-9. doi: 10.1016/j.jstrokecerebrovasdis.2013.07.020. Epub 2013 15 августа. J Инсульт Цереброваскулярная дис. 2013. PMID: 23954599 Бесплатная статья ЧВК.
Инфекция, связанная с инсультом, является независимым предиктором 3-месячного плохого функционального исхода и смертности.
Суда С., Аоки Дж. , Шимояма Т., Судзуки К., Сакамото Ю., Катано Т., Окубо С., Нито С., Нишияма Ю., Мишина М., Кимура К. Суда С. и др. Дж Нейрол. 2018 февраль; 265(2):370-375. doi: 10.1007/s00415-017-8714-6. Epub 2017 16 декабря. Дж Нейрол. 2018. личный номер: 29249057
, Шимояма Т., Судзуки К., Сакамото Ю., Катано Т., Окубо С., Нито С., Нишияма Ю., Мишина М., Кимура К. Суда С. и др. Дж Нейрол. 2018 февраль; 265(2):370-375. doi: 10.1007/s00415-017-8714-6. Epub 2017 16 декабря. Дж Нейрол. 2018. личный номер: 29249057
Предикторы постинсультной лихорадки и инфекций: систематический обзор и метаанализ.
Wästfelt M, Cao Y, Ström JO. Вестфельт М. и соавт. БМК Нейрол. 2018 23 апр; 18(1):49. doi: 10.1186/s12883-018-1046-z. БМК Нейрол. 2018. PMID: 29685118 Бесплатная статья ЧВК. Обзор.
Посмотреть все похожие статьи
Эпидемиология, факторы риска и предикторы инвалидности в когорте иорданских пациентов с первым ишемическим инсультом.
Кавасмех М.А., Алдаббур Б., Момани А., Обьедат Д., Альхайек К., Кофахи Р., Ясин А., Эль-Салем К. Кавасмех М.А. и соавт. Лечение инсульта. 2020 4 июня; 2020:1920583. дои: 10.1155/2020/1920583. Электронная коллекция 2020. Лечение инсульта. 2020. PMID: 32566121 Бесплатная статья ЧВК.
Количество и соотношение лейкоцитов позволяют прогнозировать исход инсульта и геморрагические осложнения независимо от инфекций.
Семерано А., Страмбо Д., Мартино Г., Коми Г., Филиппи М., Ровери Л., Бачигалуппи М. Семерано А. и др. Фронт Нейрол. 2020 3 апр; 11:201. doi: 10.3389/fneur.2020.00201. Электронная коллекция 2020. Фронт Нейрол. 2020. PMID: 32308640 Бесплатная статья ЧВК.
Местные и периферические иммунные реакции на инсульт: последствия для терапевтического развития.
Зера К.А., Бакволтер М.С. Зера К.А. и соавт. Нейротерапия. 2020 апр; 17 (2): 414-435. doi: 10.1007/s13311-020-00844-3. Нейротерапия. 2020. PMID: 32193840 Бесплатная статья ЧВК. Обзор.
Регуляторные Т-клетки участвуют в восстановлении пациентов с ишемическим инсультом.
Сантамария-Кадавид М., Родригес-Кастро Э., Родригес-Яньес М., Ариас-Ривас С., Лопес-Декидт И., Перес-Мато М., Родригес-Перес М., Лопес-Лоурейро И., Эрвелла П., Кампос Ф., Кастильо Х. , Иглесиас-Рей Р., Собрино Т. Сантамария-Кадавид М. и др. БМК Нейрол. 2020 28 февраля; 20 (1): 68. doi: 10.1186/s12883-020-01648-w. БМК Нейрол. 2020. PMID: 32111174 Бесплатная статья ЧВК.
Шкала Брейдена для оценки пневмонии после острого ишемического инсульта.