2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Тиреотоксикоз (синоним — гипертиреоз) — это состояние, обусловленное повышением концентраций свободных T4 и T3 — гормонов щитовидной железы. Причиной тиреотоксикоза служат самые разные заболевания.
Самая частая причина тиреотоксикоза — диффузный токсический зоб; на его долю приходится от 60 до 90% случаев (частота зависит от возрастной группы и местности). На втором месте по частоте стоят многоузловой токсический зоб и токсическая аденома щитовидной железы, на долю которых приходится 10—40% случаев тиреотоксикоза. Оба заболевания чаще встречаются у пожилых. От 5 до 20% случаев тиреотоксикоза обусловлены тиреоидитом (подострым гранулематозным и подострым лимфоцитарным). Прочие причины тиреотоксикоза, в том числе передозировка левотироксина (препарата, применяемого при обратном тиреотоксикозу состоянии — гипотиреозе) встречаются гораздо реже.
Клиническая картина и тяжесть тиреотоксикоза зависят от возраста больного, сопутствующих заболеваний и скорости развития болезни. Симптомы могут нарастать постепенно либо волнообразно и по выраженности колебаться от едва заметных до тяжелейших.
Типичные жалобы: повышенная возбудимость, раздражительность, суетливость, бессонница, тремор рук, потливость, сердцебиение. Часто наблюдаются похудание и непереносимость жары, зуд. Больным зачастую бывает трудно подниматься по лестнице и вставать со стула: так проявляется слабость мышц. Усиление работы кишечника может привести к учащению стула, а в некоторых случаях — к нарушениям всасывания и поносу. Может обостриться стенокардия. У женщин встречаются нарушения менструального цикла, у мужчин — снижение полового влечения и импотенция.
Реже отмечаются тошнота, рвота и нарушения глотания. Одышка при физической нагрузке обусловлена повышенным потреблением кислорода и слабостью дыхательных мышц. Изредка ее причиной служит сдавление трахеи большим зобом.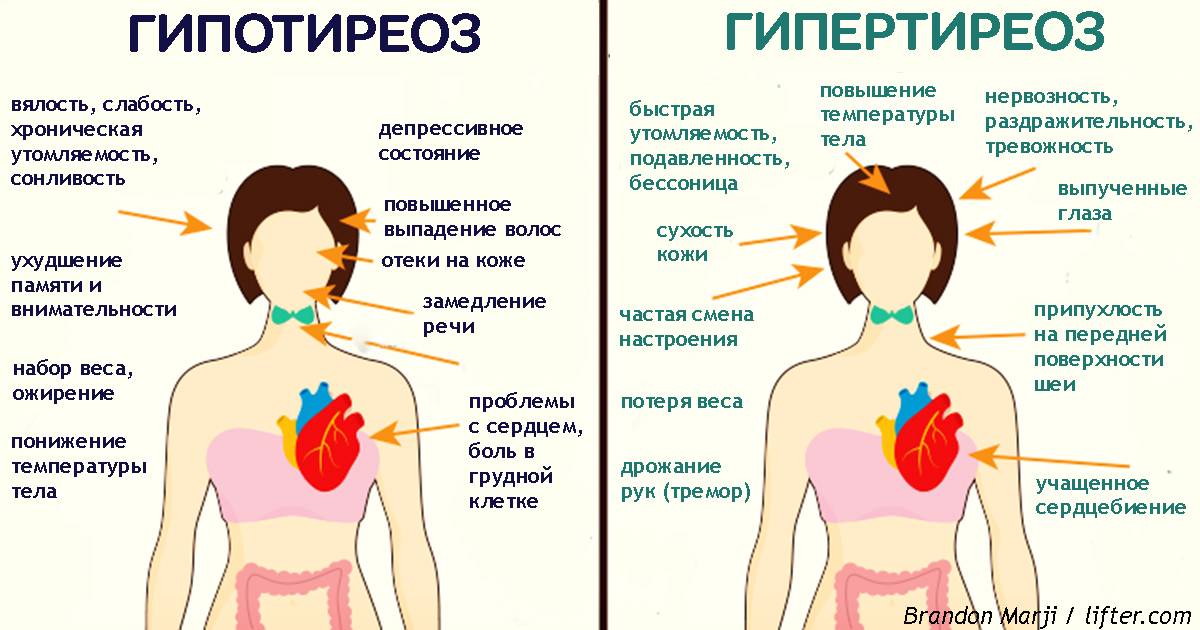
У большинства больных диффузным токсическим зобом обе доли щитовидной железы увеличены равномерно, плотные и безболезненные. При хроническом лимфоцитарном тиреоидите железа бывает особенно плотной. При многоузловом токсическом зобе железа обычно асимметричная, бугристая, с неоднородной консистенцией. Токсическая аденома — это, как правило, одиночный узел диаметром более 3 см. Болезненность щитовидной железы при пальпации заставляет заподозрить подострый гранулематозный тиреоидит.
Сердечная симптоматика обусловлена как прямым действием тиреоидных гормонов на сердечно-сосудистую систему, так и повышением основного обмена и потребления кислорода. Характерны синусовая тахикардия, повышение систолического (верхнего) артериального давления. Помимо синусовой тахикардии — самого частого нарушения ритма сердца при тиреотоксикозе — у 10—25% больных отмечаются другие аритмии, особенно мерцательная. Мерцательная аритмия чаще всего встречается у пожилых и бывает основным проявлением тиреотоксикоза.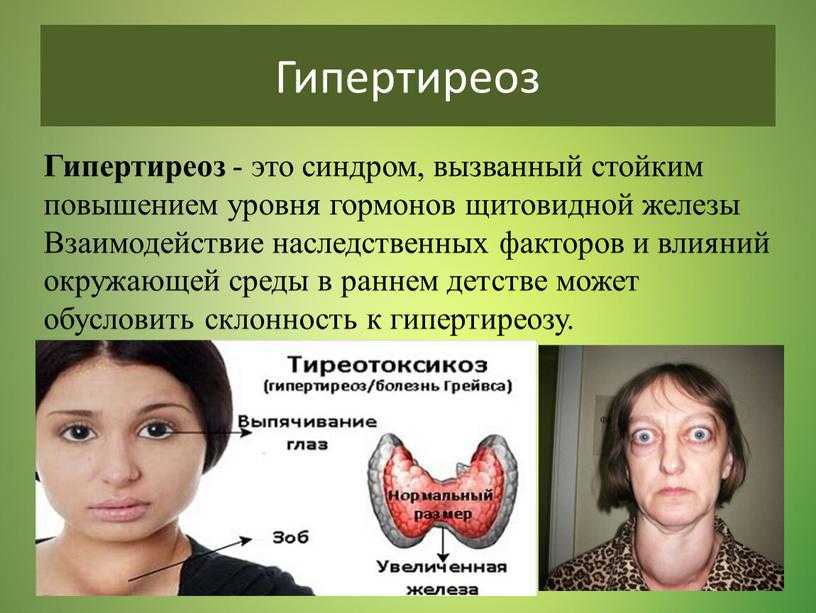
Признаки тиреотоксикоза — повышенные уровни тиреоидных гормонов и пониженный уровень тиреотропного гормона (ТТГ). Повышены как общие, так и свободные T 4 и T3; иногда наблюдается повышение уровня только одного из гормонов. Увеличение концентрации тироксинсвязывающего глобулина или его сродства к T4, что бывает при беременности и заместительной терапии эстрогенами, может повысить общий T4 до уровня, характерного для тиреотоксикоза.
Антитиреоидные антитела (к тиреоглобулину и к йодидпероксидазе) обнаруживаются примерно у 70% больных диффузным токсическим зобом. Определение титра антител не является необходимым, но оно помогает поставить диагноз, особенно в отсутствие поражения глаз (офтальмопатии).
Течение тиреотоксикоза при диффузном токсическом зобе характеризуется сменой обострений и ремиссий, хотя бывают и неуклонно прогрессирующее течение, и одиночные приступы. Лечения, направленного на причину болезни нет, и по-настоящему излечить диффузный токсический зоб невозможно. Поэтому лечение направлено на снижение уровней тиреоидных гормонов в крови — либо за счет подавления их синтеза, либо путем разрушения ткани щитовидной железы. Есть три основных пути достижения этой цели: 1) антитиреоидные средства, 2) радиоактивный йод, 3) хирургическое вмешательство. Антитиреоидные средства, подавляя синтез тиреоидных гормонов, позволяют изменить течение болезни и вызвать ремиссию тиреотоксикоза. Лечение радиоактивным йодом и операция уменьшают количество ткани щитовидной железы. Выбор лечения должен быть индивидуальным; он определяется пожеланиями больного и наличием опытных хирургов.
Лечения, направленного на причину болезни нет, и по-настоящему излечить диффузный токсический зоб невозможно. Поэтому лечение направлено на снижение уровней тиреоидных гормонов в крови — либо за счет подавления их синтеза, либо путем разрушения ткани щитовидной железы. Есть три основных пути достижения этой цели: 1) антитиреоидные средства, 2) радиоактивный йод, 3) хирургическое вмешательство. Антитиреоидные средства, подавляя синтез тиреоидных гормонов, позволяют изменить течение болезни и вызвать ремиссию тиреотоксикоза. Лечение радиоактивным йодом и операция уменьшают количество ткани щитовидной железы. Выбор лечения должен быть индивидуальным; он определяется пожеланиями больного и наличием опытных хирургов.
Антитиреоидные средства. Обычная начальная доза тиамазола (Мерказолила) — 20—40 мг/сутки внутрь в один прием, пропилтиоурацила (Пропицила) — 300—450 мг/сутки внутрь в 2—3 приема. При тяжелом тиреотоксикозе, а также при очень большом зобе могут потребоваться большие дозы. По достижении эутиреоидного состояния (нормализации уровней тиреоидных гормонов), обычно через 12 недель, дозу антитиреоидного средства можно снизить. Поддерживающие дозы составляют 5—10 мг/сутки для тиамазола и 50—200 мг/сутки для пропилтиоурацила. Затем рекомендуются повторные визиты к врачу каждые 3 месяца.
По достижении эутиреоидного состояния (нормализации уровней тиреоидных гормонов), обычно через 12 недель, дозу антитиреоидного средства можно снизить. Поддерживающие дозы составляют 5—10 мг/сутки для тиамазола и 50—200 мг/сутки для пропилтиоурацила. Затем рекомендуются повторные визиты к врачу каждые 3 месяца.
Через год после отмены антитиреоидного средства ремиссия сохраняется у 10—90% больных (в среднем у 50%). Чем дольше длится лечение, тем более вероятна ремиссия.
Рецидив диффузного токсического зоба обычно происходит в первые несколько месяцев после отмены антитиреоидного средства. В таких случаях лучше прибегнуть к радикальному лечению, но можно назначить и повторный курс антитиреоидного средства. Многолетнее применение антитиреоидных средств считается безопасным у больных, которые не способны сохранить ремиссию после отмены препарата и не соглашаются лечиться радиоактивным йодом или подвергаться операции. Больные, у которых наступила ремиссия, должны обследоваться на предмет рецидива каждые 3—6 месяцев или при появлении симптомов.
Самый тяжелый побочный эффект антитиреоидных средств — агранулоцитоз (критическое снижение количества нейтрофилов в крови), который обычно (но не всегда) развивается в первые 3 месяца лечения. Пропилтиоурацил и тиамазол вызывают агранулоцитоз с одинаковой частотой — 0,1—0,5%. Риск агранулоцитоза, вызванного тиамазолом, зависит от его дозы; при дозах менее 30 мг/сут этот побочный эффект наблюдается редко. Для пропилтиоурацила зависимость от дозы не отмечена. Каждого больного предупреждают, что при появлении лихорадки или боли в горле нужно прекратить прием антитиреоидного средства и срочно обратиться к врачу.
Лечение радиоактивным йодом. Радиоактивный йод захватывается щитовидной железой и разрушает ее клетки. Многие врачи предпочитают этот способ лечения, особенно у пожилых. Радиоактивный йод не назначают детям, беременным и кормящим женщинам.
Нормализация функции щитовидной железы и уровня ТТГ обычно происходит через 1—2 месяца, но может наступить и через год. За редкими исключениями повторную дозу радиоактивного йода назначают не раньше чем через 3—6 месяцев после первой.
За редкими исключениями повторную дозу радиоактивного йода назначают не раньше чем через 3—6 месяцев после первой.
Хирургическое лечение. Субтотальную резекцию щитовидной железы проводят: 1) больным с большим зобом, 2) детям, страдающим аллергией к антитиреоидным средствам, 3) беременным, страдающим аллергией к антитиреоидным средствам (обычно во II триместре), 4) больным, которые предпочитают операцию лечению антитиреоидными средствами и радиоактивным йодом.
Самые частые осложнения субтотальной резекции щитовидной железы — огрубление голоса из-за повреждения возвратного гортанного нерва и гипопаратиреоз. Если операцию проводит опытный хирург, частота этих осложнений низка (менее 1%). Примерно у 5% больных возникает рецидив тиреотоксикоза, примерно у 60% развивается гипотиреоз.
Опубликовано: 06.05.2021 13:00:00 Обновлено: 06.05.2021 Просмотров: 99062
Тиреотоксикоз – патологическое состояние, вызванное избытком гормонов щитовидной железы. Другое название этого заболевания – гипертиреоз. Состояние противоположно гипотиреозу, при котором наблюдается дефицит тиреоидных гормонов.
Другое название этого заболевания – гипертиреоз. Состояние противоположно гипотиреозу, при котором наблюдается дефицит тиреоидных гормонов.
По самому слову «тиреотоксикоз» ясно, что большое количество тиреоидных гормонов опасно (токсично) для организма. При этом гипертиреоз не является самостоятельным заболеванием, это болезненное состояние, которое возникает из-за других причин, среди которых:

Причин возникновения гипертиреоза множество, но их можно разделить на две большие группы:
 Одна из причин тиреотоксикоза – избыточное поступление йода с пищевыми добавками или лекарственными препаратами без консультации врача и лабораторных исследований.
Одна из причин тиреотоксикоза – избыточное поступление йода с пищевыми добавками или лекарственными препаратами без консультации врача и лабораторных исследований.Повышенная функция щитовидной железы проявляет себя следующими симптомами:
Щитовидную железу можно сравнить с печью, которая расходует энергию организма. Эта маленькая железа в форме бабочки отвечает за скорость метаболизма в клетках и во всем организме. Благодаря уровню гормонов контролируется расход энергии. Если тиреоидных гормонов становится слишком много, ускоряются все функции в организме: учащается сердцебиение, человек ощущает жар, становится сложнее сконцентрироваться на мысли, вес падает даже при сбалансированной диете. Представьте, что в домовую печь кладут слишком много дров: выделяется чрезмерно много энергии и тепла, дом перегревается. Примерно то же самое происходит с телом, когда в кровоток попадает слишком много тиреоидных гормонов.
Если тиреоидных гормонов становится слишком много, ускоряются все функции в организме: учащается сердцебиение, человек ощущает жар, становится сложнее сконцентрироваться на мысли, вес падает даже при сбалансированной диете. Представьте, что в домовую печь кладут слишком много дров: выделяется чрезмерно много энергии и тепла, дом перегревается. Примерно то же самое происходит с телом, когда в кровоток попадает слишком много тиреоидных гормонов.
Самое главное в организме на всех уровнях – баланс. На примере с работой щитовидной железы это видно особенно отчетливо: как недостаток гормонов, так и их дефицит разрушителен для организма.
С заболеванием сталкивается 1-2 человека из тысячи. Женщины заболевают тиреотоксикозом чаще (7-10% против 2-3% у мужчин), с возрастом частота этого состояния может достигать 21%.
В первую очередь в группе риска женщины старше 30 лет.
Другая категория – лица, употребляющие в пищу слишком много йода.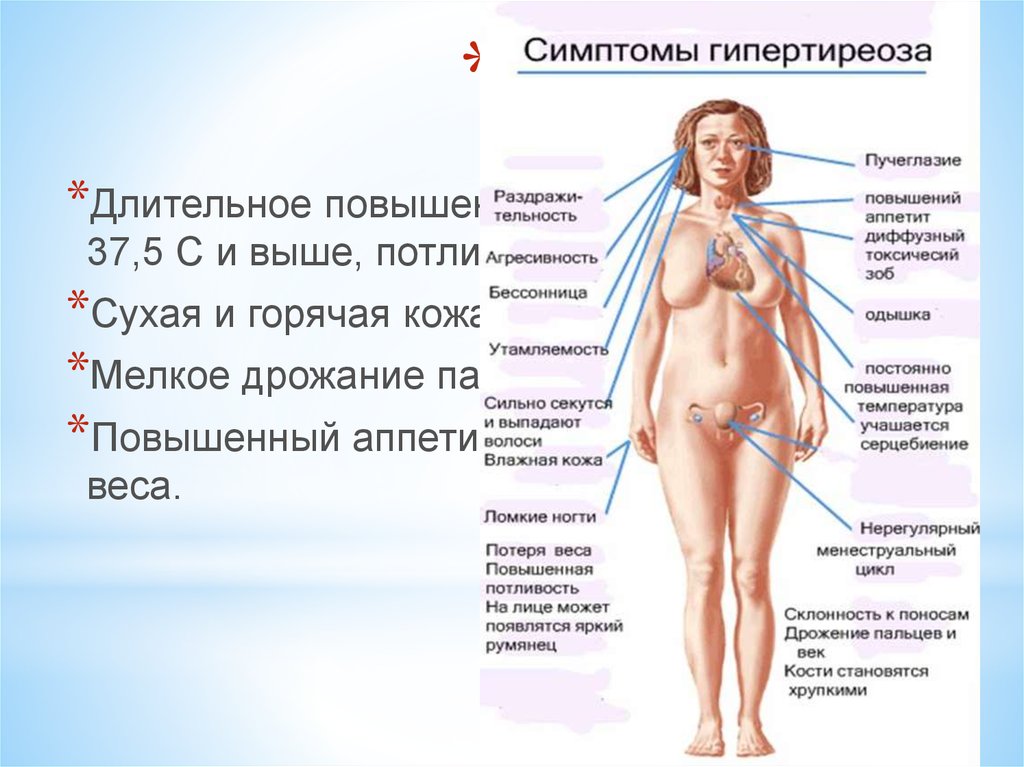 Это касается в первую очередь йодсодержащих добавок и лекарственных препаратов.
Это касается в первую очередь йодсодержащих добавок и лекарственных препаратов.
В группе риска также люди, у близких родственников которых диагностированы заболевания эндокринной системы.
Пациенту, который подозревает у себя нарушения щитовидной железы, необходимо обратиться к терапевту. Врач проведет первичный осмотр и оценит вероятность того, что состояние и симптомы действительно связаны с эндокринной системой, назначит обследование. По результатам обследования будет понятно, есть ли необходимость в лечении. Если такая необходимость возникнет, может потребоваться консультация эндокринолога.
Возможен и другой путь: пациент может сразу обратиться к эндокринологу. Это не возбраняется, но самостоятельная диагностика редко бывает эффективной. Симптомы, которые характерны для заболеваний щитовидной железы, могут быть и при заболеваниях других органов. Возможно, приоритет может быть смещен в сторону обследования сердечно-сосудистой системы или других органов – в зависимости от конкретной ситуации.
Профилактическую диагностику щитовидной железы рекомендуется проходить раз в 2-3 года, если человек здоров: если не было ранее проблем с этим органом и если ни у кого из близких родственников нет эндокринных нарушений. В ином случае нужно проверять щитовидку раз в год или чаще, по указанию врача.
Проверить функцию щитовидной железы также нужно женщинам, планирующим беременность.
Базовая первичная диагностика функции щитовидной железы включает УЗИ и несколько лабораторных анализов:
Данные исследования должны проводиться вместе, врач смотрит на соотношение ТТГ, Т3 и Т4. УЗИ не заменяет лабораторные тесты, и наоборот.
Результаты исследований оцениваются вместе с общим анамнезом. Врач уточнит наличие эндокринных заболеваний у близких родственников, было ли облучение головы или шеи, спросит, в каком регионе проживает пациент и какой диеты он придерживается.
По результатам анализов и общего осмотра могут быть назначены дополнительные обследования.
Возможно несколько вариантов лечения тиреотоксикоза:
 Избыток радиоактивного йода выводится из организма в течение недель или месяцев. При выборе этого способа лечения самое важное – правильная дозировка и регулярный контроль показателей, потому что при чрезмерном снижении функции щитовидной железы может развиться гипотиреоз – дефицит гормонов щитовидной железы. Радиойодтерапия не вызывает риска образования рака и генетических мутаций, доза облучения сопоставима с облучением при выполнении рентгеновского снимка.
Избыток радиоактивного йода выводится из организма в течение недель или месяцев. При выборе этого способа лечения самое важное – правильная дозировка и регулярный контроль показателей, потому что при чрезмерном снижении функции щитовидной железы может развиться гипотиреоз – дефицит гормонов щитовидной железы. Радиойодтерапия не вызывает риска образования рака и генетических мутаций, доза облучения сопоставима с облучением при выполнении рентгеновского снимка.
Длительное заболевание негативно сказывается на состоянии костей: снижается их плотность, увеличивается риск переломов. Особенно опасно для женщин в периоде менопаузы, когда кости ослабевают из-за гормональной перестройки, а гипертиреоз только усугубляет ситуацию.
Особенно опасно для женщин в периоде менопаузы, когда кости ослабевают из-за гормональной перестройки, а гипертиреоз только усугубляет ситуацию.
Также возможны сердечно-сосудистые нарушения с риском тромбоэмболических осложнений. Без своевременной диагностики и лечения заболевания щитовидной железы разрушают весь организм.
Eur Thyroid J. 2015 Сентябрь; 4(3): 143–148.
Опубликовано в Интернете 21 августа 2015 г. doi: 10.1159/000438909
Информация об авторе Информация об авторских правах и лицензии Отказ от ответственности
ранее опубликованные рекомендации ETA по субклиническому гипотиреозу (SHypo) [2,3] предлагают современные рекомендации по ведению пациентов с субклинической дисфункцией щитовидной железы. Руководство в этой области приветствуется из-за сохраняющейся неопределенности в отношении того, улучшит ли терапевтическое вмешательство результаты лечения.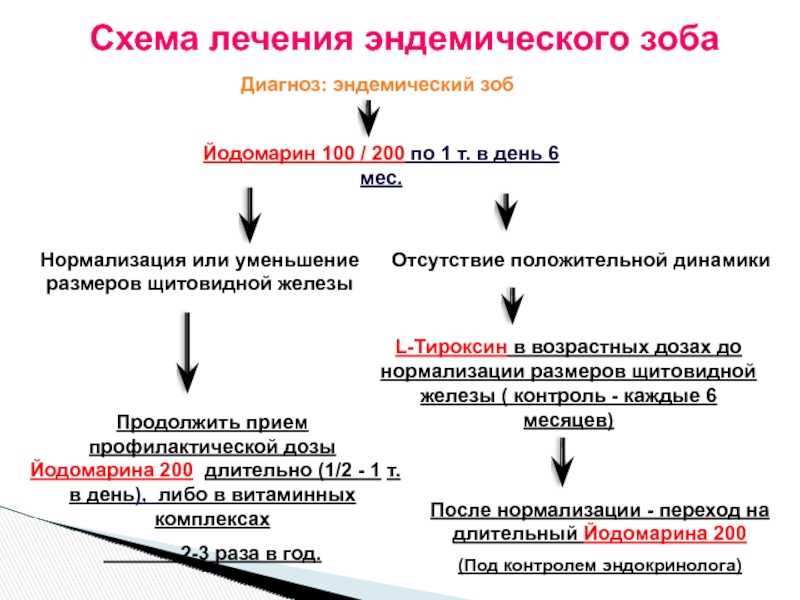 Хотя доказательства связи между SHyper или SHypo и неблагоприятными последствиями для здоровья стали намного сильнее за последнее десятилетие, отсутствуют доказательства того, что восстановление эутиреоидного состояния обращает вспять риск неблагоприятных последствий для здоровья. Нет долгосрочных рандомизированных клинических испытаний, демонстрирующих, что лечение принесет больше пользы, чем вреда [4]. На этом фоне можно задаться вопросом, не переоценены ли степени доказательности некоторых рекомендаций. Тем не менее, рекомендации могут быть очень полезными при принятии решений о лечении. Однако в этой редакционной статье я хотел бы исследовать вопрос, действительно ли мы продвигаемся вперед в наших мыслях о SHyper и SHypo. Другими словами, какие темы не были рассмотрены в настоящих руководящих принципах? Есть ли менее заметные, но все же клинически значимые проблемы?
Хотя доказательства связи между SHyper или SHypo и неблагоприятными последствиями для здоровья стали намного сильнее за последнее десятилетие, отсутствуют доказательства того, что восстановление эутиреоидного состояния обращает вспять риск неблагоприятных последствий для здоровья. Нет долгосрочных рандомизированных клинических испытаний, демонстрирующих, что лечение принесет больше пользы, чем вреда [4]. На этом фоне можно задаться вопросом, не переоценены ли степени доказательности некоторых рекомендаций. Тем не менее, рекомендации могут быть очень полезными при принятии решений о лечении. Однако в этой редакционной статье я хотел бы исследовать вопрос, действительно ли мы продвигаемся вперед в наших мыслях о SHyper и SHypo. Другими словами, какие темы не были рассмотрены в настоящих руководящих принципах? Есть ли менее заметные, но все же клинически значимые проблемы?
SHyper и SHypo являются неправильными терминами, поскольку термин «субклинический» предполагает отсутствие симптомов и признаков избытка или дефицита гормонов щитовидной железы, соответственно. Однако иногда могут присутствовать такие симптомы и признаки, например, мерцательная аритмия является хорошо известным проявлением тиреотоксикоза, и ее распространенность увеличивается при SHyper [5]. Кроме того, у субъектов с SHypo балл по клинической шкале гипотиреоза несколько выше, чем у контрольной группы [6]. Таким образом, следует избегать сбивающего с толку термина «субклинический» [7], и требуется более точная терминология. SHyper и SHypo определяются исключительно по биохимическим критериям (ТТГ снаружи, но FT 9).0013 4 и FT 3 в пределах соответствующих контрольных диапазонов). Эверед и др. [8] 40 лет назад предложили классифицировать гипотиреоз по биохимическим критериям. Они различали гипотиреоз I степени (субклинический), II степени (легкий) и III степени (явный) (таблица) [8]. ТТГ становится прогрессивно выше, а FT 4 прогрессивно ниже при переходе от I к III степени. Система оценок Evered et al. не был принят медицинским сообществом, но, на мой взгляд, не потерял своей привлекательности.
Однако иногда могут присутствовать такие симптомы и признаки, например, мерцательная аритмия является хорошо известным проявлением тиреотоксикоза, и ее распространенность увеличивается при SHyper [5]. Кроме того, у субъектов с SHypo балл по клинической шкале гипотиреоза несколько выше, чем у контрольной группы [6]. Таким образом, следует избегать сбивающего с толку термина «субклинический» [7], и требуется более точная терминология. SHyper и SHypo определяются исключительно по биохимическим критериям (ТТГ снаружи, но FT 9).0013 4 и FT 3 в пределах соответствующих контрольных диапазонов). Эверед и др. [8] 40 лет назад предложили классифицировать гипотиреоз по биохимическим критериям. Они различали гипотиреоз I степени (субклинический), II степени (легкий) и III степени (явный) (таблица) [8]. ТТГ становится прогрессивно выше, а FT 4 прогрессивно ниже при переходе от I к III степени. Система оценок Evered et al. не был принят медицинским сообществом, но, на мой взгляд, не потерял своей привлекательности. С учетом текущих рекомендаций руководства, возможно, стало бы еще более актуальным назначать левотироксин при SHypo со значениями ТТГ ≥10 мЕд/л (по крайней мере, у лиц моложе 70 лет), но быть более консервативным при значениях ТТГ от 4 до 10 мЕд. /л [2]. Мое предложение состояло бы в том, чтобы разделить степень I (SHypo) на степень IA (ТТГ от >4,0 до <10 мЕд/л) и степень IB (≥10 мЕд/л). Та же самая система классификации может быть применена при гипертиреозе: степень III указывает на явный гипертиреоз, степень II указывает на умеренный гипертиреоз или Т9.0013 3 токсикоз, а I степень - SHyper (таблица). Опять же, ввиду более высокого риска неблагоприятных исходов для здоровья при значениях ТТГ ≤0,1 мЕд/л по сравнению со значениями ТТГ от >0,1 до <0,4 мЕд/л и текущих рекомендаций по вмешательству при уровне ТТГ ≤0,1 мЕд/л [1] , степень I можно разделить на степень IA (ТТГ >0,1–<0,4 мЕд/л) и степень IB (ТТГ ≤0,1 мЕд/л). Авторы настоящего руководства SHyper уже применяют систему оценок, которая, хотя и немного отличается от моего предложения, приветствуется, поскольку оценка более понятна, чем термины «низкие» или «подавленные» значения.
С учетом текущих рекомендаций руководства, возможно, стало бы еще более актуальным назначать левотироксин при SHypo со значениями ТТГ ≥10 мЕд/л (по крайней мере, у лиц моложе 70 лет), но быть более консервативным при значениях ТТГ от 4 до 10 мЕд. /л [2]. Мое предложение состояло бы в том, чтобы разделить степень I (SHypo) на степень IA (ТТГ от >4,0 до <10 мЕд/л) и степень IB (≥10 мЕд/л). Та же самая система классификации может быть применена при гипертиреозе: степень III указывает на явный гипертиреоз, степень II указывает на умеренный гипертиреоз или Т9.0013 3 токсикоз, а I степень - SHyper (таблица). Опять же, ввиду более высокого риска неблагоприятных исходов для здоровья при значениях ТТГ ≤0,1 мЕд/л по сравнению со значениями ТТГ от >0,1 до <0,4 мЕд/л и текущих рекомендаций по вмешательству при уровне ТТГ ≤0,1 мЕд/л [1] , степень I можно разделить на степень IA (ТТГ >0,1–<0,4 мЕд/л) и степень IB (ТТГ ≤0,1 мЕд/л). Авторы настоящего руководства SHyper уже применяют систему оценок, которая, хотя и немного отличается от моего предложения, приветствуется, поскольку оценка более понятна, чем термины «низкие» или «подавленные» значения.
Proposed grading of hypothyroidism and hyperthyroidism
| TSH | FT 4 | FT 3 | |
|---|---|---|---|
| Hypothyroidism grade IA | increased, >4.0 to <10 мЕд/л | в норме | в норме |
| Гипотиреоз степени IB | повышен, >10 мЕд/л | в норме | в норме |
| Hypothyroidism grade II | increased | decreased | normal |
| Hypothyroidism grade III | increased | decreased | decreased |
| | |||
| Hyperthyroidism grade IA | decreased, >0. 1 to <4.0 мЕд/л 1 to <4.0 мЕд/л | в норме | в норме |
| Гипертиреоз степени IB | снижение, <0,1 мЕд/л | в норме | normal |
| Hyperthyroidism grade II | decreased | normal | increased |
| Hyperthyroidism grade III | decreased | increased | increased |
Open in a separate window
Normal, увеличилось, уменьшилось: значения в пределах, выше, ниже соответствующих контрольных интервалов.
Классификация гипертиреоза и гипотиреоза по степени тяжести (IA, IB, II, III) позволяет достаточно точно оценить тяжесть состояния. Система оценок соответствует естественному течению обоих состояний (начиная со степени IA и часто заканчивая степенью III), а обратная последовательность оценок возникает после начала лечения для восстановления эутиреоза (с нормализацией сначала FT 9).0013 4 , затем Т 3 , в последнюю очередь ТТГ при гипертиреозе и с нормализацией сначала Т 3 , затем ФТ 4 , и в последнюю очередь ТТГ при гипотиреозе) [9]. Четыре международные ассоциации щитовидной железы могут рассмотреть вопрос о создании комитета для изучения того, имеет ли система оценок достаточные преимущества для ее повсеместного принятия.
Текущее определение SHyper и SHypo основано только на биохимических критериях и не указывает, что биохимическая аномалия должна быть связана с заболеванием щитовидной железы. Хотя подавляющее большинство значений ТТГ выходит за пределы референтного диапазона при нормальном ФТ 4 и Т 3 обусловлены заболеванием щитовидной железы и последствиями его лечения, то же самое биохимическое созвездие может иметь место при состояниях, не связанных с патологией щитовидной железы. Примерами являются влияние гетерофильных антител на анализ ТТГ, избыток или дефицит глюкокортикоидов, нетиреоидные заболевания и ожирение. Таким образом, то, что мы называем субклинической дисфункцией щитовидной железы, иногда вызывается измененной регуляцией оси гипоталамус-гипофиз-щитовидная железа и не связано с заболеваниями самой щитовидной железы. Например, слегка повышенный уровень ТТГ у лиц с ожирением нормализуется при снижении веса, и нет никаких доказательств того, что в этих обстоятельствах будет полезен левотироксин [10]. Я бы воздержался от лечения SHyper радиоактивным йодом или антитиреоидными препаратами, если нет положительных доказательств того, что низкий или подавленный ТТГ вызван патологией щитовидной железы. Точно так же я бы начал лечение левотироксином SHypo с большей уверенностью, если бы знал о наличии патологии щитовидной железы. Аутоиммунный тиреоидит является наиболее частой причиной SHypo, но антитела к ТПО и/или ТГ не обнаруживаются примерно в 20% случаев.
Примерами являются влияние гетерофильных антител на анализ ТТГ, избыток или дефицит глюкокортикоидов, нетиреоидные заболевания и ожирение. Таким образом, то, что мы называем субклинической дисфункцией щитовидной железы, иногда вызывается измененной регуляцией оси гипоталамус-гипофиз-щитовидная железа и не связано с заболеваниями самой щитовидной железы. Например, слегка повышенный уровень ТТГ у лиц с ожирением нормализуется при снижении веса, и нет никаких доказательств того, что в этих обстоятельствах будет полезен левотироксин [10]. Я бы воздержался от лечения SHyper радиоактивным йодом или антитиреоидными препаратами, если нет положительных доказательств того, что низкий или подавленный ТТГ вызван патологией щитовидной железы. Точно так же я бы начал лечение левотироксином SHypo с большей уверенностью, если бы знал о наличии патологии щитовидной железы. Аутоиммунный тиреоидит является наиболее частой причиной SHypo, но антитела к ТПО и/или ТГ не обнаруживаются примерно в 20% случаев. У таких пациентов УЗИ щитовидной железы может предоставить ранние доказательства аутоиммунитета щитовидной железы [2]. В идеале должно быть продемонстрировано заболевание щитовидной железы, но во всех случаях должны быть исключены причины, не связанные со щитовидной железой. Таким образом, можно рассмотреть добавление наличия патологии щитовидной железы в качестве еще одного критерия для диагноза: SHyper и SHypo определяются аномальным уровнем ТТГ (в присутствии нормальных свободных гормонов щитовидной железы), который связан с заболеванием щитовидной железы. Это облегчило бы принятие решений о лечении, поскольку субъекту с аномальным уровнем ТТГ, не связанным с патологией щитовидной железы, вряд ли будет полезна терапия, направленная на дефицит или избыток гормонов щитовидной железы.
У таких пациентов УЗИ щитовидной железы может предоставить ранние доказательства аутоиммунитета щитовидной железы [2]. В идеале должно быть продемонстрировано заболевание щитовидной железы, но во всех случаях должны быть исключены причины, не связанные со щитовидной железой. Таким образом, можно рассмотреть добавление наличия патологии щитовидной железы в качестве еще одного критерия для диагноза: SHyper и SHypo определяются аномальным уровнем ТТГ (в присутствии нормальных свободных гормонов щитовидной железы), который связан с заболеванием щитовидной железы. Это облегчило бы принятие решений о лечении, поскольку субъекту с аномальным уровнем ТТГ, не связанным с патологией щитовидной железы, вряд ли будет полезна терапия, направленная на дефицит или избыток гормонов щитовидной железы.
Применение контрольных диапазонов для определения того, является ли данное значение ТТГ ненормальным, не так просто, как кажется. «Что нормально?» — вопрос почти философский, и ответ на него (то, что не ненормально) сопряжен с трудностями. Моя любимая цитата по этому вопросу принадлежит Бенсону [11]: «Нормальный диапазон играет неясную, но утешительную роль в лабораторной медицине. Он маячит на горизонте нашего сознания, совершенно симметричный, как гора Фудзияма, несколько туманный в своих значениях, но с благодарностью почитаемый и признанный. Однако далеко не простое и чистое, как заветная иллюзия детства, при ближайшем рассмотрении оно оказывается безумно сложным и действительно представляет собой одну из самых упорных и трудных проблем, ограничивающих полезность клинических лабораторных данных». Исследование III, проведенное в США, стало важным исследованием для установления надежных референтных диапазонов ТТГ [12]. В их так называемой «эталонной популяции» средний уровень ТТГ составлял 1,39.мЕд/л с референсным интервалом 0,45–4,12 мЕд/л (P2,5–P97,5). Однако наблюдалось четкое возрастное влияние на значения ТТГ: медианные значения ТТГ и их референтные диапазоны в возрастных группах 20-29, 60-69, 70-79 и ≥80 лет составляют 1,26 (0,40-3,56), 1,67.
Моя любимая цитата по этому вопросу принадлежит Бенсону [11]: «Нормальный диапазон играет неясную, но утешительную роль в лабораторной медицине. Он маячит на горизонте нашего сознания, совершенно симметричный, как гора Фудзияма, несколько туманный в своих значениях, но с благодарностью почитаемый и признанный. Однако далеко не простое и чистое, как заветная иллюзия детства, при ближайшем рассмотрении оно оказывается безумно сложным и действительно представляет собой одну из самых упорных и трудных проблем, ограничивающих полезность клинических лабораторных данных». Исследование III, проведенное в США, стало важным исследованием для установления надежных референтных диапазонов ТТГ [12]. В их так называемой «эталонной популяции» средний уровень ТТГ составлял 1,39.мЕд/л с референсным интервалом 0,45–4,12 мЕд/л (P2,5–P97,5). Однако наблюдалось четкое возрастное влияние на значения ТТГ: медианные значения ТТГ и их референтные диапазоны в возрастных группах 20-29, 60-69, 70-79 и ≥80 лет составляют 1,26 (0,40-3,56), 1,67.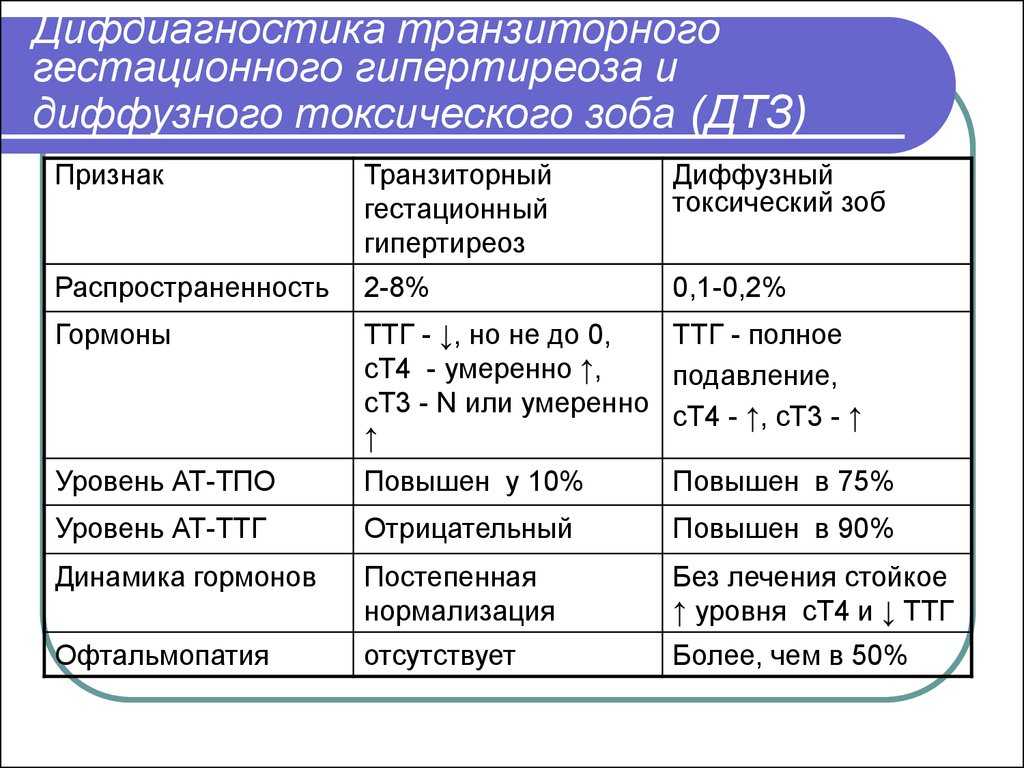 (0,49–4,33), 1,76 (0,45–5,90) и 1,90 (0,33–7,50) мЕд/л соответственно [12]. Принимая во внимание более высокие значения ТТГ с возрастом, распространенность SHypo может быть значительно завышена, если только не используется возрастной диапазон ТТГ [13]. В рекомендациях не предлагаются референтные диапазоны для определенного возраста (что я бы счел вполне логичным), но рекомендуется очень консервативный подход к назначению левотироксина пациентам с SHypo в возрасте 70 лет и старше, но на основании других соображений, помимо верхней границы нормы. ТТГ, который увеличивается с возрастом [2].
(0,49–4,33), 1,76 (0,45–5,90) и 1,90 (0,33–7,50) мЕд/л соответственно [12]. Принимая во внимание более высокие значения ТТГ с возрастом, распространенность SHypo может быть значительно завышена, если только не используется возрастной диапазон ТТГ [13]. В рекомендациях не предлагаются референтные диапазоны для определенного возраста (что я бы счел вполне логичным), но рекомендуется очень консервативный подход к назначению левотироксина пациентам с SHypo в возрасте 70 лет и старше, но на основании других соображений, помимо верхней границы нормы. ТТГ, который увеличивается с возрастом [2].
Напротив, потребность в референтных диапазонах ТТГ для конкретных триместров у беременных женщин общепризнанна [3,14]. Проблема, однако, заключается в том, что большинство лабораторий не установили свои собственные диапазоны ТТГ по триместрам для женщин, проживающих в своем регионе и применяющих свой собственный анализ ТТГ. В этом случае рекомендации предлагают использовать так называемые «международные референтные диапазоны для конкретных триместров» с верхними нормальными пределами ТТГ 2,5, 3,0 и 3,5 в 1-м, 2-м и 3-м триместрах соответственно. В настоящее время опубликовано несколько статей, демонстрирующих, что верхние нормальные пределы ТТГ, установленные в местном регионе, почти без исключения намного выше международных [15,16]. По сравнению с региональными референтными диапазонами применение международных референтных диапазонов приводит к значительно более высоким показателям распространенности SHypo в каждом триместре. Следует сделать вывод, что, следуя рекомендациям предыдущих руководств по лечению SHypo во время беременности с применением международных референтных диапазонов ТТГ, многие женщины могли бы лечиться левотироксином, что было бы ненужным, если бы применялись региональные референсные диапазоны.
В настоящее время опубликовано несколько статей, демонстрирующих, что верхние нормальные пределы ТТГ, установленные в местном регионе, почти без исключения намного выше международных [15,16]. По сравнению с региональными референтными диапазонами применение международных референтных диапазонов приводит к значительно более высоким показателям распространенности SHypo в каждом триместре. Следует сделать вывод, что, следуя рекомендациям предыдущих руководств по лечению SHypo во время беременности с применением международных референтных диапазонов ТТГ, многие женщины могли бы лечиться левотироксином, что было бы ненужным, если бы применялись региональные референсные диапазоны.
Другим ограничением референтных диапазонов является узкая индивидуальная вариация уровня ТТГ в сыворотке [17]. Значения ТТГ у отдельного субъекта, по-видимому, всегда находятся в узкой области где-то в гораздо более широком референтном диапазоне; таким образом, у одного субъекта значения ТТГ могут быть на нижнем конце референтного диапазона, а у другого всегда на верхнем конце. Что касается дисперсии анализов ТТГ, аналитические, внутрииндивидуальные и межиндивидуальные коэффициенты вариации результатов ТТГ составляют 7,5, 16,2 и 31,7% соответственно [18]. Отношение внутрииндивидуальной вариации к межиндивидуальной вариации можно использовать для надежности эталонных диапазонов. Если отношение > 1,4, референтный диапазон на основе популяции работает, как предполагалось. Если отношение <0,6, референтный диапазон на основе популяции является нечувствительным показателем для большинства субъектов. На самом деле, соотношение составляет <0,6 для всех тестов функции щитовидной железы. Для ТТГ в литературе упоминается соотношение 0,36 [19], 0,49 [17] и 0,50 [18]. Существенная индивидуальная вариация ТТГ может объяснить, почему среди субъектов с SHypo и одинаковыми значениями ТТГ и FT 4 у одних есть симптомы, а у других нет: исходное значение ТТГ у тех, у кого есть симптомы, могло быть намного ниже, чем те, у кого нет симптомов, и они должны пройти большее расстояние по линии регрессии ТТГ/ФТ 4 , чтобы получить такое же значение ТТГ.
Что касается дисперсии анализов ТТГ, аналитические, внутрииндивидуальные и межиндивидуальные коэффициенты вариации результатов ТТГ составляют 7,5, 16,2 и 31,7% соответственно [18]. Отношение внутрииндивидуальной вариации к межиндивидуальной вариации можно использовать для надежности эталонных диапазонов. Если отношение > 1,4, референтный диапазон на основе популяции работает, как предполагалось. Если отношение <0,6, референтный диапазон на основе популяции является нечувствительным показателем для большинства субъектов. На самом деле, соотношение составляет <0,6 для всех тестов функции щитовидной железы. Для ТТГ в литературе упоминается соотношение 0,36 [19], 0,49 [17] и 0,50 [18]. Существенная индивидуальная вариация ТТГ может объяснить, почему среди субъектов с SHypo и одинаковыми значениями ТТГ и FT 4 у одних есть симптомы, а у других нет: исходное значение ТТГ у тех, у кого есть симптомы, могло быть намного ниже, чем те, у кого нет симптомов, и они должны пройти большее расстояние по линии регрессии ТТГ/ФТ 4 , чтобы получить такое же значение ТТГ. Следовательно, их падение концентраций FT 4 в пределах референтного диапазона больше, что повышает вероятность появления симптомов [9].].
Следовательно, их падение концентраций FT 4 в пределах референтного диапазона больше, что повышает вероятность появления симптомов [9].].
Связь между аномальными тестами функции щитовидной железы и неблагоприятными последствиями для здоровья также верна для результатов тестов в пределах референтного диапазона. Например, чем выше значение FT 4 находится в пределах референтного диапазона 10–22 пмоль/л, тем выше распространенность фибрилляции предсердий [20], и чем ниже значение ТТГ находится в референтном диапазоне 0,5–5,0 мЕд. /л, тем выше распространенность остеопороза у здоровых женщин в постменопаузе [21]. Вероятность неблагоприятных исходов для более высоких уровней ТТГ в пределах референтного диапазона по сравнению с более низкими уровнями ТТГ в пределах референтного диапазона значительна для комбинированных сердечно-сосудистых исходов (ОШ 1,21, 9).5% ДИ: 1,15–1,27), для комбинированных метаболических исходов (ОШ 1,37, 95% ДИ: 1,27–1,48) и для комбинированных костных исходов (ОШ 0,55, 95% ДИ: 0,41–0,72) [22]. Неудивительно, что риск неблагоприятных последствий для здоровья увеличивается до значений в пределах референтного диапазона, поскольку нет веских физиологических причин, по которым риск должен останавливаться на границах (произвольно определенного) референтного диапазона. Я согласен с комментарием о том, что «континуум эффектов в референтном диапазоне функции щитовидной железы предполагает, что было бы более уместно рассматривать уровни гормонов щитовидной железы как «факторы риска» заболевания (аналогично артериальному давлению или холестерину при сердечно-сосудистых заболеваниях). чем считать тот или иной уровень нормальным или ненормальным» [22]. В том же духе исследование среди проживающих в сообществе субъектов США в возрасте ≥65 лет показало, что более высокий уровень ТТГ и более низкий уровень FT 4 концентрации в пределах эутиреоидного диапазона (ТТГ: 0,45–4,5 мЕд/л) связаны с более низким риском множественных нежелательных явлений, включая смертность [23]. Это предполагает толерантность к более низким уровням гормонов щитовидной железы у пожилых людей, что согласуется с рекомендациями относительно консервативного назначения левотироксина пожилым людям с SHypo [2].
Неудивительно, что риск неблагоприятных последствий для здоровья увеличивается до значений в пределах референтного диапазона, поскольку нет веских физиологических причин, по которым риск должен останавливаться на границах (произвольно определенного) референтного диапазона. Я согласен с комментарием о том, что «континуум эффектов в референтном диапазоне функции щитовидной железы предполагает, что было бы более уместно рассматривать уровни гормонов щитовидной железы как «факторы риска» заболевания (аналогично артериальному давлению или холестерину при сердечно-сосудистых заболеваниях). чем считать тот или иной уровень нормальным или ненормальным» [22]. В том же духе исследование среди проживающих в сообществе субъектов США в возрасте ≥65 лет показало, что более высокий уровень ТТГ и более низкий уровень FT 4 концентрации в пределах эутиреоидного диапазона (ТТГ: 0,45–4,5 мЕд/л) связаны с более низким риском множественных нежелательных явлений, включая смертность [23]. Это предполагает толерантность к более низким уровням гормонов щитовидной железы у пожилых людей, что согласуется с рекомендациями относительно консервативного назначения левотироксина пожилым людям с SHypo [2]. Данные подтверждают смещение верхнего нормального предела референтного диапазона ТТГ вверх у пожилых людей [13]. Совсем недавно анализ данных отдельных участников 14 когорт не выявил связи уровней ТТГ в пределах референтного диапазона (0,45-4,5 мЕд/л) с риском развития ишемической болезни сердца или смертности, но обнаружил U-образную связь с FT 4 уровней в пределах референтного диапазона [24]; по мнению авторов, нельзя полностью исключить случайные находки.
Данные подтверждают смещение верхнего нормального предела референтного диапазона ТТГ вверх у пожилых людей [13]. Совсем недавно анализ данных отдельных участников 14 когорт не выявил связи уровней ТТГ в пределах референтного диапазона (0,45-4,5 мЕд/л) с риском развития ишемической болезни сердца или смертности, но обнаружил U-образную связь с FT 4 уровней в пределах референтного диапазона [24]; по мнению авторов, нельзя полностью исключить случайные находки.
Наблюдаемые связи между SHyper и SHypo и неблагоприятными последствиями для здоровья не являются доказательством причинно-следственной связи. Причинность, однако, вероятна ввиду ее биологической достоверности (например, гипертиреоз является определенным фактором риска фибрилляции предсердий и потери костной массы) и наличия зависимости доза-реакция. Последнее обеспечивает обоснование рекомендации по вмешательству при гипертиреозе степени IB (SHyper ТТГ ≤0,1 мЕд/л) и при гипотиреозе IB степени (SHypo ТТГ ≥10 мЕд/л). Руководящие принципы сходятся во мнении, что при степени IA при принятии решения о вмешательстве или воздержании от лечения следует учитывать другие факторы риска. При гипертиреозе степени IA (SHyper ТТГ >0,1–<0,4 мЕд/л) наличие пожилого возраста (> 65 лет), постменопаузы, остеопороза и сердечно-сосудистых факторов риска должно склонить чашу весов в пользу вмешательства, которое, как мы надеемся, принесет больше пользы, чем вреда. ; однако при гипотиреозе степени IA (SHypo ТТГ от >4,0 до <10 мЕд/л) возраст <70 лет, симптомы, беременность (желание) и сердечно-сосудистые факторы риска благоприятствовали бы назначению левотироксина. В этих рекомендациях значения ТТГ рассматриваются как еще один фактор риска конкретного заболевания, и решение лечить или не лечить зависит от контекста субъекта в отношении возраста и других факторов риска. Это напоминает мне клиническое принятие решения о том, когда начинать прием антигипертензивных препаратов или статинов у внешне здоровых людей с риском сердечно-сосудистых заболеваний.
Руководящие принципы сходятся во мнении, что при степени IA при принятии решения о вмешательстве или воздержании от лечения следует учитывать другие факторы риска. При гипертиреозе степени IA (SHyper ТТГ >0,1–<0,4 мЕд/л) наличие пожилого возраста (> 65 лет), постменопаузы, остеопороза и сердечно-сосудистых факторов риска должно склонить чашу весов в пользу вмешательства, которое, как мы надеемся, принесет больше пользы, чем вреда. ; однако при гипотиреозе степени IA (SHypo ТТГ от >4,0 до <10 мЕд/л) возраст <70 лет, симптомы, беременность (желание) и сердечно-сосудистые факторы риска благоприятствовали бы назначению левотироксина. В этих рекомендациях значения ТТГ рассматриваются как еще один фактор риска конкретного заболевания, и решение лечить или не лечить зависит от контекста субъекта в отношении возраста и других факторов риска. Это напоминает мне клиническое принятие решения о том, когда начинать прием антигипертензивных препаратов или статинов у внешне здоровых людей с риском сердечно-сосудистых заболеваний. Высокое кровяное давление и высокий уровень холестерина связаны с неблагоприятными последствиями для здоровья, но решение о лечении может зависеть и от других факторов риска (например, возраста, пола, курения, диабета). Для решения этой проблемы были разработаны диаграммы, которые сразу же визуализируют, когда лечение оправдано: определенно, если сердечно-сосудистый риск в течение следующих 10 лет составляет >20% (рис. ) [25]. Возникает вопрос, можно ли построить аналогичные диаграммы для оценки полезности лечения определенного уровня ТТГ в сочетании с другими факторами риска.
Высокое кровяное давление и высокий уровень холестерина связаны с неблагоприятными последствиями для здоровья, но решение о лечении может зависеть и от других факторов риска (например, возраста, пола, курения, диабета). Для решения этой проблемы были разработаны диаграммы, которые сразу же визуализируют, когда лечение оправдано: определенно, если сердечно-сосудистый риск в течение следующих 10 лет составляет >20% (рис. ) [25]. Возникает вопрос, можно ли построить аналогичные диаграммы для оценки полезности лечения определенного уровня ТТГ в сочетании с другими факторами риска.
Открыть в отдельном окне
Таблица прогнозирования риска сердечно-сосудистых заболеваний Объединенного британского общества для женщин без диабета (слева) и мужчин (справа) [25]. САД = систолическое артериальное давление; TC:HDL = отношение общего холестерина сыворотки к холестерину HDL; зеленая, оранжевая и красная области обозначают риск сердечно-сосудистых заболеваний <10, 10-20 и >20% в течение следующих 10 лет соответственно; белая кривая обозначает риск сердечно-сосудистых заболеваний 30% в течение следующих 10 лет.
За последнее десятилетие был достигнут значительный прогресс, особенно благодаря Сотрудничеству по изучению щитовидной железы. Этот консорциум объединил данные 11 международных проспективных когортных исследований, что позволило проанализировать данные отдельных участников из примерно 55 000 человек с периодом наблюдения около 543 000 человеко-лет. Анализ данных отдельных участников обычно считается высшим уровнем нерандомизированных доказательств, и они обеспечивают надежные количественные оценки сопутствующих рисков. Однако вопрос о том, принесет ли профилактическое вмешательство больше пользы, чем вреда, требует проведения рандомизированных клинических испытаний с большим размером выборки и длительным наблюдением. Делать такие испытания непросто. Испытание на SHyper, сравнивающее 131 I лечение плацебо было прекращено, потому что набор был очень низким. К счастью, Европейская комиссия недавно профинансировала исследование TRUST, многоцентровое двойное слепое плацебо-контролируемое рандомизированное исследование с участием 3000 взрослых в возрасте 65 лет и старше с персистирующим SHypo ({"type":"clinical-trial","attrs":{" текст":"NCT01660126","term_id":"NCT01660126"}}NCT01660126). Тем не менее, мы не получим основанных на фактических данных указаний о том, как лечить более молодых пациентов. Финансирование таких исследований является проблемой. Тем не менее, число субъектов, принимающих препараты гормонов щитовидной железы, огромно (порядка 2,5% населения) и значительно увеличилось за последнее десятилетие: количество назначений левотироксина натрия в период 2006-2010 гг. увеличилось на 33% в Нидерландах, 37% в Великобритании и 42% в США [26,27]. Похоже, что основной причиной увеличения числа потребителей тиреоидных гормонов является лечение SHypo: медиана ТТГ в начале приема левотироксина упала с 8,7 до 7,9.мЕд/л в период с 2001 по 2009 г. с скорректированным на популяцию ОШ 1,30 (95% ДИ: 1,19-1,42) для назначения L-T 4 при уровне ТТГ ≤10 мЕд/л [27]. Таким образом, кажется вполне разумным просить финансовой помощи для создания логистики для сбора и хранения данных таких крупных испытаний, которые могли бы проводиться отдельными эндокринологами в их собственной практике в различных европейских странах.
Тем не менее, мы не получим основанных на фактических данных указаний о том, как лечить более молодых пациентов. Финансирование таких исследований является проблемой. Тем не менее, число субъектов, принимающих препараты гормонов щитовидной железы, огромно (порядка 2,5% населения) и значительно увеличилось за последнее десятилетие: количество назначений левотироксина натрия в период 2006-2010 гг. увеличилось на 33% в Нидерландах, 37% в Великобритании и 42% в США [26,27]. Похоже, что основной причиной увеличения числа потребителей тиреоидных гормонов является лечение SHypo: медиана ТТГ в начале приема левотироксина упала с 8,7 до 7,9.мЕд/л в период с 2001 по 2009 г. с скорректированным на популяцию ОШ 1,30 (95% ДИ: 1,19-1,42) для назначения L-T 4 при уровне ТТГ ≤10 мЕд/л [27]. Таким образом, кажется вполне разумным просить финансовой помощи для создания логистики для сбора и хранения данных таких крупных испытаний, которые могли бы проводиться отдельными эндокринологами в их собственной практике в различных европейских странах. Сможет ли ETA начать такие исследования?
Сможет ли ETA начать такие исследования?
Автор заявляет об отсутствии конфликта интересов.
1. Бионди Б., Барталена Л., Купер С.Д., Хегедюс Л., Лаурберг П., Кахали Г.Дж. Рекомендации Европейской ассоциации щитовидной железы 2015 г. по диагностике и лечению эндогенного субклинического гипертиреоза. Eur Thyroid J. 2015;4:149–163. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Pearce SHS, Brabant G, Duntas LH, Monzani F, Peeters RP, Razvi S, Wemeau J-L. Руководство ETA 2013 г.: Ведение субклинического гипотиреоза. Eur Thyroid J. 2013;2:215–228. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Lazarus J, Brown RS, Daumerie C, Hubalewska-Dydejczyk A, Negro R, Vaidya B. Руководство ETA 2014 г. по лечению субклинического гипотиреоза у беременных и детей. Eur Thyroid J. 2014; 3:76–92. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Stott DJ, Bauer DC, Ford I, et al. Дилемма лечения субклинического гипотиреоза: риск того, что текущие рекомендации принесут больше вреда, чем пользы.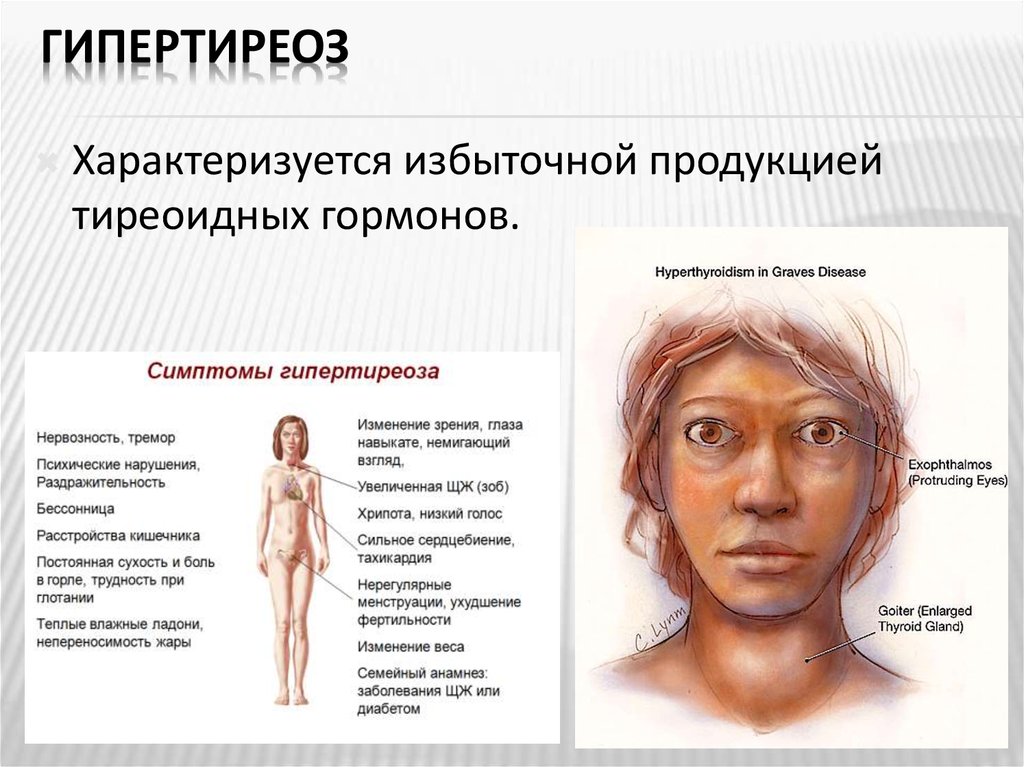 Eur Thyroid J. 2014; 3:137–138. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Eur Thyroid J. 2014; 3:137–138. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Sawin CT, Geller A, Wolf PA, et al. Низкие концентрации тиреотропина в сыворотке как фактор риска фибрилляции предсердий у пожилых людей. N Engl J Med. 1994; 331:1249–1252. [PubMed] [Google Scholar]
6. Zulewski H, Müller B, Exer P, et al. Оценка тканевого гипотиреоза по новой клинической шкале: оценка пациентов с различными степенями гипотиреоза и контроля. J Clin Endocrinol Metab. 1997; 82: 771–776. [PubMed] [Google Scholar]
7. Дунтас Л.Х. Субклинический гипотиреоз: неправильное название в поисках нового названия. Щитовидная железа. 2001; 11: 361–362. [PubMed] [Академия Google]
8. Evered DC, Ormston BJ, Smith PA, et al. Степени гипотиреоза. Br Med J. 1973; 1: 657–662. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Wiersinga WM. Гипотиреоз и микседематозная кома. В: Джеймсон Дж. Л., ДеГрут Л. Дж., редакторы. Эндокринология: взрослая и детская. Филадельфия: Эльзевир Сондерс; 2016.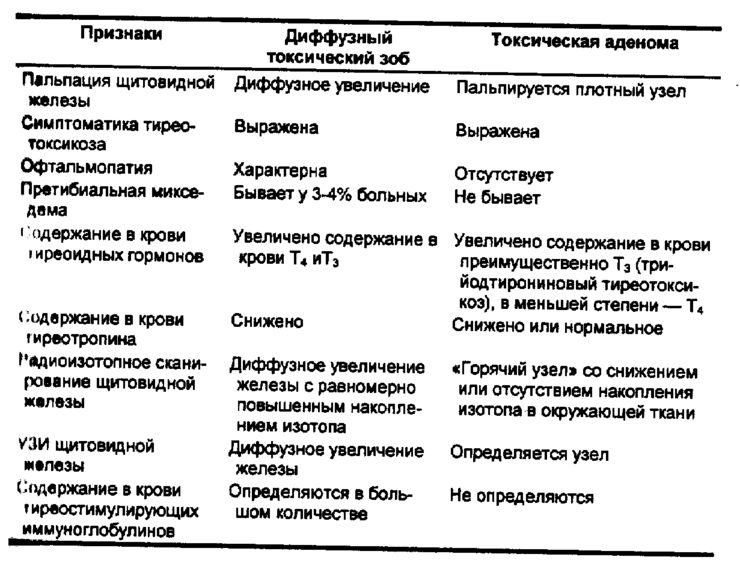 С. 1540–1556. [Google Scholar]
С. 1540–1556. [Google Scholar]
10. Лаурберг П., Кнудсен Н., Андерсен С., Карл А., Педерсен И.Б., Кармишолт Дж. Функция щитовидной железы и ожирение. Европейский щитовидная железа J. 2012; 1: 159–167. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Benson ES. Понятие нормального диапазона. Хум Патол. 1972; 3: 152–155. [PubMed] [Google Scholar]
12. Hollowell JG, Staehling NW, Flanders WD, et al. ТТГ в сыворотке, T 4 и антитела к щитовидной железе у населения США (1988–1994 гг.): Национальное обследование состояния здоровья и питания (NHANES III) J Clin Endocrinol Metab. 2002; 87: 489–499. [PubMed] [Google Scholar]
13. Surks MI, Holllowell JG. Возрастное распределение сывороточного тиреотропина и антитиреоидных антител в популяции США: влияние на распространенность субклинического гипотиреоза. J Clin Endocrinol Metab. 2007;92: 4575–4582. [PubMed] [Google Scholar]
14. Stagnaro-Green A, Abalovich M, Alexander E, et al. Рекомендации Американской ассоциации щитовидной железы по диагностике и лечению заболеваний щитовидной железы во время беременности и после родов. J Clin Endocrinol Metab. 2011; 21:1–45. [Google Scholar]
J Clin Endocrinol Metab. 2011; 21:1–45. [Google Scholar]
15. Amouzegar A, Ainy E, Khazan M, Mehran L, Hedayati M, Azizi F. Местные и международные рекомендуемые эталоны ТТГ при оценке функции щитовидной железы во время беременности. Горм Метаб Рез. 2014;46:206–210. [PubMed] [Академия Google]
16. Медичи М., Кореваар Т.И., Виссер В.Е., Виссер Т.Дж., Петерс Р.П. Функция щитовидной железы при беременности: что в норме? Клин Хим. 2015;61:704–713. [PubMed] [Google Scholar]
17. Andersen S, Pedersen KM, Bruun NH, Laurberg P. Узкие индивидуальные вариации в сыворотке T 4 и T 3 у здоровых людей: ключ к пониманию субклинического заболевания щитовидной железы . J Clin Endocrinol Metab. 2002; 87: 1068–1072. [PubMed] [Google Scholar]
18. Браунинг М.С., Форд Р.П., Каллаган С.Дж., Фрейзер К.Г. Внутри- и межиндивидуальные биологические вариации пяти аналитов, используемых при оценке функции щитовидной железы: последствия для необходимых стандартов работы и интерпретации результатов.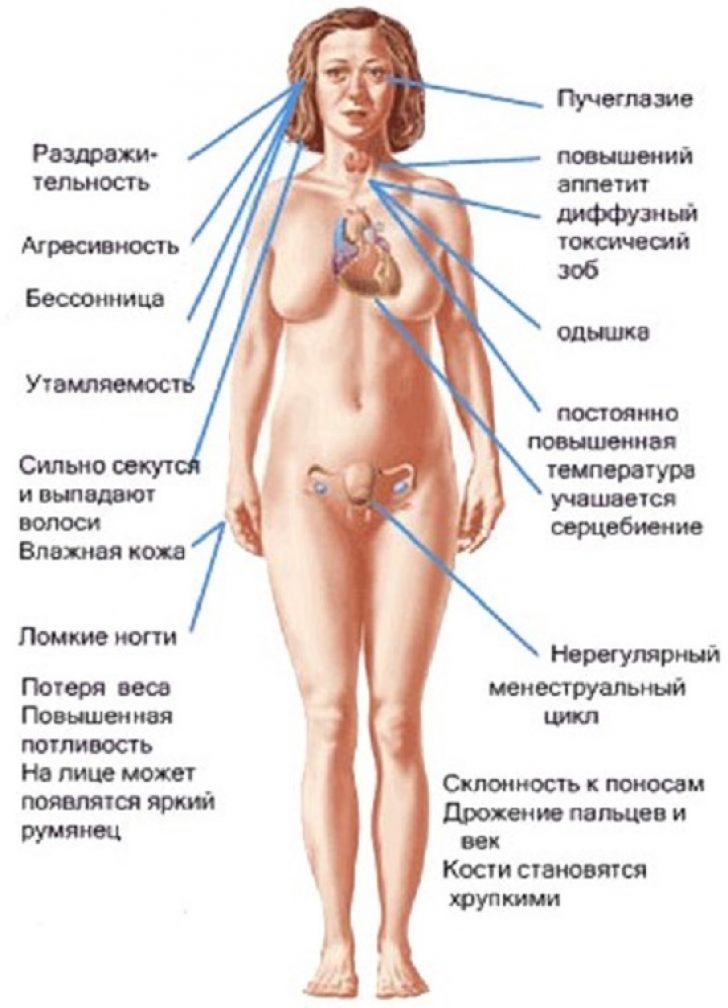 Клин Хим. 1986;32:962–966. [PubMed] [Google Scholar]
Клин Хим. 1986;32:962–966. [PubMed] [Google Scholar]
19. Нагаяма И., Ямамото К., Сайто К., Кузуя Т., Сайто Т. Субъектные референсные значения в тестах функции щитовидной железы. Endocr J. 1993; 40: 557–562. [PubMed] [Google Scholar]
20. Gammage MD, Parle JV, Holder RL, et al. Связь между концентрацией свободного тироксина в сыворотке крови и мерцательной аритмией. Arch Intern Med. 2007; 167: 928–934. [PubMed] [Google Scholar]
21. Kim DJ, Khang YH, Koh JM, Shong YK, Kim GS. Низкий нормальный уровень ТТГ связан с низкой минеральной плотностью костей у здоровых женщин в постменопаузе. Клин Эндокринол. 2006; 64: 86–90. [PubMed] [Google Scholar]
22. Taylor PN, Razvi S, Pearce SH, Dayan CM. Обзор клинических последствий изменения функции щитовидной железы в пределах референтного диапазона. J Clin Endocrinol Metab. 2013;98:3562–3571. [PubMed] [Google Scholar]
23. Каппола А.Р., Арнольд А.М., Вулчин К., Карлсон М., Роббинс Дж., Псати Б.М. Функция щитовидной железы в эутиреоидном диапазоне и неблагоприятные исходы у пожилых людей. J Clin Endocrinol Metab. 2015; 100:1088–1096. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Clin Endocrinol Metab. 2015; 100:1088–1096. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Asvold BO, Vatten LJ, Bjoro T, et al. Функция щитовидной железы в пределах нормы и риск ишемической болезни сердца: анализ данных отдельных участников 14 когорт. JAMA Стажер Мед. 2015; 175:1037–1047. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Британское кардиологическое общество. Британское общество гипертонии, Diabetes UK, HEART UK. Общество сердечно-сосудистых заболеваний первичной медико-санитарной помощи. The Stroke Association JBS2: Рекомендации объединенных британских обществ по профилактике сердечно-сосудистых заболеваний в клинической практике. Сердце. 2005;91 (приложение V): 1–52. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. de Jong NW, Baljet GM. Использование T 4 , T 4 + T 3 и T 3 среди населения Нидерландов. Eur Thyroid J. 2012; 1:135–136. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Taylor PN, Iqbal A, Minassian C, et al. Неудачный порог для лечения пограничных повышенных уровней тиреотропина – баланс преимуществ и рисков: данные крупного исследования на базе сообщества. JAMA Стажер Мед. 2014; 174:32–39. [PubMed] [Google Scholar]
Taylor PN, Iqbal A, Minassian C, et al. Неудачный порог для лечения пограничных повышенных уровней тиреотропина – баланс преимуществ и рисков: данные крупного исследования на базе сообщества. JAMA Стажер Мед. 2014; 174:32–39. [PubMed] [Google Scholar]
1. Bahn Chair RS, Burch HB, Cooper DS, Garber JR, Greenlee MC, Klein I, et al. Гипертиреоз и другие причины тиреотоксикоза: рекомендации по ведению Американской ассоциации щитовидной железы и Американской ассоциации клинических эндокринологов. Щитовидная железа. 2011;21(6):593–646. doi: 10.1089/thy.2010.0417. [PubMed] [CrossRef] [Google Scholar]
2. Hollowell JG, Staehling NW, Flanders WD, Hannon WH, Gunter EW, Spencer CA, et al. Сывороточный ТТГ, Т(4) и антитела к щитовидной железе у населения США (19с 88 по 1994 г.): Национальное обследование состояния здоровья и питания (NHANES III). J Clin Endocrinol Metab. 2002;87(2):489–99. [PubMed] [Google Scholar]
3. Spencer CA, Hollowell JG, Kazarosyan M, Braverman LE. Взаимосвязь между тиреотропным гормоном (ТТГ) и антителами к тиреопероксидазе, проведенная Национальным исследованием здоровья и питания III, показывает, что верхние референсные пределы ТТГ могут быть искажены скрытой дисфункцией щитовидной железы. J Clin Endocrinol Metab. 2007;92(11):4236–40. doi: 10.1210/jc.2007-0287. [PubMed] [CrossRef] [Академия Google]
Взаимосвязь между тиреотропным гормоном (ТТГ) и антителами к тиреопероксидазе, проведенная Национальным исследованием здоровья и питания III, показывает, что верхние референсные пределы ТТГ могут быть искажены скрытой дисфункцией щитовидной железы. J Clin Endocrinol Metab. 2007;92(11):4236–40. doi: 10.1210/jc.2007-0287. [PubMed] [CrossRef] [Академия Google]
4. Baskin HJ, Cobin RH, Duick DS, Gharib H, Guttler RB, Kaplan MM, et al. Медицинские рекомендации Американской ассоциации клинических эндокринологов для клинической практики по оценке и лечению гипертиреоза и гипотиреоза. Эндокр Практ. 2002;8(6):457–69. [PubMed] [Google Scholar]
5. Surks MI, Boucai L. Референтные пределы сывороточного тиреотропина на основе возраста и расы. J Clin Endocrinol Metab. 2010;95(2):496–502. doi: 10.1210/jc.2009-1845. [PubMed] [CrossRef] [Академия Google]
6. Boucai L, Hollowell JG, Surks MI. Подход к разработке возрастных, гендерных и этнических референтных пределов тиреотропина. Щитовидная железа. 2011;21(1):5–11. doi: 10.1089/thy.2010.0092. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Щитовидная железа. 2011;21(1):5–11. doi: 10.1089/thy.2010.0092. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Baloch Z, Carayon P, Conte-Devolx B, Demers LM, Feldt-Rasmussen U, Henry JF, et al. Руководство по лабораторной медицине. Лабораторная поддержка диагностики и мониторинга заболеваний щитовидной железы. Щитовидная железа. 2003;13(1):3–126. дои: 10.1089/105072503321086962. [PubMed] [CrossRef] [Google Scholar]
8. Фатуречи В. Верхний предел нормального уровня тиреотропного гормона в сыворотке: движущаяся цель, а теперь и старение? J Clin Endocrinol Metab. 2007;92(12):4560–2. doi: 10.1210/jc.2007-2285. [PubMed] [CrossRef] [Google Scholar]
9. Surks MI, Hollowell JG. Возрастное распределение сывороточного тиреотропина и антитиреоидных антител в популяции США: влияние на распространенность субклинического гипотиреоза. J Clin Endocrinol Metab. 2007;92(12):4575–82. doi: 10.1210/jc.2007-1499. [PubMed] [CrossRef] [Google Scholar]
10. Galofré JC, Frühbeck G, Salvador J. Ожирение и функция щитовидной железы: патофизиологические и терапевтические последствия. Горячий тиреодол. 2010 [Google Scholar]
Ожирение и функция щитовидной железы: патофизиологические и терапевтические последствия. Горячий тиреодол. 2010 [Google Scholar]
11. Galofré JC, Payeras F, Silva C, Salvador J. Эндокринные функциональные тесты. В: Prieto JM, Yuste V, Ara JR, редакторы. Эльзевир Массон. Барселона: 2010. С. 329–406. [Google Scholar]
12. Купер Д.С. Субклиническое заболевание щитовидной железы: консенсус или загадка? Клин Эндокринол (Oxf). 2004;60(4):410–2. doi: 10.1111/j.1365-2265.2004.02031.x. [PubMed] [CrossRef] [Академия Google]
13. де лос Сантос Э.Т., Старич Г.Х., Маццаферри Э.Л. Чувствительность, специфичность и экономическая эффективность чувствительного анализа тиреотропина в диагностике заболеваний щитовидной железы у амбулаторных пациентов. Arch Intern Med. 1989;149(3):526–32. [PubMed] [Google Scholar]
14. Митчелл А.Л., Пирс С.Х. Как следует лечить пациентов с низкой концентрацией тиреотропина в сыворотке крови? Клин Эндокринол (Oxf). 2010;72(3):292–6. doi: 10. 1111/j.1365-2265.2009.03694.x. [PubMed] [CrossRef] [Академия Google]
1111/j.1365-2265.2009.03694.x. [PubMed] [CrossRef] [Академия Google]
15. Купер Д.С. Подход к пациенту с субклиническим гипертиреозом. J Clin Endocrinol Metab. 2007;92(1):3–9. doi: 10.1210/jc.2006-2472. [PubMed] [CrossRef] [Google Scholar]
16. Wartofsky L. Лечение субклинического гипертиреоза. J Clin Endocrinol Metab. 2011;96(1):59–61. doi: 10.1210/jc.2010-2409. [PubMed] [CrossRef] [Google Scholar]
17. Galofre JC, Davies TF. Аутоиммунные заболевания щитовидной железы у беременных: обзор. J Женское здоровье (Larchmt). 2009;18(11):1847–56. дои: 10.1089/jwh.2008.1234. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Galofre JC. [Лечение субклинического гипертиреоза]. Преподобный Медицинский Университет Наварры. 2007;51(1):18–22. [PubMed] [Google Scholar]
19. Parle JV, Franklyn JA, Cross KW, Jones SC, Sheppard MC. Распространенность и последующее наблюдение аномальных концентраций тиреотрофина (ТТГ) у пожилых людей в Соединенном Королевстве. Клин Эндокринол (Oxf). 1991;34(1):77–83. [PubMed] [Google Scholar]
Клин Эндокринол (Oxf). 1991;34(1):77–83. [PubMed] [Google Scholar]
20. Bjorndal MM, Sandmo Wilhelmsen K, Lu T, Jorde R. Распространенность и причины невыявленного гипертиреоза у взрослого здорового населения. Исследование Тромсё. Дж Эндокринол Инвест. 2008;31(10):856–60. [PubMed] [Академия Google]
21. Меерович Дж., Ротман-Пикельный П., Шерф М., Баттат Э., Леви Ю., Суркс М.И. Измерения сывороточного тиротропина в сообществе: пятилетнее наблюдение в большой сети врачей первичной медико-санитарной помощи. Arch Intern Med. 2007;167(14):1533–1538. doi: 10.1001/archinte.167.14.1533. [PubMed] [CrossRef] [Google Scholar]
22. Woeber KA. Наблюдения относительно естественного течения субклинического гипертиреоза. Щитовидная железа. 2005;15(7):687–91. doi: 10.1089/thy.2005.15.687. [PubMed] [CrossRef] [Академия Google]
23. Полковник Н.Ф., Суркс М.И., Дэниелс Г.Х. Субклиническое заболевание щитовидной железы: клиническое применение. ДЖАМА. 2004;291(2):239–43. дои: 10. 1001/jama.291.2.239. [PubMed] [CrossRef] [Google Scholar]
1001/jama.291.2.239. [PubMed] [CrossRef] [Google Scholar]
24. Diez JJ. Гипертиреоз у пациентов старше 55 лет: анализ этиологии и лечение. Геронтология. 2003;49(5):316–23. doi: 10.1159/000071713. [PubMed] [CrossRef] [Google Scholar]
25. Casey BM, Dashe JS, Wells CE, McIntire DD, Leveno KJ, Cunningham FG. Субклинический гипертиреоз и исходы беременности. Акушерство Гинекол. 2006; 107 (2 часть 1): 337–41. дои: 10.1097/01.АОГ.0000197991.64246.9а. [PubMed] [CrossRef] [Google Scholar]
26. Schouten BJ, Brownlie BE, Frampton CM, Turner JG. Субклинический тиреотоксикоз в амбулаторной популяции - предикторы исхода. Клин Эндокринол (Oxf). 2011;74(2):257–61. doi: 10.1111/j.1365-2265.2010.03908.x. [PubMed] [CrossRef] [Google Scholar]
27. Rosario PW. Естественная история субклинического гипертиреоза у пациентов в возрасте до 65 лет. Клин Эндокринол (Oxf). 2008;68(3):491–2. doi: 10.1111/j.1365-2265.2007.03030.x. [PubMed] [CrossRef] [Академия Google]
28. Льюис Г. Ф., Алесси К.А., Империал Дж.Г., Рефетофф С. Низкий индекс свободного тироксина в сыворотке у пожилых людей, передвигающихся пешком, обусловлен сбросом порога подавления обратной связи тиротропина. J Clin Endocrinol Metab. 1991;73(4):843–9. [PubMed] [Google Scholar]
Ф., Алесси К.А., Империал Дж.Г., Рефетофф С. Низкий индекс свободного тироксина в сыворотке у пожилых людей, передвигающихся пешком, обусловлен сбросом порога подавления обратной связи тиротропина. J Clin Endocrinol Metab. 1991;73(4):843–9. [PubMed] [Google Scholar]
29. Mariotti S, Barbesino G, Caturegli P, Bartalena L, Sansoni P, Fagnoni F, et al. Комплексное изменение функции щитовидной железы у здоровых долгожителей. J Clin Endocrinol Metab. 1993;77(5):1130–4. [PubMed] [Google Scholar]
30. Кляйн И., Данзи С. Заболевания щитовидной железы и сердце. Тираж. 2007;116(15):1725–35. doi: 10.1161/CIRCULATIONAHA.106.678326. [PubMed] [CrossRef] [Академия Google]
31. Surks MI, Ortiz E, Daniels GH, Sawin CT, Col NF, Cobin RH, et al. Субклиническое заболевание щитовидной железы: научный обзор и рекомендации по диагностике и лечению. ДЖАМА. 2004;291(2):228–38. doi: 10.1001/jama.291.2.228. [PubMed] [CrossRef] [Google Scholar]
32. Bauer DC, Ettinger B, Nevitt MC, Stone KL. Риск переломов у женщин с низким уровнем тиреотропного гормона в сыворотке крови. Энн Интерн Мед. 2001;134(7):561–8. [PubMed] [Google Scholar]
Риск переломов у женщин с низким уровнем тиреотропного гормона в сыворотке крови. Энн Интерн Мед. 2001;134(7):561–8. [PubMed] [Google Scholar]
33. Vadiveloo T, Donnan PT, Cochrane L, Leese GP. Исследование эпидемиологии, аудита и исследований щитовидной железы (TEARS): заболеваемость у пациентов с эндогенным субклиническим гипертиреозом. J Clin Endocrinol Metab. 2011;96 (5): 1344–1351. doi: 10.1210/jc.2010-2693. [PubMed] [CrossRef] [Google Scholar]
34. Yavuz DG, Yazici D, Toprak A, Deyneli O, Aydin H, Yuksel M, et al. Экзогенный субклинический гипертиреоз нарушает функцию эндотелия у больных узловым зобом. Щитовидная железа. 2008;18(4):395–400. doi: 10.1089/thy.2007.0299. [PubMed] [CrossRef] [Google Scholar]
35. Biondi B, Cooper DS. Клиническое значение субклинической дисфункции щитовидной железы. Endocr Rev. 2008;29(1):76–131. doi: 10.1210/er.2006-0043. [PubMed] [CrossRef] [Академия Google]
36. Сгарби Дж.А., Виллака Ф.Г., Гарбелин Б., Вильяр Х.Э., Ромальдини Дж. Х. Эффекты ранней антитиреоидной терапии при эндогенном субклиническом гипертиреозе при клинических и сердечных аномалиях. J Clin Endocrinol Metab. 2003; 88 (4): 1672–7. [PubMed] [Google Scholar]
Х. Эффекты ранней антитиреоидной терапии при эндогенном субклиническом гипертиреозе при клинических и сердечных аномалиях. J Clin Endocrinol Metab. 2003; 88 (4): 1672–7. [PubMed] [Google Scholar]
37. Faber J, Wiinberg N, Schifter S, Mehlsen J. Гемодинамические изменения после лечения субклинического и явного гипертиреоза. Евр Дж Эндокринол. 2001;145(4):391–6. [PubMed] [Google Scholar]
38. Biondi B, Palmieri EA, Fazio S, Cosco C, Nocera M, Sacca L, et al. Эндогенный субклинический гипертиреоз влияет на качество жизни, морфологию и функцию сердца у пациентов молодого и среднего возраста. J Clin Endocrinol Metab. 2000;85(12):4701–5. [PubMed] [Академия Google]
39. Sawin CT, Geller A, Wolf PA, Belanger AJ, Baker E, Bacharach P, et al. Низкие концентрации тиреотропина в сыворотке как фактор риска фибрилляции предсердий у пожилых людей. N Engl J Med. 1994;331(19):1249–52. doi: 10.1056/NEJM199411103311901. [PubMed] [CrossRef] [Google Scholar]
40. Cappola AR, Fried LP, Arnold AM, Danese MD, Kuller LH, Burke GL, et al. Состояние щитовидной железы, сердечно-сосудистый риск и смертность у пожилых людей. ДЖАМА. 2006;295(9):1033–41. дои: 10.1001/jama.295.9.1033. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Состояние щитовидной железы, сердечно-сосудистый риск и смертность у пожилых людей. ДЖАМА. 2006;295(9):1033–41. дои: 10.1001/jama.295.9.1033. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
41. Parle JV, Maisonneuve P, Sheppard MC, Boyle P, Franklyn JA. Прогнозирование смертности от всех причин и смертности от сердечно-сосудистых заболеваний у пожилых людей по одному результату низкого уровня тиреотропина в сыворотке: 10-летнее когортное исследование. Ланцет. 2001;358(9285):861–5. doi: 10.1016/S0140-6736(01)06067-6. [PubMed] [CrossRef] [Google Scholar]
42. Ochs N, Auer R, Bauer DC, Nanchen D, Gussekloo J, Cornuz J, et al. Метаанализ: субклиническая дисфункция щитовидной железы и риск ишемической болезни сердца и смертности. Энн Интерн Мед. 2008;148(11):832–45. [PubMed] [Академия Google]
43. Haentjens P, Van Meerhaeghe A, Poppe K, Velkeniers B. Субклиническая дисфункция щитовидной железы и смертность: оценка относительной и абсолютной избыточной смертности от всех причин на основе данных когортных исследований о времени до события. Евр Дж Эндокринол. 2008;159(3):329–41. doi: 10.1530/EJE-08-0110. [PubMed] [CrossRef] [Google Scholar]
Евр Дж Эндокринол. 2008;159(3):329–41. doi: 10.1530/EJE-08-0110. [PubMed] [CrossRef] [Google Scholar]
44. Kalmijn S, Mehta KM, Pols HA, Hofman A, Drexhage HA, Breteler MM. Субклинический гипертиреоз и риск деменции. Роттердамское исследование. Клин Эндокринол (Oxf). 2000;53(6):733–7. [PubMed] [Академия Google]
45. Roberts LM, Pattison H, Roalfe A, Franklyn J, Wilson S, Hobbs FD, et al. Связана ли субклиническая дисфункция щитовидной железы у пожилых людей с депрессией или когнитивной дисфункцией? Энн Интерн Мед. 2006;145(8):573–81. [PubMed] [Google Scholar]
46. Гариб Х., Таттл Р.М., Баскин Х.Дж., Фиш Л.Х., Сингер П.А., Макдермотт М.Т. Субклиническая дисфункция щитовидной железы: совместное заявление по ведению Американской ассоциации клинических эндокринологов, Американской ассоциации щитовидной железы и Эндокринологического общества. J Clin Endocrinol Metab. 2005;90 (1): 581–5. обсуждение 6-7. [PubMed] [Google Scholar]
47. Papi G, Pearce EN, Braverman LE, Betterle C, Roti E. Клинический и терапевтический подход к тиреотоксикозу только с подавлением тиреотропного гормона. Am J Med. 2005;118(4):349–61. doi: 10.1016/j.amjmed.2005.01.004. [PubMed] [CrossRef] [Google Scholar]
Клинический и терапевтический подход к тиреотоксикозу только с подавлением тиреотропного гормона. Am J Med. 2005;118(4):349–61. doi: 10.1016/j.amjmed.2005.01.004. [PubMed] [CrossRef] [Google Scholar]
48. Biondi B, Palmieri EA, Klain M, Schlumberger M, Filetti S, Lombardi G. Субклинический гипертиреоз: клинические особенности и варианты лечения. Евр Дж Эндокринол. 2005; 152(1):1–9. [PubMed] [Google Scholar]
49. Тофт А.Д. Клиническая практика. Субклинический гипертиреоз. N Engl J Med. 2001;345(7):512–6. doi: 10.1056/NEJMcp010145. [PubMed] [CrossRef] [Google Scholar]
50. Фатуречи В. Субклиническое заболевание щитовидной железы. Мэйо Клин Proc. 2001;76(4):413–6. викторина 6-7. [PubMed] [Google Scholar]
51. Pearce EN, Farwell AP, Braverman LE. Тиреоидит. N Engl J Med. 2003;348(26):2646–55. doi: 10.1056/NEJMra021194. [PubMed] [CrossRef] [Академия Google]
52. Mudde AH, Houben AJ, Nieuwenhuijzen Kruseman AC. Костный метаболизм при лечении эндогенного субклинического гипертиреоза антитиреоидными препаратами.