2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Нарушение липидного обмена – это расстройство процесса выработки и расщепления жиров в организме, что происходит в печени и жировой ткани. Подобное расстройство может быть у любого человека. Наиболее частой причиной развития такой болезни выступает генетическая предрасположенность и неправильное питание. Помимо этого, не последнюю роль в формировании играют гастроэнтерологические заболевания.
Онлайн консультация по заболеванию «Нарушение липидного обмена».
Задайте бесплатно вопрос специалистам: Эндокринолог.Подобное расстройство имеет довольно специфическую симптоматику, а именно увеличение печени и селезёнки, быстрый набор массы тела и образование ксантом на поверхности кожного покрова.
Поставить правильный диагноз можно на основании данных лабораторных исследований, которые покажут изменение состава крови, а также при помощи информации, полученной в ходе объективного физикального осмотра.
Лечить подобное расстройство метаболизма принято при помощи консервативных методик, среди которых основное место отведено диете.
Подобное заболевание очень часто развивается при протекании различных патологических процессов. Липиды – это жиры, которые синтезирует печень или поступают в человеческий организм вместе с пищей. Подобный процесс выполняет большое количество важных функций, а любые сбои в нём могут привести к развитию довольно большого количества недугов.
Причины нарушения могут быть как первичными, так и вторичными. Первая категория предрасполагающих факторов заключается в наследственно-генетических источниках, при которых происходят единичные или множественные аномалии тех или иных генов, отвечающих за продуцирование и утилизацию липидов. Провокаторы вторичной природы обуславливаются нерациональным образом жизни и протеканием ряда патологий.
Таким образом, вторая группа причин может быть представлена:
Помимо этого, клиницисты выделяют несколько групп факторов риска, наиболее подверженных разладам жирового обмена. К ним стоит отнести:
В медицинской сфере существует несколько разновидностей подобного недуга, первая из которых делит его в зависимости от механизма развития:
По уровню того, какие липиды повышены, есть такие формы нарушений липидного обмена:
Отдельно стоит выделить самую редкую разновидность – гипохолестеринемию. Её развитию способствуют повреждения печени.
Современные методы исследования дали возможность выделить такие типы протекания болезни:
Вторичные и наследственные нарушения липидного обмена приводят к большому количеству изменений в человеческом организме, отчего заболевание имеет множество как внешних, так и внутренних клинических признаков, наличие которых можно выявить только после лабораторных диагностических обследований.
Недуг имеет следующие наиболее ярко выраженные симптомы:
Вышеуказанные клинические признаки нарушения липидного обмена появляются при повышении уровня липидов. В случаях их недостатка симптомы могут быть представлены:
Всю вышеуказанную симптоматику целесообразно относить как к взрослым, так и к детям.
Чтобы поставить правильный диагноз, клиницисту необходимо ознакомиться с данными широкого спектра лабораторных исследований, однако перед их назначением врач должен в обязательном порядке самостоятельно выполнить несколько манипуляций.
Таким образом, первичная диагностика направлена на:
Лабораторная диагностика нарушенного липидного обмена включает в себя:
Липидограмма норма у женщин
Инструментальная диагностика в виде КТ и УЗИ, МРТ и рентгенографии показана в тех случаях, когда у клинициста возникают подозрения касательно развития осложнений.
Устранить нарушение липидного обмена можно при помощи консервативных способов терапии, а именно:
Немедикаментозные методы лечения предполагают:
Диета при подобном нарушении метаболизма основывается на таких правилах:
Все рекомендации относительно питания предоставляет только лечащий врач, поскольку отклонение от диетотерапии может только усугубить протекание недуга.
Лечение при помощи лекарственных средств направлено на приём:
Помимо этого, допускается терапия народными средствами, но только после предварительной консультации с клиницистом. Наиболее эффективными являются отвары, приготовленные на основе:
Бессмертник
При необходимости используют экстракорпоральные методики терапии, которые заключаются в изменении состава крови вне организма пациента. Для этого используются специальные приборы. Такое лечение разрешено женщинам в положении и детям, вес которых превышает двадцать килограмм. Наиболее часто применяют:
Нарушение липидного обмена при метаболическом синдроме может привести к возникновению таких последствий:
Для снижения вероятности развития нарушения жирового обмена не существует специфических профилактических мероприятий, отчего людям рекомендуется придерживаться общих рекомендаций:
Прогноз будет индивидуальным для каждого пациента, поскольку зависит от нескольких факторов – уровень липидов в крови, скорость развития атеросклеротических процессов, локализация атеросклероза. Тем не менее исход зачастую благоприятный, а осложнения развиваются довольно редко.
Все ли корректно в статье с медицинской точки зрения?
Ответьте только в том случае, если у вас есть подтвержденные медицинские знанияПоделиться статьей:
Читать нас на Яндекс.Дзен
Заболевания со схожими симптомами:
Ожирение – это такое состояние организма, при котором в его клетчатке, тканях и органах начинают накапливаться в избытке жировые отложения. Ожирение, симптомы которого заключаются в увеличении веса от 20% и более при сопоставлении со средними величинами, является не только причиной общего дискомфорта. Оно также приводит к появлению психо-физических проблем на этом фоне, проблем с суставами и позвоночником, проблем, связанных с сексуальной жизнью, а также проблем, связанных с развитием других состояний, сопутствующих такого рода изменениям в организме.
...Заболевание, которому свойственно нарушение целостности тканей печени вследствие их острого или хронического повреждения, называется печёночной недостаточностью. Это заболевание считается комплексным, в силу того, что после поражения печени происходит нарушение метаболических процессов. Если не принимать соответствующих мер по излечению заболевания, то при определённых состояниях печёночная недостаточность может быстро и стремительно развиваться и привести к летальному исходу.
...Сахарный диабет у женщин — широко распространенная патология, возникающая на фоне дисфункции эндокринной системы. Происходят обменные нарушения жидкости и углеводов, вызывающие сбой в работе поджелудочной железы, отвечающей за выработку инсулина.
...Аутоиммунный гепатит - является медленно развивающимся поражением клеток печени, называющихся гепатоциты, причём происходит это из-за влияния иммунной системы собственного организма. Примечательно то, что заболевание может развиваться как у взрослого, так и у ребёнка, однако основную группу риска составляют представительницы женского пола.
...Бактериальный эндокардит – воспалительный процесс во внутренней оболочке сердца, вызванный влиянием патологических микроорганизмов, главным из которых является стрептококк. Зачастую эндокардит является вторичным проявлением, развившимся на фоне других заболеваний, но именно бактериальное поражение оболочки является самостоятельным расстройством. Поражает людей любой возрастной группы, отчего нередко диагностируется эндокардит у детей. Отличительной чертой является то, что мужчины страдают от такого заболевания в несколько раз чаще, нежели женщины.
...Нарушение процессов производства и расщепления жиров в организме, происходящих в печени и жировой ткани. Причиной этого расстройства чаще всего становится генетическая предрасположенность, чуть реже - недоедание, запущенные формы заболеваний желудочно-кишечного тракта, атеросклероз, вредные привычки, сахарный диабет, почечная недостаточность, гипертиреоз, панкреатит и др.Заболевание проявляется в увеличении печени и селезенки, быстром увеличении массы тела, появлении ксантомы на коже (очаговые новообразования, содержащие жировые включения), при недостатке липидов - нефрозе, потере веса, выпадении волос, проблемы с ногтями, экзема, нарушения менструального цикла. По механизму развития нарушения липидного обмена подразделяются на первичные (врожденные), вторичные (последствия заболеваний желудочно-кишечного тракта, печени, почек, эндокринной системы) и алиментарные (избыток животного жира в рационе).Нарушения липидного обмена лечатся диетой, комплексом упражнений, отказом от вредных привычек, курсом приема лекарств.
От 65 € за 1 день полный пансион и лечение
9,2 /10От 86 € за 1 день полный пансион и лечение
9,1 /10 Показать все спа отели в городе БирштонасНе уверены, по каким критериям следует выбрать курорт или спа-отель?
Не знаете как забронировать?
Позвоните нам, и наш персонал поддержки поможет вам.
Вопросы-ОтветыМарина Починская Лидер службы поддержки
Бесплатная помощь врача-курорта
Если у вас возникли трудности с выбором курорта или спа-отеля, который подходит для лечения ваших заболеваний, воспользуйтесь бесплатной консультацией курортного врача Елены Хорошевой.
Задайте свой вопрос здесьЕлена Хорошева Главный врач sanatoriums.com
,Пробиотики определяются как жизнеспособные микроорганизмы, которые оказывают благотворное влияние на здоровье хозяина [1]. Теперь известно, что пробиотики обладают физиологическими функциями, такими как ингибирование патогенов, содействие пищеварению, иммунорегуляторная активность и противоопухолевая активность [2]. Здесь мы обсуждаем влияние пробиотика на метаболизм липидов в семи основных аспектах, включая анамнез, антиоксидантный эффект, влияние на липопротеин, вид микрофлоры, гормоны, рецепторы и новые механизмы.
Еще в 1974 году Манн и Сперри обнаружили, что жители африканских племен масаи поддерживают более низкий уровень липидов в крови из-за высокого потребления ферментированного молока [3]. В дальнейшем предполагается, что живые лактобациллы, входящие в ферментированное молоко, могут способствовать снижению уровня холестерина [4]. Уменьшающий холестерин эффект пробиотика стал более очевидным с открытием способности деконъюгирования и усвоения холестерина солью Lactobacillus [5] [6].После этого был разработан набор процедур скрининга in vitro и vivo для оценки пробиотиков, снижающих уровень холестерина [7]. Многие пробиотические штаммы, в основном L. acidophilus , были подвергнуты скринингу со снижающим холестерин свойством [8].
Новое исследование, проведенное Lye и соавторами, показало, что существует пять возможных пробиотических механизмов, включая ассимиляцию холестерина во время роста, связывание холестерина с клеточной поверхностью, нарушение мицеллы холестерина, деконъюгацию активности желчной соли и гидролазы желчной соли (BSH) [9 ].Теперь, с развитием молекулярной биологии, мы можем судить о снижении уровня холестерина в первую очередь по обнаружению гена BSH и его экспрессии в пробиотическом геноме. Недавнее исследование, проведенное Шридеви и соавторами, показало, что Lactobacillus buchneri ATCC 4005 продемонстрировали отличную способность снижать уровень холестерина благодаря оптимальным условиям производства гидролазы желчной соли [10]. В результате мета-анализа, введение пробиотика может оказать положительное влияние на уровень общего холестерина и ЛПНП-холестерина у человека [11].
Имеются некоторые сообщения, что ферментированное соевое молоко пробиотиками также показало благоприятную функцию регуляции уровня липидов [12]. Преимущества ферментированного соевого молока состоят в том, что нежелательные олигосахариды соевых бобов могут гидролизоваться, обеспечивая питательные компоненты для пробиотика, и вырабатывается большое разнообразие пептидов и аминокислот, а также активная агликоновая форма изофлавонов [13]. Улучшенный профиль холестерина наблюдался при ежедневном приеме пробиотического соевого продукта [14]. Представляется возможным, что живые пробиотики и функциональные изофлавоны взаимодействуют в регуляции липидного профиля.
Пробиотик, полученный в результате исследований долголетия хорошо известного Эли Метниковаффа. Как мы все знаем, различные опубликованные данные свидетельствуют о том, что снижение окислительного стресса привело к увеличению продолжительности жизни в соответствии со свободной радикальной теорией старения Хармана [15]. Эти два наблюдения вдохновили исследование антиоксидантной способности пробиотиков.
Окислительный стресс, вызванный ожирением, приводит к образованию избыточных активных форм кислорода (АФК), которые могут вызвать дальнейшее повреждение по механизму свободнорадикальной цепной реакции [16].АФК оказывают вредное влияние на полиненасыщенные липиды в клеточной мембране, приводя к повреждению клеточной структуры и малонового диальдегида (МДА), который также токсичен для ДНК и белка и одновременно образует маркер перекисного окисления липидов [17] [18]. Что касается окислительного стресса, то в организме человека имеется собственная система антиоксидантной защиты, включающая супероксиддисмутазу (SOD), каталазу (CAT), глутатионпероксидазу (GSH-Px), глутатион (GSH) и т. Д. [19]. Многие штаммы Lactobacillus с антиоксидантными эффектами не только снижали уровень MDA, но и увеличивали выработку антиоксидантов (таблица 1).
| Штаммы | Модель | Антиоксидантные эффекты | Renferences | |||||||||
| Йогурт с пробиотиками, содержащий Lactobacillus acidophilus La5 и Bifidobacterium lactis | Bb120039Сыворотка | Пациенты | Сыворотка | Сыворотка | Пациенты с ожирением | СывороткаТип пациента: 3938 | [20] | |||||
| Пробиотический йогурт, содержащий Lactobacillus acidophilus LA-5 и Bifidobacterium BB-12 | Беременные женщины | Повышенные уровни глутатионредуктазы в эритроцитах, глутатиона в плазме и 900-оксо-7,8-дигидрогуина в 8-оксо-7,8-дигидрогуане [21] | ||||||||||
| Lactobacillus casei Чжан | Крыса с высоким содержанием жира | Снижение MDA и увеличение SOD и GSH-Px в сыворотке и печени | [22] | |||||||||
| Lactobacillus fermentum | свиней | Увеличение общего количества анти емкость окислителя , активность SOD и GSH-Px в сыворотке крови, а также CAT и печень SOD в мышцах; Снижение уровня MDA в сыворотке и мышцах | [23] | |||||||||
| Пробиотический йогурт, содержащий Lactobacillus acidophilus LA-5 и Bifidobacterium BB-12 | человек | Увеличение активности СОД и каталазы | [24] | |||||||||
| Bacillus polyfermenticus | Крысы с карциногенезом толстой кишки | Более низкие уровни перекисного окисления липидов в плазме и более высокие уровни общего антиоксиданта в плазме | [25] | |||||||||
| пробиотиков, содержащих Lactobacillus acidophilus и Lac case 95038 и L Крысы с высоким содержанием фруктозы | Более низкие значения TBARS и более высокие значения глутатиона в тканях печени и поджелудочной железы | [26] | ||||||||||
| Lactobacillus fermentum ME-3 | человек | Улучшенный общий антиоксидантный статус | [27 ] | |||||||||
| Bacillus polyfermenti cus SCD | Крыса с высоким содержанием жиров и холестерина в крови | Увеличение общего потенциала антиоксидантного захвата радикалов (TRAP) и уменьшение содержания сопряженных диенов в плазме | [28] | |||||||||
| Streptococcus thermophilus YIT 2001 | Iron overloade-d 9009 | Значительное снижение перекиси липидов в слизистой оболочке толстой кишки | [29] | |||||||||
| VSL # 3 | ob / ob мышей | Бета-окисление низших жирных кислот | [30] | |||||||||
| л.acidophilus | крысы | Более высокая активность GSH-Px в эритроцитах | [31] | |||||||||
| л .rhamnosus SBT 2257 | крысы | Ингибирование гемолиза эритроцитов в состоянии витамина Е dificient | [32] |
Антиоксидантное действие пробиотиков
Транспорт липопротеинов играет важную роль в накоплении уровня липополисахаридов в организме (LPS) [33].Исследования, проведенные Cani и соавторами, показали, что повышенный уровень LPS рассматривается как триггерный фактор, участвующий в патогенезе ожирения и метаболического риска посредством врожденного иммунного механизма [34]. LPS-связывающий белок (LBP) и липопротеины оказывают синергетический эффект на снижение уровня токсического LPS [35].
Было продемонстрировано, что некоторые пробиотики, содержащие ферментированное молоко, снижают уровень холестерина липопротеинов низкой плотности (LDL-c) и холестерина липопротеинов очень низкой плотности (VLDL-c) у животных и человека [26] [36] [37].Недавно было доказано, что L. casei Shirota снижает уровень LBP в плазме у мышей с ожирением, а йогурт L. reuteri NCIMB 30242 может улучшить уровень ApoB-100 у пациентов с гиперхолестеринемией, предполагая, что пробиотик обладает функцией снижения LPS для отсрочки риск ожирения [38] [39].
Микробы кишечника не только Lactobacillus также могут проявлять эффект деконъюгирования соли желчных кислот [40], предполагая, что другие микробы обладают способностью снижать липиды.Таким образом, общая микрофлора кишечника была принята во внимание при оценке липидного обмена. В последние несколько лет исследования были сосредоточены на новых областях микрофлоры и липидного обмена с разработкой независимых от культуры методов для понимания общего микробного разнообразия [41].
Кишечник человека состоит из микробного сообщества из 10 14 бактерий, по крайней мере, с 1000 видами, и весь микробиом более чем в 100 раз превосходит геном человека [42]. Эти исследования подчеркивают значимость вклада всего кишечного микробиома для сбора энергии и взаимосвязи между ожирением и изменениями кишечного микробиома [43].Более подробно, ожирение в основном характеризуется повышенным соотношением Firmicutes / Bacteroidetes в кишечнике [44]. Пробиотики служат одним из эффективных агентов для регуляции микрофлоры кишечника, они могут оказывать положительное влияние на метаболизм липидов, снижая соотношение Firmicutes / Bacteroidetes . Другие бактерии, такие как Methanobrevibacter smithii , также находятся на низком уровне у тучных людей [45]. Интересно, что недавно было обнаружено, что атеросклеротическое заболевание, вызванное накоплением холестерина и воспалением, его микробиота атеросклеротических бляшек была связана с микробиотой полости рта и кишечника посредством высокопроизводительного 454 пиросеквенирования генов 16S рРНК [46].
Кроме того, такая огромная микрофлора обеспечивает большой резервуар молекул LPS для циркуляции через колонизацию грамотрицательных бактерий в кишечнике [47]. Недавнее исследование показало, что Bifidobacteria с генами, кодирующими переносчик углеводов типа АТФ-связывающей кассеты, могут защищать от грамотрицательной колонизации кишечной палочки E. coli O157: H7 из-за образования ацетата [48]. Таким образом, пробиотик может ограничивать связанные с ЛПС микробные сообщества в кишечнике.
Микрофлора кишечника также известна как мишень для метаболизма лекарств из-за разнообразных микробных трансформаций [49].Считалось, что манипуляция комменсальной микробной композицией с помощью антибиотиков, пробиотиков или пребиотиков повышает метаболическую активность и выработку эффективных метаболитов [50]. Было высказано предположение, что симвастатин, который является ингибитором HMG-CoA и широко используется для регуляции выработки холестерина в печени, обладает измененными фармакологическими свойствами за счет деградации микрофлоры за счет изменения его способности связываться с соответствующими рецепторами [51]. Указано, что пробиотики могут влиять на метаболизм липидорегулирующих препаратов в кишечнике.
Гормоны, такие как лептин, адипонектин и остеокальцин, играют важную роль в метаболизме липидов. Тучная популяция характеризовалась значительным снижением уровня остеокальцина и адипонектина, а также высоким уровнем лептина (устойчивым к лептину), о котором сообщалось в литературе. В настоящее время все более широко признается, что лептин может регулировать потребление пищи и расход энергии через гипоталамус, а адипонектин может усиливать окисление жировой ткани до нижних уровней жирных кислот и содержание триглицеридов в ткани, связанных с чувствительностью к инсулину [52].Что касается остеокальцина, предполагается, что лептин модулирует биологическую активность остеокальцина, а остеокальцин может стимулировать синтез адипонектина [53] [54].
Лептин, гормон против ожирения, вырабатываемый жировой тканью, как сообщается, регулирует массу тела, контролируя потребление пищи и расход энергии [55]. Тем не менее, ожирение имеет тенденцию демонстрировать заметно более высокий уровень лептина в сыворотке с симптомом резистентности к лептину. В нескольких исследованиях сообщалось о снижении лептина при введении пробиотика.У мышей с высоким содержанием жира Lee и соавторы подтвердили, что Lactobacillus rhamnosus PL60 продемонстрировали снижение уровня лептина и эффект против ожирения из-за продукции конъюгированной линолевой кислоты [56]. Более того, концентрация лептина в сыворотке была снижена на Lactobacillus gasseri SBT205 у худых крыс Цукера, связанных с уменьшенным размером адипоцитов [57]. В другом исследовании также сообщалось, что уровень лептина был снижен комбинированными бифидобактериями ( B. pseudocatenulatum SPM 1204, B. longum SPM 1205 и B.longum SPM 1207) у тучных крыс [58]. Интересно и спорно, прямая инъекция Lactobacillus ацидофильных супернатантов (росток бесплатно) в головном мозге крыс приводит к потере веса с увеличением экспрессии лептина в нейронах и жировой ткани [59].
Лептин-понижающее действие пробиотиков также наблюдалось у человека. Аналогичным образом, Naruszewicz и соавторы исследовали, оказывает ли пероральное введение L. plantarum 299v благотворное влияние на курильщиков путем выявления факторов риска сердечно-сосудистых заболеваний [60].В этом исследовании курильщики показали значительное снижение концентрации лептина в плазме и противовоспалительных свойств при добавлении пробиотика. К сожалению, два месяца потребления Lactobacillus acidophilus и Bifidobacterium longum не смогли снизить уровень лептина в плазме у мужских равных экскреторов [61].
Как сывороточный белок, полученный из адипоцитов, адипонектин играет важную роль в метаболизме глюкозы и липидов, поскольку дефицит адипонектина связан с резистентностью к инсулину, воспалением, дислипидемией и риском атерогенных сосудистых заболеваний [62].Параллельно было показано, что адипонектин подавляет образование пенистых клеток макрофагов при атеросклерозе [63]. Несколько исследований показали, что пробиотическая терапия улучшает уровень адипонектина или экспрессию гена адипонектина. Одно сравнительное исследование, проведенное на мышах с нормальной микрофлорой (NMF) и без микробов (GF), выявило, что экспрессия гена адипонектина (Adipoq) была повышена в группах Lactobacillus мышей, свободных от бактерий [64]. Более того, Higurashi et al. Сообщили, что пробиотический сыр может предотвратить накопление жировой ткани в брюшной полости и поддерживать концентрацию адипонектина в сыворотке крови у высококалорийных крыс, получавших питание [65].Тем не менее, штамма Lactobacillus plantarum № 14 оказывают белое жироредуцирующее действие на мышей с высоким содержанием жира без изменения адипонектина [66].
Kadooka и др. Использовали пробиотик L. gasseri SBT2055 для регуляции ожирения в брюшной полости у взрослых, страдающих ожирением, где пробиотическое лечение включало значительное уменьшение областей висцерального и подкожного жира в брюшной полости от исходного уровня и значительное увеличение высокомолекулярного адипонектина в их сыворотке. [67]. Кроме того, недавнее крупномасштабное клиническое исследование, проведенное Luoto и соавторами, подтвердило, что беременные женщины с потреблением комбинированных пробиотиков Lactobacillus rhamnosus GG и Bifidobacterium lactis имели более высокую концентрацию адипонектина молозива по сравнению с плацебо, которая коррелировала обратно пропорционально увеличению массы тела во время беременности. беременность [68].
В последние годы остеокальцин, секретируемый остеобластами, вызвал большой интерес, связанный с функцией β-клеток, продукцией адипонектина, расходом энергии и ожирением [69]. У людей с ожирением сохранялся низкий уровень остеокальцина в сыворотке [70]. Единственное исследование, проведенное Naughton et al., Показало, что уровни остеокальцина были слегка повышены у крыс среднего возраста при потреблении богатого инулином молока, ферментированного Lactobacillus GG и Bifidobacterium lactis [71].Интересно, что остеокальцин является витамин К-зависимым белком, и два основных типа, включая витамин К1 и витамин К2, соответственно вырабатываются из диетической растительной и микрофлоры [72]. Как эффективный способ изменить микрофлору, пробиотики могут повысить выработку витамина К2 и связанный с ним уровень остеокальцина за счет изменения микрофлоры.
Различные рецепторы участвуют в регуляции важных генов в транспорте и метаболизме липидов и выбираются в качестве потенциальных терапевтических мишеней при дислипидемии и атеросклерозе.Недавние исследования были сосредоточены на ядерных рецепторах (NR), связанных с G-белком рецепторах (GPR) и Toll-подобных рецепторах (TLR) в качестве факторов, регулируемых введением пробиотиков. Но перекрестные помехи между NR, TLR и GPR не были четко объяснены. Единственное исследование о перекрестных помехах между NR, TLR и микрофлорой между специфическими свободными от патогенов (SPF) и свободными от микробов (GF) мышами показало, что LXR-альфа, ROR-гамма и CAR экспрессия были снижены, тогда как TLR-2 и TLR-5 увеличились в SPF по сравнению с мышами GF [73].
В соответствии с изложенным выше, было обнаружено, что некоторые пробиотики эффективны для снижения уровня холестерина в крови, и одним из возможных механизмов является повышение уровня фекальных желчных кислот. Как один из важных липидных медиаторов, было подтверждено, что желчные кислоты влияют на ряд NR, включая рецептор фарнезоида X (FXR), рецептор прегнана-X (PXR), рецептор конститутивного андростана (CAR), рецептор, активируемый пролифератором пероксисом (PPAR) X-рецептор печени (LXR), глюкокортикоидный рецептор (GR) и рецептор витамина D (VDR) [74-76].
В последнее время Lactobacillus acidophilus ATCC 4356 может действовать как агонист рецептора X-рецептора печени (LXR) и ингибировать клеточное поглощение мицеллярного холестерина в клетках Caco-2 [77]. Аналогичное исследование, проведенное с Yoon et al. С использованием комбинации L. rhamnosus BFE5264 и L. plantarum NR74, также показало активацию экспрессии LXR и стимулирование оттока холестерина в клетках Caco-2 [78]. Это идентично действию препарата секвестрантов желчных кислот, который также может вызывать повышение активности LXR в печени [79].
Как мы все знаем, PPAR играют ключевую роль в воспалении и метаболизме глюкозы в крови. Некоторые исследования показали, что пробиотик регулирует экспрессию PPAR в экспериментальной модели воспаления [80]. Фактически, PPARs также является целевым геном энергетического гомеостаза и адипогенеза [81]. Связанный с транскрипцией гена ApoE, PPAR-γ нуждается в LXR-пути для регуляции баланса триглицеридов адипоцитов [82]. Авелла и др. Сообщили, что диетические пробиотики могут модифицировать экспрессию PPAR-α, PPAR-β, VDR-α, RAR-γ и GR у морской рыбы, что указывает на обширные перекрестные помехи среди NRs, активированных пробиотиком [83].Относительно NRs и липидного обмена, связанного с пробиотиком, Aronsson и др. Отметили, что L. paracasei F19 может уменьшить накопление жира, связанное с резкими изменениями PPAR [84]. Одно из последних исследований, проведенных Zhao et al., Также продемонстрировало, что пробиотик Pediococcus pentosaceus LP28 может также действовать как агонист PPAR-γ одновременно с значительным снижением уровня триглицеридов и холестерина у мышей с ожирением [85].
Являясь важными рецепторами распознавания образов, TLR участвуют в распознавании и распознавании ряда микробных компонентов, таких как пептидогликан (TLR2) и LPS (TLR4), для активации иммунных реакций [86].На сегодняшний день связь между TLR и метаболизмом липидов в основном состоит из двух аспектов. С одной стороны, передача сигналов TLR может напрямую связываться с метаболизмом холестерина в макрофагах и вмешиваться в него [87]. С другой стороны, передача сигналов TLR (главным образом, TLR4) участвует во взаимодействии LPS с жирной кислотой, липопротеином и повреждением органов (особенно печени и кишечника). Существуют доказательства того, что низкая доза ЛПС может стимулировать синтез жирных кислот de novo , липолиз и выработку липопротеинов в печени, что приводит к гипертриглицеридемии печени [88].У мышей умеренно более высокий уровень LPS может быть увеличен за счет диеты, обогащенной жирами, и может способствовать воспалению слабой степени [34]. У кроликов высокое потребление холестерина плюс низкие дозы ЛПС ускоряли развитие атеросклероза [89]. Эти два исследования рассматриваются как результат перекрестных помех между LPS и TLR, приводящих к повреждению слизистой оболочки кишечника, связанному с воспалительным ответом. Кроме того, было показано, что образование пенистых клеток при атеросклерозе опосредуется TLR2 и 4, а другие TLR, такие как TLR3, 7 и 9, также могут участвовать в атеросклерозе [90] [91].
TLR4, по-видимому, тесно связан с высоким содержанием жиров, LPS и воспалением. Известно, что пробиотики восстанавливают LPS-содержащие грамотрицательные организмы (такие как E. coli ) в кишечнике и приток LPS в кровоток [92] [93]. Большое количество пробиотиков также способно специфически модулировать путь NF-κB (один из наиболее важных воспалительных путей) в эпителиальных клетках кишечника и макрофагах [94].
Из-за дефицита TLR4 с антиобезигенскими эффектами и восприимчивости к колиту, мало информации о влиянии пробиотика на метаболизм липидов получено в модели нокаута TLR4, тогда как у мышей, нокаутированных по TLR4, наблюдался защитный эффект пробиотика VSL # 3 от воспаления [95]. [96].Что касается роли TLR4 в развитии метаболических нарушений, Andreasen и др. Считают, что L. acidophilus NCFM могут снижать приток LPS из кишечника в кровоток и подавлять передачу сигналов TLR4 и провоспалительные цитокины у людей. [97].
Гомеостаз иммунитета также оказывает важное влияние на метаболизм липидов. В целом, общепризнанно, что пробиотические бактерии способны поддерживать иммунитет Th2 и Th3 посредством регуляции провоспалительных и противовоспалительных цитокинов [98].Кроме того, Agrawal et al. Подтвердили, что передача сигналов, происходящая от TLR2, главным образом усиливает высвобождение Th3-цитокинов, тогда как TLR4, запускаемый LPS, стимулирует ответы Th2-типа [99]. Интересно, что Voltan et al. Обнаружили, что L. crispatus M247 могут повышать уровень мРНК TLR2 и снижать уровни мРНК TLR4 и белка в слизистой оболочке толстой кишки, предполагая, что L. crispatus M247 поддерживают гомеостаз Th2 / Th3 через бластанс TLR2 / TLR4 [ 100].
Хорошо известно, что пробиотические бактерии оказывают благотворное влияние на кишечник, особенно его антимикробные свойства, продуцируя органические кислоты или регулируя органическую кислотопродуцирующую флору [93].Сообщалось также, что GPR41 и GPR43 могут активироваться короткоцепочечными жирными кислотами (SCFA) [101]. Таким образом, возможно, что пробиотик может влиять на GPRs через продукцию SCFAs в кишечнике. Тем не менее, эти отношения между ними еще не установлены. Исследование, проведенное на мышах с дефицитом Gpr41 в условиях отсутствия микробов или в обычной среде, показало, что наличие микрофлоры было связано с получением короткоцепочечных жирных кислот из рациона, которые контролируют степень ожирения [102].
Насколько нам известно, только одно исследование изучало влияние пребиотика, который может специфически увеличивать кишечные пробиотические бифидобактерии на экспрессию GPR43 через модифицированный липидный профиль [103]. Используя модель грызунов с высоким содержанием жиров, авторы изучили влияние пребиотика на изменения микрофлоры, профиля жировых кислот и экспрессии рецепторов. Диета с высоким содержанием жиров способна увеличить экспрессию GPR43 и TLR4, а также экспрессию PPAR-γ благодаря продукции олеиновой и α-линоленовой кислот, в то время как пребиотик снижает избыточную экспрессию GPR43 и TLR4.
В последние годы были предложены новые механизмы пробиотиков по метаболизму липидов. Исследования Khedara и др. Показали, что более низкий уровень оксида азота является причиной гиперлипидемии, поскольку эндогенный оксид азота может снизить окисление жирных кислот [104]. Некоторые пробиотики обладали способностью вызывать синтез оксида азота путем активации индуцибельной синтазы оксида азота [105] [106]. Таким образом, модифицированная доступность NO пробиотиками играет важную роль в метаболизме липидов.
Кроме того, Tanida и др. Продемонстрировали, что Lactobacillus paracasei ST11 может увеличить липолиз жировой ткани за счет усиления активности вегетативного нерва [107]. В печени пробиотики также проявляют липидоснижающее действие [108]. Ма и др. Продемонстрировали, что пробиотики VSL # 3 могут увеличить количество NKT-клеток в печени, чтобы ослабить стеатоз, вызванный диетой с высоким содержанием жиров [109]. Хуанг и соавторы обнаружили, что L. acidophilus 4356 могут снижать уровень C1-Like 1 (NPC1L1) Нимана-Пика в двенадцатиперстной кишке и тощей кишке крыс с высоким содержанием жира [110].Другое недавнее исследование, проведенное Aronsson и соавторами, выявило новый механизм Lactobacillus paracasei F19 для снижения накопления жира путем повышения уровня белка Angiopoietin-Like 4 (ANGPTL4) у мышей [84].
ТехнологияOmics позволяет по-новому взглянуть на механизмы липидного обмена под влиянием пробиотиков. Lee и соавторы продемонстрировали, что ген ccpA (кодирует контрольный белок катаболита A) выполняет функцию снижения уровня холестерина in vivo, сравнивая штамм, снижающий уровень холестерина л.acidophilus A4 и мутантный штамм BA9 без гиполипидемического эффекта [111]. Кроме того, шесть основных различных экспрессированных белков, вовлеченных в эти два разных штамма in vitro , были идентифицированы протеомным анализом, включающим регулятор транскрипции, FMN-связывающий белок, суперсемейную пермеазу-посредник, гликогенфосфорилазу, белок YknV и фруктозо-тагатозобисфосфат-альдолазу.
Анализ микрочипов пробиотика L. casei Влияние Чжана на печень крыс с высоким содержанием жиров, получавших диету, показало, что L.администрация casei Zhang способствует β-окислению метаболизма жирных кислот путем усиления экспрессии пяти генов (Acsl1, Hadh, Acaa2, Acads и gcdH). Более того, L. casei Zhang может сильно активировать экспрессию глюкокортикоидного рецептора (ген NR3C1), который может быть связан с защитой от воспаления низкой степени тяжести, вызванного [112].
В последнее время протеомы тонкого кишечника у поросят-отъемышей, которые по-разному реагируют на пробиотик ( Lactobacillus fermentum I5007) и добавки антибиотиков (ауреомицин) с точки зрения метаболизма липидов, показали, что усиленное пробиотиками слизистое SAR1B может предотвратить появление поросят-отъемышей от жировой ткани.Что еще более важно, высокое содержание EIF4A и KRT10 в слизистой оболочке у пробиотиков, обработанных пробиотиками, может способствовать улучшению общей целостности кишечника, что предполагает потенциальное снижение притока LPS [113].
В заключение, пробиотик - лучшая стратегия профилактики и лечения для регуляции липидного гомеостаза с высокой распространенностью ожирения, бремени изумительного избыточного веса и развития хронических заболеваний в современном мире. Несмотря на то, что люди слишком обращают внимание на тонкий результат, чтобы пренебречь побочным эффектом препарата, пробиотик может этого избежать для достижения здорового веса.Усиление притока желчных кислот и усвоение кишечного холестерина считалось классической теорией для пробиотиков, снижающих уровень холестерина. Тем не менее, последние исследования сосредоточены на антиоксидантной активности и взаимодействии с липопротеинами, гормонами и всей микробиотой. Кроме того, перекрестные помехи между NR, GPR и TLR пробиотиками являются новыми рубежами для механических исследований. Однако необходимы дальнейшие исследования для выявления различных реакций, связанных с метаболизмом липидов под влиянием пробиотиков.
Мы благодарим профессора Хэпинга Чжана за редактирование этой статьи.Мы также благодарим сотрудников лаборатории факультета биологической науки и техники, которую возглавляет Ючжэнь Ван в нашем университете, за полезные советы по молекулярной биологии.
Последнее обновление 2 июля 2020 г. в 11:29
Синтез жирных кислот и бета-окисление, как и гликолиз и глюконеогенез, являются противоположными процессами.Синтез жирных кислот ингибирует бета-окисление, как это. Во время синтеза жирных кислот ацетил-КоА-карбоксилаза (АСС) продуцирует малонил-КоА. Малонил-КоА аллостерически ингибирует карнитинацилтрансферазу I (CAT I), ограничивающий скорость фермент бета-окисления.
Бета-окисление напрямую не ингибирует синтез жирных кислот, но косвенно, так как гормоны, стимулирующие бета-окисление, ингибируют синтез жирных кислот и наоборот.
Ковалентное регулирование
Ацетил-КоА-карбоксилаза является ограничивающим скорость ферментом синтеза жирных кислот и, следовательно, является точкой регуляции.ACC ингибируется PKA и, следовательно, глюкагоном и адреналином. Это также запрещено AMPK. ACC активируется PP2A и, следовательно, инсулином.
Регламент транскрипции
Транскрипционный фактор, называемый белком, связывающим углеводный ответный элемент ( ChREBP ), участвует в регуляции транскрипции синтеза жирных кислот. Этот транскрипционный фактор живет в цитоплазме. AMPK и PKA фосфорилируют фактор транскрипции, который предотвращает его проникновение в ядро, тем самым ингибируя его.
PP2A дефосфорилирует фактор транскрипции. После дефосфорилирования ChREBP перейдет в ядро, где увеличит транскрипцию ферментов, таких как синтаза жирных кислот, ACC и пируваткиназа .
Инсулинтакже стимулирует два других фактора транскрипции, SRF и Elk1, которые усиливают транскрипцию многих генов, включая синтаз жирных кислот , ACC и пируваткиназ .
Аллостерическое регулирование
В дополнение к упомянутым выше факторам, АКК также регулируется аллостерически.Цитрат активирует ACC как механизм прямой связи, в то время как пальмитоил-КоА (пальмитат) ингибирует его как механизм отрицательной обратной связи.
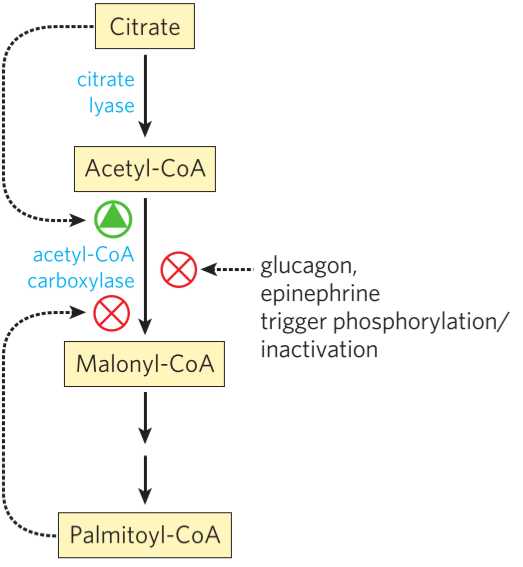
Как ACC, и, следовательно, синтез жирных кислот, регулируется. Обратите внимание, что этот показатель не включает все регулирующие факторы.
Рецепторы, активируемые пролифератором пероксисом (PPAR), являются лиганд-активируемыми факторами транскрипции. Это означает, что они активируются, когда связывают лиганд. Существует 3 типа: PPARα, PPARβ / δ и PPARγ.Все они активируются полиненасыщенными жирными кислотами в организме, особенно арахидоновой кислотой.
PPARα включает гены, необходимые для поглощения и окисления жирных кислот, что снижает уровень триацилглицерина в крови. Препараты, которые связываются с PPARα (фибратами), используются для лечения высоких уровней триацилглицерина в крови.
PPARβ / δ включает гены, необходимые для β-окисления и для расцепления митохондрий. Разъединение митохондрий приводит к менее эффективному окислительному фосфорилированию, что вызывает повышенное использование энергии и выработку тепла.Активация этих препаратов была целью лечения ожирения, но ранние тесты показывают быстрое развитие рака.
PPARγ включает гены, необходимые для поглощения и синтеза липидов. Одним из генов является PEPCK. Фосфоенолпируваткарбоксикиназа (PEPCK) является ферментом в глюконеогенезе, но также используется для синтеза глицерина (глицероногенез). PEPCK присутствует в жировой ткани для синтеза глицерина, который будет использоваться в качестве основы для триацилглицеролов. Тип препаратов под названием тиазолидиндионы связываются с PPARγ и активируют его.Их можно использовать для лечения сахарного диабета 2 типа, но их редко используют из-за побочных эффектов.
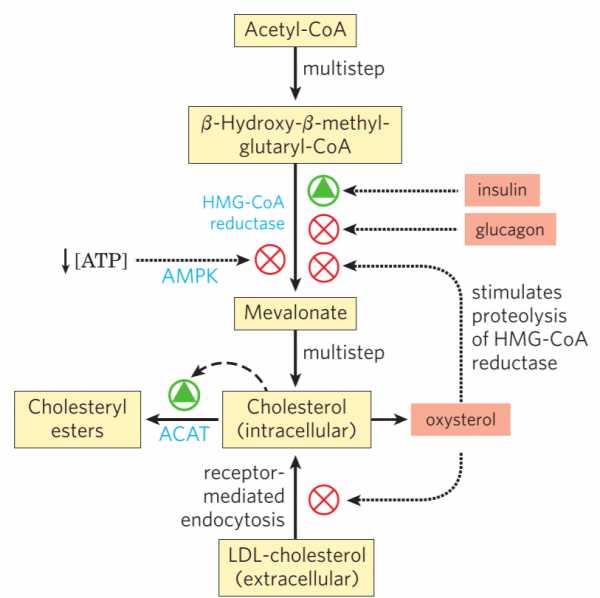
Регуляция синтеза холестерина. Наиболее важными являются гормоны и АМПК. Транскрипционная регуляция не изображена.
Холестерин не может быть разрушен для использования в качестве энергии. Поэтому важно, чтобы его синтез строго регулировался и регулировался доступностью организма.Все регулирование происходит на HMG-CoA редуктазе. Уровень холестерина в клетке можно регулировать пятью способами:
1. В краткосрочной перспективе HMG-CoA редуктаза ковалентно регулируется PP2A , PKA и AMPK. Инсулин активирует HMG-CoA редуктазу с по PP2A , в то время как глюкагон и адреналин ингибируют его через PKA . AMPK также тормозит это.
Важно отметить, что краткосрочная регуляция зависит не от уровня холестерина в клетке, а только от гормонов, присутствующих в настоящее время в крови.Следующие четыре механизма регуляции зависят исключительно от уровня холестерина.
2. Долгосрочная регуляция происходит на уровне транскрипции. Это означает, что регулирование количества присутствующих молекул HMG-CoA редуктазы является наиболее важным. Если их слишком много, транскрипция новых должна замедлиться. Если их слишком мало, транскрипцию следует стимулировать.
Регуляция транскрипции осуществляется парой белков, называемых SREBP и SCAP.Они оба встроены в мембрану ER. Когда уровень холестерина в клетке падает, они оба мигрируют в Гольджи, где SCAP отщепит часть SREBP. Когда это происходит, эта небольшая часть (регуляторный домен) будет проникать в ядро и работать как фактор транскрипции для увеличения транскрипции различных ферментов, включая HMG-CoA редуктазу .
SREBP = стерол-регуляторный элемент, связывающий белок. SCAP = белок, активирующий расщепление SREBP
3.Повышенный уровень холестерина в клетке активирует ACAT . Этот фермент присоединяет жирные кислоты к молекулам холестерина, так что они превращаются в сложные эфиры холестерина.
4. Повышенный уровень холестерина заставляет клетку поглощать меньше ЛПНП в результате эндоцитоза. ЛПНП содержит много холестерина, поэтому, принимая меньше ЛПНП, клетки не будут накапливать слишком много холестерина.
5. Наконец, высокий уровень холестерина в клетке заставляет клетку удалять молекулы HMG-CoA редуктазы путем протеолиза.За счет уменьшения количества этого фермента синтез холестерина будет замедлен.
Когда в печени закончатся запасы гликогена и субстратов глюконеогенеза, жиры будут расщепляться для получения энергии. Бета-окисление даст ацетил-КоА из жирных кислот.
Напомним, что оксалоацетат является глюконеогенетическим субстратом. В этом случае в печени закончились легко доступные глюконеогенетические субстраты, включая оксалоацетат.Оксалоацетат необходим для метаболизма ацетил-КоА в течение цикла TCA. Поскольку нет оксалоацетата, ацетил-КоА будет накапливаться. Именно накопление ацетил-КоА стимулирует синтез кетонового тела, так как ацетил-КоА больше некуда идти.
Чтобы поддерживать уровень сахара в крови на минимальном уровне, организм начинает расщеплять белки на глюкогенные аминокислоты и использовать их в качестве субстратов для глюконеогенеза. Однако этого недостаточно для обеспечения энергией всех органов.
Гормоны также влияют на синтез кетонового тела. Ген HMG-CoA-синтазы регулируется транскрипционным фактором, называемым FOXA2. Инсулин ингибирует этот фактор транскрипции, тем самым ингибируя синтез кетонового тела. Глюкагон активирует его, тем самым стимулируя синтез кетонового тела.
Белок, называемый SIRT3, активирует HMG-CoA-синтазу путем ее деацетилирования. SIRT3 активируется постом.
Гиперхолестеринемия
Гиперхолестеринемия - это состояние, при котором повышен уровень холестерина и ЛПНП в крови.Это приводит к атеросклерозу и сердечно-сосудистым заболеваниям, включая инфаркт миокарда и инсульт.
Большинство случаев гиперхолестеринемии связано с плохим питанием и малоподвижностью. Однако есть некоторые генетические причины. Семейная гиперхолестеринемия происходит из-за дефектных рецепторов ЛПНП. С этими рецепторами дефектные клетки не могут принимать ЛПНП, вызывая его накопление в крови. Холестерин накапливается в коже, и ранний атеросклероз вызывает сердечно-сосудистые заболевания в очень раннем возрасте.
Гиперхолестеринемия обычно лечится с помощью упражнений и улучшенной диеты. В случае неудачи лекарства могут быть использованы. Одним из наиболее важных лекарств в лечении сердечно-сосудистых заболеваний являются статинов . Эти препараты ингибируют редуктазу HMG-CoA, снижают синтез холестерина.
Нарушения окисления жирных кислот
Дефицит ацил-КоА-дегидрогеназы или дефицит первичного карнитина уменьшает образование кетоновых тел.Жир накапливается в тканях, вызывая токсическое повреждение.
Ацидотические расстройства
Эти расстройства вызывают ацидоз, снижение рН крови. M этилмалоновая ацидемия вызвана генетическим дефектом В12-зависимого фермента метилмалонил-КоА мутазы . Пропионовая ацидемия вызвана генетическим дефектом биотин-зависимого фермента пропионил-КоА-карбоксилазы . Эти заболевания вызывают накопление органических кислот в крови.
Сфинголипидозы
Сфинголипидозы - это тип лизосомных болезней накопления, вызванных нарушением метаболизма сфинголипидов. К ним относятся болезнь Тея-Сакса, болезнь Фабри, болезнь Гоше, болезнь Ниманна-Пика и болезнь Краббе.
Следующая страница:
11. Аминокислотный обмен; Судьба аминогруппы