2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Внимание! При положительных и сомнительных результатах, срок выдачи результата может быть увеличен до 10-ти рабочих дней.
Антитела к ВИЧ 1, 2 типа, антиген p 24 — исследование специфических антител, возникших в организме в ответ на инфицирование вирусом иммунодефицита человека (ВИЧ) 1, 2 типов и антигена p 24 вируса иммунодефицита человека.
ВИЧ (вирус иммунодефицита человека) — вирус семейства ретровирусов (вирус с медленной репликацией), который поражает клетки иммунной системы человека (CD4, Т-хелперы) и вызывает синдром приобретенного иммунодефицита.
Длительность инкубационного периода обычно составляет 3–6 недель. В редких случаях антитела к ВИЧ начинают обнаруживаться только через несколько месяцев и более после инфицирования. Уровень их концентрации может заметно снижаться в терминальном периоде заболевания. В редких случаях антитела к ВИЧ-инфекции могут исчезать на длительный срок.
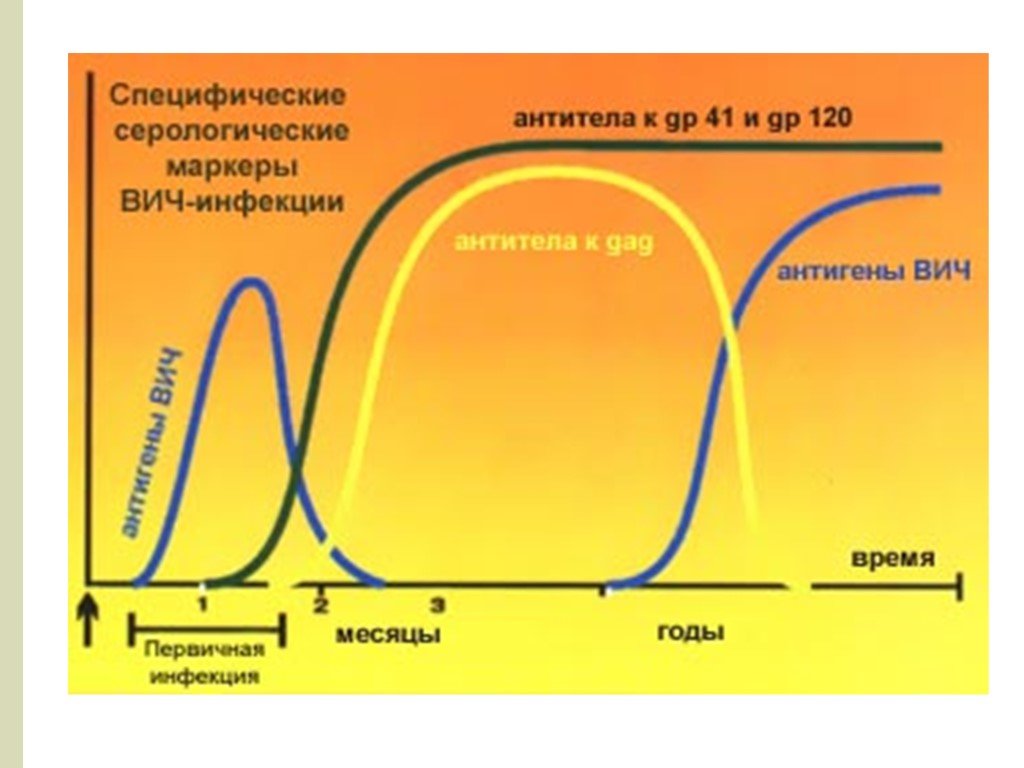
Антиген р 24 ВИЧ 1,2 типа, выявленный в сыворотке крове, свидетельствует о раннем этапе заболевания. В течение нескольких первых недель после заражения количество вируса и антигена р 24 в крови стремительно нарастает. Как только начинают вырабатываться антитела к ВИЧ 1, 2, уровень антигена р 24 начинает снижаться.
Определение антигена р 24 позволяет проводить диагностику ВИЧ-инфекции на ранних стадиях инфицирования, до выработки антител.
Одновременное выявление антител к вирусу ВИЧ-1,2 и антигена вируса р 24 повышает диагностическую ценность исследования.
Данный анализ позволяет обнаружить антитела к ВИЧ-1,2, а также антиген р 24 ВИЧ-1,2. Анализ позволяет диагностировать ВИЧ-инфекцию на ранних стадиях.
Пути передачи ВИЧ-инфекции
Существуют 3 способа передачи вируса иммунодефицита:
1. Половой путь — является наиболее частым. Заражение происходит при незащищённом сексуальном контакте, при этом вирус проникает внутрь организма через слизистые оболочки. Ранки на слизистой оболочке, язвочки, воспаления —повышают вероятность заражения. У лиц, страдающих инфекциями, передающимися половым путём, риск заражения при контакте с инфицированным человеком выше в 2–5 раз. Для передачи вируса важна не только степень интимности контакта, но и количество возбудителя. При незащищённом сексе вероятность заражения женщины от мужчины примерно в три раза выше, поскольку в её организм попадает большее количество вируса, и у женщины значительно больше площадь поверхности, через которую вирус может проникнуть в организм (слизистая влагалища). Риск заражения наиболее высок при анальном сексуальном контакте и наименее — при оральном.
Ранки на слизистой оболочке, язвочки, воспаления —повышают вероятность заражения. У лиц, страдающих инфекциями, передающимися половым путём, риск заражения при контакте с инфицированным человеком выше в 2–5 раз. Для передачи вируса важна не только степень интимности контакта, но и количество возбудителя. При незащищённом сексе вероятность заражения женщины от мужчины примерно в три раза выше, поскольку в её организм попадает большее количество вируса, и у женщины значительно больше площадь поверхности, через которую вирус может проникнуть в организм (слизистая влагалища). Риск заражения наиболее высок при анальном сексуальном контакте и наименее — при оральном.
2. Контакт с кровью инфицированного человека:
а) при использовании общих игл, шприцев, посуды для приготовления наркотиков, нестерильного медицинского инструментария;
б) введение наркотиков, в приготовлении которых используется кровь;
в) использование, переливание инфицированной донорской крови и изготовленных из неё препаратов (риск крайне низок, поскольку все доноры, а также кровь тщательно проверяются).
3. От ВИЧ-инфицированной матери (вертикальный путь) к плоду в течение беременности, при прохождении через родовые пути, при кормлении грудью.
Вирус не стабилен и способен жить только в жидкостях организма человека и только внутри клеток. В связи с этим не существует опасности заразиться при поцелуях и бытовых контактах, при пользовании общим туалетом, через укусы насекомых, через слюну, питьевую воду и пищевые продукты.
Диагностика носительства вируса иммунодефицита человека
Диагностика ВИЧ-инфекции — комплексный процесс, основанный на данных лабораторного, клинического и эпидемиологического обследования, причем главную роль в постановке диагноза играет лабораторное исследование крови.
Основным методом лабораторной диагностики является обнаружение антител к вирусу с помощью иммуноферментного анализа.
Порядок проведения лабораторного исследования на наличие антигенов вируса иммунодефицита человека и антител к этому вирусу строго регламентирован приказами Министерства здравоохранения Российской Федерации и включает в себя:
- этап скринингового (отборочного) исследования иммуноферментными (ИФА) методами, разрешёнными к использованию;
- этап верификационного (подтверждающего) исследования методом иммуноблота в лаборатории городского центра СПИД.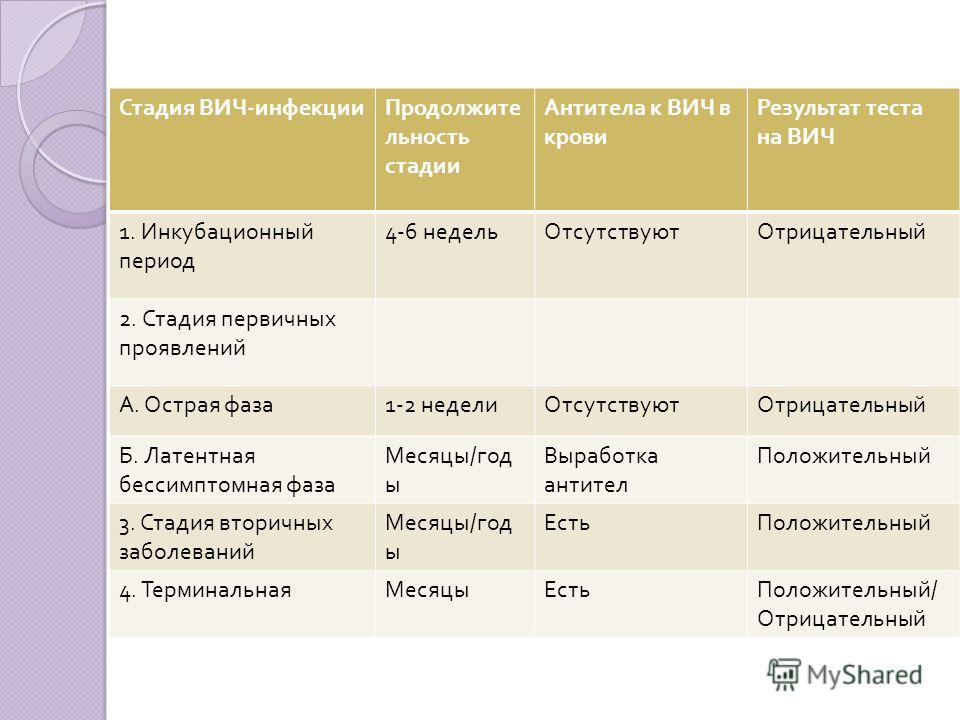
Лабораторная диагностика наличия вируса иммунодефицита у детей, рождённых от инфицированных этим вирусом матерей имеет свои особенности. В крови детей до 15 месяцев от момента рождения могут циркулировать материнские антитела к вирусу (класса Ig G). Отсутствие антител к вирусу у новорождённых не означает, что он не проник через плацентарный барьер. Дети матерей, инфицированных вирусом иммунодефицита, подлежат лабораторно-диагностическому обследованию в течение 36 месяцев после рождения.
Кровь рекомендуется сдавать утром натощак или не ранее, чем через 8-12 часа после приема пищи, допускается употребление воды без газа и сахара.
Накануне анализа следует отказаться от алкоголя, исключить физическое и эмоциональное перенапряжение.
Отказаться от курения за 1 час до исследования.
А также не стоит сдавать кровь в период приема медикаментов, если врач не назначил иное.
Оформление заявок для проведения исследований в ДНКОМ осуществляется по паспорту или документу, его заменяющему (миграционная карта, временная регистрация по месту жительства, удостоверение военнослужащего, справка из паспортного стола при утере паспорта, регистрационная карта учёта из гостиницы). Предъявленный документ в обязательном порядке должен содержать информацию о временной или постоянной регистрации на территории РФ и фотографию. При отсутствии паспорта (документа его заменяющего) пациент вправе оформить анонимную заявку для сдачи биоматериала. При анонимном обследовании, заявке и полученному от клиента образцу биоматериала присваивается номер, известный только пациенту, и медперсоналу, оформлявшему заказ.
При анонимном обследовании, заявке и полученному от клиента образцу биоматериала присваивается номер, известный только пациенту, и медперсоналу, оформлявшему заказ.
Результаты исследований, выполненных анонимно, не могут быть представлены для госпитализации, профессиональных осмотров и не подлежат регистрации в ОРУИБ.
Тест на антитела к ВИЧ 1/2 является качественным. При отсутствии антител выдается ответ «отрицательно».
Отрицательный результат:
Положительный результат:
*Специфичность скрининговой тест-системы антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo, Abbott), по оценкам, представленным производителем реагентов, составляет около 99,6% как в общей популяции, так и в группе пациентов с потенциальными интерференциями (инфекции HBV, HCV, Rubella, HAV, EBV, HNLV-I, HTLV-II, E. coli, Chl.trach. и др., аутоиммунные патологии (включая ревматоидный артрит, присутствие антинуклеарных антител), беременность, повышенный уровень IgG, IgM, моноклональные гаммапатии, гемодиализ, множественные гемотрансфузии).
coli, Chl.trach. и др., аутоиммунные патологии (включая ревматоидный артрит, присутствие антинуклеарных антител), беременность, повышенный уровень IgG, IgM, моноклональные гаммапатии, гемодиализ, множественные гемотрансфузии).
Исследование специфических антител и антигена p24 вируса иммунодефицита человека.
Синонимы русские
Антитела к ВИЧ 1, 2, антитела к вирусу иммунодефицита человека, ВИЧ-1 p24, ВИЧ-1 антиген, p24-антиген, антитела IgM и IgG суммарно.
Синонимы английские
Anti-HIV, HIV antibodies, human immunodeficiency virus antibodies, HIV-1 p24, HIV-1 Ag, p24-antigen, IgG, IgM total antibody test.
Метод исследования
Электрохемилюминесцентный иммуноанализ (ECLIA).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
 При конфиденциальном обследовании в обязательном порядке необходимо предъявление паспорта.
При конфиденциальном обследовании в обязательном порядке необходимо предъявление паспорта.Общая информация об исследовании
ВИЧ (вирус иммунодефицита человека) – вирус семейства ретровирусов, который поражает клетки иммунной системы человека (CD4, Т-хелперы). Вызывает СПИД.
ВИЧ-1 – наиболее распространенный тип вируса, чаще всего встречающийся в России, США, Европе, Японии и Австралии (как правило, субтип В).
ВИЧ-2 – редкий тип, распространен в Западной Африке.
Для диагностики вируса иммунодефицита человека используется комбинированная тест-система четвертого поколения, способная определять ВИЧ-инфекцию уже через 2 недели после попадания вируса в кровь, тогда как тест-системы первого поколения делают это только через 6-12 недель с момента инфицирования.
Преимуществом этого комбинированного ВИЧ-анализа является выявление, благодаря использованию антител к ВИЧ-1 p24 в качестве реагентов, специфического антигена p24 (белка вирусного капсида), который может быть обнаружен данным тестом уже через 1-4 недели с момента инфицирования, т. е. еще до сероконверсии, что значительно сокращает "период окна".
е. еще до сероконверсии, что значительно сокращает "период окна".
Кроме того, такой анализ на ВИЧ выявляет в крови антитела к ВИЧ-1 и ВИЧ-2 (с использованием реакции антиген-антитело), которые вырабатываются в достаточном количестве для определения тест-системой через 2-8 недель с момента заражения.
После сероконверсии антитела начинают связываться с антигеном p24, в результате чего тест на антитела к ВИЧ будет положительным, а тест на p24 – отрицательным. Однако спустя некоторое время в крови будут определяться и антитела, и антиген одновременно. На терминальной стадии СПИД-тест на антитела к ВИЧ может давать отрицательный результат, так как нарушается механизм выработки антител.
Стадии ВИЧ-инфекции

Несмотря на то что ВИЧ-инфекция неизлечима, сегодня существует высокоактивная антиретровирусная терапия (АРВТ), которая может значительно продлить жизнь ВИЧ-инфицированного и улучшить ее качество.
Данный тест имеет особенно высокую диагностическую ценность, если инфицирование ВИЧ произошло незадолго до момента тестирования (за 2-4 недели).
Для чего используется исследование?
Анализ используется для ранней диагностики ВИЧ, что позволяет предотвратить дальнейшую передачу вируса другим людям, а также своевременно начать антиретровирусную терапию и лечение заболеваний, способствующих прогрессированию ВИЧ-инфекции.
Когда назначается исследование?

Что означают результаты?
Референсные значения
Результат: отрицательный.
Причины отрицательного результата:

Причины положительного результата:
Важные замечания


Кто назначает исследование?
Врач общей практики, терапевт, инфекционист, дерматовенеролог.
. 2002 1 августа; 186 (3): 321-31.
дои: 10.1086/341661. Epub 2002 8 июля.
Цзяньминь Чен 1 , Лицян Ван, Дженни Дж. И. Чен, Гаутам К. Саху, Стивен Тайринг, Кит Рэмси, Александр Дж. Индриковс, Джон Р. Петерсен, Дэвид Паар, Майлз В. Клойд
Принадлежности
 [email protected]
[email protected] Цзяньминь Чен и др. J заразить Dis. .
. 2002 1 августа; 186 (3): 321-31.
дои: 10.1086/341661. Epub 2002 8 июля.
Цзяньминь Чен 1 , Лицян Ван, Дженни Дж. И. Чен, Гаутам К. Саху, Стивен Тайринг, Кит Рэмси, Александр Дж. Индриковс, Джон Р. Петерсен, Дэвид Паар, Майлз В. Клойд
 [email protected]
[email protected] На основании исследований вируса иммунодефицита человека (ВИЧ) укола иглой время до сероконверсии для анти-ВИЧ-антител составляет 1-9 месяцев (в среднем приблизительно 2-3 месяца). Однако часто встречается более ранний маркер иммунного ответа на ВИЧ — антитела к ВИЧ в сыворотке, реагирующие с живыми инфицированными ВИЧ клетками, называемые «ранними антителами к ВИЧ». Специфичность этих антител характеризуется распознаванием типоспецифических конформационных эпитопов гликопротеина оболочки ВИЧ (gp) 160 и gp41. При использовании нативного иммуноферментного анализа (ИФА) gp160 ВИЧ(IIIB) третьего поколения выявление антител к ВИЧ происходило в среднем на 33 дня раньше, чем при коммерческом ИФА, и на 25 дней раньше, чем при обнаружении эталонным антигеном и обратным антигеном. - анализы транскрипционной полимеразной цепной реакции (RT-PCR) в 3 из 5 панелей сероконверсии ВИЧ. Четвертая панель содержала ранние антитела к ВИЧ, которые реагировали с ВИЧ(213), но не с ВИЧ(IIIB), что позволяло обнаруживать антитела к ВИЧ примерно на 3 недели раньше, чем с помощью ОТ-ПЦР или других современных тестов.
- анализы транскрипционной полимеразной цепной реакции (RT-PCR) в 3 из 5 панелей сероконверсии ВИЧ. Четвертая панель содержала ранние антитела к ВИЧ, которые реагировали с ВИЧ(213), но не с ВИЧ(IIIB), что позволяло обнаруживать антитела к ВИЧ примерно на 3 недели раньше, чем с помощью ОТ-ПЦР или других современных тестов.
Обнаружение очень ранних антител к нативным антигенам ВИЧ с помощью анализов нейтрализации ВИЧ и иммунофлуоресценции живых клеток.
Пан Дж., Чен Дж., Ли Х., Саху Г.К., Поаст Дж.С., Тайринг С., Клойд М., Барон С. Пан Дж. и др. Противовирусный рез. 2006 г., июнь; 70 (2): 21-7. doi: 10.1016/j.antiviral.2005.12.008. Epub 2006 26 января. Противовирусный рез. 2006. PMID: 16513186
Раннее выявление антител к вирусу иммунодефицита человека 1 методом иммуноферментного анализа третьего поколения. Сравнительное исследование с результатами иммуноанализов второго поколения и вестерн-блоттинга.
Сравнительное исследование с результатами иммуноанализов второго поколения и вестерн-блоттинга.
Барбе Ф., Кляйн М., Бадоннель Ю. Барбе Ф. и др. Энн Биол Клин (Париж). 1994;52(5):341-5. Энн Биол Клин (Париж). 1994. PMID: 7856933
Многоцентровая оценка нового теста для скрининга на ВИЧ 4-го поколения Elecsys HIV combi.
Вебер Б., Орази Б., Райнери А., Торстенссон Р., Бюргиссер П., Мюльбахер А., Ареал С., Эйрас А., Вильяэскуза Р., Камачо Р., Диого И., Рот Х.Дж., Зан И., Бартель Дж., Босси В., Пиро Ф., Атамасирикул К., Пермпикул П., Уэббер Л., Сингх С. Вебер Б. и др. Клин Лаборатория. 2006;52(9-10):463-73. Клин Лаборатория. 2006. PMID: 17078473
[Недавний прогресс в скрининговых тестах на ВИЧ и тестах на нуклеиновые кислоты].
Имаи М., Като С. Имаи М. и др. Нихон Ринсё. 2010 март; 68 (3): 433-8. Нихон Ринсё. 2010. PMID: 20229786 Рассмотрение. Японский язык.
Вирусологическая диагностика ВИЧ-инфекции у детей.
Рузиу К. Рузиу С. Патол Биол (Париж). 1992 г., сен; 40 (7): 720-3. Патол Биол (Париж). 1992. PMID: 1480408 Рассмотрение. Французский.
Посмотреть все похожие статьи
Создание и применение непрямого иммуноферментного анализа для измерения антител к GPI-заякоренному белку 52 (P52) у инфицированных собак Babesia gibsoni .
Лю К., Чжан С., Ли Д., Чжао Дж., Вэй Х., Альзан Х., Хе Л. Лю Кью и др. Животные (Базель). 2022 6 мая; 12(9)):1197. дои: 10.3390/ани12091197. Животные (Базель). 2022. PMID: 35565622 Бесплатная статья ЧВК.
Животные (Базель). 2022 6 мая; 12(9)):1197. дои: 10.3390/ани12091197. Животные (Базель). 2022. PMID: 35565622 Бесплатная статья ЧВК.
Характеристики результатов скрининга и подтверждающих тестов на ВИЧ в Сиане, Китай.
Ван Л., Чжоу К.Х., Чжао Х.П., Ван Дж.Х., Чжэн Х.К., Ю.И., Чен В. Ван Л. и др. ПЛОС Один. 7 июля 2017 г .; 12 (7): e0180071. doi: 10.1371/journal.pone.0180071. Электронная коллекция 2017. ПЛОС Один. 2017. PMID: 28686629Бесплатная статья ЧВК.
Вирусные гликопротеины: биологическая роль и применение в диагностике.
Банерджи Н., Мукхопадхьяй С. Банерджи Н. и др. Вирусное заболевание. 2016 март; 27(1):1–11. doi: 10.1007/s13337-015-0293-5. Epub 2016 18 января. Вирусное заболевание.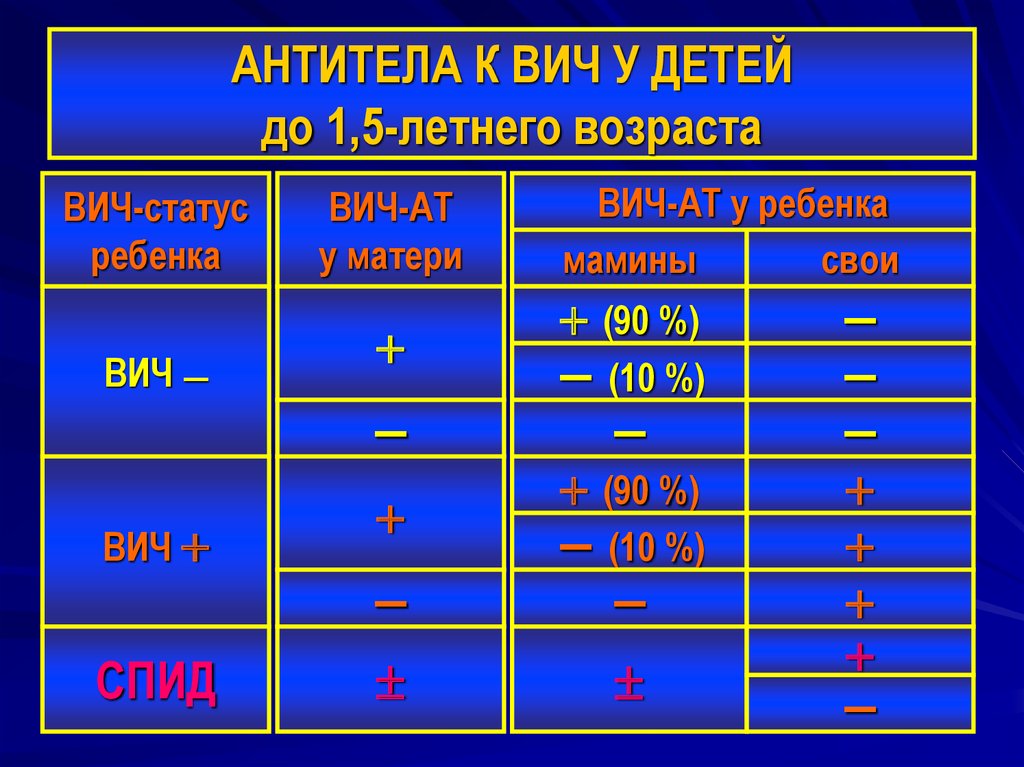 2016. PMID: 26925438 Бесплатная статья ЧВК. Рассмотрение.
2016. PMID: 26925438 Бесплатная статья ЧВК. Рассмотрение.
Гликопротеин оболочки ВИЧ-1, экспрессируемый почти полной длиной Escherichia coli, является высокочувствительным и специфичным диагностическим антигеном.
Талха С.М., Немани С.К., Салминен Т., Кумар С., Сваминатан С., Соукка Т., Петтерссон К., Ханна Н. Талха С.М. и др. BMC Infect Dis. 2012 27 ноя; 12:325. дои: 10.1186/1471-2334-12-325. BMC Infect Dis. 2012. PMID: 23186021 Бесплатная статья ЧВК.
1. Allen TM, Vogel TU, Fuller DH, Mothé BR, Steffen S, Boyson JE , Шипли Т., Фуллер Дж., Ханке Т., Сетте А., Альтман Дж. Д., Мосс Б., МакМайкл А. Дж., Уоткинс Д. И. Индукция активности ЦТЛ, специфичных для вируса СПИДа, в свежих, нестимулированных лимфоцитах периферической крови макак-резусов, вакцинированных ДНК-праймом/ модифицированный режим вакцинации против вируса коровьей оспы Ankara. Дж Иммунол. 2000;164:4968–4978. [PubMed] [Google Scholar]
Allen TM, Vogel TU, Fuller DH, Mothé BR, Steffen S, Boyson JE , Шипли Т., Фуллер Дж., Ханке Т., Сетте А., Альтман Дж. Д., Мосс Б., МакМайкл А. Дж., Уоткинс Д. И. Индукция активности ЦТЛ, специфичных для вируса СПИДа, в свежих, нестимулированных лимфоцитах периферической крови макак-резусов, вакцинированных ДНК-праймом/ модифицированный режим вакцинации против вируса коровьей оспы Ankara. Дж Иммунол. 2000;164:4968–4978. [PubMed] [Google Scholar]
2. Баруш Д. Х., Сантра С., Шмитц Дж. Э., Курода М. Дж., Фу Т-М., Вагнер В., Билска М., Крайу А., Чжэн X X, Кривулка Г. Р., Бодри К., Лифтон М. А., Никерсон С. Э., Тригона В.Л., Пунт К., Фрид Д.К., Гуан Л., Дубей С., Касимиро Д., Саймон А., Дэвис М.Э., Честейн М., Стром Т.Б., Гельман Р.С., Монтефиори Д.К., Льюис М.Г., Эмини Э.А., Шивер Дж.В., Летвин Н.Л. Контроль виремии и профилактики клинического СПИДа у макак-резусов с помощью вакцинации ДНК с добавлением цитокинов. Наука. 2000;290: 486–492. [PubMed] [Google Scholar]
3. Bauer S, Groh V, Wu J, Steinle A, Phillips JH, Lanier LL, Spies T. Активация NK-клеток и Т-клеток с помощью NKG2D, рецептора стресс-индуцируемой MICA. Наука. 1999; 285:727–729. [PubMed] [Google Scholar]
Активация NK-клеток и Т-клеток с помощью NKG2D, рецептора стресс-индуцируемой MICA. Наука. 1999; 285:727–729. [PubMed] [Google Scholar]
4. Baum L L, Cassutt K J, Knigge K, Khattri R, Margolick J, Rinaldo C, Kleeberger CA, Nishanian P, Henrard DR, Phair J. ВИЧ-1, специфичный к gp120, зависимый от антител клеточно-опосредованная цитотоксичность коррелирует со скоростью прогрессирования заболевания. Дж Иммунол. 1996;157:2168–2173. [PubMed] [Google Scholar]
5. Бинли Дж. М., Клас Б., Гетти А., Весанен М., Монтефиори Д. К., Сойер Л., Бут Дж., Льюис М., Маркс П. А., Бонхеффер С., Мур Дж. П. Пассивная инфузия иммунной сыворотки вирусом иммунодефицита обезьян, инфицированных макаками-резусами с быстрым течением заболевания, оказывает минимальное влияние на виремию в плазме. Вирусология. 2000; 270: 237–249. [PubMed] [Google Scholar]
6. Borrow P, Lewicki H, Hahn BH, Shaw GM, Oldstone MB. Вирус-специфическая активность цитотоксических Т-лимфоцитов CD8 + , связанная с контролем виремии при первичном типе вируса иммунодефицита человека.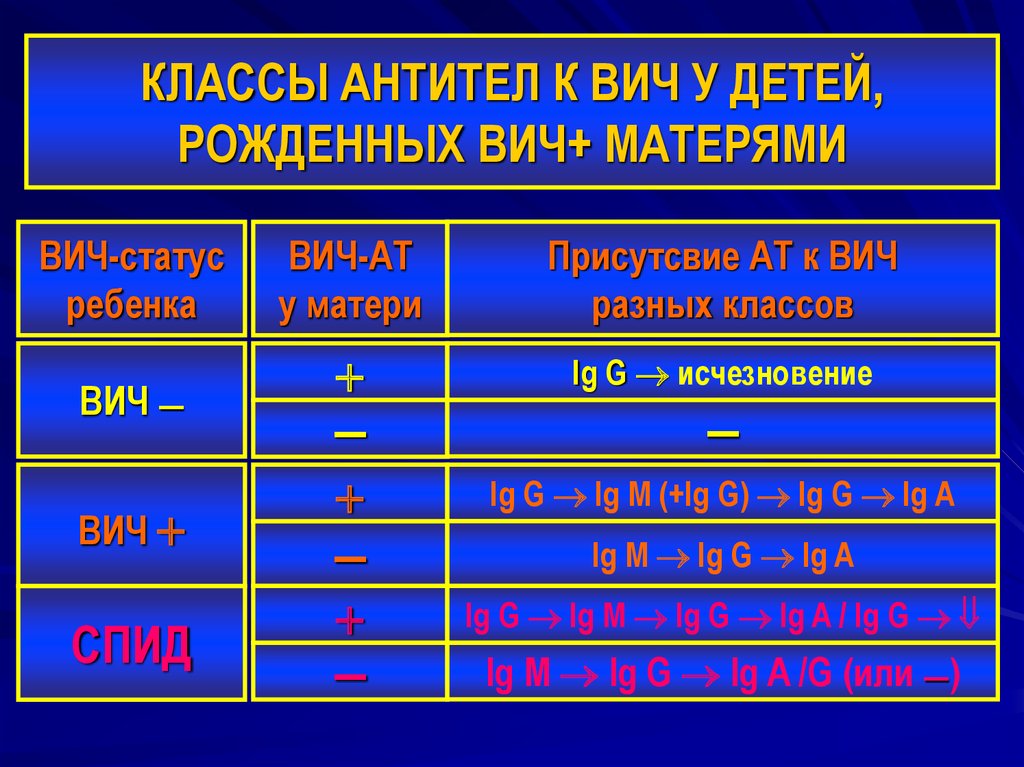 1 инфекция. Дж Вирол. 1994;68:6103–6110. [Бесплатная статья PMC] [PubMed] [Google Scholar]
1 инфекция. Дж Вирол. 1994;68:6103–6110. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Брауд В. М., Аллан Д. С., О'Каллаган С. А., Седерстрем К., Д'Андреа А., Огг Г. С., Лазети С., Янг Н. Т., Белл Дж. И., Филлипс Дж. Х., Lanier L L, McMichael A J. HLA-E связывается с рецепторами естественных клеток-киллеров CD94/NKG2A, B и C. Nature. 1998; 391: 795–799. [PubMed] [Google Scholar]
8. Carter DL, Shieh TM, Blosser RL, Chadwick KR, Margolick JB, Hildreth JEK, Clements JE, Zink MC. CD56 идентифицирует моноциты, а не естественные клетки-киллеры у макак-резусов. Цитометрия. 1999;37:41–50. [PubMed] [Google Scholar]
9. Коэн Г. Б., Ганди Р. Т., Дэвис Д. М., Мандельбойм О., Чен Б. К., Стромингер Дж. Л., Балтимор Д. Избирательное подавление белков главного комплекса гистосовместимости класса I с помощью ВИЧ-1 защищает ВИЧ-инфицированных клеток из NK-клеток. Иммунитет. 1999; 10: 661–671. [PubMed] [Google Scholar]
10. Колонна М., Борселлино Г., Фалько М., Феррара Г. Б., Стромингер Дж.Л. HLA-C является ингибирующим лигандом, определяющим доминантную устойчивость к лизису со стороны NK1- и NK2-специфических естественных клеток-киллеров. . Proc Natl Acad Sci USA. 1993;90:12000–12004. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Б., Стромингер Дж.Л. HLA-C является ингибирующим лигандом, определяющим доминантную устойчивость к лизису со стороны NK1- и NK2-специфических естественных клеток-киллеров. . Proc Natl Acad Sci USA. 1993;90:12000–12004. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Connick E, Marr DG, Zhang X Q, Clark SJ, Saag M S, Schooley RT, Curiel T J. ВИЧ-специфические клеточные и гуморальные иммунные ответы при первичной ВИЧ-инфекции . AIDS Res Human Retrovir. 1996; 12:1129–1140. [PubMed] [Google Scholar]
12. Daar E S, Moudgil T, Meyer R D, Ho D D. Преходящие высокие уровни виремии у пациентов с первичной инфекцией вирусом иммунодефицита человека 1 типа. N Engl J Med. 1991; 324: 961–964. [PubMed] [Академия Google]
13. Dragie T, Litwin V, Allaway GP, Martin S R, Huang Y, Nagashima K A, Cayanan C, Maddon P J, Koup R A, Moore J P, Paxton WA. Вход ВИЧ-1 в клетки CD4 + опосредуется хемокиновым рецептором CC-CKR-5. Природа. 1996; 381: 667–673. [PubMed] [Google Scholar]
14. Forthal DN, Landucci G, Keenan B. Взаимосвязь между антителозависимой клеточной цитотоксичностью, РНК ВИЧ-1 в плазме и количеством лимфоцитов CD4 + . AIDS Res Hum Retrovir. 2001; 17: 553–561. [PubMed] [Академия Google]
Forthal DN, Landucci G, Keenan B. Взаимосвязь между антителозависимой клеточной цитотоксичностью, РНК ВИЧ-1 в плазме и количеством лимфоцитов CD4 + . AIDS Res Hum Retrovir. 2001; 17: 553–561. [PubMed] [Академия Google]
15. Джаведони Л.Д., Веласкильо М.С., Пароди Л.М., Хаббард Г.Б., Ходара В.Л. Экспрессия цитокинов, активация естественных клеток-киллеров и фенотипические изменения в лимфоидных клетках макак-резусов во время острой инфекции патогенным вирусом иммунодефицита обезьян. Дж Вирол. 2000; 74: 1648–1657. [Статья бесплатно PMC] [PubMed] [Google Scholar]
16. Jewett A, Giorgi JV, Bonavida B. Антителозависимая клеточная цитотоксичность против ВИЧ-покрытых клеток-мишеней моноцитами периферической крови ВИЧ-серопозитивных бессимптомных пациентов. Дж Иммунол. 1990;145:4065–4071. [PubMed] [Google Scholar]
17. Koup R A, Safrit J T, Cao Y, Andrews CA, McLeod G, Borkowsky W, Farthing C, Ho D D. Временная связь клеточных иммунных ответов с начальным контролем виремии при первичных синдром вируса иммунодефицита человека 1 типа.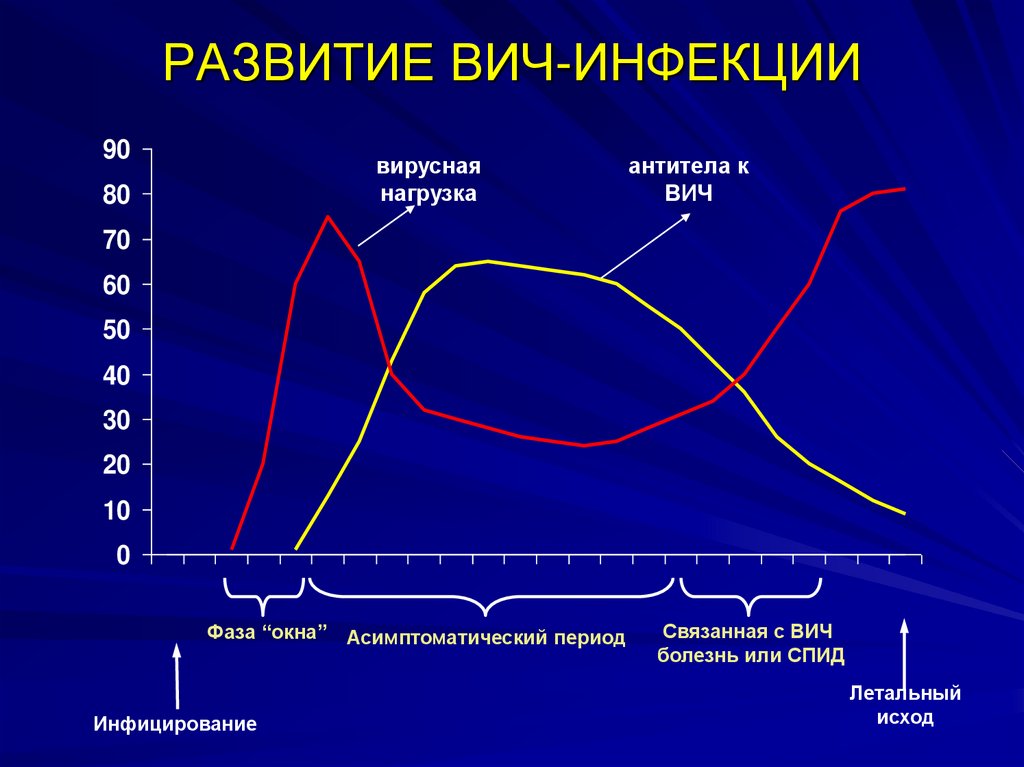 Дж Вирол. 1994;68:4650–4655. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Дж Вирол. 1994;68:4650–4655. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Legrand E, Pellegrin I, Neau D, Pellegrin J L, Ragnaud J M, Dupon M, Guillemain B, Fleury H J. Курс специфической цитотоксичности Т-лимфоцитов, плазмы и клеточная вирусная нагрузка и титры нейтрализующих антител у 17 пациентов, инфицированных ВИЧ типа 1, недавно перенесших сероконверсию. AIDS Res Hum Retrovir. 1997;13:1383–1394. [PubMed] [Google Scholar]
19. Летвин Н.Л., Шмитц Дж.Э., Джордан Х.Л., Сет А., Хирш В.М., Рейманн К.А., Курода М.Дж. Цитотоксические Т-лимфоциты, специфичные для вируса иммунодефицита обезьян. Immunol Rev. 1999; 170:127–134. [PubMed] [Google Scholar]
20. Леунг Н.Дж., Альдовини А., Янг Р., Джарвис М.А., Смит Дж.М., Мейер Д., Андерсон Д.Е., Карлос М.П., Гарднер М.Б., Торрес Дж.В. Кинетика специфических иммунных реакций при резус-факторе обезьян, инокулированных живой рекомбинантной БЦЖ, экспрессирующей SIV Gag. Белки Pol, Env и Nef. Вирусология. 2000;268:94–103. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
21. Lyerly HK, Matthews TJ, Langlois AJ, Bolognesi DP, Weinhold KJ. Гликопротеин IIIB Т-клеточного лимфотропного вируса человека (gp120), связанный с детерминантами CD4 на нормальных лимфоцитах и экспрессируемый инфицированными клетками. служит мишенью для иммунной атаки. Proc Natl Acad Sci USA. 1987; 84: 4601–4605. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Меллорс Дж. В., Ринальдо С. Р., младший, Гупта П., Уайт Р. М., Тодд Дж. А., Кингсли Л. А. Прогноз при ВИЧ-1-инфекции определяется количеством вируса в плазма. Наука. 1996;272:1167–1170. [PubMed] [Google Scholar]
23. Moog C, Fleury HJ, Pellegrin I, Kirn A, Aubertin AM. Ответы аутологичных и гетерологичных нейтрализующих антител после начальной сероконверсии у людей, инфицированных вирусом иммунодефицита человека типа 1. Дж Вирол. 1997;71:3734–3741. [Статья бесплатно PMC] [PubMed] [Google Scholar]
24. Moore J P, Cao Y, Ho DD, Koup R A. Развитие ответа антител против gp120 во время сероконверсии к вирусу иммунодефицита человека типа 1.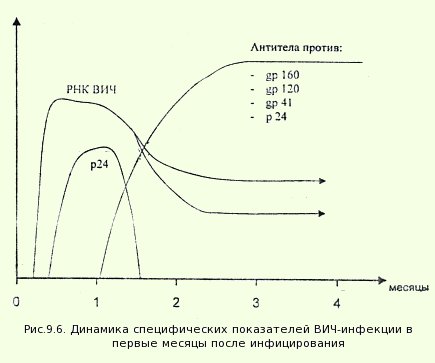 J Virol. 1994;68:5142–5155. [Статья бесплатно PMC] [PubMed] [Google Scholar]
J Virol. 1994;68:5142–5155. [Статья бесплатно PMC] [PubMed] [Google Scholar]
25. Morrison L A, Zhu L, Thebeau L G. Сывороточный иммуноглобин, индуцированный вакциной, способствует защите от вируса простого герпеса 2 типа генитальной инфекции в присутствии иммунных Т-клеток. Дж Вирол. 2001; 75: 1195–1204. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Мюллер Х., Фальк С., Шмидтс Х.Л., Штутте Х.Дж. Иммунофенотипирование лимфоцитов/макрофагов in situ: классификация лимфаденопатии, стадирование и патофизиология ВИЧ-инфекции. Рез Вирол. 1990;141:171–184. [PubMed] [Google Scholar]
27. Musey L, Hughes J, Schacker T, Shea T, Corey L, McElrath M J. Реакция цитотоксических Т-клеток, вирусная нагрузка и прогрессирование заболевания при раннем вирусе иммунодефицита человека типа 1 инфекционное заболевание. N Engl J Med. 1997; 337:1267–1274. [PubMed] [Google Scholar]
28. Олива А., Кинтер А. Л., Ваккарецца М., Рубберт А., Катандзаро А., Мойр С., Монако Дж., Элер Л. , Мизелл С., Джексон Р., Ли И., Романо Дж. В., Фаучи А. С. Естественные клетки-киллеры от людей, инфицированных вирусом иммунодефицита человека (ВИЧ), являются важным источником CC-хемокинов и подавляют проникновение и репликацию ВИЧ-1 in vitro. Дж. Клин Инвестиг. 1998;102:223–231. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Мизелл С., Джексон Р., Ли И., Романо Дж. В., Фаучи А. С. Естественные клетки-киллеры от людей, инфицированных вирусом иммунодефицита человека (ВИЧ), являются важным источником CC-хемокинов и подавляют проникновение и репликацию ВИЧ-1 in vitro. Дж. Клин Инвестиг. 1998;102:223–231. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Orenstein J M, Feinberg M, Yoder C, Schrager L, Mican JM, Schwartzentruber D J, Davey R T, Jr, Walker R E, Falloon J, Kovacs J A, Miller K D , Fox C, Metcalf JA, Masur H, Polis MA. Архитектура лимфатических узлов до и после 6 месяцев мощной противовирусной терапии: фолликулярная гиперплазия сохраняется параллельно с восстановлением антигена p24 после инволюции и истощения клеток CD4 у больного СПИДом. СПИД. 1999;13:2219–2229. [PubMed] [Google Scholar]
30. Пилигрим А.К., Панталео Г., Коэн О.Дж., Финк Л.М., Чжоу Дж.Ю., Чжоу Дж.Т., Болоньези Д.П., Фаучи А.С., Монтефиори Д.С. инфекция и длительно непрогрессирующая инфекция. J заразить Dis. 1997; 176: 924–932. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
31. Прайс Д. А., Гоулдер П. Дж., Кленерман П., Сьюэлл А. К., Истербрук П. Дж., Троуп М., Бэнгэм С. Р., Филлипс Р. Э. Положительный отбор вариантов ускользания цитотоксических Т-лимфоцитов ВИЧ-1 во время первичной инфекции . Proc Natl Acad Sci USA. 1997;94:1890–1895. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Ravetch JV, Perussia B. Альтернативные мембранные формы Fc gamma RIII (CD16) на естественных клетках-киллерах и нейтрофилах человека. Специфическая для типа клеток экспрессия двух генов, различающихся заменами одиночных нуклеотидов. J Эксперт Мед. 1989; 170: 481–497. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33. Розенберг Э.С., Биллингсли Дж.М., Калиендо А.М., Босуэлл С.Л., Сакс П.Е., Каламс С.А., Уокер Б.Д. Энергичный ВИЧ-1-специфический CD4 + Т-клеточные ответы, связанные с контролем виремии. Наука. 1997; 278:1447–1450. [PubMed] [Google Scholar]
34. Ruppach H, Nara P, Raudonat I, Elanjikal Z, Rübsamen-Waigmann H, Dietrich U. Положительная сыворотка на вирус иммунодефицита человека (ВИЧ), полученная вскоре после сероконверсии, нейтрализует аутологичные изоляты ВИЧ типа 1. на первичных макрофагах, но не на лимфоцитах. Дж Вирол. 2000; 74: 5403–5411. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Положительная сыворотка на вирус иммунодефицита человека (ВИЧ), полученная вскоре после сероконверсии, нейтрализует аутологичные изоляты ВИЧ типа 1. на первичных макрофагах, но не на лимфоцитах. Дж Вирол. 2000; 74: 5403–5411. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Шакер Т.В., Хьюз Дж.П., Ши Т., Кумбс Р.В., Кори Л. Биологические и вирусологические характеристики первичной ВИЧ-инфекции. Энн Интерн Мед. 1998;128:613–620. [PubMed] [Google Scholar]
36. Schmitz JE, Kuroda MJ, Santra S, Sasseville VG, Simon MA, Lifton MA, Racz P, Tenner-Racz K, Dalesandro M, Scallon BJ, Ghrayeb J, Forman MA, Montefiori D C, Rieber E P, Letvin N L, Reimann K A. KA. Контроль виремии при заражении вирусом иммунодефицита обезьян с помощью CD8+ лимфоцитов. Наука. 1999; 283: 857–860. [PubMed] [Google Scholar]
37. Schwartz O, Maréchal V, Le Gall S, Lemonnier F, Heard J M. Эндоцитоз молекул главного комплекса гистосовместимости класса I индуцируется белком Nef ВИЧ-1. Нат Мед.