2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
1. Lebwohl M, Rivera-Oyola R, Murrell DF. Should biologics for psoriasis be interrupted in the era of COVID-19? J Am Acad Dermatol. 2020;82(5):1217-1218. doi: 10.1016/j.jaad.2020.03.031.
2. Singh JA, Wells GA, Christensen R, et al. Adverse effects of biologics: a network meta-analysis and Cochrane overview. Cochrane Database Syst Rev. 2011;2011(2):CD008794. doi: 10.1002/14651858.CD008794.pub2.
3. Hoshi D, Nakajima A, Inoue E, et al. Incidence of serious respiratory infections in patients with rheumatoid arthritis treated with tocilizumab. Mod Rheumatol. 2012;22(1):122-127. doi: 10.1007/s10165-011-0488-6.
4. Pawar A, Desai RJ, Solomon DH, et al. Risk of serious infections in tocilizumab versus other biologic drugs in patients with rheumatoid arthritis: a multidatabase cohort study. Ann Rheum Dis. 2019;78(4):456-464. doi: 10.1136/annrheumdis-2018-214367.
5. Van Vollenhoven RF, Emery P, Bingham CO, et al. Longterm safety of patients receiving rituximab in rheumatoid arthritis clinical trials. J Rheumatol. 2010;37(3):558-567. doi: 10.3899/jrheum.090856.
6. Papp KA, Griffiths CE, Gordon K, et al. Long-term safety of ustekinumab in patients with moderate-to-severe psoriasis: final results from 5 years of follow-up. Br J Dermatol. 2013;168(4): 844-854. doi: 10.1111/bjd.12214.
7. Frieder J, Kivelevitch D, Menter A, et al. Secukinumab: a review of the anti-IL-17A biologic for the treatment of psoriasis. Ther Adv Chronic Dis. 2018;9(1):5-21. doi: 10.1177/2040622317738910.
8. Jaillette E, Girault C, Brunin G, et al. Biological therapies in the treatment of inflammatory disease and cancer: impact on pulmonary infection. Ann Intensive Care. 2016;6(Suppl 1):50. doi: 10.1186/s13613-016-0114-z.
9. Cascella M, Rajnik M, Cuomo A, et al. Features, evaluation and treatment coronavirus (COVID-19) [updated 2020 Mar 20]. Treasure Island (FL): StatPearls Publishing; 2020. Available from: https://www. ncbi.nlm.nih.gov/books/NBK554776/.
ncbi.nlm.nih.gov/books/NBK554776/.
10. Monteleone G, Sarzi-Puttini PC, Ardizzone S. Preventing COVID-19-induced pneumonia with anticytokine therapy. Lancet Rheumatol. 2020. doi: 10.1016/s2665-9913(20)30092-8.
11. Conforti C, Giuffrida R, Dianzani C, et al. COVID-19 and psoriasis: is it time to limit treatment with immunosuppressants? A call for action. Dermatol Ther. 2020. doi: 10.1111/dth.13298.
12. Bardazzi F, Loi C, Sacchelli L, Di Altobrando A. Biologic therapy for psoriasis during the COVID-19 outbreak is not a choice. J Dermatolog Treat. 2020;31(4):320-321. doi: 10.1080/09546634.2020.1749545.
13. De Wit E, van Doremalen N, Falzarano D, et al. SARS and MERS: recent insights into emerging coronaviruses. Nat Rev Microbiol. 2016;14:523-534. doi: 10.1038/nrmicro.2016.81.
14. Fehr AR, Perlman S. Coronaviruses: an overview of their replication and pathogenesis. Methods Mol Biol. 2015;1282:1-23. doi: 10.1007/978-1-4939-2438-7_1.
15. Li X, Geng M, Peng Y, et al.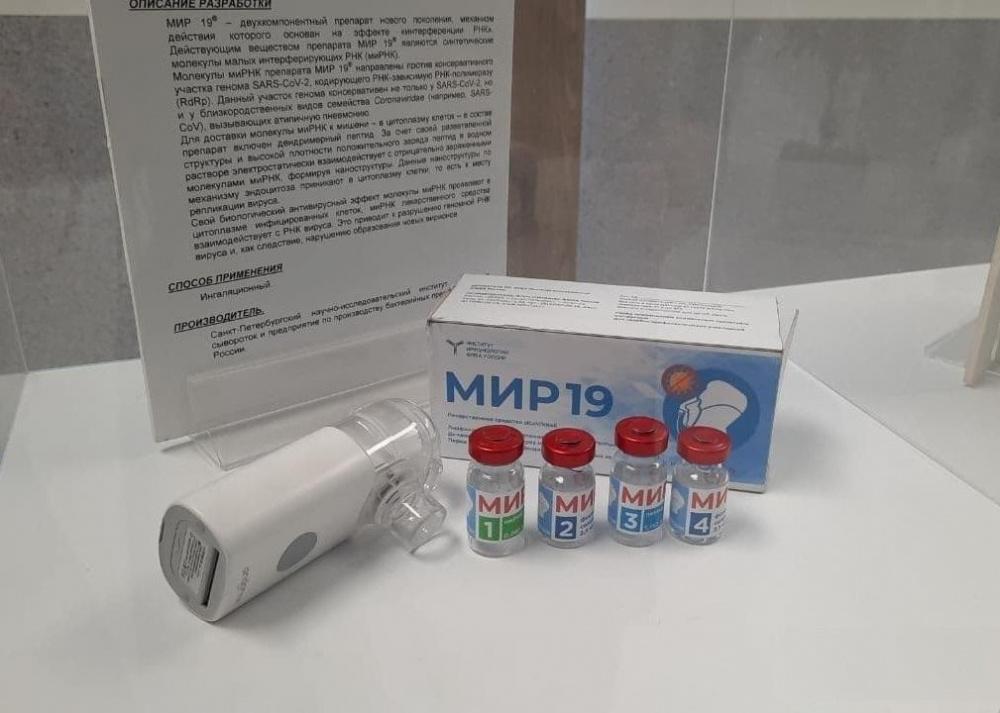 Molecular immune pathogenesis and diagnosis of COVID-19. J Pharm Anal. 2020;10(2):102-108. doi: 10.1016/j.jpha.2020.03.001.
Molecular immune pathogenesis and diagnosis of COVID-19. J Pharm Anal. 2020;10(2):102-108. doi: 10.1016/j.jpha.2020.03.001.
16. Lin L, Lu L, Cao W, Li T. Hypothesis for potential pathogenesis of SARS-CoV-2 infection — a review of immune changes in patients with viral pneumonia. Emerg Microbes Infect. 2020;9(1):727-732. doi: 10.1080/22221751.2020.1746199.
17. Kuba K, Imai Y, Rao S, et al. A crucial role of angiotensin converting enzyme 2 (ACE2) in SARS coronavirus — induced lung injury. Nat Med. 2005;11:875-879. doi: 10.1038/nm1267.
18. Rabi FA, Al Zoubi MS, Kasasbeh GA, et al. SARS-CoV-2 and coronavirus disease 2019: what we know so far. Pathogens. 2020;9(3):231. doi: 10.3390/pathogens9030231.
19. Fehr AR, Perlman S. Coronaviruses: an overview of their replication and pathogenesis. Coronaviruses. Methods Mol Biol. 2015; 1282:1-23. doi: 10.1007/978-1-4939-2438-7_1.
20. Cheng H, Wang Y, Wang GQ. Organ protective effect of angiotensin converting enzyme 2 and its effect on the prognosis of COVID-19.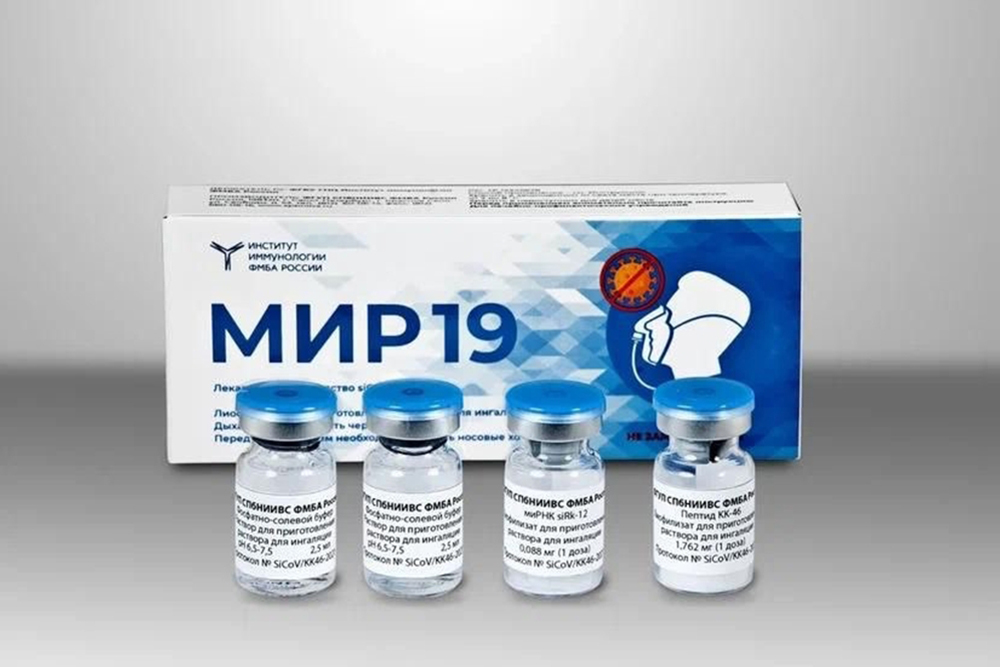 J Med Virol. 2020. doi: 10.1002/jmv.25785.
J Med Virol. 2020. doi: 10.1002/jmv.25785.
21. Minodier L, Charrel RN, Ceccaldi P, et al. Prevalence of gastrointestinal symptoms in patients with influenza, clinical significance, and pathophysiology of human influenza viruses in faecal samples: what do we know? Virol J. 2015;12:215. doi: 10.1186/s12985-015-0448-4.
22. Letko M, Marzi A, Munster V. Functional assessment of cell entry and receptor usage for SARS-CoV-2 and other lineage B betacoronaviruses. Nat Microbiol. 2020;5:562-569. doi: 10.1038/s41564-020-0688-y.
23. Cristiani L, Mancino E, Matera L, et al. Will children reveal their secret? The coronavirus dilemma. Eur Respir J. 2020; in press. doi: 10.1183/13993003.00749-2020.
24. Manjarrez-Zavala ME, Rosete-Olvera DP, Gutierrez-Gonzalez LH, et al. Pathogenesis of viral respiratory infection. Respiratory disease and infection — a new insight. Submitted: April 26th 2012. Reviewed: October 12th 2012. Published: February 6th 2013. doi: 10.5772/54287.
25. Totura AL, Baric RS. SARS coronavirus pathogenesis: host innate immune responses and viral antagonism of interferon. Curr Opin Virol. 2012;2(3):264-275. doi: 10.1016/j.coviro.2012.04.004.
Totura AL, Baric RS. SARS coronavirus pathogenesis: host innate immune responses and viral antagonism of interferon. Curr Opin Virol. 2012;2(3):264-275. doi: 10.1016/j.coviro.2012.04.004.
26. Rokni M, Ghasemi V, Tavakoli Z. Immune responses and pathogenesis of SARS-CoV-2 during an outbreak in Iran: Comparison with SARS and MERS. Rev Med Virol. 2020. doi: 10.1002/rmv.2107.
27. Kollmann TR, Crabtree J, Rein-Weston A, et al. Neonatal innate TLR-mediated responses are distinct from those of adults. J Immunol. 2009;183:7150-7160.
28. Prompetchara E, Ketloy C, Palaga T. Immune responses in COVID-19 and potential vaccines: Lessons learned from SARS and MERS epidemic. Asian Pac J Allergy Immunol. 2020;38(1):1-9. doi: 10.12932/AP-200220-0772.
29. Snijder EJ, van der Meer Y, Zevenhoven-Dobbe J, et al. Ultrastructure and origin of membrane vesicles associated with the severe acute respiratory syndrome coronavirus replication complex. J Virol. 2006;80:5927-5940. doi: 10.1128/JVI. 02501-05.
02501-05.
30. Fung SY, Yuen KS, Ye ZW, et al. A tug-of-war between severe acute respiratory syndrome coronavirus 2 and host antiviral defence: lessons from other pathogenic viruses. Emer Microb Inf. 2020;(1): 558-570. doi: 10.1080/22221751.2020.1736644.
31. Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020. doi: 10.1016/S0140-6736(20)30183-5.
32. Xu Z, Shi L, Wang Y, et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Resp Med. 2020. doi: 10.1016/S2213-2600(20)30076-X.
33. Channappanavar R, Perlman S. Pathogenic human coronavirus infections: causes and consequences of cytokine storm and immunopathology. Semin Immunopathol. 2017;39:529-539. doi: 10.1007/s00281-017-0629-x.
34. Zhou G, Zhao Q. Perspectives on therapeutic neutralizing antibodies against the Novel Coronavirus SARS-CoV-2. Int J Biol Sci. 2020;16(10):1718-1723. doi: 10.7150/ijbs. 45123.
45123.
35. Liu WJ, Zhao M, Liu K, et al. T-cell immunity of SARS-CoV: Implications for vaccine development against MERS-CoV. Antiviral Res. 2017;137:82-92.
36. Mysliwska J, Trzonkowski P, Szmit E, et al. Immunomodulating effect of influenza vaccination in the elderly differing in health status. Exp Gerontol. 2004;39:1447-1458. doi: 10.1016/j.exger.2004.08.005.
37. Belz GT, Smith CM, Kleinert L, et al. Distinct migrating and nonmigrating dendritic cell populations are involved in MHC class I-restricted antigen presentation after lung infection with virus. Proc Natl Acad Sci USA. 2004;101(23):8670-8675. doi: 10.1073/pnas.0402644101.
38. Li G, Fan Y, Lai Y, et al. Coronavirus infections and immune responses. J Med Virol. 2020. doi: 10.1002/jmv.25685.
39. Liu L, Wei Q, Lin Q, et al. Anti-spike IgG causes severe acute lung injury by skewing macrophage responses during acute SARS-CoV infection. JCI Insight. 2019;4:e123158.
40. COVID-19 Science Report: Pathogenesis and Host Immune Response to SARS-CoV-2. Jointly Developed by: NUS Yong Loo Lin School of Medicine, Department of Microbiology and Immunology. Singapore Immunology Network (SIgN), A*STAR As; 2020.
Jointly Developed by: NUS Yong Loo Lin School of Medicine, Department of Microbiology and Immunology. Singapore Immunology Network (SIgN), A*STAR As; 2020.
41. Channappanavar R, Zhao J, Perlman S. T cell-mediated immune response to respiratory coronaviruses. Immunol Res. 2014; 59(1-3):118-128. doi: 10.1007/s12026-014-8534-z.
42. Scheller J, Chalaris A, Schmidt-Arras D, Rose-John S. The pro- and anti-inflammatory properties of the cytokine interleu-kin-6. BBA Mol Cell Res. 2011;1813(5):878-888. doi: 10.1016/j.bbamcr.2011.01.034.
43. Murthy H, Iqbal M, Chavez JC, Kharfan-Dabaja MA. Cytokine release syndrome: current perspectives. Immunotargets Ther. 2019; 8:43-52. doi: 10.2147/ITT.S202015.
44. Cokic VP, Mitrovic-Ajtic O, Beleslin-Cokic BB, et al. Proinflam-matory cytokine IL-6 and JAK-STAT signaling pathway in myeloproliferative neoplasms. Mediators Inflamm. 2015;2015:453020. doi: 10.1155/2015/453020.
45. FDA approves tisagenlecleucel for B-cell ALL and tocilizumab for cytokine release syndrome. FDA [WWW Document]. Available from: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-tisagenlecleucel-b-cell-all-and-tocilizumab-cytokine-release-syndrome.
FDA [WWW Document]. Available from: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-tisagenlecleucel-b-cell-all-and-tocilizumab-cytokine-release-syndrome.
46. Lee DW, Gardner R, Porter DL, et al. Current concepts in the diagnosis and management of cytokine release syndrome. Blood. 2014;124(2):188-195. doi: 10.1182/blood-2014-05-552729.
47. Feldmann M, et al. Trials of anti-tumour necrosis factor therapy for COVID-19 are urgently needed. Lancet. 2020. doi: 10.1016/S0140-6736(20)30858-8.
48. Das R, Guan P, Sprague L, et al. Janus kinase inhibition lessens inflammation and ameliorates disease in murine models of hemophagocytic lymphohistiocytosis. Blood. 2016;127(13): 1666-1675. doi: 10.1182/blood-2015-12-684399.
49. Huarte E, O'Connor RS, et al. Prophylactic Itacitinib (INCB039110) for the prevention of cytokine release syndrome induced by chimeric antigen receptor T-Cells (CAR-T-cells) therapy. Blood. 2019;134 (Suppl 1):1934. doi: 10.1182/blood-2019-128288.
50. Hotez P, Bottazzi ME, Corry D. The potential role of Th27 immune responses in coronavirus immunopathology and vaccine-induced immune enhancement. Preprints. 2020;2020040159.
51. Zhang Y, Li J, Zhan Y, et al. Analysis of serum cytokines in patients with severe acute respiratory syndrome. Infect Immun. 2004;72(8):4410-4415. doi: 10.1128/IAI.72.8.4410-4415.2004.
52. Cheung PF, Wong CK, Lam CW. Molecular mechanisms of cytokine and chemokine release from eosinophils activated by IL-17A, IL-17F, and IL-23: implication for Th27 lymphocytesmediated allergic inflammation. J Immunol. 2008;180:5625-5635.
53. Wu D, Yang XO. Th27 responses in cytokine storm of COVID-19: An emerging target of JAK2 inhibitor Fedratinib. J Microbiol Immunol Infect. 2020;53(3):368-370. doi: 10.1016/j.jmii.2020.03.005.
54. Murdock BJ, Falkowski NR, Shreiner AB, et al. Interleukin-17 drives pulmonary eosinophilia following repeated exposure to Aspergillus fumigatus conidia. Infect Immun. 2012;80(4): 1424-1436. doi: 10.1128/IAI.05529-11.
2012;80(4): 1424-1436. doi: 10.1128/IAI.05529-11.
55. Guo T, Fan Y, Chen M, et al. Cardiovascular implications of fatal outcomes of patients with coronavirus disease 2019 (COVID-19). JAMA Cardiol. 2020;e201017. doi: 10.1001/jamacardio.2020.1017.
56. Myers JM, Cooper LT, Kem DC, et al. Cunningham MW. Cardiac myosin-Th27 responses promote heart failure in human myocarditis. JCI Insight. 2016;1(9):e85851. doi: 10.1172/jci.insight.85851.
57. Zumla A, Hui DS, Azhar EI, et al. Reducing mortality from 2019-nCoV: host-directed therapies should be an option. Lancet. 2020;395(10224):e35-e36. doi: 10.1016/S0140-6736(20)30305-6.
58. Augustin M, von Kiedrowsky R, Korber A, et al. Recommendations for systemic therapy in persons with psoriasis during the pandemic phase of SARS-COV-2 (corona virus). PsoNet; 2020.
59. Stefferl A, Hopkins SJ, Rothwell NJ, Luheshi GN. The role of TNF-alpha in fever: opposing actions of human and murine TNF-alpha and interactions with IL-beta in the rat. Br J Pharmacol. 1996;118(8): 1919-1924. doi: 10.1111/j.1476-5381.1996.tb15625.x.
Br J Pharmacol. 1996;118(8): 1919-1924. doi: 10.1111/j.1476-5381.1996.tb15625.x.
60. Serrato VA, Azevedo VF, Sabatoski V, et al. Influenza h2N1 infection in a patient with psoriatic arthritis in treatment with Adalimumab: a case report. Clin Rheumatol. 2013;32(S1):21-23.
61. Zingone F, Savarino EV. Viral screening before initiation of biologics in patients with inflammatory bowel disease during the COVID-19 outbreak. Lancet Gastroenterol Hepatol. 2020;5(6):525. doi: 10.1016/S2468-1253(20)30085-6.
62. Reich K, Ortonne JP, Gottlieb AB, et al. Successful treatment of moderate to severe plaque psoriasis with the PEGylated Fab' certolizumab pegol: results of a phase II randomized, placebo-controlled trial with a re-treatment extension. Br J Dermatol. 2012;167(1):180-190.
63. Ortonne JP, Taieb A, Ormerod AD, et al. Patients with moderate-to-severe psoriasis recapture clinical response during re-treatment with etanercept. Br J Dermatol. 2009;161(5):1190-1195.
64. Blauvelt A, Papp KA, Sofen H, et al. Continuous dosing versus interrupted therapy with ixekizumab: an integrated analysis of two phase 3 trials in psoriasis. J Eur Acad Dermatol Venereol. 2017;31(6):1004-1013. doi: 10.1111/jdv.14163.
Blauvelt A, Papp KA, Sofen H, et al. Continuous dosing versus interrupted therapy with ixekizumab: an integrated analysis of two phase 3 trials in psoriasis. J Eur Acad Dermatol Venereol. 2017;31(6):1004-1013. doi: 10.1111/jdv.14163.
65. American Academy of Dermatology. Guidance on the use of biologic agents during COVID-19 outbreak. [updated 2020 March 18] Available from: https://assets.ctfassets.net/1ny4yoiyrqia/PicgNuD0IpYd9MSOwab47/023ce3cf6eb82cb304b4ad4a8ef50d56/Biologics_and_COVID-19.pdf.
66. National Multiple Sclerosis Society website. Disease modifying treatment guidelines for coronavirus (COVID-19). [accessed 2020 April 11] Available from: nationalmssociety.org/What-you-need-to-know-about-Coronavirus-(COVID-19)/DMT-Guidelines-for-Coronavirus-(COVID-19)-and.
67. ECCO Crisis Task Force. 1st Interview COVID-19 ECCO Taskforce. [accessed: 2020 April 11] Available from: https://www.ecco-ibd.eu/images/6_Publication/6_8_Surveys/1st_interview_COVID-19%20ECCOTaskforce_published. pdf.
pdf.
Наука
Российские ученые разработали препарат, который обезвреживает дельта и гамма-штаммы коронавируса. Отмечается, что лекарство создано на основе моноклональных тел, которые вырабатывают имунные клетки, происходящие от плазматической клетки-предшественницы.
В России разработали препарат против коронавирусной инфекции, который обезвреживает вирус. Разработчиками лекарства на основе моноклональных антител являются специалисты Института молекулярной биологии имени Энгельгардта (ИМБ) РАН, рассказал директор института академик Александр Макаров на совещании у Владимира Путина по развитию генетических технологий.
По его словам, это лекарство было разработано на основе первых тест-систем для анализа антител к коронавирусу, которая использовалась в поиске доноров для переливания крови тяжелобольным пациентам.
Антикоронавирусное средство нейтрализует как дельта, так и гамма-варианты вируса. Макаров заметил, что оно создавалось учеными ИМБ вместе с медиками ФМБА и специалистами Сибирского отделения РАН.
Глава института добавил, что специалисты зафиксировали высокую эффективность препарата во время лабораторных испытаний, в том числе и на животных.
«Подобрана доза антител, снижающая вирусную нагрузку в сто тысяч раз, что не уступает результатам применения известного американского препарата «Регенерон», — отметил Макаров.
Как пишет РИА «Новости», моноклональные антитела, на которых основан препарат, вырабатывают иммунные клетки, которые происходят от одной плазматической клетки-предшественницы. Их можно получить практически для любого природного антигена и использовать в дальнейшем для его обнаружения или очистки, отмечает агентство.
В России есть еще один препарат от коронавируса — «Арепливир». 12 ноября российские специалисты зарегистрировали инъекционную форму лекарства. Как отметили в пресс-службе компании-производителя «Промомед» во время разговора с РИА «Новости», новый формат лучше проникает в клетки, чем аналогичный препарат в таблетках. Инъекционную форму также характеризует «более интенсивное проникновение и распределение в клетках, более длительное удержание терапевтической концентрации в тканях, а также улучшенный профиль безопасности».
Как отметили в пресс-службе компании-производителя «Промомед» во время разговора с РИА «Новости», новый формат лучше проникает в клетки, чем аналогичный препарат в таблетках. Инъекционную форму также характеризует «более интенсивное проникновение и распределение в клетках, более длительное удержание терапевтической концентрации в тканях, а также улучшенный профиль безопасности».
Препарат поступит в продажу уже в декабре этого года. Разработчики пообещали сначала им обеспечить россиян, а потом запустить производство на экспорт.
По словам председателя совета директоров «Промомеда» Петра Белого, этот препарат будет «более доступный чем импортные аналоги», которых не так много. Отмечается, что несколько фармкомпаний работают над инъекционной формулой препарата. «Это трудно, потому что молекула, в принципе, нерастворима. Она относится к классу нерастворимых порошков», — сказал Белый агентству.
«Благодаря тому, что мы сразу поставили такую задачу перед учеными, мы смогли очень быстро получить такой научно-практический результат», — добавил он о новинке российской фармацевтики.
Планируется также создать ингаляционную форму «Арепливира», так как особенность коронавирусной инфекции в том, что вирус поселяется «именно в легких».
«И в этом смысле местная доставка лекарственных объектов, не только противовирусных, но и коктейля препаратов, видится очень перспективным направлением для лечения коронавируса и для профилактики тяжелых легочных последствий», — отметили в компании-производителе.
Кембриджские ученые использовали синтетическую биологию для создания искусственных ферментов, запрограммированных на нацеливание на генетический код SARS-CoV-2 и уничтожение вируса. Этот подход можно использовать для разработки противовирусных препаратов нового поколения.
Ферменты — это встречающиеся в природе биологические катализаторы, которые обеспечивают химические преобразования, необходимые для функционирования нашего организма, — от преобразования генетического кода в белки до переваривания пищи. Хотя большинство ферментов являются белками, некоторые из этих важнейших реакций катализируются РНК, химическим родственником ДНК, которая может складываться в ферменты, известные как рибозимы. Некоторые классы рибозимов способны нацеливаться на определенные последовательности в других молекулах РНК и точно их разрезать.
В 2014 году доктор Алекс Тейлор и его коллеги обнаружили, что искусственный генетический материал, известный как XNA, — другими словами, синтетические химические альтернативы РНК и ДНК, не встречающиеся в природе, — можно использовать для создания первых в мире полностью искусственных ферментов, которые Тейлор назвал XNAzymes.
Вначале XNAzymes были неэффективны, для их работы требовались нереальные лабораторные условия. Однако ранее в этом году его лаборатория сообщила о новом поколении XNAzymes, значительно более стабильного и эффективного в условиях внутри клеток. Эти искусственные ферменты могут разрезать длинные сложные молекулы РНК и настолько точны, что если целевая последовательность отличается всего на один нуклеотид (основная структурная единица РНК), они распознают, что не разрезают ее. Это означает, что их можно запрограммировать на атаку мутировавших РНК, вызывающих рак или другие заболевания, оставляя нормальные молекулы РНК в покое.
Однако ранее в этом году его лаборатория сообщила о новом поколении XNAzymes, значительно более стабильного и эффективного в условиях внутри клеток. Эти искусственные ферменты могут разрезать длинные сложные молекулы РНК и настолько точны, что если целевая последовательность отличается всего на один нуклеотид (основная структурная единица РНК), они распознают, что не разрезают ее. Это означает, что их можно запрограммировать на атаку мутировавших РНК, вызывающих рак или другие заболевания, оставляя нормальные молекулы РНК в покое.
Теперь, в исследовании, опубликованном сегодня в журнале Nature Communications , Тейлор и его команда из Кембриджского института терапевтической иммунологии и инфекционных заболеваний (CITIID) Кембриджского университета сообщают, как они использовали эту технологию для успешного «убийства» живых атипичных пневмоний. -Вирус КоВ-2.
Тейлор, научный сотрудник сэра Генри Дейла и аффилированный исследователь в колледже Святого Иоанна в Кембридже, сказал: «Проще говоря, XNAzymes — это молекулярные ножницы, которые распознают определенную последовательность в РНК, а затем разрезают ее. Как только ученые опубликовали РНК последовательность SARS-CoV-2, мы начали сканирование в поисках последовательностей для атаки наших XNAzymes».
Как только ученые опубликовали РНК последовательность SARS-CoV-2, мы начали сканирование в поисках последовательностей для атаки наших XNAzymes».
Хотя эти искусственные ферменты можно запрограммировать на распознавание определенных последовательностей РНК, каталитическое ядро XNAzyme — механизм, управляющий «ножницами», — не меняется. Это означает, что создание новых XNAzymes может быть выполнено за гораздо меньшее время, чем обычно требуется для разработки противовирусных препаратов.
Как объяснил Тейлор: «Это похоже на ножницы, общая конструкция которых остается неизменной, но вы можете менять лезвия или ручки в зависимости от материала, который хотите разрезать. работая в лаборатории в начале пандемии, я смог сгенерировать и проверить несколько таких XNAzymes за считанные дни».
Затем Тейлор объединился с доктором Николасом Мэтисоном, чтобы показать, что его XNAzymes были активны против живого вируса SARS-CoV-2, воспользовавшись преимуществами современной лаборатории CITIID уровня сдерживания 3 — крупнейшего академического учреждения для изучения высоких биологических агентов, таких как SARS-CoV-2, в стране.
«Очень обнадеживает то, что впервые — и это было большой целью в этой области — мы действительно заставили их работать как ферменты внутри клеток и ингибировать репликацию живого вируса», — сказал доктор Пеуэн Перейра Гербер, который выполнил эксперименты над SARS-CoV-2 в лаборатории Мэтисона.
«То, что мы продемонстрировали, является доказательством принципа, и это еще рано, — добавил Мэтисон, — Однако стоит помнить, что удивительно успешные вакцины Pfizer и Moderna COVID-19 сами основаны на синтетических молекулах РНК, это действительно захватывающая и быстро развивающаяся область с огромным потенциалом».
Тейлор проверил целевые вирусные последовательности по базам данных человеческих РНК, чтобы убедиться, что они не присутствуют в нашей собственной РНК. Поскольку XNAzymes являются высокоспецифичными, теоретически это должно предотвратить некоторые из «нецелевых» побочных эффектов, которые могут вызывать аналогичные, менее точные молекулярные терапевтические средства, такие как токсичность для печени.
SARS-CoV-2 обладает способностью развиваться и изменять свой генетический код, что приводит к появлению новых вариантов, против которых вакцины менее эффективны. Чтобы обойти эту проблему, Тейлор не только нацелился на области вирусной РНК, которые мутируют реже, но также разработал три XNAzyme для самосборки в «наноструктуру», которая вырезает разные части вирусного генома.
«Мы нацелены на несколько последовательностей, поэтому, чтобы вирус уклонился от терапии, он должен мутировать сразу в нескольких местах», — сказал он. «В принципе, вы можете объединить множество этих XNAzymes вместе в коктейль. Но даже если появится новый вариант, способный обойти это, поскольку у нас уже есть каталитическое ядро, мы можем быстро создавать новые ферменты, чтобы опережать их. Это."
XNAzymes потенциально можно вводить в качестве лекарств для защиты людей, подвергшихся воздействию COVID-19, для предотвращения распространения вируса или для лечения пациентов с инфекцией, помогая избавить организм от вируса. Такой подход может быть особенно важен для пациентов, которые из-за ослабленной иммунной системы пытаются избавиться от вируса самостоятельно.
Такой подход может быть особенно важен для пациентов, которые из-за ослабленной иммунной системы пытаются избавиться от вируса самостоятельно.
Следующим шагом для Тейлора и его команды является создание еще более специфичных и надежных XNAzymes — «пуленепробиваемых», как он говорит, — позволяющих им дольше оставаться в организме и действовать как еще более эффективные катализаторы в меньших дозах. .
Дополнительная информация: XNAzymes, нацеленные на геном SARS-CoV-2, ингибируют вирусную инфекцию, Nature Communications (2022). DOI: 10.1038/s41467-022-34339-w
Предоставлено Кембриджский университет
Цитата : Синтетическая биология встречается с медициной: «Программируемые молекулярные ножницы» могут помочь в борьбе с COVID-19инфекция (2022, 16 ноября) получено 6 декабря 2022 г. с https://phys.org/news/2022-11-synthetic-biology-medicine-programmable-молекулярно.html
Этот документ защищен авторским правом. Помимо любой добросовестной сделки с целью частного изучения или исследования, никакие часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в ознакомительных целях.
Помимо любой добросовестной сделки с целью частного изучения или исследования, никакие часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в ознакомительных целях.
1. Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, Zhang L, Fan G, Xu J, Gu X. Клинические особенности пациентов, инфицированных новым коронавирусом 2019 года в Ухане, Китай. Ланцет. 2020; 395: 497–506. doi: 10.1016/S0140-6736(20)30183-5. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2. Wang C, Horby PW, Hayden FG, Gao GF. Новая вспышка коронавируса, вызывающая глобальную озабоченность в области здравоохранения. Ланцет. 2020; 395: 470–473. doi: 10.1016/S0140-6736(20)30185-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Хан К., Лин К., Джин С., Ю Л. Коронавирус 2019-nCoV: краткий обзор с передовой. J заразить. 2020; 80: 373–377. doi: 10.1016/j.jinf. 2020.02.010. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2020.02.010. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Li Q, Guan X, Wu P, Wang X, Zhou L, Tong Y, Ren R, Leung KS, Lau EH, Wong JY. Динамика ранней передачи новой коронавирусной пневмонии в Ухане, Китай. N Engl J Med. 2020 г.: 10.1056/NEJMoa2001316. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Peiris J, Guan Y, Yuen K. Тяжелый острый респираторный синдром. Нат Мед. 2004; 10: S88–S97. doi: 10.1038/nm1143. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Кришнакумар Б., Рана С. COVID 19 в ИНДИИ: стратегии борьбы с комбинированной угрозой жизни и средствам к существованию. J Microbiol Immunol Infect. 2020 г.: 10.1016/j.jmii.2020.03.024. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Kan B, Wang M, Jing H, Xu H, Jiang X, Yan M, Liang W, Zheng H, Wan K, Liu Q. Molecular анализ эволюции и географическое исследование коронавирусоподобного вируса тяжелого острого респираторного синдрома у пальмовых циветт на рынке животных и на фермах.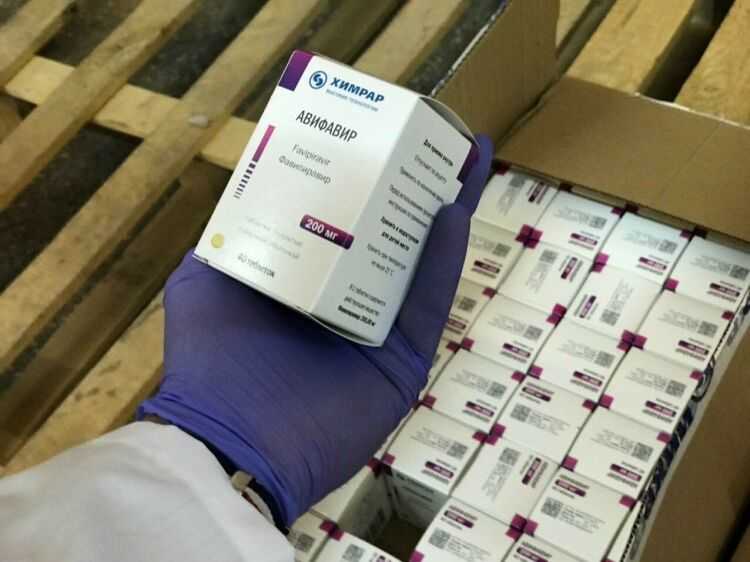 Дж Вирол. 2005;79: 11892–11900. doi: 10.1128/ОВИ.79.18.11892-11900.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж Вирол. 2005;79: 11892–11900. doi: 10.1128/ОВИ.79.18.11892-11900.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
8. Shi Z, Hu Z. Обзор исследований животных-резервуаров коронавируса SARS. Вирус рез. 2008; 133:74–87. doi: 10.1016/j.virusres.2007.03.012. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Paden C, Yusof M, Al Hammadi Z, Queen K, Tao Y, Eltahir Y, Elsayed E, Marzoug B, Bensalah O, Khalafalla A. Зоонозное происхождение и передача коронавируса ближневосточного респираторного синдрома в ОАЭ. Зоонозы Общественное здравоохранение. 2018;65:322–333. doi: 10.1111/zph.12435. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Huynh J, Li S, Yount B, Smith A, Sturges L, Olsen JC, Nagel J, Johnson JB, Agnihothram S, Gates JE. Доказательства, подтверждающие зоонозное происхождение штамма NL63 коронавируса человека. Дж Вирол. 2012;86:12816–12825. doi: 10.1128/ОВИ.00906-12. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Chan JF-W, Kok K-H, Zhu Z, Chu H, To KK-W, Yuan S, Yuen KY. Геномная характеристика нового патогенного для человека коронавируса 2019 года, выделенного от пациента с атипичной пневмонией после посещения Ухани. Новые микробы заражают. 2020;9: 221–236. doi: 10.1080/22221751.2020.1719902. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Chan JF-W, Kok K-H, Zhu Z, Chu H, To KK-W, Yuan S, Yuen KY. Геномная характеристика нового патогенного для человека коронавируса 2019 года, выделенного от пациента с атипичной пневмонией после посещения Ухани. Новые микробы заражают. 2020;9: 221–236. doi: 10.1080/22221751.2020.1719902. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Zhang C, Zheng W, Huang X, Bell EW, Zhou X, Zhang Y (2020) Повторный анализ структуры и последовательности белка 2019-nCoV геном не указывает на змей как на его промежуточных хозяев или на уникальное сходство между вставками шиповидных белков и ВИЧ-1. Препринт arXiv. 10.1021/acs.jproteome.0c00129 [бесплатная статья PMC] [PubMed]
13. Hui DS, Azhar E, Madani TA, Ntoumi F, Kock R, Dar O, Ippolito G, Mchugh TD, Memish ZA, Drosten C. продолжение 2019Эпидемическая угроза новых коронавирусов -nCoV глобальному здравоохранению — последняя вспышка нового коронавируса 2019 года в Ухане, Китай. Int J Infect Dis. 2020; 91: 264–266. doi: 10. 1016/j.ijid.2020.01.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1016/j.ijid.2020.01.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Hemida MG, Alnaeem A. Some One Health, основанные на стратегиях борьбы с коронавирусом ближневосточного респираторного синдрома. Одно здоровье. 2019 г.: 10.1016/j.onehlt.2019.100102. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Chan JF-W, To KK-W, Tse H, Jin D-Y, Yuen KY. Межвидовая передача и появление новых вирусов: уроки летучих мышей и птиц. Тенденции микробиол. 2013; 21: 544–555. doi: 10.1016/j.tim.2013.05.005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Эльфикий А.А., Махди С.М., Эльшемей В.М. Количественная взаимосвязь структура-активность и молекулярный докинг выявили активность препаратов против вируса гепатита С в отношении вирусов короны человека. J Med Virol. 2017;89:1040–1047. doi: 10.1002/jmv.24736. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Ибрагим И.М., Абдельмалек Д.Х., Эльфикий А.А. GRP78: реакция клетки на стресс. Жизнь наук. 2019 г.: 10.1016/j.lfs.2019.04.022. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Жизнь наук. 2019 г.: 10.1016/j.lfs.2019.04.022. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Li X, Zai J, Zhao Q, Nie Q, Li Y, Foley BT, Chaillon A. Эволюционная история, потенциальное промежуточное животное-хозяин и межвидовой анализ SARS-CoV-2. J Med Virol. 2020 г.: 10.1002/jmv.25731. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Paules CI, Marston HD, Fauci AS. Коронавирусные инфекции — больше, чем просто простуда. ДЖАМА. 2020; 323: 707–708. doi: 10.1001/jama.2020.0757. [PubMed] [CrossRef] [Google Scholar]
20. Wrapp D, Wang N, Corbett KS, Goldsmith JA, Hsieh C-L, Abiona O, Graham BS, McLellan JS. Крио-ЭМ структура 2019Всплеск -nCoV в конформации префузии. Наука. 2020;367:1260–1263. doi: 10.1126/science.abb2507. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
21. Виллар Дж., Чжан Х., Слуцкий А.С. Восстановление и регенерация легких при ОРДС: роль передачи сигналов PECAM1 и Wnt. Грудь. 2019; 155: 587–594. doi: 10.1016/j.chest.2018.10.022. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1016/j.chest.2018.10.022. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Channappanavar R, Perlman S (2017) Патогенные коронавирусные инфекции человека: причины и последствия цитокинового шторма и иммунопатологии. В: Semin Immunopathol, т. 5. Springer, стр. 529.–539. 10.1007/s00281-017-0629-x [бесплатная статья PMC] [PubMed]
23. Wang H, Ma S. Цитокиновый шторм и факторы, определяющие последовательность и тяжесть органной дисфункции при синдроме полиорганной дисфункции. Am J Emerg Med. 2008; 26: 711–715. doi: 10.1016/j.ajem.2007.10.031. [PubMed] [CrossRef] [Google Scholar]
24. Chen N, Zhou M, Dong X, Qu J, Gong F, Han Y, Qiu Y, Wang J, Liu Y, Wei Y. Эпидемиологические и клинические характеристики 99 случаи новой коронавирусной пневмонии 2019 года в Ухане, Китай: описательное исследование. Ланцет. 2020;395: 507–513. doi: 10.1016/S0140-6736(20)30211-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Diao B, Wang C, Tan Y, Chen X, Liu Y, Ning L, Chen L, Li M, Liu Y, Wang G. Сокращение и функциональное истощение Т-клеток у пациентов с коронавирусной болезнью 2019 (COVID-19) Front Immunol. 2020 г.: 10.3389/fimmu.2020.00827. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Сокращение и функциональное истощение Т-клеток у пациентов с коронавирусной болезнью 2019 (COVID-19) Front Immunol. 2020 г.: 10.3389/fimmu.2020.00827. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Kuba K, Imai Y, Rao S, Gao H, Guo F, Guo B, Huan Y, Yang P, Zhang Y, Deng W. A решающую роль ангиотензинпревращающего фермента 2 (ACE2) в поражении легких, вызванном коронавирусом SARS. Нат Мед. 2005; 11: 875–879.. doi: 10.1038/nm1267. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Радж В.С., Моу Х., Смитс С.Л., Деккерс Д.Х., Мюллер М.А., Дейкман Р., Мут Д., Деммерс Дж.А., Заки А., Фушье Р.А. Дипептидилпептидаза 4 является функциональным рецептором нового человеческого коронавируса-EMC. Природа. 2013; 495: 251–254. doi: 10.1038/nature12005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Lu C-w, Liu X-f, Jia Z-f. Нельзя игнорировать передачу 2019-nCoV через поверхность глаза. Ланцет. 2020;395:e39. doi: 10.1016/S0140-6736(20)30313-5. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
[PMC free article] [PubMed] [CrossRef] [Google Scholar]
29. Xia J, Tong J, Liu M, Shen Y, Guo D. Оценка коронавируса в слезах и секретах конъюнктивы пациентов с SARS-CoV-2 инфекционное заболевание. J Med Virol. 2020 г.: 10.1002/jmv.25725. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
30. Holshue ML, DeBolt C, Lindquist S, Lofy KH, Wiesman J, Bruce H, Spitters C, Ericson K, Wilkerson S, Tural A. First случай нового коронавируса 2019 года в Соединенных Штатах. N Engl J Med. 2020 г.: 10.1056/NEJMoa2001191. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Zhang H, Kang Z, Gong H, Xu D, Wang J, Li Z, Cui X, Xiao J, Meng T, Zhou W , Пищеварительная система является потенциальным путем заражения 2019-nCov: биоинформатический анализ, основанный на транскриптомах отдельных клеток. БиоРксив. 2020 г.: 10.1101/2020.01.30.927806. [CrossRef] [Google Scholar]
32. Wang D, Hu B, Hu C, Zhu F, Liu X, Zhang J, Wang B, Xiang H, Cheng Z, Xiong Y. Клинические характеристики 138 госпитализированных пациентов с 2019 г.Новая коронавирусная пневмония в Ухане, Китай. ДЖАМА. Doi 2020: 10.1001/jama.2020.1585. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Клинические характеристики 138 госпитализированных пациентов с 2019 г.Новая коронавирусная пневмония в Ухане, Китай. ДЖАМА. Doi 2020: 10.1001/jama.2020.1585. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Корман В.М., Ландт О., Кайзер М., Моленкамп Р., Мейер А., Чу Д.К., Блейкер Т., Брюнинк С., Шнайдер Дж., Шмидт М.Л. Обнаружение нового коронавируса 2019 года (2019-nCoV) методом ОТ-ПЦР в реальном времени. Евронаблюдение. 2020 г.: 10.2807/1560-7917.ES.2020.25.3.2000045. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. To KK-W, Tsang OT-Y, Yip CC-Y, Chan K-H, Wu TC, Chan JM-C, Leung WS, Chik TS -H, Чой CY-C, Кандамби DH. Последовательное обнаружение 2019 годановый коронавирус в слюне. Клин Инфекция Дис. 2020 г.: 10.1093/cid/ciaa149. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
35. Chang Z, Babiuk LA, Hu J. Терапевтический и профилактический потенциал малых интерферирующих РНК при тяжелом остром респираторном синдроме. Биопрепараты. 2007; 21:9–15. doi: 10.2165/00063030-200721010-00002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Биопрепараты. 2007; 21:9–15. doi: 10.2165/00063030-200721010-00002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
36. Zorzitto J, Galligan CL, Ueng JJ, Fish EN. Характеристика противовирусных эффектов интерферона-α в отношении SARS-подобной короновирусной инфекции in vitro. Сотовый рез. 2006; 16: 220–229. doi: 10.1038/sj.cr.7310030. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Haagmans BL, Kuiken T, Martina BE, Fouchier RA, Rimmelzwaan GF, Van Amerongen G, van Riel D, De Jong T, Itamura S, Chan К-Х. Пегилированный интерферон-α защищает пневмоциты 1 типа от коронавирусной инфекции SARS у макак. Нат Мед. 2004; 10: 290–293. doi: 10.1038/nm1001. [PMC бесплатная статья] [PubMed] [CrossRef] [Google Scholar]
38. Loutfy MR, Blatt LM, Siminovitch KA, Ward S, Wolff B, Lho H, Pham DH, Deif H, LaMere EA, Chang M. Интерферон альфакон-1 плюс кортикостероиды при тяжелом остром респираторном синдроме: предварительное исследование. ДЖАМА. 2003;290:3222–3228. doi: 10.1001/jama.290.24.3222. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1001/jama.290.24.3222. [PubMed] [CrossRef] [Google Scholar]
39. Pulido F, Arribas JR, Delgado R, Cabrero E, Gonzalez-García J, Pérez-Elias MJ, Arranz A, Portilla J, Pasquau J, Iribarren JA. Монотерапия лопинавиром-ритонавиром по сравнению с лопинавиром-ритонавиром и двумя нуклеозидами для поддерживающей терапии ВИЧ. СПИД. 2008;22:F1–F9. doi: 10.1097/QAD.0b013e3282f4243b. [PubMed] [CrossRef] [Google Scholar]
40. Lin S, Shen R, Guo X. Оценка молекулярного моделирования связывающих способностей ритонавира и лопинавира с протеазами коронавируса уханьской пневмонии. БиоРксив. 2020 г.: 10.1101/2020.01.31.929695. [CrossRef] [Google Scholar]
41. Саварино А., Ди Трани Л., Донателли И., Кауда Р., Кассоне А. Новое понимание противовирусных эффектов хлорохина. Ланцет Infect Dis. 2006; 6: 67–69. doi: 10.1016/S1473-3099(06)70361-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Yan Y, Zou Z, Sun Y, Li X, Xu K-F, Wei Y, Jin N, Jiang C. Противомалярийный препарат хлорохин очень эффективен при лечении инфекции, вызванной вирусом птичьего гриппа A H5N1, на животной модели. Сотовый рез. 2013; 23:300–302. doi: 10.1038/cr.2012.165. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Сотовый рез. 2013; 23:300–302. doi: 10.1038/cr.2012.165. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Zhang J, Zhou L, Yang Y, Peng W, Wang W, Chen X. Терапевтические и сортировочные стратегии для новой коронавирусной болезни 2019 года в лихорадочных клиниках. Ланцет Респир Мед. 2020;8:e11–e12. doi: 10.1016/S2213-2600(20)30071-0. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
44. Biot C, Daher W, Chavain N, Fandeur T, Khalife J, Dive D, De Clercq E. Дизайн и синтез производных гидроксиферрокина с противомалярийными и противовирусная активность. J Med Chem. 2006; 49: 2845–2849. doi: 10.1021/jm0601856. [PubMed] [CrossRef] [Академия Google]
45. Yao X, Ye F, Zhang M, Cui C, Huang B, Niu P, Liu X, Zhao L, Dong E, Song C. Противовирусная активность in vitro и прогноз оптимизированной схемы дозирования гидроксихлорохина для лечения тяжелый острый респираторный синдром коронавирус 2 (SARS-CoV-2) Clin Infect Dis. 2020 г.: 10.1093/cid/ciaa237. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Blaising J, Polyak SJ, Pécheur E-I. Арбидол как противовирусный препарат широкого спектра действия: обновление. Противовирусный рез. 2014; 107: 84–94. doi: 10.1016/j.antiviral.2014.04.006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. Cao Y-c, Deng Q-x, Dai S-x. Ремдесивир для лечения тяжелого острого респираторного синдрома, вызванного коронавирусом 2, вызывающего COVID-19: оценка доказательств. Travel Med Infect Dis. 2020 г.: 10.1016/j.tmaid.2020.101647. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
48. Duan Y, Zhu HL, Zhou C. Продвижение многообещающих целей и агентов против 2019-nCoV в Китае. Наркотиков Дисков сегодня. 2020 г.: 10.1016/j.drudis.2020.02.011. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
49. Lythgoe M, Middleton P. Текущие клинические испытания для лечения пандемии COVID-19. Trends Pharmacol Sci. Doi 2020: 10.1016/j.tips. 2020.03.006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2020.03.006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Араби Ю.М., Мандура Ю., Аль-Хамид Ф., Синди А.А., Альмехлафи Г.А., Хусейн М.А., Хосе Дж., Пинто Р., Аль-Омари А., Хараба А. Кортикостероидная терапия тяжелобольных с ближневосточным респираторным синдромом. Am J Respir Crit Care Med. 2018; 197: 757–767. doi: 10.1164/rccm.201706-1172OC. [PubMed] [CrossRef] [Академия Google]
51. Хуанг Л., Лю Ю., Луо Р., Цзэн Л., Телегина И., Власов В.В., Чжан Л. Арбидол для профилактики и лечения гриппа у взрослых и детей. Cochrane Database Syst Rev. 2017 doi: 10.3390/molecules25071577. [CrossRef] [Google Scholar]
52. Chen F, Chan K, Jiang Y, Kao R, Lu H, Fan K, Cheng V, Tsui W, Hung I, Lee T. In vitro чувствительность 10 клинических изолятов SARS коронавируса на отдельные противовирусные соединения. Джей Клин Вирол. 2004; 31: 69–75. doi: 10.1016/j.jcv.2004.03.003. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Hammer Q, Rückert T, Romagnani C. Специфичность естественных клеток-киллеров при вирусных инфекциях. Нат Иммунол. 2018;19:800–808. doi: 10.1038/s41590-018-0163-6. [PubMed] [CrossRef] [Google Scholar]
Специфичность естественных клеток-киллеров при вирусных инфекциях. Нат Иммунол. 2018;19:800–808. doi: 10.1038/s41590-018-0163-6. [PubMed] [CrossRef] [Google Scholar]
54. Arase H, Mocarski ES, Campbell AE, Hill AB, Lanier LL. Прямое распознавание цитомегаловируса путем активации и ингибирования рецепторов NK-клеток. Наука. 2002; 296:1323–1326. doi: 10.1126/science.1070884. [PubMed] [CrossRef] [Google Scholar]
55. Spanholtz J, Tordoir M, Eissens D, Preijers F, van der Meer A, Joosten I, Schaap N, de Witte TM, Dolstra H. Высокое логарифмическое расширение функциональные человеческие естественные клетки-киллеры из CD34-позитивных клеток пуповинной крови для адоптивной иммунотерапии рака. ПЛОС ОДИН. 2010 год: 10.1371/journal.pone.0009221. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
56. Matthay MA, Goolaerts A, Howard JP, Lee JW. Мезенхимальные стволовые клетки при остром повреждении легких: доклинические данные. Крит Уход Мед. 2010;38:S569. doi: 10. 1097/CCM.0b013e3181f1ff1d. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
1097/CCM.0b013e3181f1ff1d. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
57. Moodley Y, Atienza D, Manuelpillai U, Samuel CS, Tchongue J, Ilancheran S, Boyd R, Trounson A. Мезенхимальные стволовые клетки пуповины человека уменьшают фиброз блеомицин-индуцированного повреждения легких. Ам Джей Патол. 2009 г.;175:303–313. doi: 10.2353/ajpath.2009.080629. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Van Griensven J, Edwards T, de Lamballerie X, Semple MG, Gallian P, Baize S, Horby PW, Raoul H, Magassouba NF, Antierens A , Оценка реконвалесцентной плазмы для болезни, вызванной вирусом Эбола, в Гвинее. N Engl J Med. 2016; 374:33–42. doi: 10.1056/NEJMoa1511812. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Cheng Y, Wong R, Soo Y, Wong W, Lee C, Ng M, Chan P, Wong K, Leung C, Cheng G. Использование терапии реконвалесцентной плазмой у пациентов с атипичной пневмонией в Гонконге. Eur J Clin Microbiol Infect Dis. 2005; 24:44–46. дои: 10.1007/s10096-004-1271-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
дои: 10.1007/s10096-004-1271-9. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
60. Traggiai E, Becker S, Subbarao K, Колесникова L, Uematsu Y, Gismondo MR, Murphy BR, Rappuoli R, Lanzavecchia A. Эффективный метод сделать человеческие моноклональные антитела из В-клеток памяти: мощная нейтрализация коронавируса SARS. Нат Мед. 2004; 10: 871–875. doi: 10.1038/nm1080. [Статья PMC free] [PubMed] [CrossRef] [Google Scholar]
61. Wong SK, Li W, Moore MJ, Choe H, Farzan M. 193-аминокислотный фрагмент S-белка коронавируса SARS эффективно связывает ангиотензин- конвертирующий фермент 2. J Biol Chem. 2004;279: 3197–3201. doi: 10.1074/jbc.C300520200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
62. Tian X, Li C, Huang A, Xia S, Lu S, Shi Z, Lu L, Jiang S, Yang Z, Wu Y. Potent связывание шиповидного белка нового коронавируса 2019 с человеческим моноклональным антителом, специфичным к коронавирусу SARS. Новые микробы заражают. 2020; 9: 382–385. doi: 10.1080/22221751.2020.1729069. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1080/22221751.2020.1729069. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. Nagle V, Gaikwad M, Pawar Y, Dasgupta S (2020) Marine Red Alga Порфиридиум зр. как источник сульфатированных полисахаридов (СП) для борьбы с COVID-19 (препринты)
64. GuhaRay A, Guoxiong M, Sarkar A, Bordoloi S, Garg A, Pattanayak S. Геотехническая и химическая характеристика обширной глинистой почвы с поправками биоуголь, полученный из инвазивных видов сорняков Prosopis juliflora . Иннов Инфраструктура Солют. 2019;4:44. doi: 10.1007/s41062-019-0231-2. [CrossRef] [Google Scholar]
65. Singh R, Adhikari R (2020) Возрастное влияние социального дистанцирования на COVID-19эпидемия в Индии. Препринт arXiv
66. Дас И., Дас С., Чакраборти И., Гангрекар М. Удаление биорефрактерных загрязнителей с использованием микробных электрохимических технологий: краткий обзор. J Indian Chem Soc. 2019; 96: 493–497. [Google Scholar]
67. фон Мобеж К. П. Геосинтетические барьеры в правилах и рекомендациях в соответствии с руководством по проектированию ISO? Иннов Инфраструктура Солют. 2018;3:75. doi: 10.1007/s41062-018-0177-9. [CrossRef] [Google Scholar]
П. Геосинтетические барьеры в правилах и рекомендациях в соответствии с руководством по проектированию ISO? Иннов Инфраструктура Солют. 2018;3:75. doi: 10.1007/s41062-018-0177-9. [CrossRef] [Google Scholar]
68. Phale PS, Sharma A, Gautam K (2019) Микробная деградация ксенобиотиков, таких как ароматические загрязнители из земной среды. В: Фармацевтические препараты и средства личной гигиены: управление отходами и технология обработки. Эльзевир, стр. 259–278. 10.1016/B978-0-12-816189-0.00011-1
69. Маллапати С. Как сточные воды могут выявить истинный масштаб вспышки коронавируса. Природа. 2020; 580: 176–177. doi: 10.1038/d41586-020-00973-x. [PubMed] [CrossRef] [Google Scholar]
70. Gundy PM, Gerba CP, Pepper IL. Выживаемость коронавирусов в воде и сточных водах. Пищевая среда Вирол. 2009 г.;1:10. doi: 10.1007/s12560-008-9001-6. [CrossRef] [Google Scholar]
71. Wang X, Li J, Guo T, Zhen B, Kong Q, Yi B, Li Z, Song N, Jin M, Xiao W. Концентрация и обнаружение коронавируса SARS в сточных водах Госпиталь Сяо Тан Шань и 309-й госпиталь Народно-освободительной армии Китая. Технологии водных наук. 2005; 52: 213–221. doi: 10.2166/wst.2005.0266. [PubMed] [CrossRef] [Google Scholar]
Технологии водных наук. 2005; 52: 213–221. doi: 10.2166/wst.2005.0266. [PubMed] [CrossRef] [Google Scholar]
72. ван Доремален Н., Бушмейкер Т., Моррис Д.Х., Холбрук М.Г., Гэмбл А., Уильямсон Б.Н., Тамин А., Харкорт Дж.Л., Торнбург, штат Нью-Джерси, Гербер С.И. Аэрозольная и поверхностная стабильность SARS-CoV-2 по сравнению с SARS-CoV-1. N Engl J Med. 2020 г.: 10.1056/NEJMc2004973. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Гонг Б., Чжан С., Юань Л., Чен К.З. Баланс: минимизация экономических потерь при контроле новой коронавирусной пневмонии. J Chin Gov. 2020 doi: 10.1080/23812346.2020.1741940. [CrossRef] [Google Scholar]
74. Гоял К., Чаухан П., Чхикара К., Гупта П., Сингх М.П. Страх перед COVID-2019: первый случай самоубийства в Индии. Азиатская психиатрия J. 2020;49:e101989–e101989. doi: 10.1016/j.ajp.2020.101989. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
75. Винер Р.М., Рассел С.Дж., Крокер Х., Пакер Дж., Уорд Дж.