2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Одно из первых мест среди множества патогенных микроорганизмов занимает стафилококк: как передается инфекция, как избежать заражения – обоснованно часто задаваемые вопросы.
При активном росте бактерий появляются ярко выраженные, весьма характерные признаки, игнорировать которые нельзя. Своевременное лечение поможет избежать развития серьезных осложнений.

СодержаниеПоказать
Стафилококк – грамположительная бактерия в виде шара, отличается малой подвижностью, образует группы, схожие с гроздью винограда. Этот патогенный микроорганизм относится к условно-патогенной микрофлоре, обитает в носу, зеве и на кожных покровах, активизируется на фоне ослабленного иммунитета и хронических заболеваний.
Какие виды бактерий наиболее опасны для человека:
Стафилококк показывает высокую сопротивляемость к антибиотикам, антисептикам, высоким и низким температурам, долго сохраняет жизнеспособность в окружающей среде. Инфекции, которые возникают при заражении этими бактериями, трудно подаются медикаментозной терапии и требуют длительного лечения.
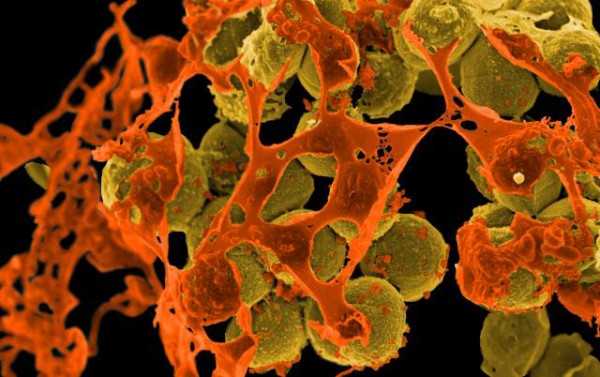
Стафилококк быстро размножается, проникает в кровь, подкожную клетчатку, поражает внутренние органы и головной мозг, у детей часто развиваются бактериальная форма пневмонии, остеомиелит, менингит, сепсис.
Заразен ли стафилококк или нет? Бактерии передаются от человека к человеку во время сексуальных и бытовых контактов, проникают в организм с водой, продуктами питания, пылью, часто проникают в организм ребенка от зараженной матери.
Выделяют аутоинфекционный путь заражения – переход стадии носительства в активную форму заболевания. Чаще это происходит у детей на фоне ОРВИ, гриппа. У взрослых патология развивается на фоне неразумного приема антибиотиков, наличия ВИЧ, злокачественных опухолей, после оперативных вмешательств.

Автор:
Трофимова Ирина
Не разобрался в материале статьи или нужна помощь? Задай вопрос сейчас и получи на него ответ.
Задать вопрос авторуЭто наиболее распространенный путь распространения инфекции между людьми. Бактерии преимущественно обитают на слизистых носа и горла, при кашле, чихании, разговоре проникают в воздух, который вдыхают другие люди. Таким способом патология часто распространяется в детских дошкольных учреждениях, поскольку дети не всегда прикрывают нос и рот, тесно контактируют друг с другом.

В эту группу относят и воздушно-пылевой путь инфицирования – стафилококк может жить вне организма человека долгое время, при вдыхании грязного воздуха бактерии проникают в организм, начинают активно размножаться.
Наиболее подвержены заражению стафилококком груднички, дошкольники, люди преклонного возраста, диабетики.
Основным источником заражения служит больной человек – инфицирование происходит при личных контактах или через общие предметы обихода.
Основные факторы передачи стафилококка:
Часто заражение стафилококком происходит в медицинских учреждениях, стоматологических клиниках, в салонах маникюра и тату – при ненадлежащей обработке инструментов бактерии могут проникнуть в кровь, быстро развиваются инфекционные, воспалительные и гнойные процессы.
Заразиться стафилококком можно и через поцелуй – во рту обитает большое количество бактерий, которые вместе со слюной проникают в организм здорового человека.
Заразиться стафилококком можно при употреблении плохо вымытых, или недостаточно термически обработанных продуктов питания, грязной воды. Чаше всего бактерии обитают на овощах и фруктах, которые контактируют с почвой, в молочной продукции, салатах с майонезом.

Заражение маленьких детей происходит через грудное молоко, если в организме матери присутствуют активные очаги стафилококковой инфекции – мастит, эндометрит, тонзиллит, гайморит. Бактерии могут присутствовать в молоке и после исчезновения клинических проявлений патологий.
Собаки и кошки часто болеют стафилококковыми инфекциями, при укусе в рану попадает зараженная слюна, что и становится причиной развития болезни у человека.
Клиническая картина стафилококковых патологий зависит от того, какой орган атаковали бактерии. Имеет значение состояние иммунной системы человека.
Наиболее частые признаки стафилококка:
Воспалительные процессы часто сопровождаются выраженным болевым синдромом различной локализации – отечные ткани начинают сдавливать нервные окончания.
При появлении признаков заболевания необходимо посетить терапевта или педиатра, пройти полное обследование. Основные методы диагностики – мазок из зева или половых органов, анализ выделений из гнойников, копрограмма, исследование кала на дисбактериоз, ИФА.
Количество бактерий в мазке из носоглотки менее 10 в 3 степени указывает на бессимптомное носительство стафилококка. При более высоких показателях необходима антибактериальная терапия.
Основа терапии стафилококка – антибактериальные препараты, их назначают после получения результатов анализов на чувствительность бактерий к активным веществам лекарственных средств.
Группы препаратов:
При лечении стафилококкового фурункулеза используют метод аутогемотрансфузии – больному вводят внутримышечно его собственную венозную кровь, после разрушения продукты распада начинают стимулировать местный иммунитет. Если лечение не приносит желаемого результата, абсцессы и фурункулы вскрывают хирургическим путем.
Метициллинрезистентный золотистый стафилококк устойчив к большинству антибактериальных препаратов, справиться с микробом может только Линезолид, Фузидин, Ванкомицин, их необходимо принимать совместно с Бисептолом.
Чтобы избежать стафилококковых инфекций, необходимо постоянно укреплять защитные силы организма – у ребенка и взрослого с сильным иммунитетом шанс заражения невелик.
Профилактика стафилококковых инфекций:
Поскольку стафилококк часто начинает активно размножаться во время беременности, необходимо заранее пройти диагностику, постоянно контролировать количество патогенных бактерий в организме.
Из видео вы узнаете о частых ошибках в лечении стафилококка по результатам анализов:
Стафилококковые инфекции опасны для жизни и здоровья человека, особенно для детей. Своевременная диагностика и правильно подобранные препараты поможет избежать развития тяжелых осложнений, а соблюдение простых мер профилактики сводит риск заражения или рецидива заболевания к минимуму.
Победить паразитов можно!
Антипаразитарный комплекс® - Надежное и безопасное избавление от паразитов за 21 день!
Сейчас действует акция на бесплатную упаковку.Читать мнение экспертов.
ДЭВИД М. БАМБЕРГЕР, М.Д., и САРА Э. БОЙД, М.Д. 2005 дек. 15; 72 (12): 2474-2481.
Из-за высокой заболеваемости, заболеваемости и устойчивости к противомикробным препаратам инфекции Staphylococcus aureus вызывают все большую обеспокоенность у семейных врачей. Штаммы S. aureus, устойчивые к ванкомицину, теперь признаны. Увеличение заболеваемости нераспознанным сообществом приобретенного метициллинрезистентного S.инфекции aureus представляют высокий риск заболеваемости и смертности. Хотя заболеваемость сложными инфекциями S. aureus растет, в качестве лечения доступны новые противомикробные препараты, в том числе даптомицин и линезолид. S. aureus является распространенным патогеном при инфекциях кожи, мягких тканей, катетеров, костей, суставов, легких и центральной нервной системы. S. aureus bacteremias особенно проблематичны из-за высокой частоты ассоциированных осложненных инфекций, включая инфекционный эндокардит.Соблюдение мер предосторожности, рекомендованных Центрами по контролю и профилактике заболеваний, особенно мытья рук, является неоптимальным.
Приблизительно 20 процентов здоровых людей являются постоянными носителями золотистого стафилококка, а 60 процентов - прерывистыми носителями. Частота колонизации повышается у пациентов, находящихся на гемодиализе, потребителей запрещенных инъекционных наркотиков, хирургических пациентов и пациентов с инсулинозависимым или плохо контролируемым диабетом1. Национальная система эпиднадзора за внутрибольничными инфекциями2 обнаружила, что 60 процентов приобретенных в стационаре S.изоляты aureus в 2003 г. были устойчивы к метициллину S. aureus (MRSA). У госпитализированных пациентов с инфекцией S. aureus риск внутрибольничной смертности в пять раз выше, чем у стационарных пациентов без этой инфекции. Уровень доказательности
Ванкомицин (ванкоцин) не следует применять при известных метициллин-восприимчивых инфекциях Staphylococcus aureus, если только нет аллергии на беталактам.
C
10, 11
Врачи должны знать о региональной распространенности внебольничных MRSA и планировать эмпирическую терапию для инфекций S. aureus соответственно.
C
8
У пациентов с бактериемией нетуннелированные центральные венозные катетеры и туннелированные катетеры с туннельной, карманной или экситозной инфекцией должны быть удалены.
C
20
Все центральные венозные катетеры должны быть удалены, если у пациента бактериемия в течение более 72 часов.
C
16, 20
Большинству взрослых пациентов с остеомиелитом требуется от четырех до шести недель парентеральной терапии или длительных курсов (от трех до шести месяцев) пероральных антибиотиков с высокой биодоступностью. Некоторые дети с острым гематогенным остеомиелитом восприимчивых организмов отвечают на более короткий курс парентеральной терапии с последующим курсом пероральной терапии.
C
22, 23
Большинство инфицированных аппаратных устройств, таких как шунты центральной нервной системы, устройства для ортопедической фиксации и протезные суставы, необходимо удалить, но имеются ограниченные доказательства того, что ранняя стабильность Инфекции протезов суставов могут отвечать на длительные курсы комбинированной терапии хинолон-рифампином (рифадином) для чувствительных организмов.
B
22, 25
Для большинства абсцессов и эмпием требуется дренаж, но имеются ограниченные данные из клинических случаев о том, что некоторые небольшие абсцессы чувствительных организмов у клинически стабильных пациентов реагируют на медикаментозную терапию без дренажа ,
C
28
Госпитализированные пациенты, инфицированные или колонизированные MRSA, должны находиться в контактных мерах предосторожности.Использование культур активного наблюдения может предотвратить распространение MRSA среди госпитализированных пациентов.
C
29–31
| Клиническая рекомендация | Оценка доказательств | Ссылки |
|---|---|---|
| Ванкомицин не должен используется для известных чувствительных к метициллину инфекций Staphylococcus aureus, если нет аллергии на беталактам. | C | 10, 11 |
| Врачи должны знать о региональной распространенности внебольничных MRSA и планировать эмпирическую терапию для инфекций S. aureus соответственно. | C | 8 |
| У пациентов с бактериемией нетуннелированные центральные венозные катетеры и туннелированные катетеры с туннельной, карманной или экситозной инфекцией должны быть удалены. | C | 20 |
| Все центральные венозные катетеры должны быть удалены, если у пациента бактериемия в течение более 72 часов. |
Золотой стафилококк может распространяться при контакте кожа-на-коже или при контакте с загрязненными поверхностями. Плохая личная гигиена и отсутствие покрытия открытых ран может привести к заражению золотым стафилококком. Тщательное мытье рук и ведение домашнего хозяйства, такие как влажное пыление, очень важны, поскольку золотой стафилококк является частью нашей окружающей среды.
Устойчивые штаммы золотистого стафилококка известны как мультирезистентные S.aureus (MRSA). Ненужное или чрезмерное использование антибиотиков стимулирует лекарственно-устойчивые штаммы. Злоупотребление дезинфицирующими средствами в целом также может привести к лекарственной устойчивости. В большинстве случаев достаточно хорошей чистки или мытья с мылом и теплой водой.
устойчивых к метициллину штаммов золотистого стафилококка возникли в 1970-х годах и поставили больниц по всему миру в постоянные инфекции у пациентов. Устойчивый к ванкомицину штамм золотистого стафилококка появился в Японии, а штаммы с частичной устойчивостью к ванкомицину были обнаружены в США, Австралии и других странах.
Стандартные правила гигиены, применяемые персоналом больницы, включают:
Эти инфекции называются «приобретенный сообществом золотой стафилококк» или «приобретенный сообществом MRSA». Они похожи, но отличаются от штаммов золотистого стафилококка, обнаруженных в больницах, и могут вызывать легкие или тяжелые инфекции.
Предотвращение распространения золотого стафилококкаНакройте все открытые раны водонепроницаемой окклюзионной повязкой до полного заживления.
Использование растворов для протирания рук на спиртовой основе в «чистых» ситуациях, когда руки заметно чисты, особенно когда вода недоступна, может быть полезна, например, во время путешествий или на пикнике.Эти решения не нужны в домашних условиях или на работе.
В некоторых ситуациях спиртовые растворы для протирания рук следует использовать , а не - например, вместо мытья после посещения туалета. Руки должны быть вымыты с мылом и теплой водой и высушены.
Стафилококковая пищевая болезнь (SFD) является одной из самых распространенных болезней пищевого происхождения в мире, возникающих в результате загрязнения пищи предварительно образованными энтеротоксинами S. aureus . Это одна из наиболее распространенных причин зарегистрированных болезней пищевого происхождения в Соединенных Штатах. Хотя было выявлено несколько стафилококковых энтеротоксинов (SE), SEA, высоко термостабильная SE, является наиболее распространенной причиной SFD во всем мире. Расследования вспышек показали, что ненадлежащая практика обращения с пищевыми продуктами в розничной торговле является причиной большинства вспышек SFD.Тем не менее, в нескольких исследованиях задокументирована распространенность S. aureus во многих пищевых продуктах, включая сырое розничное мясо, что указывает на потенциальный риск колонизации и последующей инфекции S. aureus . Наличие патогенных микроорганизмов в пищевых продуктах создает потенциальную опасность для потребителей и приводит к серьезным экономическим потерям и снижению продуктивности человека из-за болезней пищевого происхождения. Симптомы SFD включают тошноту, рвоту и спазмы в животе с диареей или без нее. Профилактические меры включают безопасную практику обработки и обработки пищевых продуктов, поддержание холодовой цепи, надлежащую очистку и дезинфекцию оборудования, предотвращение перекрестного загрязнения в доме и на кухне, а также предотвращение загрязнения от фермы до вилки.В этом документе представлен краткий обзор SFD, факторов, способствующих этому, для потребителей, текущих пробелов в исследованиях и профилактических мер.
Пищевые заболевания являются серьезной проблемой общественного здравоохранения во всем мире [1, 2]. ВОЗ определяет болезни пищевого происхождения (FBD) как «заболевания инфекционной или токсической природы, вызванные или предположительно вызванные потреблением пищи или воды» [2]. Ежегодно в Соединенных Штатах около 76 миллионов заболеваний, 325 000 госпитализаций и 5000 смертей вызваны болезнями пищевого происхождения [3].Среди этих случаев 31 известный патоген вызывает 9,4 миллиона заболеваний, 56 000 госпитализаций и 1300 смертей [4]. Используя данные за 2000–2008 годы, исследователи подсчитали, что патогенными микроорганизмами, которые были вовлечены в большинство случаев FBD, были норовирус (5,5 млн., 58%), нетифоидный Salmonella spp. (1,0 млн., 11%), Clostrodium perfringens (1,0 млн., 10%) и Campylobacter spp. (0,8 млн, 9%). Среди многих пищевых патогенов нетифоидные Salmonella spp. и Campylobacter spp.являются основными причинами FBD в Соединенных Штатах, Англии и Австралии [4].
S. aureus является значительной причиной FBD, вызывая, по оценкам, 241 000 заболеваний в год в Соединенных Штатах [4]. Тем не менее, истинная частота заболевания пищевого происхождения (SFD), вызванного Staphylococcus aureus, может быть намного выше, поскольку спорадическое заболевание пищевого происхождения, вызванное S. aureus , не регистрируется в Соединенных Штатах [5]. Некоторые другие факторы, способствующие низкой частоте возникновения SFD, включают ошибочный диагноз, неправильный сбор образцов и лабораторное обследование [6], отсутствие обращения за медицинской помощью со стороны пострадавших, затрудняющее лабораторное подтверждение [5, 7], и отсутствие рутинного наблюдения за клиническим стулом экземпляры за с.aureus или его энтеротоксины [5, 8, 9]. Отсутствие предполагаемой пищи для подтверждения лабораторных испытаний во время исследования вспышки еще более усложняет проблему [5]. Важно отметить, что ФБД, подтвержденное лабораторными исследованиями и переданное в органы здравоохранения, составляет лишь небольшую часть заболеваний [4]. FBD налагает большое экономическое бремя, составляя 50–80 млрд. Долл. США ежегодно в «расходах на здравоохранение, снижении производительности и снижении качества жизни» в Соединенных Штатах [10, 11].По оценкам, каждый случай SFD стоит 695 долларов, что составляет в Соединенных Штатах общую сумму в 167 597 860 долларов в год [10]. Институт медицины признал FBD как высокий приоритет [12]. «Вероятность того, что пищевые продукты будут вовлечены в возникновение или повторное возникновение микробных угроз для здоровья, высока, в значительной степени потому, что существует множество моментов, в которых безопасность пищевых продуктов может быть поставлена под угрозу». Хотя в последние годы FBD снизился, он по-прежнему превышает цели «Здоровые люди 2020» () [10].Наличие пищевых патогенных микроорганизмов в готовых к употреблению продуктах, мясе и мясных продуктах подвергает потребителей высокому риску и несет серьезные экономические потери для производителей из-за отзывов о причастных пищевых продуктах [13, 14].
S. aureus является комменсальным и условно патогенным микроорганизмом, который может вызывать широкий спектр инфекций, от поверхностных инфекций кожи до тяжелых и потенциально смертельных инвазивных заболеваний [15]. Эта вездесущая бактерия является важным патогеном благодаря сочетанию «токсин-опосредованной вирулентности, инвазивности и устойчивости к антибиотикам».Этот организм стал основным патогеном как для внутрибольничных, так и для внебольничных инфекций. S. aureus не образует спор, но может вызвать загрязнение пищевых продуктов во время приготовления и обработки пищи. S. aureus может расти в широком диапазоне температур (от 7 ° до 48,5 ° C; оптимально от 30 до 37 ° C), pH (от 4,2 до 9,3; оптимально от 7 до 7,5) и концентрации хлорида натрия до 15% NaCl , S. aureus - устойчивый к осушению организм, способный выживать в потенциально сухих и стрессовых условиях, таких как человеческий нос, а также на коже и неодушевленных поверхностях, таких как одежда и поверхности [16].Эти характеристики способствуют росту организма во многих пищевых продуктах [2]. S. aureus может оставаться жизнеспособным на руках и поверхностях окружающей среды в течение продолжительных периодов времени после первоначального контакта [17, 18].
SFD является одним из наиболее распространенных случаев FBD и вызывает серьезную обеспокоенность в программах общественного здравоохранения во всем мире [1, 2, 19]. Это одна из наиболее распространенных причин зарегистрированного FBD в Соединенных Штатах [1, 20–22]. Первое задокументированное событие SFD из-за потребления загрязненного сыра было исследовано Воганом и Штернбергом в Мичигане, США, в 1884 году [19].Типичная FBD, вызванная S. aureus , имеет быстрое начало после приема зараженной пищи (обычно 3–5 часов). Это связано с продукцией одного или нескольких токсинов бактериями во время роста при допустимых температурах [2]. Однако инкубационный период SFD зависит от количества потребляемого токсина [22]. Очень маленькая доза SE может вызвать SFD. Например, в одном сообщении указывалось, что концентрация SE, приблизительно 0,5 нг / мл, загрязненная шоколадным молоком, вызвала большую вспышку [22, 23].
Наступление SFD происходит внезапно. Симптомы включают гиперсаливацию, тошноту, рвоту и спазмы в животе с диареей или без нее. Если значительная жидкость теряется, физическое обследование может выявить признаки дегидратации и гипотонии [1, 6, 22, 24]. Спазмы в животе, тошнота и рвота являются наиболее распространенными [2]. Хотя SFD, как правило, самоограничивается и проходит через 24–48 часов после начала заболевания, он может быть тяжелым, особенно у младенцев, пожилых людей и пациентов с ослабленным иммунитетом [1, 6, 22]. Антибиотики не используются для терапии [7].Приблизительно 10% людей, подвергшихся SFD, будут доставлены в больницу [22, 24]. Управление СФО является поддерживающим. Уровень атаки SFD может достигать 85% [22]. S. aureus не может быть обнаружен культурой в случаях, когда пища загрязнена и токсин образуется до приготовления [22, 25]. Исследование, включающее 7126 случаев, показало, что уровень летальности SFD составляет 0,03%; все смерти были у пожилых пациентов [22]. Восстановление завершается примерно через 20 часов [22, 24].
Неоспоримые диагностические критерии SFD основаны на обнаружении стафилококковых энтеротоксинов в пище [26] или восстановлении не менее 10 5 S.aureus из остатков пищи [19]. S. aureus энтеротоксин может быть обнаружен на основе трех типов методов: биоанализы, молекулярная биология и / или иммунологические методы [19, 27]. Для оценки токсического потенциала штамма могут быть проведены полимеразная цепная реакция (ПЦР), ПЦР с обратной транскрипцией (ОТ-ПЦР) и ОТ-количественная ПЦР [19]. Ферментный иммуноанализ и ферментно-связанный флуоресцентный анализ являются наиболее часто используемыми иммунологическими методами, основанными на использовании антиэнтеротоксиновых поликлональных или моноклональных антител [19].Несколько методов молекулярного типирования широко используются для генетической характеристики S. aureus , таких как многолокусное типирование последовательности, spa , SCC mec типирование и гель-электрофорез в импульсном поле (PFGE). Эти методы предоставляют средства для отслеживания эпидемиологически связанных штаммов, ведущих к отслеживанию происхождения загрязнения [28]. Тем не менее, эти методы имеют различия в их способности различать и могут быть увеличены путем объединения методов [29].Молекулярные методы предоставляют информацию об источнике загрязнения (человеческого или животного происхождения). Типирование PFGE и spa можно использовать отдельно или совместно для сбора информации о происхождении загрязнения S. aureus [19].
Различные виды пищи служат оптимальной средой для роста S. aureus. Пищевые продукты, которые часто причастны к SFD, - это мясо и мясные продукты, птица и яичные продукты, молоко и молочные продукты, салаты, хлебобулочные изделия, особенно выпечка и пирожные с кремом, а также начинки для сэндвичей [2, 6, 30].Пища, связанная с SFD, варьируется от страны к стране, особенно из-за различий в потреблении и пищевых привычках [2]. Если пища готовится в центральном месте и широко распространена, вспышки SFD могут иметь серьезные последствия, затрагивающие тысячи людей. Например, более 13 000 случаев SFD произошло в Японии в 2000 году в результате загрязнения молока на молочно-пищевом комбинате [22, 31].
S. aureus продуцирует широкие массивы токсинов.Стафилококковые энтеротоксины (SE) представляют собой семейство из девяти основных серологических типов термостабильных энтеротоксинов (SEA, SEB, SEC, SED, SEE, SEG, SEH, SEI и SEJ), которые относятся к большому семейству пирогенных суперантигенов токсинов [1, 6]. Пирогенные токсины вызывают суперантигенную активность, такую как иммуносупрессия и неспецифическая пролиферация Т-клеток [2]. Предполагается, что суперантигенная активность SE помогает облегчить трансситоз, который позволяет токсину проникать в кровоток, что позволяет ему взаимодействовать с антигенпрезентирующими клетками и Т-клетками, что приводит к активности суперантигена [1, 6, 19].Считается, что большинство эффектов SE при SFD вызваны инициированием фокальной кишечной воспалительной реакции вследствие их суперантигенной активности или воздействием на тучные клетки кишечника, вызывающие их дегрануляцию [1, 22, 32].
SE обладают высокой стабильностью и высокой термостойкостью и устойчивы к таким условиям окружающей среды, как замерзание и сушка [2, 19]. Они также устойчивы к протеолитическим ферментам, таким как пепсин или трипсин, и низким pH, что позволяет им полностью функционировать в желудочно-кишечном тракте после приема внутрь [2, 6].Характеристика термостабильности S. aureus представляет значительную угрозу в пищевой промышленности [1]. Механизмы СЭ, вызывающих пищевое отравление, точно не известны. Однако считается, что СЭ непосредственно влияют на эпителий кишечника и блуждающий нерв, вызывая стимуляцию рвотного центра [2, 19]. Все стафилококковые энтеротоксины вызывают рвоту [22, 32]. По оценкам, 0,1 μ г SE могут вызывать стафилококковое пищевое отравление у людей [2].
SE, продуцируемых некоторыми штаммами S.aureus являются возбудителями SFD, а SEA является наиболее распространенным токсином, вовлеченным в такие события. SEA обладает высокой устойчивостью к протеолитическим ферментам. СЭО была восстановлена после 77,8% всех вспышек SFD в США, за которыми следовали SED (37,5%) и SEB (10%) [1, 6]. SEA является наиболее часто встречающимся энтеротоксином среди вспышек SFD в Японии, Франции и Великобритании [6]. Тем не менее, SEC и SEE также связаны с SFD. Вспышка желудочно-кишечного тракта через зараженный салат из капусты в Соединенных Штатах была вызвана SEC, продуцируемой устойчивым к метициллину S.aureus (MRSA) от бессимптомного обработчика пищи [33]. SEC был связан со вспышкой SFD в 1980 году в Канаде [34]. SEC также участвовал в вспышке SFD в 2001–2003 гг. На Тайване [35] и в 2009 г. в Японии [36]. S. aureus часто связан с копринным маститом [37]. У овец, коз и крупного рогатого скота SEC был преобладающим типом токсина, обнаруженным в S. aureus , выделенных из молока от мастита [38]. Другие исследования показали, что производители SEC являются наиболее распространенным производящим энтеротоксин S.aureus выделен из козьего молока [39] и козьей кожи вымени, сосков и молока [40]. Шесть вспышек SFD во Франции в 2009 году были вызваны наличием ЮВЕ в мягком сыре, изготовленном из непастеризованного молока [26]. Несмотря на редкость, ЮВЕ также участвует в вспышках SFD в США и Великобритании [6]. Были идентифицированы различные новые SE (от SEG до SE × U2). Однако только штаммы, продуцирующие SEH, были вовлечены в вспышки SFD [6].
S. aureus может выживать у нескольких видов хозяев.Молекулярная типизация, такая как многолокусная типовая последовательность (MLST), помогла получить представление о структуре популяции S. aureus . Исследования выявили более 2200 типов последовательностей (ST) S. aureus с использованием методов MLST. ST могут быть сгруппированы в клональные комплексы (CC). Несколько исследований показали, что большинство связанных с домашним скотом ST принадлежит небольшому количеству связанных с животными клонов. Например, CC97, ST151, CC130 и CC126 обычно встречаются при бычьих инфекциях.CC133 распространены среди мелких жвачных, таких как овцы или козы. ST1, ST8, CC5, ST 121 и ST398 обнаружены у человека-хозяина [41]. ST5 преобладает среди изолятов птицы [42]. CC133 и ST522 чаще всего связаны с маститом у овец и коз. Одно датское исследование показало, что ST133 был преобладающей линией у овец и коз [42].
В Соединенных Штатах приблизительно 30% и 1,5% населения колонизированы чувствительными к метициллину S.aureus (MSSA) [43] и MRSA соответственно [43–45], причем наиболее важным местом для колонизации являются передние ноздри (ноздри) [46]. Хотя сама колонизация не наносит вреда хозяину, она является фактором риска развития последующих симптоматических инфекций [43, 47]. Эти колонизированные здоровые люди, отнесенные к категории постоянных носителей и прерывистых носителей, служат карьеру S. aureus и способны передавать бактерии восприимчивым лицам [46].
S. aureus является распространенным возбудителем бычьего мастита в молочных стадах.Исследование, проведенное в Миннесоте с целью оценки слышимости S. aureus из сыпучего молока в резервуарах, показало, что распространенность MSSA и MRSA по слухам составляла 84% и 4% соответственно [48]. Другие исследования показали, что распространенность S. aureus в резервуаре для насыпного молока составляла 31% в Пенсильвании и 35% в пробах коровьего молока в Луизиане [48]. Исследования в Аргентине [49], Бразилии [50], Ирландии [51] и Турции [52] подтвердили наличие генов стафилококкового энтеротоксина и продукцию SE к S.aureus бычьего происхождения. Вымя с клиническим и субклиническим стафилококковым маститом может способствовать загрязнению молока S. aureus через прямое выведение организмов из молока [38] с большими колебаниями в
.