2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
SOVREMENNAYA PEDIATRIYA.2015.4(68):103-110; doi 10.15574/SP.2015.68.103
Эпштейн—Барр вирусная инфекция у детей
Волоха А. П.
Национальная медицинская академия последипломного образования имени П.Л. Шупика, г. Киев, Украина
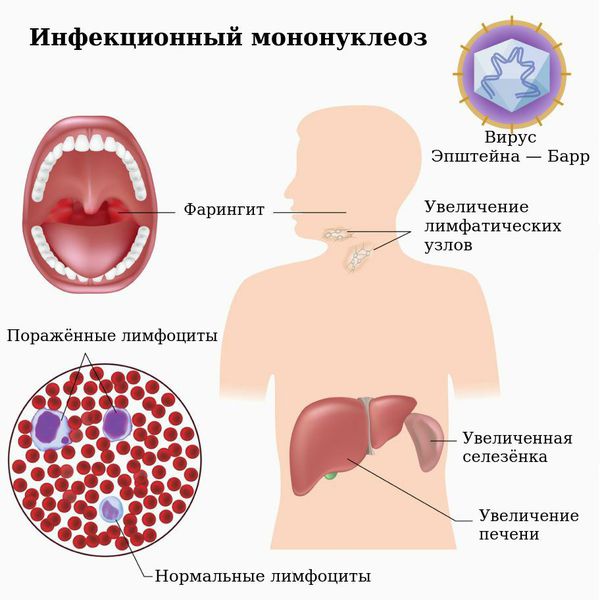
Вирус Эпштейн—Барр (EBV) — чрезвычайно распространенный в популяции вирус, возбудитель инфекционного мононуклеоза, персистирует бессимптомно на протяжении всей жизни у инфицированных лиц. В отличие от других герпесвирусов, реактивация EBV не имеет существенного значения в клинической практике, за исключением иммуноскомпрометированных пациентов (Х-сцепленный лимфопролиферативный синдром, иммуносупрессия после трансплантации), у которых развиваются лимфопролиферативные заболевания. Вирус Эпштейн—Барр ассоциируется с развитием злокачественных опухолей. Первичная EBV-инфекция обычно бессимптомная у детей раннего возраста, в старшем возрасте протекает с классическими симптомами: лихорадка, фарингит, лимфаденопатия.
Выздоровление полное через несколько недель после начала заболевания. Основой лечения EBV-индуцированного инфекционного мононуклеоза является симптоматическая терапия. Назначение противовирусных препаратов и кортикостероидов в лечении первичной EBV-инфекции остается дискутабельным и в целом не рекомендуется.
Ключевые слова: вирус Эпштейн—Барр, инфекционный мононуклеоз, дети.
Литература:
1. Candy B, Hotopf M. 2006. Steroids for symptom control in infectious mononucleosis. Cochrane Database Syst Rev. 3: CD004402. http://dx.doi.org/10.1002/14651858.cd004402.pub2
2. Carbone A, Gloghini A, Dotti G. 2008. EBV-Associated lymphoproliferative disorders: classification and treatment. The Oncologist. 13: 577—585. http://dx.doi.org/10.1634/theoncologist.2008-0036; PMid:18515742
3. Centers for Disease Control and Prevention, National Center for Infectious Diseases. Epstein—Barr virus and infectious mononucleosis. Updated May 16, 2006. http://www.cdc.gov/ncidod/diseases/ebv. htm. Accessed December 20, 2011.
htm. Accessed December 20, 2011.
4. Ebell MH. 2004. Epstein—Barr virus infectious mononucleosis. Am Fam Physician. 70(7): 1279—1287. PMid:15508538
5. Hellwig T, Jude K, Meyer B. 2013. Management options for infectious mononucleosis. US Pharmacist. 38(5): 38—41.
6. Macsween KF, Higgins CD, McAulay KA et al. 2010. Infectious mononucleosis in university students in the United Kingdom: evaluation of the clinical features and consequences of the disease. Clinical Infectious Diseases. 50: 699—706. http://dx.doi.org/10.1086/650456; PMid:20121570
7. Johanssen EC, Kaye KM. 2010. Epstein—Barr virus (Infectious mononucleosis, Epstein—Barr virus_associated malignant diseases, and other diseases). Douglas and Bennett's Principles and Practice of Infectious Diseases. Mandell GL, Bennett JE, Dolin R Mandell. 7th Ed. Churchill Livingstone Elsevier: 1989—2010.
8. Junker AK. 2005. Epstein—Barr virus. Pediatrics in review. 26(3): 79—85. http://dx.doi. org/10.1542/pir.26-3-79; PMid:15743754
org/10.1542/pir.26-3-79; PMid:15743754
9. Katz BZ. 2008. Epstein—Barr virus (mononucleosis and lymphoproliferative disorders). Principles and Practice of Pediatric Infectious Diseases. Long SS, Pickering LK, Prober CG. Churchill Livingstone: 1036—1044.
10. Luzuriaga K, Sullivan JL. 2010. Infectious mononucleosis. N Engl J Med. 362;7: 1993-2000. http://dx.doi.org/10.1056/NEJMcp1001116; PMid:20505178
11. Odumade OA. 2011. Progress and problems in understanding and managing primary Epstein—Barr virus infections. Clin Microbiology review. 24(1): 193—209. http://dx.doi.org/10.1128/CMR.00044-10; PMid:21233512 PMCid:PMC3021204
12. Paschale M, Clerici P. 2012. Serological diagnosis of Epstein—Barr virus infection: Problems and solutions. World J Virol. 1(1): 31—43. http://dx.doi.org/10.5501/wjv.v1.i1.31; PMid:24175209 PMCid:PMC3782265
13. Rezaei N, Hedayat M, Aghamohammadi A, Nichols KE. 2011. Primary immunodeficiency diseases associated with increased susceptibility to viral infections and malignancies.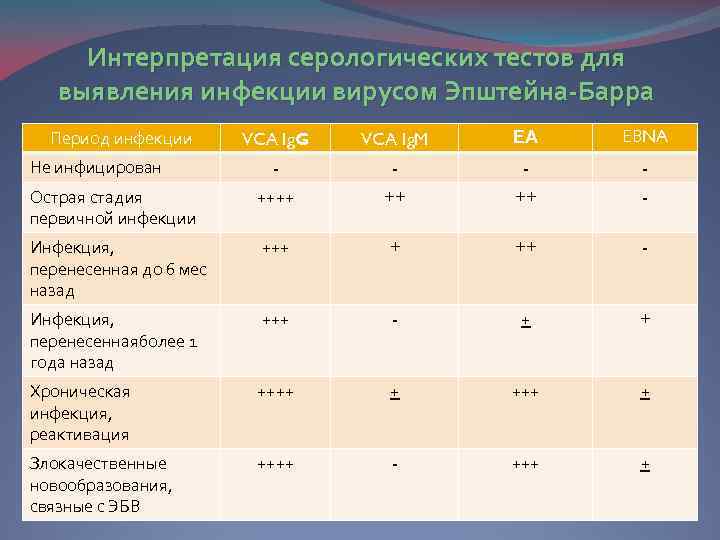 J Allergy Clin Immunol. 127: 1329—41. http://dx.doi.org/10.1016/j.jaci.2011.02.047; PMid:21514636
J Allergy Clin Immunol. 127: 1329—41. http://dx.doi.org/10.1016/j.jaci.2011.02.047; PMid:21514636
14. Kimura H, Morishima T, Kanegane H et al. 2003. Prognostic factors for chronic active Epstein—Barr Virus infection. The Journal of Infectious Diseases. 187: 527—33. http://dx.doi.org/10.1086/367988; PMid:12599068
15. Sumaya CV. 2009. Epstein—Barr virus. Textbook of Pediatric Infectious Diseases. RD Feigin, JD Cherry. 4th Ed. Philadelphia, W.B. Saunders: 1751—1762.
16. Valachis A, Kofteridis DP. 2012. Mononucleosis and Epstein—Barr virus infection: treatment and medication. Virus Adaptation and Treatment. 4: 23—28.
17. Williams H, Crawford DH. 2006. Epstein—Barr virus: the impact of scientific advances on clinical practice. Blood. 107: 862—869. http://dx.doi.org/10.1182/blood-2005-07-2702; PMid:16234359
В статье приведены современные представления об особенностях иммунопатогенеза, диагностики и терапии вирусной инфекции Эпштейна — Барр в зависимости от фазы заболевания и клинических форм.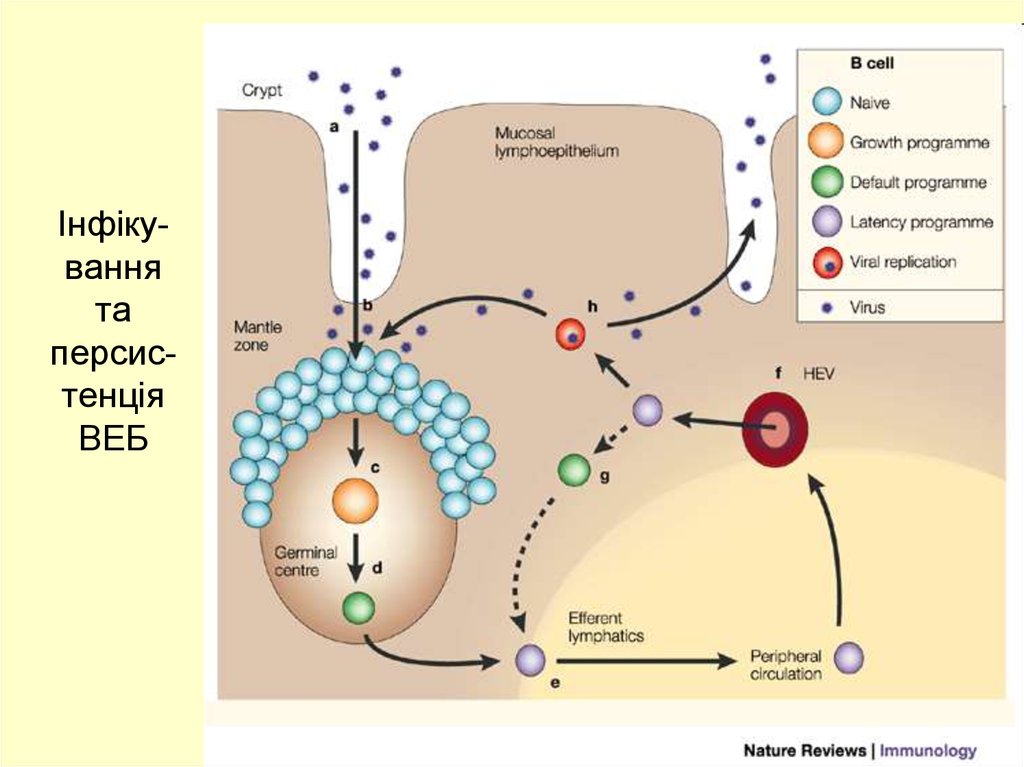 Представлены клинические примеры острой и хронической инфекции
Представлены клинические примеры острой и хронической инфекции
Одной из актуальных проблем современной медицины является высокая заболеваемость герпесвирусными инфекциями, которые достаточно широко распространены в человеческой популяции. Сложная по сравнению с другими ДНК-содержащими вирусами структура генома вирусов семейства герпеса обусловливает основные различия в их репликативном цикле. Гены, кодирующие структурные белки, составляют у герпесвирусов всего лишь 15% ДНК, большую же часть генома составляют участки, ответственные за синтез регуляторных протеинов и ферментов, и именно эта особенность позволяет им реализовывать совершенно уникальную программу, включающую возможность латентного, персистентного и реактивированного состояния в инфицированном организме [1].
Особое место среди герпесвирусов занимает Эпштейна — Барр вирус (ЭБВ), которым инфицировано 95% населения и, как и все герпесвирусы, он способен поражать практически все органы и системы организма, вызывая латентную, острую и хроническую формы инфекции, склонные к реактивации в условиях иммуносупрессии. Активная пролиферация вируса во всех органах и системах, имеющих лимфоидную ткань, приводит к структурным изменениям, оказывающим неблагоприятное воздействие на организм в целом. Доказана ключевая роль ЭБВ в развитии таких заболеваний, как острый, хронический мононуклеоз, интерстициальный пневмонит, миокардит, гепатит, опухоли лимфоидной и эпителиальной тканей, гемофагоцитарный лимфогистиоцитоз, лейкоплакия языка и посттрансплантационные лимфопролиферативные осложнения.
Активная пролиферация вируса во всех органах и системах, имеющих лимфоидную ткань, приводит к структурным изменениям, оказывающим неблагоприятное воздействие на организм в целом. Доказана ключевая роль ЭБВ в развитии таких заболеваний, как острый, хронический мононуклеоз, интерстициальный пневмонит, миокардит, гепатит, опухоли лимфоидной и эпителиальной тканей, гемофагоцитарный лимфогистиоцитоз, лейкоплакия языка и посттрансплантационные лимфопролиферативные осложнения.
Наиболее известным и изученным проявлением Эпштейна — Барр вирусной инфекции (ЭБВИ) является инфекционный мононуклеоз (ИМ). В настоящее время неясны иммунопатологические основы индивидуальных различий течения ИМ и его исходов. Клинические проявления, диагностика и лечение ИМ представлены в таблице 1.
Метаанализ 5 рандомизированных плацебо-контролируемых испытаний с участием 339 больных показал отсутствие эффекта от ацикловира у больных ИМ ЭБВ этиологии [5].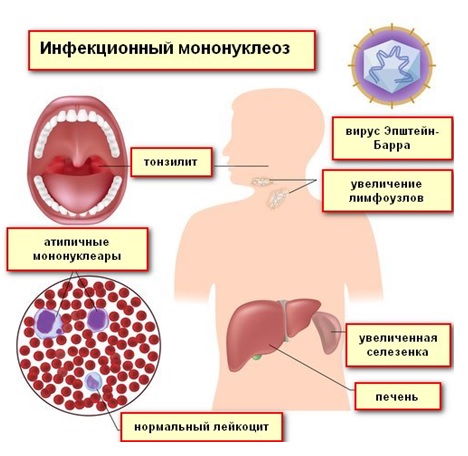
ЭБВ обладает множественными механизмами иммуносупрессии и ускользания от иммунного ответа в организме человека, что может приводить к формированию хронической ЭБВИ (ХЭБВИ) [6], в ходе которой иммунологические нарушения усугубляются, подавляется продукция интерферонов, блокируются механизмы апоптоза, что формирует вторичный иммунодефицит, способствующий развитию аутоиммунных и опухолевых процессов у генетически предрасположенных лиц.
Клинические формы ХЭБВИ представлены в таблице 2.
Накоплено немало данных об этиологической роли ЭБВ в формировании синдрома хронической усталости, развитии системных васкулитов, специфического колита, имеются данные о триггерной роли ЭБВ в развитии рассеянного склероза и системной красной волчанки [15, 16].
Описаны такие кожные проявления ХЭБВИ, как гиперчувствительность к укусам комаров и световая оспа (Hydroa vacciniforme, HV) (см. табл. 2). Световая оспа — заболевание, характеризующееся развитием поэтапной полиморфной некротической сыпи на участках кожи, подверженных солнечному облучению. Заболевание зачастую носит семейный характер, однако у ряда пациентов при гистохимическом анализе поражений кожи имеет место инфильтрация Т-клетками, экспрессирующими малую РНК, кодируемую ЭБВ. Совпадение наличия ХЭБВИ и световой оспы (HV) может перерасти в развитие злокачественной лимфомы, которая была включена в классификацию ВОЗ 2008 г. как HV-подобная лимфома [14].
Заболевание зачастую носит семейный характер, однако у ряда пациентов при гистохимическом анализе поражений кожи имеет место инфильтрация Т-клетками, экспрессирующими малую РНК, кодируемую ЭБВ. Совпадение наличия ХЭБВИ и световой оспы (HV) может перерасти в развитие злокачественной лимфомы, которая была включена в классификацию ВОЗ 2008 г. как HV-подобная лимфома [14].
Активная ЭБВИ (см. табл. 2) может служить триггером для развития идиопатической тромбоцитопенической пурпуры [17] — аутоиммунного гематологического заболевания, в основе которого лежит тромбоцитопения с развитием геморрагического синдрома. Характерными признаками данного заболевания являются множественные, полиморфные кровоизлияния в кожный покров и слизистые оболочки, а также кровотечения различной локализации (нос, десны и др.).
Гемофагоцитарный лимфогистиоцитоз (ГЛГ) — одно из наиболее опасных, жизнеугрожающих осложнений ЭБВИ, основными симптомами которого являются: лихорадка, рефрактерная к антимикробной терапии, геморрагический и отечный синдромы, желтуха, экзантема, гепатоспленомегалия, симптомы поражения центральной нервной системы (возбудимость, угнетение сознания, судороги, менингеальные знаки) [18]. Развитие ГЛГ сопряжено с расстройством иммунной регуляции в результате бесконтрольной активации и пролиферации макрофагов и Т-клеток, что проявляется избыточной продукцией цитокинов, воспалением и повреждением тканей. Выделяют первичный ГЛГ, характеризующийся наличием семейного анамнеза и определенного генетического дефекта, и вторичный ГЛГ, ассоциированный с инфекцией, аутоиммунными и онкологическими заболеваниями, а также иммунодефицитным состоянием [19].
Развитие ГЛГ сопряжено с расстройством иммунной регуляции в результате бесконтрольной активации и пролиферации макрофагов и Т-клеток, что проявляется избыточной продукцией цитокинов, воспалением и повреждением тканей. Выделяют первичный ГЛГ, характеризующийся наличием семейного анамнеза и определенного генетического дефекта, и вторичный ГЛГ, ассоциированный с инфекцией, аутоиммунными и онкологическими заболеваниями, а также иммунодефицитным состоянием [19].
Доказана ключевая роль ЭБВ в развитии лимфопролиферативных заболеваний. Одной из ключевых лимфом, ассоциированных с ВЭБ, считается лимфома Беркитта [20]. Клиническими проявлениями лимфом служат увеличение лимфатических узлов, спленомегалия, цитопения, лихорадка. Считается, что наличие латентной ЭБВИ в эпителии носоглотки является ранней стадией патогенеза недифференцированной назофарингеальной карциномы [21].
Диагностика ЭБВИ сложна и не всегда возможна в рутинной практике клинициста. Критериями диагностики ИМ ЭБВ-этиологии являются клинико-лабораторные данные (см. табл. 1). При этом оценка результатов серологического обследования имеет некоторые особенности. Так, не всегда первоначальная продукция IgM к VCA предшествует выработке антител класса IgG к VCA, возможно одновременное появление или полное отсутствие их выработки при иммуносупрессии у пациента с ЭБВИ. Может наблюдаться длительная (более 3–4 мес.) персистенция IgM к VCA (паст-инфекция). Наличие IgG к ранним антигенам (EA) не всегда свидетельствует о ранней стадии инфекции, они могут выявляться у 70% больных острым ИМ и у большинства здоровых доноров, а также при реактивации ЭБВИ [22, 23].
Критериями диагностики ИМ ЭБВ-этиологии являются клинико-лабораторные данные (см. табл. 1). При этом оценка результатов серологического обследования имеет некоторые особенности. Так, не всегда первоначальная продукция IgM к VCA предшествует выработке антител класса IgG к VCA, возможно одновременное появление или полное отсутствие их выработки при иммуносупрессии у пациента с ЭБВИ. Может наблюдаться длительная (более 3–4 мес.) персистенция IgM к VCA (паст-инфекция). Наличие IgG к ранним антигенам (EA) не всегда свидетельствует о ранней стадии инфекции, они могут выявляться у 70% больных острым ИМ и у большинства здоровых доноров, а также при реактивации ЭБВИ [22, 23].
Методом ПЦР определяют ДНК ЭБВ в крови или другом биологическом материале (слюна, мазки из ротоглотки), а при необходимости и в биоптатах печени, лимфоузлов, слизистой кишечника и т. д.), но качественный анализ не позволяет в клинической практике отличить здоровое носительство от активной репликации вируса. В связи с этим некоторые исследователи указывают на необходимость использования количественного варианта ПЦР [3, 22, 23], при этом определение в пробе 10 копий ДНК ЭБВ (1000 ГЭ/мл в 1 мл образца) характеризуется как здоровое носительство, а выявление 100 и более копий (10000 ГЭ/мл в 1 мл образца) указывает на активную фазу ЭБВИ.
В связи с этим некоторые исследователи указывают на необходимость использования количественного варианта ПЦР [3, 22, 23], при этом определение в пробе 10 копий ДНК ЭБВ (1000 ГЭ/мл в 1 мл образца) характеризуется как здоровое носительство, а выявление 100 и более копий (10000 ГЭ/мл в 1 мл образца) указывает на активную фазу ЭБВИ.
Критериями диагностики ХЭБВИ являются признаки инфицирования более 6 мес.: лихорадка, лимфаденопатия и спленомегалия (мононуклеозоподобный синдром), выраженное повышение титров антител к антигену вирусного капсида ЭБВ (VCA ≥ 1:5120) или ранним антигенам (EA ≥1:640), обнаружение ДНК ЭБВ в крови, ДНК, мРНК или белков вируса в пораженных тканях в отсутствие другой причины иммуносупрессии [23, 24]. Важно помнить о возможном отсутствии IgM при нарастании титров IgG к вирусным белкам.
Дополнительную информацию о течении инфекции можно получить с помощью иммуноблота. Иммуноблоттинг — это высокоспецифичный и высокочувствительный референтный метод, с помощью которого определяют широкий спектр вирусспецифических белков (р125, р65, р42, р41, р40, p33, р22), характеризующих определенную фазу заболевания.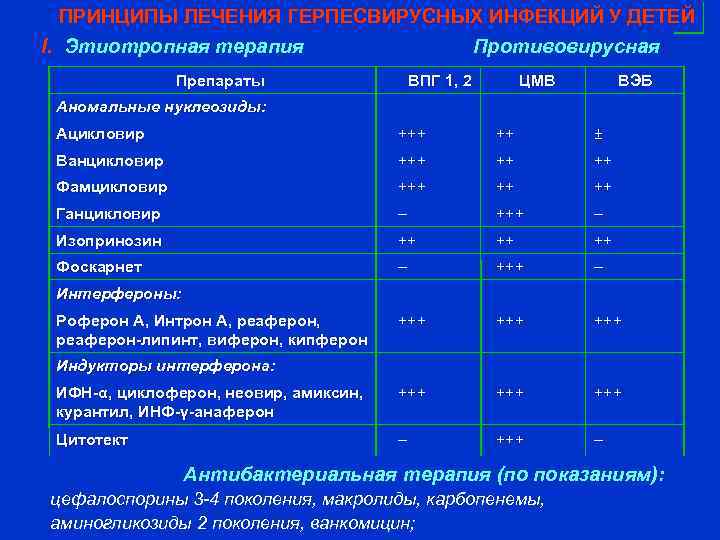 Так, выявление белка VCA 125 указывает на раннюю фазу инфекции; о поздней фазе течения инфекции свидетельствует обнаружение VCA 22, который выявляется одиночно или совместно с EBNA 1 (p-79), он длительно присутствует у перенесших заболевание и убедительно свидетельствует о перенесенной инфекции. Отмечается частое присутствие IgM p-45 и IgM p-79 при активном процессе [3]. Но, к сожалению, эти методы не совсем доступны в амбулаторной практике.
Так, выявление белка VCA 125 указывает на раннюю фазу инфекции; о поздней фазе течения инфекции свидетельствует обнаружение VCA 22, который выявляется одиночно или совместно с EBNA 1 (p-79), он длительно присутствует у перенесших заболевание и убедительно свидетельствует о перенесенной инфекции. Отмечается частое присутствие IgM p-45 и IgM p-79 при активном процессе [3]. Но, к сожалению, эти методы не совсем доступны в амбулаторной практике.
Таким образом, для постановки диагноза ЭБВИ, особенно ХЭБВИ, помимо проведения общеклинического обследования, необходимы серологические исследования специфических противовирусных антител, количественное определение ДНК вируса в различном биологическом материале и определение индекса авидности в динамике.
Лечение любой формы ЭБВИ, а особенно ХЭБВИ, составляет большую проблему для современной медицины. До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ЭБВ, также нет патогенетически обоснованной схемы лечения больных ЭБВИ, а данные отечественных исследователей об эффективности терапии не имеют достаточной доказательной базы и все указания носят рекомендательный характер [1, 24–26].
Ведущее место среди этиотропных препаратов в терапии герпесвирусных инфекций занимают ациклические аналоги гуанозина (уровень доказательности А), препараты интерферонов и иммуноглобулинов, которые являются важной дополнительной составляющей лечения (уровень доказательности В). Чувствительность различных герпесвирусов к ацикловиру можно расположить в порядке убывания следующим образом: ВПГ-1, ВПГ-2, ВГ-3 > ЭБВ, ЦМВ-5 > ВГЧ-6, ВГЧ-7, ВГЧ-8.
Доказательная база свидетельствует, что ацикловир наиболее эффективен при инфекциях, вызванных альфа-герпесвирусами (ВПГ-1, 2, ВГ-3), имеет ограниченную эффективность при ЭБВИ и назначается только в случаях тяжелого ИМ с высокой вирусной нагрузкой. Однако он практически неэффективен при инфекциях, вызванных ВГЧ-6, 7, 8. Различная чувствительность к ацикловиру обусловлена разным содержанием вирусной тимидинкиназы у герпесвирусов. В отличие от ацикловира, к валацикловиру чувствительны все вирусы герпеса и наиболее высокая чувствительность — у альфа-подсемейства [26].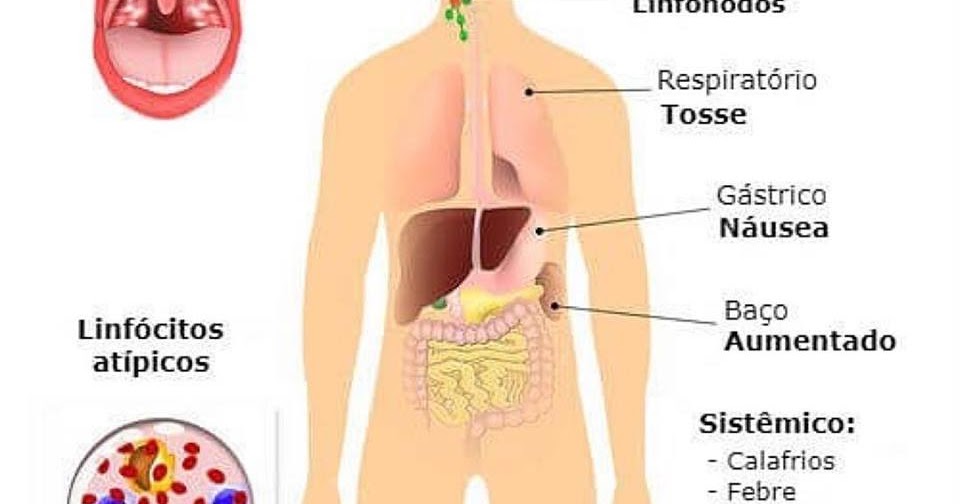
Лечение больных ИМ проводят в амбулаторных условиях, госпитализируют лиц с длительной лихорадкой, выраженным синдромом интоксикации, тяжелым тонзиллитом, гепатитом, желтухой, анемией, обструкцией дыхательных путей и при развитии осложнений [24, 26]. Базисная терапия ИМ (см. табл. 1) включает охранительный режим, симптоматическую терапию: адекватную регидратацию (обильное питье), полоскание горла антисептиками и по необходимости жаропонижающие средства. Применение антибиотиков необходимо только в случаях наслоения бактериальной инфекции с явлениями лакунарной или некротической ангины, при этом препаратами выбора будут цефалоспорины 2–3-го поколения, макролиды, карбапенемы [1, 26].
Противовирусные препараты неэффективны при латентном течении ХЭБВИ [25, 26], т. к. они ингибируют ДНК-полимеразу и репликацию литической фазы вируса в инфицированных клетках, которые экспрессируют вирусную ДНК-полимеразу. При ХЭБВИ в инфицированных клетках вирус находится в латентной фазе, экспрессируя латентные белки, для синтеза которых не требуется ДНК-полимераза [2, 23, 27].
По поводу назначения глюкокортикостероидов (ГКС) мнения также расходятся. Они рекомендуются больным с тяжелым течением ИМ, обструкцией дыхательных путей, неврологическими гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [27, 28]. При латентной ЭБВИ ГКС приводят к реактивации инфекции с литической репликацией ЭБВ через индуцирование раннего гена BZLF1 и литического трансактивирующего белка ZEBRA. Интересными представляются исследования по применению моноклональных антител к СD20 (ритуксимаб) у пациентов с иммунной тромбоцитопенической пурпурой [26]. Иммуносупрессивные препараты дают кратковременный положительный эффект в виде уменьшения симптомов ХЭБВИ без долгосрочной ремиссии и могут быть назначены при начальной фазе гемофагоцитарного лимфогистиоцитоза, который часто осложняет ХЭБВИ [18, 19]. Положительные результаты в лечении ХЭБВИ достигнуты при применении трансплантации гемопоэтических стволовых клеток. Начинать данную терапию рекомендовано в начале заболевания ввиду ее тяжелой переносимости [27, 28].
На основании изучения фармакодинамики и собственного обширного клинического опыта многие исследователи считают препараты α-интерферонов (уровень доказательности D) средством выбора в лечении тяжелых форм ЭБВИ и при нейроинфекциях как дополнение к специфическим препаратам, особенно показаны детям первых 3 лет жизни и подросткам. Эти препараты тормозят репликацию вирусов за счет разрушения вирусной мРНК, модулируют иммунный ответ, стимулируют выработку цитокинов, повышают функциональную активность макрофагов, нейтрофилов и стабилизируют клеточные мембраны. Так, в многочисленных работах [28–33] показана эффективность α-интерферона при инфекционном мононуклеозе у детей по сравнению с контрольной группой, при активации хронического мононуклеоза с интермиттирующей лихорадкой, цитопенией, дисфункцией печени, гепатоспленомегалией, аномальными титрами специфических антител и положительным геномом вируса у больного ХЭБВИ, при посттрансплантационном лимфопролиферативном синдроме, ассоциированном с ВЭБ, а также у больных ХЭБВИ при общем вариабельном иммунодефиците.
Препараты β-интерферонов снижают проницаемость гематоэнцефалического барьера и могут иметь определенные преимущества при рассеянном склерозе, ассоциированном с ЭБВ, с ремиттирующим течением, но доказательная база у таких препаратов значительно меньше, чем у α-интерферонов [32, 33].
Есть несколько исследований, указывающих на эффективность препаратов рекомбинантного γ-интерферона при ЭБВИ, которые оказывают ограниченное прямое противовирусное воздействие. Их клинический эффект опосредован усилением клеточного иммунитета, контролирующего эндогенный вирус. Терапевтический эффект этой группы препаратов продемонстрировали при тяжелой активной ХЭБВИ [34–38], рецидивирующей назофарингеальной карциноме, тяжелом лимфопролиферативном синдроме, вызванном ЭБВ. Учитывая синергическое действие, их можно применять как дополнение к терапии α-интерферонами [35, 37]. Показано, что противовирусный и иммуномодулирующий эффекты α-интерферонов частично опосредованы вторичной индукцией синтеза γ-интерферона Т-лимфоцитами [23, 36, 37]. Индукторы интерферонов имеют низкую доказательную базу при ЭБВИ, несмотря на широкое применение в клинической практике в странах постсоветского пространства.
Индукторы интерферонов имеют низкую доказательную базу при ЭБВИ, несмотря на широкое применение в клинической практике в странах постсоветского пространства.
Ряд авторов рекомендуют комплексную терапию ЭБВИ с введением препаратов иммуноглобулинов класса G. В отличие от интерферонов препараты иммуноглобулинов действуют преимущественно на внеклеточный вирус в виде вирионов. Этиотропный эффект иммуноглобулинов выражается в вируцидном и вирустатическом действии препарата и развитии антителозависимой комплемент-опосредованной цитотоксичности. Убедительно доказана их эффективность при первичной или вторичной гипоиммуноглобулинемии, а также в качестве базисной терапии при аутоиммунных осложнениях (синдром Гийена — Барре, тромбоцитопеническая пурпура, синдром Кавасаки, хроническая демиелинизирующая полинейропатия и системная красная волчанка) [36, 37]. В контролируемом нерандомизированном исследовании продемонстрирована эффективность комбинированной иммунотерапии при ЭБВИ, проявляющейся гипертрофией лимфоидных органов лимфоглоточного кольца, при реактивированной ЭБВИ с различными органными поражениями и при трудно поддающихся лечению формах болезни [37, 39], а также в профилактике виремии при ХЭБВИ. Многие исследователи [26, 38, 39] считают целесообразным применение специфического иммуноглобулина в комплексной терапии для профилактики ЭБВ-ассоциированного лимфопролиферативного синдрома у реципиентов солидных органов, при гемофагоцитарном синдроме, ассоциированном с ЭБВ, указывая на необходимость дальнейших исследований. Некоторым пациентам необходимо хирургическое лечение: удаление селезенки иногда выполняют при ИМ ЭБВ-этиологии при угрозе разрыва или начавшемся внутреннем кровотечении; возможна трахеостомия у больных с тяжелым ИМ при наличии фарингеальной обструкции и асфиксии.
Многие исследователи [26, 38, 39] считают целесообразным применение специфического иммуноглобулина в комплексной терапии для профилактики ЭБВ-ассоциированного лимфопролиферативного синдрома у реципиентов солидных органов, при гемофагоцитарном синдроме, ассоциированном с ЭБВ, указывая на необходимость дальнейших исследований. Некоторым пациентам необходимо хирургическое лечение: удаление селезенки иногда выполняют при ИМ ЭБВ-этиологии при угрозе разрыва или начавшемся внутреннем кровотечении; возможна трахеостомия у больных с тяжелым ИМ при наличии фарингеальной обструкции и асфиксии.
В клинической практике диагностика и ведение пациентов с ЭБВИ всегда сложны и неодназначны. Приводим два клинических случая.
Случай 1. Пациентка Ю., 26 лет, доставлена в инфекционную клиническую больницу № 2 (ИКБ № 2) с жалобами на повышение температуры тела, слабость, появление одышки, ощущение сердцебиения при физической нагрузке.
Из анамнеза известно, что заболела 15 дней назад, когда появились повышение температуры тела до 39,0 °С, боль в горле, слабость, возникновение одышки при физической нагрузке. В последующие дни сохранялась повышенная температура тела, появились тяжесть в правом подреберье, потемнение мочи. Обследована амбулаторно: в клиническом анализе крови обнаружены лимфомоноцитоз, атипичные мононуклеары, снижение уровня гемоглобина до 73 г/л. Была госпитализирована в ИКБ № 2 с диагнозом: «Инфекционный мононуклеоз. Анемия тяжелой степени».
При поступлении состояние пациентки средней тяжести. Температура тела 38,0 °С. Выраженная слабость. Кожные покровы бледные, сыпи, геморрагий, кровоточивости нет. Склеры инъецированы, отмечается краевая иктеричность. Слизистая ротоглотки слабо гиперемирована, миндалины увеличены до II степени, имеются гнойные наложения в лакунах. Пальпируются подчелюстные, шейные до 1–1,5 см лимфатические узлы, плотные, безболезненные. Дыхание через нос свободное. Выделений из носа нет. В легких дыхание ослабленное. Хрипы не выслушиваются. ЧДД 20 в минуту. Тоны сердца приглушены, ритмичные. На верхушке сердца выслушивается систолический шум. ЧСС 80 в минуту. АД 110/70 мм рт. ст. Язык влажный, обложен белым налетом Живот при пальпации мягкий, чувствительный в правом подреберье. Перистальтика выслушивается. Перитонеальных знаков нет. Печень выступает из-под края реберной дуги на 4 см, плотная, чувствительная при пальпации. Пальпируется увеличенная селезенка, плотная, безболезненная. Симптом поколачивания по поясничной области отрицательный с обеих сторон. Физиологические отправления не нарушены. Очаговых и менингеальных знаков нет. Больной назначена терапия цефтриаксоном 2,0 г × 2 р./сут внутривенно, полоскание ротоглотки раствором фурациллина, внутривенно дезинтоксикационная терапия 5% раствором глюкозы с аскорбиновой кислотой, инъекции диклофенака при повышении температуры.
Выделений из носа нет. В легких дыхание ослабленное. Хрипы не выслушиваются. ЧДД 20 в минуту. Тоны сердца приглушены, ритмичные. На верхушке сердца выслушивается систолический шум. ЧСС 80 в минуту. АД 110/70 мм рт. ст. Язык влажный, обложен белым налетом Живот при пальпации мягкий, чувствительный в правом подреберье. Перистальтика выслушивается. Перитонеальных знаков нет. Печень выступает из-под края реберной дуги на 4 см, плотная, чувствительная при пальпации. Пальпируется увеличенная селезенка, плотная, безболезненная. Симптом поколачивания по поясничной области отрицательный с обеих сторон. Физиологические отправления не нарушены. Очаговых и менингеальных знаков нет. Больной назначена терапия цефтриаксоном 2,0 г × 2 р./сут внутривенно, полоскание ротоглотки раствором фурациллина, внутривенно дезинтоксикационная терапия 5% раствором глюкозы с аскорбиновой кислотой, инъекции диклофенака при повышении температуры.
При обследовании: в общем анализе крови отмечается снижение количества эритроцитов до 1,96×1012/л, гемоглобина до 64 г/л, лейкоцитоз 17,5×109/л, лимфоцитоз 82%, среди лимфоцитов обнаружено 18 атипичных мононуклеаров. В биохимическом анализе крови отмечается умеренное повышение печеночных трансаминаз (АЛТ 106,3 ЕД/л; АСТ 165,4 ЕД/л). Содержание сывороточного железа в норме. При ПЦР-исследовании крови обнаружена ДНК ЭБВ, в реакции ИФА на антитела к VCA — IgМ положительные, IgG отрицательные.
В биохимическом анализе крови отмечается умеренное повышение печеночных трансаминаз (АЛТ 106,3 ЕД/л; АСТ 165,4 ЕД/л). Содержание сывороточного железа в норме. При ПЦР-исследовании крови обнаружена ДНК ЭБВ, в реакции ИФА на антитела к VCA — IgМ положительные, IgG отрицательные.
Выполнено УЗИ органов брюшной полости: выявлены диффузные изменения в паренхиме печени и паренхиме поджелудочной железы, значительное увеличение и диффузные изменения в паренхиме селезенки.
Больная консультирована гематологом, заключение: картина крови соответствует лейкемоидной реакции по лимфоцитарному типу на фоне инфекционного мононуклеоза ЭБВ-этиологии. Рекомендована терапия эпоэтином бета, фолиевой кислотой, витамином В12. Больной выполнена 1 инъекция эпоэтина бета (2 тыс. Ед подкожно), далее ввиду возникновения у пациентки выраженного болевого синдрома и категорического отказа пациентки инъекции прекращены.
На 11-й день пребывания пациентки в стационаре отсутствует положительная динамика от проводимого лечения: в общем анализе крови сохраняется снижение эритроцитов до 1,84×1012/л, гемоглобина до 62 г/л, в биохимическом анализе крови отмечается повышенный уровень печеночных трансаминаз (АЛТ 110,4 ЕД/л; АСТ 160,1 ЕД/л). Больной назначена терапия ганцикловиром по 250 мг 2 р./сут внутривенно.
Больной назначена терапия ганцикловиром по 250 мг 2 р./сут внутривенно.
На 17-й день пребывания в стационаре пациентка пожаловалась на появление болей в животе, в связи с чем выполнено повторное УЗИ органов брюшной полости, выявлена зона инфаркта селезенки небольших размеров в нижнем полюсе. Больная консультирована хирургом, рекомендовано наблюдение в динамике.
В дальнейшем на фоне проводимой терапии отмечается положительная динамика в виде нормализации температуры тела, регресса явлений тонзиллита. В общем анализе крови обращает на себя внимание повышение гемоглобина до 96 г/л, эритроцитов до 3,01×1012/л, нормализация уровня лейкоцитов.
На 21-й день госпитализации больная выписана под наблюдение инфекциониста и гематолога по месту жительства.
Случай 2. Пациент Ж., 25 лет, поступил в ИКБ № 2 с жалобами на повышение температуры тела до 37,7 °С, сухой кашель.
Из анамнеза известно, что заболел 10. 03.2019: слабость, головокружение, повышение температуры тела до фебрильных цифр. 11.03.2019: повышение температуры тела до 38,5 °С. Лечился самостоятельно: принимал тилорон, азитромицин без эффекта. 14.03.2019: осмотрен терапевтом на дому, выставлен диагноз ОРВИ, назначен осельтамивир. 15.03.2019: симптомы сохранялись, появился однократный жидкий стул без патологических примесей, насморк, сухой кашель. 19.03.2019 обследован амбулаторно: выполнена обзорная рентгенография грудной клетки — без патологических изменений, в общем анализе крови отмечается небольшой лейкоцитоз (11×109/л), остальные показатели в норме. Назначен левофлоксацин без эффекта. 21.03.2019 госпитализирован в ИКБ № 2 службой скорой помощи с диагнозом «лихорадка неясной этиологии».
При осмотре состояние пациента средней степени тяжести. Температура тела 37,7 °С. Кожные покровы физиологической окраски, умеренной влажности, сыпи нет. Слизистая ротоглотки гиперемирована, фолликулы на задней стенке глотки, миндалины не увеличены, свободны от наложений.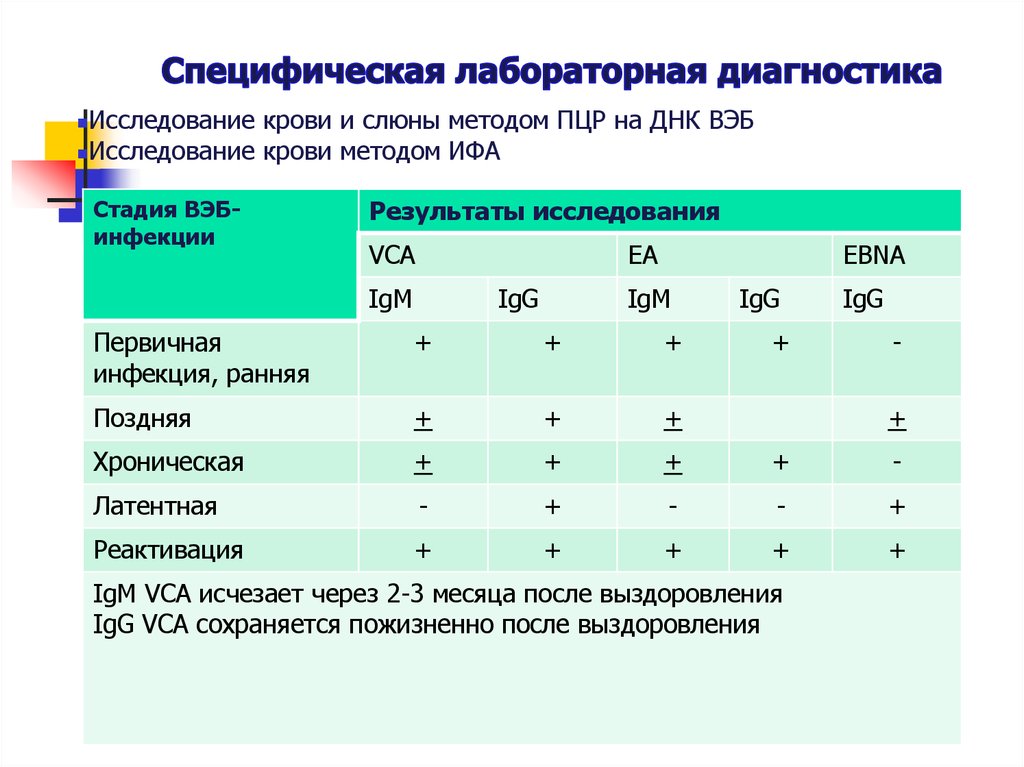 При пальпации: периферические лимфатические узлы не увеличены. Периферических отеков нет. Дыхание через нос свободное. Выделений из носа нет. В легких дыхание жесткое, проводится во все отделы, хрипы не выслушиваются, ЧДД 18 в минуту. Тоны сердца ясные, ритмичные, ЧСС 78 в минуту, АД 100/60 мм рт. ст. Живот при пальпации мягкий, безболезненный во всех отделах. Перистальтика активна. Перитонеальных знаков нет. Печень выступает из-под края реберной дуги на 2 см, селезенка не увеличена, безболезненны. Симптом поколачивания по поясничной области сомнителен с обеих сторон. Со слов больного, стул оформлен, обесцвечен. Мочеиспускание не нарушено. Моча темная. Очаговых и менингеальных знаков нет.
При пальпации: периферические лимфатические узлы не увеличены. Периферических отеков нет. Дыхание через нос свободное. Выделений из носа нет. В легких дыхание жесткое, проводится во все отделы, хрипы не выслушиваются, ЧДД 18 в минуту. Тоны сердца ясные, ритмичные, ЧСС 78 в минуту, АД 100/60 мм рт. ст. Живот при пальпации мягкий, безболезненный во всех отделах. Перистальтика активна. Перитонеальных знаков нет. Печень выступает из-под края реберной дуги на 2 см, селезенка не увеличена, безболезненны. Симптом поколачивания по поясничной области сомнителен с обеих сторон. Со слов больного, стул оформлен, обесцвечен. Мочеиспускание не нарушено. Моча темная. Очаговых и менингеальных знаков нет.
При обследовании: в общем анализе крови отмечается лейкоцитоз 10×109/л, лимфоцитоз 74%, среди лимфоцитов обнаружено 17 атипичных мононуклеаров, остальные показатели в норме. В биохимическом анализе крови отмечается умеренное повышение печеночных трансаминаз (АЛТ 61 ЕД/л; АСТ 60,4 ЕД/л).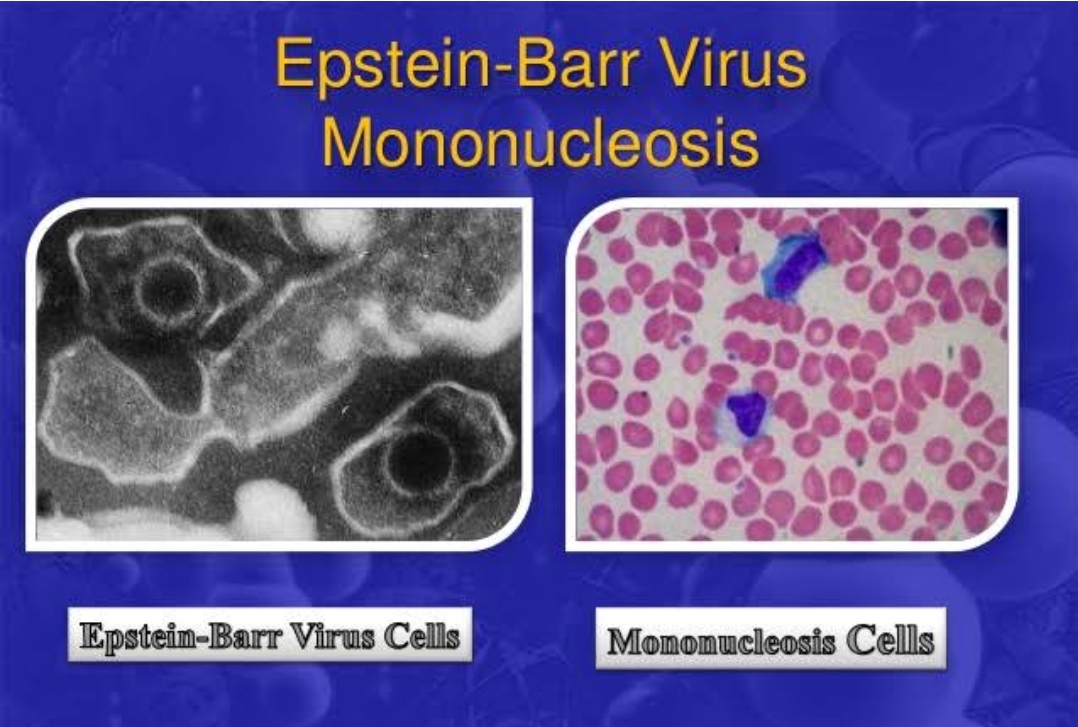 В ПЦР-исследовании крови и мазка из ротоглотки ДНК ВЭБ не обнаружена, при ИФА на антитела к VCA — реакция на IgМ и IgG положительная.
В ПЦР-исследовании крови и мазка из ротоглотки ДНК ВЭБ не обнаружена, при ИФА на антитела к VCA — реакция на IgМ и IgG положительная.
По данным УЗИ органов брюшной полости и почек отмечаются увеличение и диффузные изменения в паренхиме печени, увеличение и диффузные изменения в паренхиме селезенки, умеренные диффузные изменения в паренхиме почек.
Назначен цефотаксим по 2 г 2 р./сут внутримышечно, полоскание ротоглотки раствором хлоргексидина, цетиризин, комплекс лактобактерий ацидофильных и кефирных грибков. На 3-й день пребывания в стационаре в связи с сохраняющейся лихорадкой произведена замена антимикробной терапии на ципрофлоксацин 400 мг 2 р./сут внутривенно.
На 5-й день пребывания больного в стационаре отмечена положительная динамика в виде исчезновения лихорадки, и на 9-й день больной выписан из стационара под наблюдение врача-инфекциониста по месту жительства.
Важность проблемы изучения ЭБВИ обусловлена высокой распространенностью, специфической тропностью возбудителя к иммунокомпетентным клеткам, трудностями ранней и дифференциальной диагностики, особенностями клинического течения инфекции, отсутствием специфической профилактики и эффективной этиотропной терапии.
Учитывая разнообразие клинических форм ЭБВИ, высокий риск онкопатологии, формирование иммунодефицитов различной степени выраженности, в генезе которых ЭБВ играет ключевую роль, особое значение следует придавать своевременной диагностике и адекватной тактике ведения, т. к. они определяют исход заболевания. Необходимо более детальное и углубленное изучение иммунопатогенеза различных стадий ЭБВИ для определения критериев прогноза течения заболевания, выявления иммунологических нарушений и иммуногенетических факторов предрасположенности к ЭБВ-ассоциированным осложнениям, а также для оптимизации терапии.
Лечение больных с любой формой ЭБВИ должно быть комплексным, с учетом клинических проявлений, тяжести течения, периода болезни, что на практике бывает крайне трудно реализовать. Залогом же успешного лечения ХЭБВИ являются своевременная диагностика, правильный и строго индивидуальный подход как к этиотропной, так и к патогенетической терапии с последующим персонифицированным ведением конкретного больного на всех этапах (стационар, поликлиника). Необходимо наблюдение у инфекциониста, гематолога, иммунолога.
Необходимо наблюдение у инфекциониста, гематолога, иммунолога.
Вирус Эпштейна-Барр (EBV), также известный как вирус герпеса человека 4, является членом семейства вирусов герпеса. Это один из самых распространенных вирусов человека. ВЭБ встречается во всем мире. Большинство людей заражаются ВЭБ в какой-то момент своей жизни. ВЭБ чаще всего распространяется через жидкости организма, в первую очередь слюну. ВЭБ может вызывать инфекционный мононуклеоз, также называемый мононуклеозом, и другие заболевания.
Симптомы инфекции ВЭБ могут включать
Многие люди заражаются ВЭБ в детстве.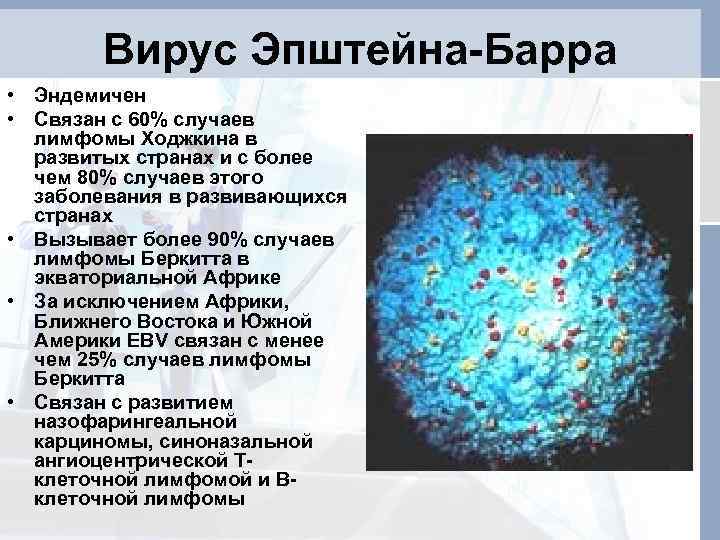 Инфекции ВЭБ у детей обычно не вызывают симптомов, или симптомы неотличимы от других легких кратковременных детских заболеваний. Люди, у которых появляются симптомы инфекции EBV, обычно подростки или взрослые, выздоравливают через две-четыре недели. Однако некоторые люди могут чувствовать усталость в течение нескольких недель или даже месяцев.
Инфекции ВЭБ у детей обычно не вызывают симптомов, или симптомы неотличимы от других легких кратковременных детских заболеваний. Люди, у которых появляются симптомы инфекции EBV, обычно подростки или взрослые, выздоравливают через две-четыре недели. Однако некоторые люди могут чувствовать усталость в течение нескольких недель или даже месяцев.
После заражения ВЭБ вирус становится латентным (неактивным) в вашем организме. В некоторых случаях вирус может реактивироваться. Это не всегда вызывает симптомы, но у людей с ослабленной иммунной системой более вероятно развитие симптомов при реактивации ВЭБ.
ВЭБ передается слюной через:
ВЭБ чаще всего распространяется через биологические жидкости, особенно слюну. Однако ВЭБ также может распространяться через кровь и сперму при половых контактах, переливаниях крови и трансплантации органов.
ВЭБ может передаваться при использовании таких предметов, как зубная щетка или стакан для питья, которыми недавно пользовался инфицированный человек. Вирус, вероятно, выживает на объекте, по крайней мере, до тех пор, пока объект остается влажным.
При первом заражении ВЭБ (первичная инфекция ВЭБ) вы можете распространять вирус в течение нескольких недель и даже до того, как у вас появятся симптомы. Как только вирус попадает в ваш организм, он остается там в латентном (неактивном) состоянии. Если вирус реактивируется, вы потенциально можете передать ВЭБ другим людям, независимо от того, сколько времени прошло с момента первоначального заражения.
Диагностика инфекции ВЭБ может быть сложной, поскольку симптомы подобны другим заболеваниям. Инфекция ВЭБ может быть подтверждена анализом крови, который обнаруживает антитела. Около девяти из десяти взрослых имеют антитела, которые показывают, что они перенесли инфекцию ВЭБ в настоящее время или в прошлом.
Дополнительную информацию см. в разделе Лабораторные испытания.
Вакцины для защиты от ВЭБ-инфекции не существует. Вы можете защитить себя, не целуясь и не делясь напитками, едой или личными вещами, такими как зубные щетки, с людьми, инфицированными ВЭБ.
Специфического лечения ВЭБ не существует. Тем не менее, некоторые вещи можно предпринять для облегчения симптомов, в том числе
Вирус Эпштейна-Барра (ВЭБ) — очень распространенная вирусная инфекция, которая распространяется через слюну и биологические жидкости. ВЭБ — это тип герпесвируса, называемый вирусом герпеса 4. В большинстве случаев ВЭБ не вызывает симптомов. Другие случаи, особенно у подростков и молодых людей, могут привести к инфекционному мононуклеозу.
Как только вы заразитесь ВЭБ, инфекция остается в вашем организме на всю жизнь в спящем состоянии, когда она неактивна или спит. Вы можете повторно активировать вирус и снова испытать симптомы, независимо от того, когда вы впервые заразились вирусом.
В большинстве случаев вирус Эпштейна-Барр поражает детей, подростков и молодых людей, но любой может заразиться вирусом.
Вирус Эпштейна-Барр очень распространен. В США примерно 50% всех детей в возрасте до 5 лет и около 95% взрослых переносят инфекцию ВЭБ в течение жизни.
Вирус Эпштейна-Барр заразен и легко распространяется через слюну (слюну). Вы можете заразиться ВЭБ, поделившись предметами, контактирующими со слюной инфицированного человека. Большинство людей заражаются ВЭБ, выпивая из одного стакана или целуя кого-то с вирусом.
Да, вирус Эпштейна-Барра заразен.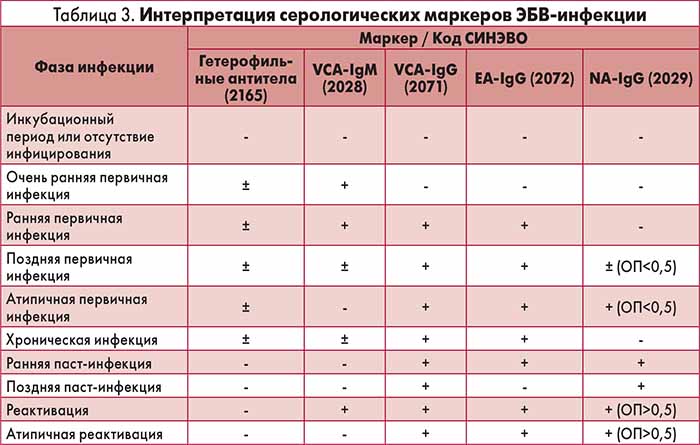 Вирус может распространяться в течение инкубационного периода (количество времени, когда кто-то подвергается воздействию вируса, до момента, когда у него появляются симптомы), который составляет от четырех до шести недель.
Вирус может распространяться в течение инкубационного периода (количество времени, когда кто-то подвергается воздействию вируса, до момента, когда у него появляются симптомы), который составляет от четырех до шести недель.
Вирус легко распространяется через слюну (слюну), но может распространяться и через другие жидкости организма. Вы можете заразиться ВЭБ от инфицированного человека:
Если у вас ВЭБ, вам не обязательно проявлять симптомы, чтобы передать вирус другому человеку. Как только вы заразитесь инфекцией, она будет жить в вашем теле в спящем (спящем или неактивном) состоянии. Определенные события могут спровоцировать пробуждение (повторную активацию) ВЭБ и сделать его заразным для других, потенциально вызывая симптомы у хозяина.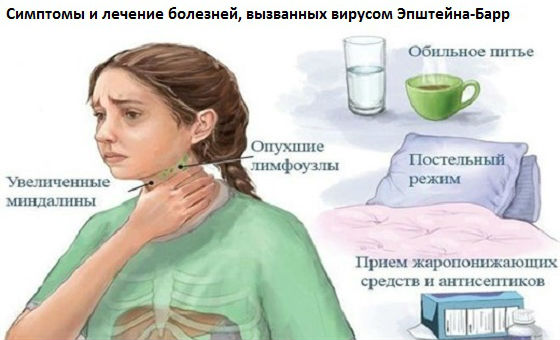 События, вызывающие реактивацию EBV, включают:
События, вызывающие реактивацию EBV, включают:
Тесный контакт между людьми вызывает высококонтагиозный вирус Эпштейна-Барр. Вирус легко распространяется через слюну (слюну) и другие биологические жидкости, такие как кровь и сперма. Вирус также может распространяться при переливании крови или трансплантации органов.
Вирус прикрепляется к лейкоцитам (лимфоцитам В-клеток) в вашем организме. Белые кровяные тельца помогают бороться с инфекцией. Когда вирус прикрепляется к вашим лейкоцитам, ваши клетки не могут должным образом бороться с инфекцией, и вы испытываете симптомы.
Симптомы различаются по степени тяжести для каждого человека, у которого диагностирован вирус Эпштейна-Барр. Симптомы включают:

Дети, у которых диагностирован вирус Эпштейна-Барр, либо не проявляют симптомов, либо их симптомы похожи на краткосрочные заболевания, такие как простуда или грипп. Подростки или взрослые, заразившиеся вирусом, могут проявлять симптомы в течение двух-четырех недель, но симптомы могут сохраняться в течение нескольких месяцев, особенно усталость.
Как только вы заражаетесь вирусом Эпштейна-Барра, инфекция деактивируется (латентно) или уходит в спящий режим. Инфекция может проснуться (реактивироваться), особенно если у вас ослаблен иммунитет. Иногда вирус не вызывает симптомов у хозяина, но все же заразен для других.
Врачу может быть сложно диагностировать вирус Эпштейна-Барр, потому что симптомы похожи на симптомы других распространенных заболеваний. Ваш лечащий врач спросит вас о ваших симптомах, о том, как долго они у вас были и контактировали ли вы с кем-либо, у кого может быть вирус. Ваш поставщик может предложить анализ крови для подтверждения диагноза.
Ваш лечащий врач спросит вас о ваших симптомах, о том, как долго они у вас были и контактировали ли вы с кем-либо, у кого может быть вирус. Ваш поставщик может предложить анализ крови для подтверждения диагноза.
Чтобы подтвердить ваш диагноз, ваш врач проведет анализ крови, называемый тестом на антитела к вирусу Эпштейна-Барр. Этот тест берет образец вашей крови для обнаружения антител, вызывающих ВЭБ. Вашему провайдеру может потребоваться повторить тест через 10 дней или две недели после первого теста, потому что антитела могут не проявляться на ранней стадии вашего диагноза.
Лечение вируса Эпштейна-Барр устраняет симптомы, связанные с инфекцией. Лечение включает:
Достаточное количество отдыха важно для предотвращения ухудшения симптомов. Особенно важно избегать чрезмерной физической активности, которая может привести к разрыву селезенки, если вирус вызовет увеличение селезенки.
Особенно важно избегать чрезмерной физической активности, которая может привести к разрыву селезенки, если вирус вызовет увеличение селезенки.
Люди, инфицированные вирусом Эпштейна-Барр, которые испытывают симптомы, обычно чувствуют себя лучше через две-четыре недели. У других могут быть затяжные симптомы усталости, когда они чувствуют себя очень усталыми в течение нескольких недель или месяцев после первоначального заражения.
Поскольку вакцины против вируса Эпштейна-Барр не существует, вы можете принять меры для предотвращения заражения вирусом:

От вируса Эпштейна-Барра нет лекарства, и нет вакцины для предотвращения распространения вируса. Лечение устраняет симптомы вируса, и симптомы должны исчезнуть через две-четыре недели.
После заражения вирусом он живет в вашем теле в дремлющем (спящем) состоянии, что означает, что он может повторно активироваться и проснуться, если ваше тело вызывает его из-за стресса или ослабленной иммунной системы. Вы можете снова испытать симптомы, если ваш организм реактивирует вирус.
Если у вас есть симптомы вируса Эпштейна-Барр или мононуклеоз, вам следует избегать школы, работы или мероприятий, на которых вы находитесь в тесном контакте с другими людьми, поскольку это заболевание очень заразно.
Ваш лечащий врач порекомендует вам оставаться дома, пока вы не почувствуете себя лучше и ваши симптомы не начнут исчезать.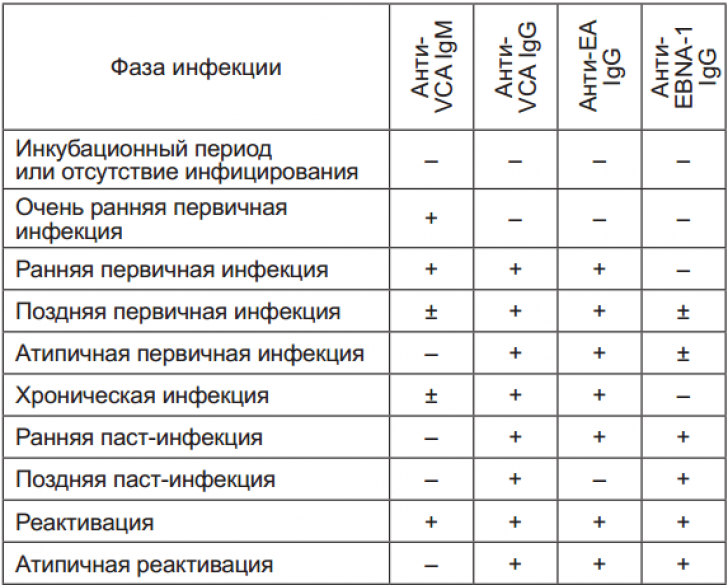 Вы можете испытывать затяжные симптомы, такие как усталость, в течение нескольких недель после исчезновения других симптомов.
Вы можете испытывать затяжные симптомы, такие как усталость, в течение нескольких недель после исчезновения других симптомов.
Если у вас появились симптомы вируса Эпштейна-Барр, обратитесь к своему лечащему врачу. Лечение вируса включает в себя отдых и прием безрецептурных лекарств для облегчения боли и дискомфорта. Если вы чувствуете сильную боль или лихорадку в течение нескольких дней, немедленно обратитесь к врачу.
Хотя вирус Эпштейна-Барр встречается редко, он может вызывать определенные виды рака, включая:

Рак, вызванный ВЭБ, является результатом вирусных генов вируса, которые изменяют цикл роста инфицированных клеток и заставляют их становиться раковыми.
Вирус Эпштейна-Барр относится к семейству вирусов герпеса человека и также известен как вирус герпеса человека 4 типа. Симптомы ВЭБ не такие, как у других вирусов семейства герпесвирусов, таких как генитальный герпес. Есть несколько распространенных состояний, которые относятся к семейству вирусов герпеса человека, таких как ветряная оспа, опоясывающий лишай и мононуклеоз. Некоторые случаи ВЭБ приводят к мононуклеозу.
Да, вирус Эпштейна-Барр может быть инфекцией, передающейся половым путем (ИППП), но не каждый случай является ИППП. Вирус может распространяться через жидкости организма, такие как кровь или сперма, но чаще всего распространяется через слюну.