2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Опубликовано: 26.02.2021 13:25:00 Обновлено: 28.06.2021 Просмотров: 899930
На днях в России зарегистрировали третью вакцину от коронавируса Sars-Cov-2 (COVID-19). Если еще пару месяцев назад мы могли только мечтать о вакцинации, то уже сейчас каждый желающий может сделать долгожданную прививку, а в скором времени появится возможность выбирать препарат.
Разбираемся, как работают три российские вакцины и в чем их различия. А заодно сравним достижения отечественной медицины с зарубежными аналогами.
С самого начала эпидемии разработка вакцины стала приоритетной задачей всех развитых стран. По последним данным ВОЗ (от 26 января 2021 года), больше 60 вакцин во всем мире уже проходят клинические испытания. Еще более 170 исследуются на животных. Главную – финальную – фазу испытаний уже прошли или проходят 22 препарата.
Три из них – российского производства. О главных игроках на рынке вакцин от коронавируса мы расскажем подробнее.
На сегодня в России зарегистрированы три вакцины. Что общего между всеми российскими достижениями против коронавируса:
Это первая вакцина в мире, поступившая в свободный оборот и, что особенно важно, уже прошедшая третью фазу испытаний. Ее действие наиболее хорошо изучено. Разработка зарегистрирована еще в августе 2020 года. Ее эффективность составляет 91,4 %, предупреждает развитие тяжелой формы заболевания в 100 % случаев. «Спутник V» зарегистрирована уже в 30 странах, и число государств, одобривших российскую вакцину для использования, растет каждый день.
Ее действие наиболее хорошо изучено. Разработка зарегистрирована еще в августе 2020 года. Ее эффективность составляет 91,4 %, предупреждает развитие тяжелой формы заболевания в 100 % случаев. «Спутник V» зарегистрирована уже в 30 странах, и число государств, одобривших российскую вакцину для использования, растет каждый день.
Данная вакцина – векторная. В ее основе лежат сразу два неопасных для человека аденовируса, в которые встроили небольшой участок генома вируса Sars-Cov-2.
«Спутник V» рекомендован взрослым людям с 18 до 60 лет, а также пожилым. Как показали исследования, вероятность осложнений в группе пожилых людей не выше, чем в других группах.
Среди побочных действий болевые ощущения в месте инъекции, в более редких случаях – повышение температуры до 39 градусов, слабость, мышечная боль. Однако негативные реакции – исключение, и встречаются они нечасто.
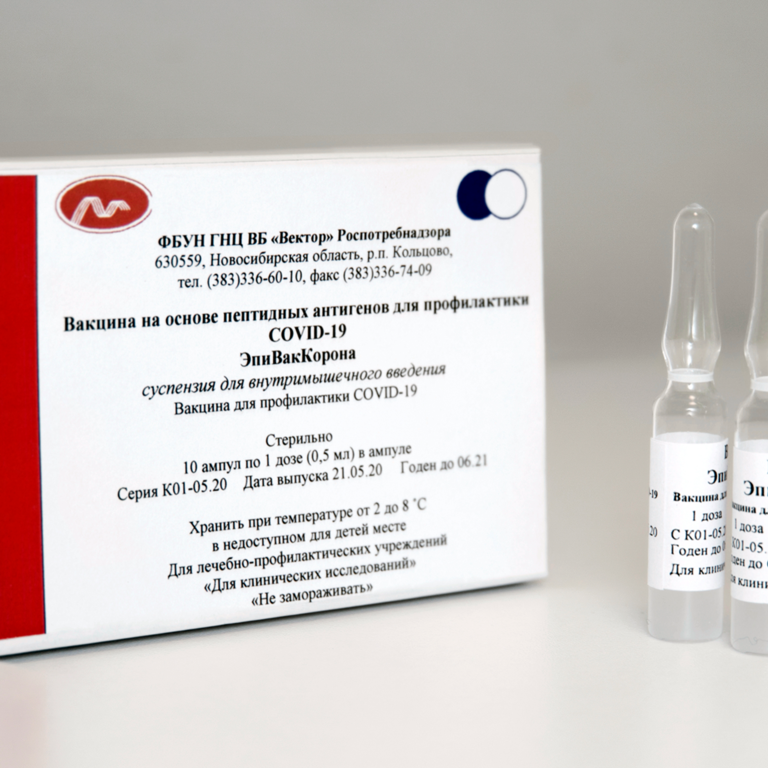
«ЭпиВакКорона» получила регистрацию в октябре 2020 года. В ее основе – синтетические аналоги участков вирусных белков, пептиды. Это значит, что в ней полностью отсутствуют биологические носители вируса, что, по идее, должно делать ее еще менее аллергенной. Иммунная система распознает эпитопы – «кусочки антигена», микроскопические частицы, на которые нацелен иммунитет. Этот термин и принцип действия отражен в названии вакцины - «ЭпиВакКорона».
В ее основе – синтетические аналоги участков вирусных белков, пептиды. Это значит, что в ней полностью отсутствуют биологические носители вируса, что, по идее, должно делать ее еще менее аллергенной. Иммунная система распознает эпитопы – «кусочки антигена», микроскопические частицы, на которые нацелен иммунитет. Этот термин и принцип действия отражен в названии вакцины - «ЭпиВакКорона».
Рекомендована для лиц в возрасте 18-60 лет, испытания на группе пожилых людей еще не завершены.
Побочные эффекты: повышенная температура, боль в месте укола. Серьезных побочных действий нет.
Последняя российская разработка. Дата регистрации – 20.02.2021.
У нее есть принципиальное преимущество: эта вакцина цельновирионная инактивированная, то есть в ее основе – «убитый» коронавирус SARS-CoV-2. По этому принципу работает большинство давно существующих и хорошо изученных прививок. Потенциально «КовиВак» должна обеспечить наибольшую защиту и полноценный иммунный ответ, потому что организм познакомится с цельным вирусом, а не только его фрагментом. «КовиВак» дает иммунной системе человека полный набор антигенов коронавируса, что, в свою очередь, произведет полный набор антител.
«КовиВак» дает иммунной системе человека полный набор антигенов коронавируса, что, в свою очередь, произведет полный набор антител.
Предварительно иммунологическая активность вакцины оценивается в 85% (то есть у 15% испытуемых не выработались необходимые антитела к 28-му дню после введения препарата, однако иммунный ответ может произойти позднее).
Инъекция «КовиВак» рекомендована лицам от 18 до 60 лет. Пока нет информации о том, как реагирует иммунная система пожилых людей на данную вакцину. Исследования на детях и пожилых ожидаются в апреле. Массовая вакцинация от коронавируса «КовиВаком» возможна уже этой весной.
Практически все вакцины (и российские, и иностранные) имеют одинаковые побочные эффекты: повышенная температура, общее недомогание, головная боль, боль в месте инъекции. Все эти симптомы возникают нечасто и являются нормальной реакцией организма на действие препарата.
Особенно внимательными нужно быть людям с острыми аллергическими реакциями. Некоторые вакцины содержат аллергены, поэтому, прежде чем отправиться на вакцинацию, рекомендуется убедиться, что нет индивидуальной непереносимости компонентов препарата.
Некоторые вакцины содержат аллергены, поэтому, прежде чем отправиться на вакцинацию, рекомендуется убедиться, что нет индивидуальной непереносимости компонентов препарата.
Вакцина, разработанная американской компанией Pfizer и ее немецким партнером BioNTech, была зарегистрирована в Евросоюзе первой. 9 ноября завершилась третья фаза клинических испытаний. Помимо стран ЕС, вакцина применяется в Австралии, Саудовской Аравии, Швейцарии, Норвегии, Исландии, Сербии и еще некоторых странах.
Эффективность разработки от Pfizer, подтвержденная последним исследованием, основанным на массовой вакцинации в Израиле (данные от 25.02.2021), составила 94%.
В ее основе – матричная РНК, кодирующая ген поверхностного, так называемого - спайкового S-белка коронавируса.
Вакцина американского производства. По своему составу очень похожа на препарат от Pfizer. Принцип действия тот же, что у BioNTech/Pfizer: препарат на основе матричной РНК (мРНК). Это генетический материал возбудителя, который воспроизводится искусственно в лабораторных условиях.
Принцип действия тот же, что у BioNTech/Pfizer: препарат на основе матричной РНК (мРНК). Это генетический материал возбудителя, который воспроизводится искусственно в лабораторных условиях.
Эффективность вакцины тоже оценивается в 94%, согласно предварительным данным клинического исследования фазы III. По решению компании, исследования продлятся до конца 2022 года.
Компания Moderna первой в мире начала проводить испытания собственной вакцины от коронавируса на людях. Уже сейчас вакцина от Moderna применяется в странах ЕС, Норвегии, Исландии, Гренландии и на Фарерских островах.
Векторная вакцина британско-шведского производства. В ее основе – аденовирус шимпанзе, переносящий ген S-белка коронавируса. По мнению ученых, тот факт, что при разработке вакцины использован аденовирус шимпанзе, а не человека, должен снизить риск аллергических реакций и выраженных побочных действий. Однако недостатком этого препарата, как и всех других векторных вакцин, можно назвать то, что сама технология новая, ранее не использовавшаяся в здравоохранении. Один из плюсов для производителей векторных препаратов – их скорость создания.
Один из плюсов для производителей векторных препаратов – их скорость создания.
Вакцина зарегистрирована для применения в странах Евросоюза. Разрешена для экстренного использования еще в 20 странах, включая Украину.
Инактивированная вакцина китайской биофармацевтической компании Sinovac Biotech, показывающая спорные результаты эффективности. По разным исследованиям, ее эффективность составляет от 50 до 91%, что в среднем существенно ниже, чем у европейских и российских аналогов. Применяется только на территории Китая. Еще 9 стран (Азербайджан, Боливия, Бразилия, Индонезия, Колумбия, Лаос, Турция, Чили, Уругвай) разрешили CoronaVac для экстренного применения.
Еще одна американская аденовирусная векторная вакцина. По итогам третьей фазы клинических испытаний, эффективность в разных регионах составила от 66 до 72%. Эффективность защиты от тяжелой формы коронавируса – 85% во всех группах испытуемых.
Еще десятки вакцин находятся в стадии разработки. Среди них и российский препарат - Sputnik Light. Ожидается, что новое изобретение будет провоцировать более быстрый, но менее продолжительный иммунный ответ – это поможет остановить распространение вируса и эпидемию. В отличие от «Спутника V», «Спутник Лайт» - однокомпонентная вакцина, основанная на успешном и уже применяемом препарате Центра имени Гамалеи.
Специальные предложения На фоне сообщений об обязательной вакцинации информация о видах прививок и названиях вакцин вызывает повышенный интерес.
11 августа 2020 года в мире появилась первая вакцина от SARS-CoV-2 – российский «Спутник V». С тех пор за два года таких препаратов в мире зарегистрировано более 10, только в России – 4. Чем отличаются, где распространены и насколько эффективны – основные вопросы планирующих прививаться. Мы постарались собрать всю доступную информацию, вот что у нас получилось.
При производстве препарата для прививки от коронавируса сегодня используется несколько основных подходов или «дизайнов»:
инактивированная вакцина,
рекомбинантная или векторная вакцина,
РНК-вакцина
ДНК-вакцина
Инактивированная вакцина – это препарат, в основе которого находится вирус (или частицы микроорганизма), который был выращен в лабораторных условиях, а после убит термическим или химическим способом. Антигенность таких вирусов существенно снижена, инфекционными (или способными быть причиной заболевания) они не являются. Одна из потенциальных проблем – недостаточная инактивация вируса.
Одна из потенциальных проблем – недостаточная инактивация вируса.
Векторная вакцина – это препарат, использующий вирус без возможности размножаться (вирус лишен гена размножения) с целью защиты организма от заражения. Такой вирус называют «вектором», его цель – транспортировка генетического материала вируса, против которого ставится прививка. Материалом этим, как правило, является белок. Наиболее часто для такой транспортировки используется вирус, извлекаемый из аденоидов, получаемый с его помощью препарат называют аденовирусной векторной вакциной.
РНК-вакцина не использует инактивированный вирус или его часть. Она создаётся на основе короткой генетической последовательности из генома вируса с помощью которой кодируется поверхностный белок (как правило), используемый вирусом для проникновения в клетку. То есть, не сам белок, а его «описание». Внутри клетки по этому описанию синтезируется сам белок, а уже на этот белок реагирует организм и вырабатывает иммунный ответ.
Сегодня ДНК-вакцины не применяют для лечения человека, против коронавируса регуляторами не зарегистрировала ни одного препарата данного типа, однако прогнозируется, что в будущем прививки такой вакциной будут довольно эффективны. В отличие от РНК-вакцины, синтез белка при использовании которой происходит в цитозоле, и не проникает в ядро клетки, ДНК-вакцине необходимо проникнуть именно в ядро клетки, где и синтезируется антиген. При внушительном наборе плюсов использования такой вакцины имеются два существенных минуса, больше похожие на угрозы: опасность интеграции чужеродной ДНК в геном клетки и «неспецифический иммунный ответ». Тем не менее, в данный момент ряд ДНК-вакцин против Covid-19 уже проходят разные фазы испытаний.
В отличие от РНК-вакцины, синтез белка при использовании которой происходит в цитозоле, и не проникает в ядро клетки, ДНК-вакцине необходимо проникнуть именно в ядро клетки, где и синтезируется антиген. При внушительном наборе плюсов использования такой вакцины имеются два существенных минуса, больше похожие на угрозы: опасность интеграции чужеродной ДНК в геном клетки и «неспецифический иммунный ответ». Тем не менее, в данный момент ряд ДНК-вакцин против Covid-19 уже проходят разные фазы испытаний.
Сегодня в России одобрено для использования 4 вакцины против Covid 19 SARS-CoV-2, все они созданы российскими учёными, большая часть в России же и производится:
Вакцина «Спутник V» НИЦЭМ им. Н. Ф. Гамалеи (Россия)
Вакцина «ЭпиВакКорона» (Россия)
Вакцина «КовиВак» производства ФНЦИРИП им. М. П. Чумакова (Россия)
Вакцина «Спутник Лайт» НИЦЭМ им. Н. Ф.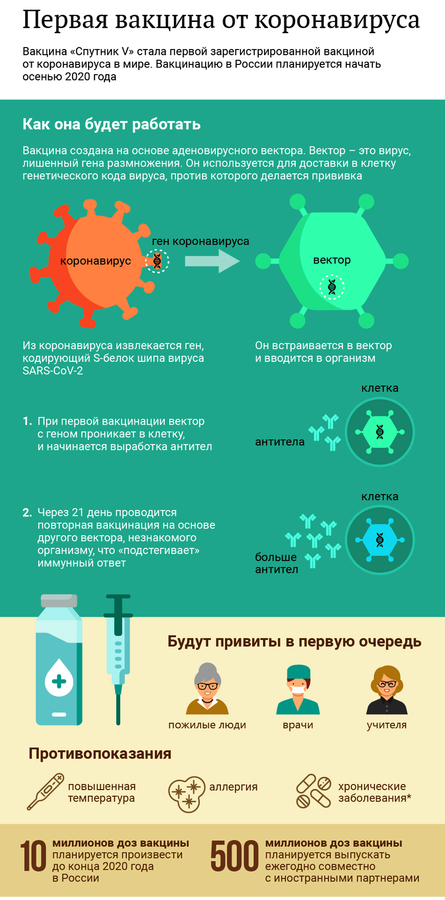 Гамалеи (Россия)
Гамалеи (Россия)
Кроме указанных выше российских производителей препаратов для прививок от коронавируса, получили одобрение регуляторов хотя бы одной страны следующие производители:
Pfizer/BioNTech (США-Германия) с вакциной BNT162b2/Comirnaty
Moderna (США) с вакциной mRNA-1273/Moderna
AstraZeneca (Великобритания) с вакциной Vaxzevria/Covishield
Sinopharm (Китай) с вакциной BBIBP-CorV/Sinopharm
Sinovac Biotech (Китай) с вакциной CoronaVac
CanSino Biologics (Китай) с вакциной Convidicea
BioNTech (Германия), Fosun Pharma (Китай), Pfizer (США) с вакциной BNT162b2/Comirnaty
Bharat Biotech (Индия) с вакциной Covaxin
НИИ ПББИ (Казахстан) с вакциной QazVac (QazCovid-in)
Janssen Pharmaceutica (Бельгия) и Johnson & Johnson (США) с вакциной Janssen
Anhui Zhifei Longcom Bio (Китай) с вакциной ZF2001
Все они получили разную степень распространения в разных странах, этого аспекта коснёмся ниже. В данный момент около 50 вакцин разных производителей проходит испытания в разных фазах.
В данный момент около 50 вакцин разных производителей проходит испытания в разных фазах.
В данный момент при отсутствии противопоказаний для вакцинации от Covid-19 каждый может быть привит любой из одобренных Минздравом вакцин. Тем не менее, в соцсетях и СМИ ежедневно появляются сообщения о ярко выраженных предпочтениях в пользу одной из вакцин.
Речь идёт о прививке вакциной КовиВак производства ФНЦИРИП им. М. П. Чумакова. Сообщения о появлении этой вакцины в пунктах вакцинации приводило к возникновению огромных очередей (иногда люди были готовы ждать более 5 часов) и окончанию запасов препарата.
СМИ попытались отыскать разгадку такой популярности, опросив ряд специалистов, но однозначного мнения найти не получилось.
Так вирусолог, доктор биологических наук, член-корреспондент РАН Сергей Нетесов предположил в интервью «Эхо Москвы», что «виной» ажиотажа служит высокая репутация производителя, оговорившись, что по эффективности вакцина уступает «Спутнику V».
Другой специалист, главврач 2-го диагностического отделения АО «Медицина» Максим Терский, предположил, что причиной феномена является распространенное среди населения мнение об «однокомпонентности», то есть полная вакцинация уже после первой прививки вакцины «КовиВак».
Молекулярный биолог, научный сотрудник МГУ Сергей Харитонов предположил, что «бестселлером» «КовиВак» стал из-за того, что в его основе старая технология, доказавшая свою эффективность ещё в советские времена.
Наше исследование указало на то, что невероятный уровень желающих прививаться именно «КовиВаком» мог возникнуть из-за высказываемых в социальных сетях так называемыми «лидерами мнений». Свой выбор они обосновывали «менее выраженными реакциями на вакцину», формированию иммунитета к «более широкому спектру» антигенов и рядом других клинически не подтверждённых тезисов. Вкупе с подогреваемым СМИ ажиотажем вокруг препарата и сообщениями о постоянном его окончании в пунктах вакцинации сформировался миф о его популярности, который позже «мутировал» в миф об эффективности.
Клинических доказательств влияния перечисленных выше плюсов на эффективность нет – слишком мало времени прошло для их появления, более того, самой вакцины «КовиВак» производится очень мало. В то же время вирусолог, профессор МГУ Алексей Аграновский сообщил РБК, что «КовиВак» менее эффективен против индийского дельта-штамма.
Ниже дадим краткую справку по вакцинам, одобренным хотя бы одним регулятором на сегодняшний день.
Первая в мире вакцина для прививки от вируса SARS-CoV-2 зарегистрирована в России 11.08.2020 в Национальном исследовательском центре эпидемиологии и микробиологии имени Н. Ф. Гамалеи. Сегодня препарат одобрен для применения более чем в 70 странах.
В основе двухкомпонентной вакцины лежит метод нереплицирующегося аденовирусного вектора. В процессе иммунизации делается 2 укола с промежутком в 21 день.
Федеральное бюджетное учреждение науки «Государственный научный центр вирусологии и биотехнологии Вектор» представил свою разработку 13 октября 2020 года, в гражданский оборот запущена в декабре 2020.
Двухкомпонентная вакцина, как и предшественник, создана на платформе аденовирусного вектора, в основе состава – три искусственно синтезированных белковых фрагмента, копирующие участки S-белка коронавируса.
Третья российская вакцина «КовиВак» была зарегистрирована в России 19 февраля 2021 года, промышленное производство препарата началось через месяц, в конце марта. Препарат отличается от «Спутника V» и «ЭпиВакКороны» используемой платформой. В его основе – традиционный метод разработки вакцин, она содержит инактивированный («убитый») вирус SARS-CoV-2, выращенный в лабораторных условиях.
Как отмечалось выше, прививка «КовиВак» оказалась невероятно популярной, несмотря на относительную «молодость», появление данного препарата в пунктах вакцинации неоднократно создавало большой ажиотаж и многочасовые очереди.
О регистрации вакцины «Спутник Лайт» объявлено 6 мая 2021 года.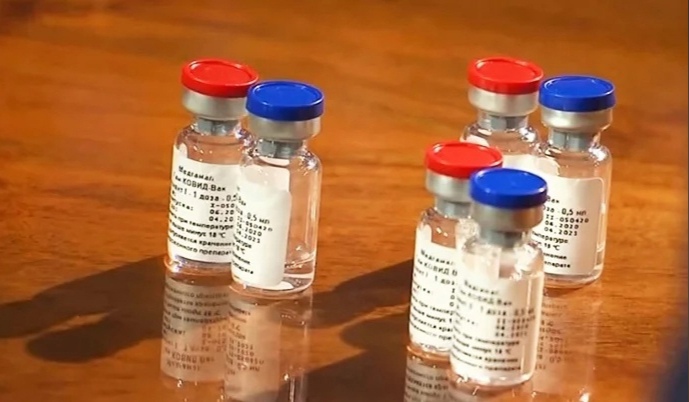 Создан препарат на платформе аденовирусного вектора человека. Отличие от предшественников – вакцина однокомпонентная, для вакцинации достаточно одного укола.
Создан препарат на платформе аденовирусного вектора человека. Отличие от предшественников – вакцина однокомпонентная, для вакцинации достаточно одного укола.
По сути, препарат «Спутник Лайт» является первым компонентом вакцины «Спутник V», что вызвало критику ряда эпидемиологов: специалисты считают уровень иммунизации недостаточным, а риск заболевания – высоким.
СМИ сообщали об использовании «Спутник Лайт» для вакцинации иностранных граждан – трудовых мигрантов.
Вакцина «AstraZeneca», разработанная в процессе сотрудничества с Оксфордским университетом, зарегистрирована в Великобритании 30 декабря 2020 года, а уже 30 марта 2021 года она была переименована в «Vaxzevria» без изменений состава. Эксперты считают, ребрендинг был вызван отказом ряда стран от использования вакцины в связи с появлением сообщений об образовании тромбов. Используемая платформа – векторный аденовирус шимпанзе.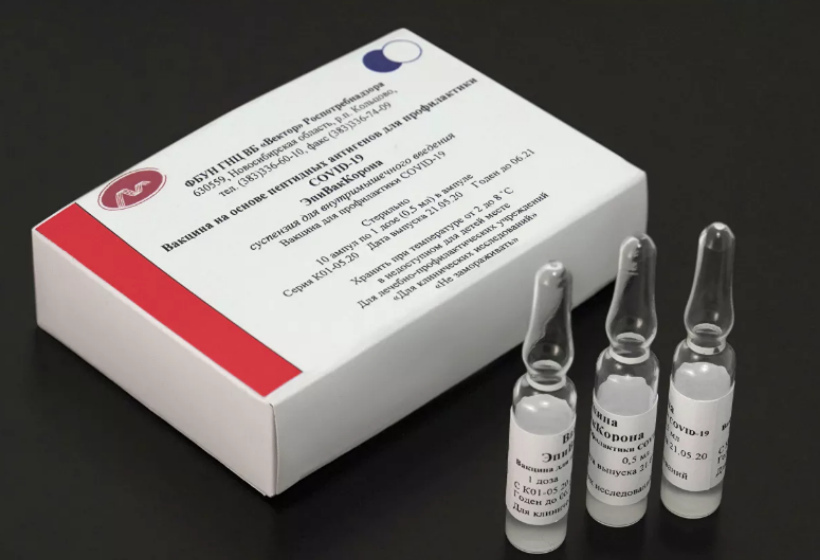
Препарат «Covishield» – название вакцины «AstraZeneca», которая производится для стран с низким уровнем дохода в Индии на заводе Serum Institute в Махараштре по лицензии разработчика. Данная вакцина активно используется на Украине.
В июле 2021 в СМИ появились сообщения о ряде случаев заражения вакцинированных «Covishield» штаммом «Дельта-плюс».
Препарат разработан американской Johnson & Johnson и бельгийской Janssen-Cilag International N.V., 27 февраля был зарегистрирован в США, 11 марта – в ЕС. Вакцина создана на платформе векторного аденовируса, возможна прививка одной или двумя компонентами.
Из-за случаев тромбоза вакциной отказалась пользоваться Дания, в США рекомендовали приостановить использование препарата, с 10го апреля он проходит дополнительные испытания на предмет появления побочных эффектов.
Вакцина немецкой биотехнологической компании BioNTech созданная на платформе мРНК в сотрудничестве с Pfizer (США) и Fosun Pharma (Китай). Первым государством, разрешившим использование данной вакцины на своей территории, стала Великобритания, позже она была одобрена в Бахрейне, США и Канаде.
Первым государством, разрешившим использование данной вакцины на своей территории, стала Великобритания, позже она была одобрена в Бахрейне, США и Канаде.
В июле 2021 года СМИ публиковали сообщения об опасности, исходящей от вакцины Pfizer со ссылкой на представителя Ассоциации врачей и хирургов США Джозеф Меркола: отмечалось, что препарат в 500 раз чаще приводит к летальным исходам, чем прививка от гриппа. Факты смерти после применения вакцины фиксировались в Норвегии, Германии, Израиле. Основная причина смертельных случаев у вакцинированных «Pfizer» – тромбоз.
Вакцина Moderna разрешена для использования в США 18 декабря 2020, в Канаде – 23 декабря, на территории ЕС – января 2021. Используемая платформа – РНК. Вакцинация проходит в два этапа с промежутком в 28 дней.
В июле 2021 в СМИ сообщалось о предупреждениях европейского регулятора в отношении вакцины Moderna, в частности, речь шла о побочных эффектах, возможности развития миокардита и перикардита у привившихся.
Препарат зарегистрирован 25 февраля в Китае, в разработке кроме Sinopharm принимали участие China National Biotec Group и знаменитый теперь на весь мир Wuhan Institute of Biological Products Co., Ltd. Платформа – инактивированный вирус, прививка делается в два приёма.
У компании есть ещё одна вакцина от Covid-19, разработанная на аналогичной платформе – BBIBP-CorV, но в «соавторах» вместо Wuhan Institute выступил Beijing Institute of Biological Products.
До октября 2021 компания предоставит 60 миллионов доз вакцины международному механизму COVAX (программа поставки вакцины от Covid-19 менее благополучным странам).
Препарат зарегистрирован 6.02.2021 в Китае биофармацевтическая компанией-разработчиком и производителем Sinovac Biotech. Вакцина создана на традиционной платформе инактивированного вируса.
По сообщениям СМИ, побочные реакции, при использовании вакцины, были незначительными, в частности такую оценку дают привившиеся в Турции и на Украине.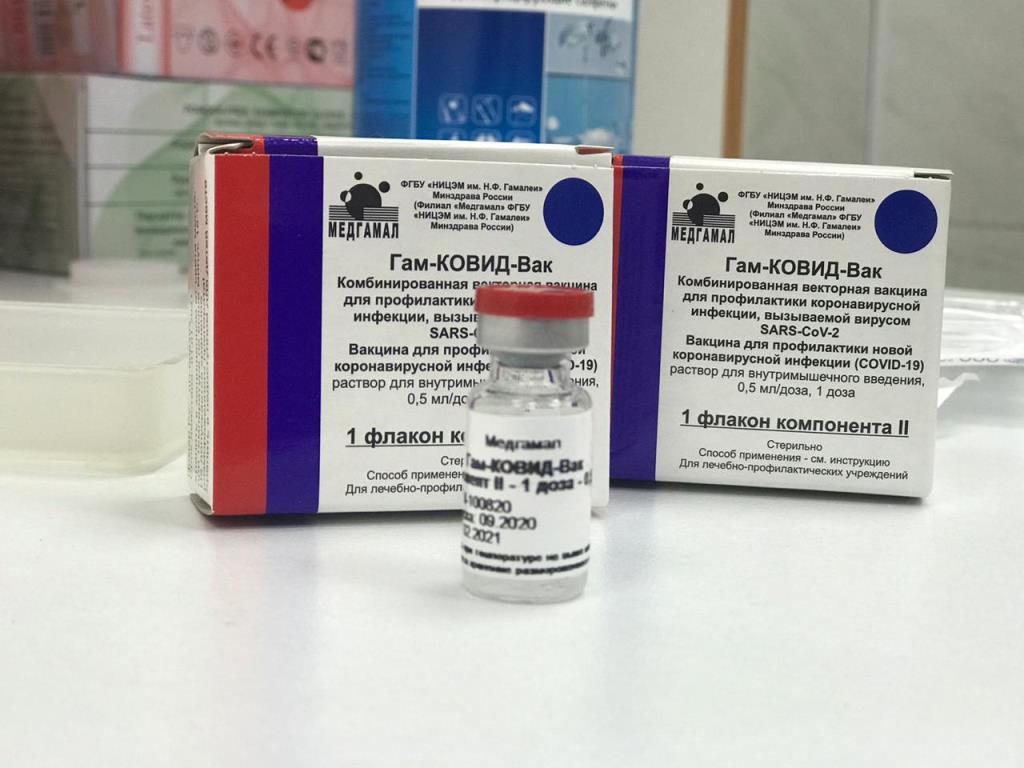 Компания Sinovac, как и коллеги из Sinopharm, участвует в программе COVAX, предоставит международному механизму помощи 50 миллионов доз своей вакцины.
Компания Sinovac, как и коллеги из Sinopharm, участвует в программе COVAX, предоставит международному механизму помощи 50 миллионов доз своей вакцины.
Convidicea – коммерческое название вакцины AD5-nCOV, разработанной и производимой китайской CanSino Biologics на платформе вирусного вектора с использованием аденовируса Ad5.
Препарат зарегистрирован 25 июня 2020 года, производится в Китае, распространяется кроме Китая в Венгрии, Пакистане и Мексике.
Convidicea – первая иностранная вакцина, документы на регистрацию которой поданы в России.
Индийская фармацевтическая компания зарегистрировала препарат 3го января 2021 года. Двухкомпонентная вакцина создана на платформе инактивированного вируса, в работе над ней принимал участие Индийский совет медицинских исследований.
Страны, одобрившие применение Covaxin: Иран, Индия, Зимбабве, в июне 2021 появились сообщения о приостановке закупки вакцины Бразилией из-за коррупционного скандала при заключении контракта.
Двухкомпонентная вакцина на платформе инактивированного вируса КазВак зарегистрирована 11 января 2021 года. Интервал между компонентами – 21 день. Специально построенный для выпуска препарата завод обеспечит выпуск 500-600 000 доз в месяц осенью 2021 года, до тех пор вакцина будет выпускаться на базе Научно-исследовательского института проблем биологической безопасности Министерства образования и науки Республики Казахстан.
Препарат создан на белковой основе изолята Ухань-1 путем создания рекомбинатного белка NCP-RBD коронавируса SARS-CoV-2 компанией Anhui Zhifei Longcom Biopharmaceutical в сотрудничестве с Institute of Microbiology (IMCAS), зарегистрирован 1го марта 2021 года в Узбекистане.
В Узбекистане вакцина получила аббревиатуру ZF-UZ-VAС2001. Титр антител после прививки тремя компонентами достигал 200 единиц, что сравнимо с показателями привитых другими вакцинами. По состоянию на 9 июля в Узбекистане использовано более 3,2 миллиона доз вакцины.
По состоянию на 9 июля в Узбекистане использовано более 3,2 миллиона доз вакцины.
| Название | Производитель | Где используют вакцину для прививки |
| Спутник V | НИЦЭМ им. Н. Ф. Гамалеи (Россия) | Россия + около70 стран |
| ЭпиВакКорона | ГНЦВБ «Вектор» (Россия) | Россия, Туркменистан |
| КовиВак | ФНЦИРИП им. М. П. Чумакова (Россия) | Россия |
| Спутник Лайт | НИЦЭМ им. Н. Ф. Гамалеи (Россия) | Россия |
| Comirnaty | Pfizer (США)/BioNTech (Германия) | Около 50 стран, включая ЕС, США |
| MRNA-1273 | Moderna (США) | Около 20 стран, включая США, ЕС, Канада |
| Covishield | AstraZeneca (Великобритания) | Около 60 стран, включая США, ЕС, Канада |
| Sinopharm | Sinopharm (Китай) | Аргентина, Бахрейн, Венгрия, Египет, Зимбабве, Иран, Ирак, Иордания, Камбоджа, Китай и другие |
| CoronaVac | Sinovac (Китай) | Более 20 стран, включая Китай |
| Convidicea | CanSino Biologics (Китай) | Китай, Мексика, Пакистан, Венгрия |
| Covaxin | Bharat Biotech (Индия) | Иран, Индия, Зимбабве |
| QazCovid-in | НИИ ПББ (Казахстан) | Казахстан |
| Janssen | Johnson & Johnson (США) | Более 10 стран, включая США, ЕС, Канада |
| ZF2001 | Anhui Zhifei Loncom Biofharmaceutical (Китай) | Китай, Узбекистан |
Важное обновление: Медицинские учреждения
Центры по контролю и профилактике заболеваний (CDC) обновили избранные способы эффективной работы систем здравоохранения в ответ на вакцинацию против COVID-19. Учить больше
Учить больше
Обзор вакцин против COVID-19
Обновлено 1 ноября 2022 г.
Распечатать
Что вам нужно знать
В США имеется четыре одобренных или разрешенных вакцины.
Эти вакцины вводятся маленьким детям в виде укола в мышцу плеча или бедра. Ингредиенты вакцины против COVID-19 считаются безопасными для большинства людей. Почти все ингредиенты COVID-19вакцины — это ингредиенты, содержащиеся во многих продуктах питания — жирах, сахаре и солях. Ни одна из вакцин против COVID-19 не влияет на нашу ДНК и не взаимодействует с ней . В вакцины включены следующие , а не :

После того, как организм выработает иммунный ответ, он выбрасывает все ингредиенты вакцины, как если бы он выбрасывал любое вещество, которое больше не нужно клеткам. Этот процесс является частью нормального функционирования организма.
Дозировка: Количество доз вакцины против COVID-19 может варьироваться в зависимости от типа вводимой вакцины или возраста реципиента.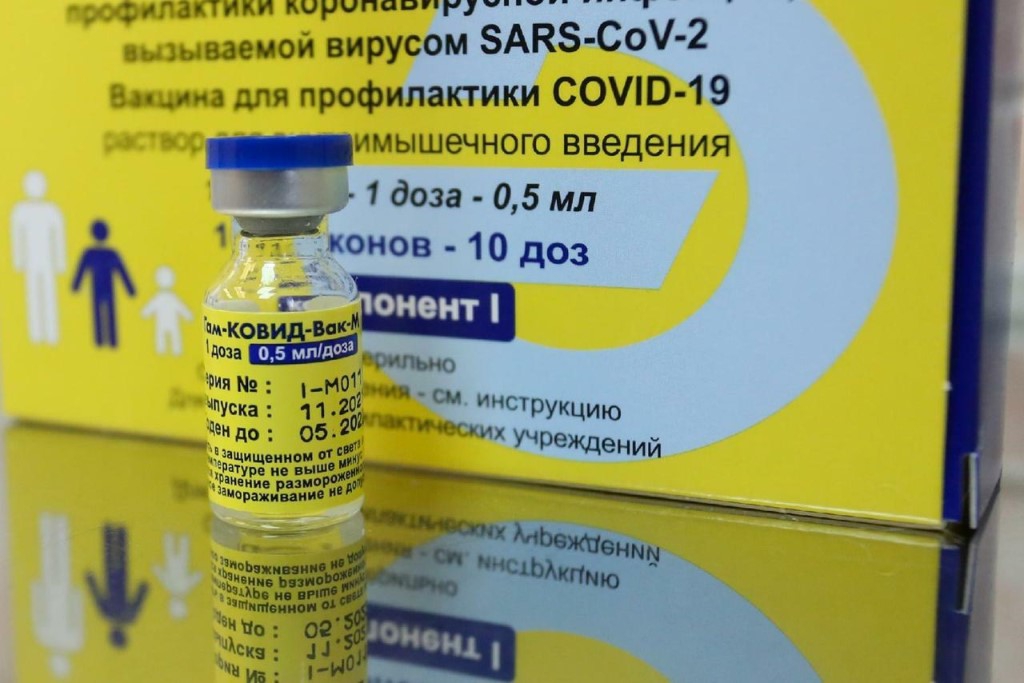
COVID-19дозы вакцины и ревакцинации, а также сроки вакцинации отличаются для людей с умеренным или тяжелым иммунодефицитом.
Вакцины для иммунодефицита
mRNA используют мРНК, созданную в лаборатории, чтобы научить наши клетки производить белок или даже часть белка, который запускает иммунную систему. реакция внутри нашего тела. мРНК из вакцин расщепляется в течение нескольких дней после вакцинации и выбрасывается из организма.
Узнайте о рекомендуемом времени между вакцинами Pfizer-BioNTech против COVID-19 и бустерами для людей:
6 месяцев–17 лет 18 лет и старше
Этикетка вакцины Pfizer-BioNTech остается для людей в возрасте от 6 месяцев до 11 лет, поскольку вакцина одобрена FDA, но еще не одобрена для этих возрастных групп.
Вакцина Pfizer-BioNTech против COVID-19 для детей в возрасте от 6 месяцев до 11 лет содержит только следующие ингредиенты:
Тип ингредиента
Тип ингредиента
Тип ингредиента
Ингредиент
Ингредиент
Состав
Назначение
Назначение
Цель
Мессенджер рибонуклеиновой кислоты (мРНК)
Тип ингредиента
Рибонуклеиновая кислота (мРНК)
Ингредиент
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19.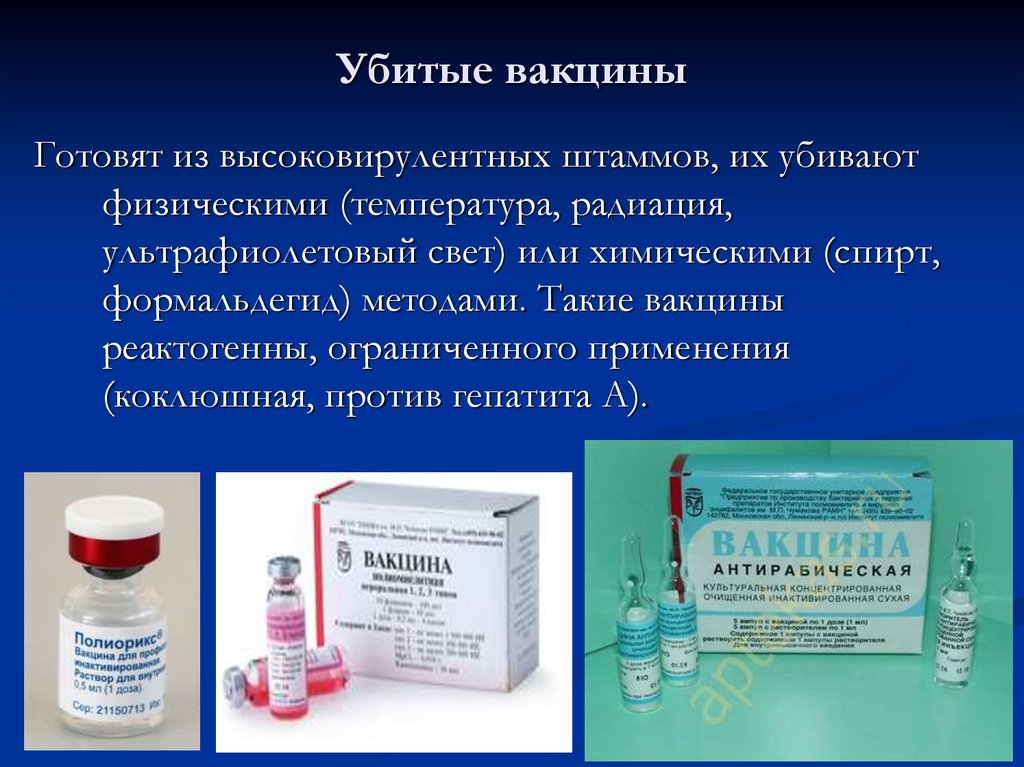 Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Назначение
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19.. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Липиды (жиры)
Тип ингредиента
Липиды (жиры)
Ингредиент
Работайте вместе, чтобы помочь мРНК проникнуть в клетки.
Назначение
Работайте вместе, чтобы помочь мРНК проникнуть в клетки.
Сахар и стабилизаторы кислот
Тип ингредиента
Сахар и стабилизаторы кислот
Ингредиент
Работайте вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, замораживается, транспортируется и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Назначение
Работайте вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, замораживается, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Мессенджер рибонуклеиновой кислоты (мРНК):
Нуклеозид-модифицированная мРНК, кодирующая гликопротеин вирусного шипа (S) SARS-CoV-2
вирус, вызывающий COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Липиды (жиры):
Цель
Совместная работа поможет мРНК проникнуть в клетки.
Сахар и стабилизаторы кислот:
Цель
Работать вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, замораживается, транспортируется и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Вакцина Pfizer-BioNTech против COVID-19 для подростков и взрослых в возрасте 12 лет и старше содержит только следующие ингредиенты:
Тип ингредиента
Тип ингредиента
Тип ингредиента
Ингредиент
Ингредиент
Ингредиент
Назначение
Назначение
Цель
Мессенджер рибонуклеиновой кислоты (мРНК)
Тип ингредиента
Информационная рибонуклеиновая кислота (мРНК)
Ингредиент
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Назначение
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19.в будущем.
Липиды (жиры)
Тип ингредиента
Липиды (жиры)
Ингредиент
Работайте вместе, чтобы помочь мРНК проникнуть в клетки.
Назначение
Работайте вместе, чтобы помочь мРНК проникнуть в клетки.
Сахар и стабилизаторы кислот
Тип ингредиента
Сахар и стабилизаторы кислот
Ингредиент
Работайте вместе, чтобы помочь сохранить вакцину в хорошем состоянии (молекулы остаются стабильными), пока вакцина производится, замораживается, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту.
Цель
Работайте вместе, чтобы помочь сохранить вакцину в хорошем состоянии (молекулы остаются стабильными), пока вакцина производится, замораживается, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Информационные бюллетени для реципиентов и лиц, осуществляющих уход. Ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:
Мессенджер рибонуклеиновой кислоты (мРНК):
Нуклеозид-модифицированная мРНК, кодирующая гликопротеин вирусного шипа (S) SARS-CoV-2
вирус, вызывающий COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Липиды (жиры):
Цель
Совместная работа поможет мРНК проникнуть в клетки.
Соль и сахар:
Цель
Работать вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, замораживается, транспортируется и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Информационные бюллетени для реципиентов и лиц, осуществляющих уход — ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:
Узнайте о рекомендуемом времени между Moderna COVID-19вакцины и бустеры для людей:
6 месяцев–17 лет 18 лет и старше
продаваться под торговой маркой Spikevax. Формула вакцины с изменением названия не менялась.
Формула вакцины с изменением названия не менялась.
Название вакцины Moderna остается для людей в возрасте от 6 месяцев до 17 лет, поскольку вакцина одобрена FDA, но еще не одобрена для этих возрастных групп.
Вакцина Moderna против COVID-19 для всех в возрасте 6 месяцев и старше содержит только следующие ингредиенты:
Тип ингредиента
Тип ингредиента
Тип ингредиента
Ингредиент
Ингредиент
Состав
Назначение
Назначение
Цель
Мессенджер рибонуклеиновой кислоты (мРНК)
Тип ингредиента
Информационная рибонуклеиновая кислота (мРНК)
Ингредиент
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. . Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Назначение
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Липиды (жиры)
Тип ингредиента
Липиды (жиры)
Ингредиент
Работайте вместе, чтобы помочь мРНК проникнуть в клетки.
Назначение
Работайте вместе, чтобы помочь мРНК проникнуть в клетки.
Соль, сахар, стабилизаторы кислот и кислоты
Тип ингредиента
Соль, сахар, стабилизаторы кислот и кислоты
Ингредиент
Работайте вместе, чтобы помочь сохранить вакцину в хорошем состоянии (молекулы остаются стабильными), пока вакцина производится, замораживается, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту.
Назначение
Работайте вместе, чтобы помочь сохранить вакцину в хорошем состоянии (молекулы остаются стабильными), пока вакцина производится, замораживается, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Информационные бюллетени для реципиентов и лиц, осуществляющих уход - Ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:
Мессенджер рибонуклеиновой кислоты (мРНК):
Нуклеозидно-модифицированная мРНК, кодирующая гликопротеин вирусного шипа (S) SARS-CoV-2
Цель
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Липиды (жиры):
Цель
Совместная работа поможет мРНК проникнуть в клетки.
Соль, сахар, стабилизаторы кислот и кислоты:
Цель
Работать вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, замораживается, транспортируется и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Информационные бюллетени для реципиентов и лиц, осуществляющих уход — Ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:
1 Если у вас аллергия на полиэтиленгликоль (ПЭГ), вам следует , а не получить вакцину Pfizer-BioNTech или Moderna против COVID-19. Если у вас аллергия на полисорбат, вам следует , а не , получить Novavax или J&J/Janssen COVID-19.вакцина. Поговорите со своим врачом о ваших вариантах.
Если у вас аллергия на полисорбат, вам следует , а не , получить Novavax или J&J/Janssen COVID-19.вакцина. Поговорите со своим врачом о ваших вариантах.
Вакцины белковых субъединиц содержат фрагменты (белки) вируса, вызывающего COVID-19. Кусочки вируса представляют собой шиповидный белок. Вакцина Novavax COVID-19 содержит еще один ингредиент, называемый адъювантом. Это помогает иммунной системе реагировать на этот шиповидный белок. Узнав, как реагировать на белок-шип, иммунная система сможет быстро реагировать на настоящий белок-шип вируса и защитить вас от COVID-19..
Узнайте о рекомендуемом времени между вакцинами Novavax COVID-19 и бустерами для людей:
12–17 лет18 лет и старше
3 получите моновалентный бустер Novavax , если вы не можете или не хотите получать обновленный (бивалентный) бустер COVID-19 от Pfizer или Moderna и , вы отвечаете следующим требованиям:
Вакцина Novavax COVID-19 содержит только следующие ингредиенты:
Тип ингредиента
Тип ингредиента
Тип ингредиента
Ингредиент
Ингредиент
Состав
Назначение
Назначение
Назначение
Белок
Тип ингредиента
Белок
Ингредиент
Вызывает иммунный ответ, помогающий защитить организм от заражения COVID-19 в будущем.
Назначение
Вызывает иммунный ответ, помогающий защитить организм от заражения COVID-19 в будущем.
Липиды (жиры)
Тип ингредиента
Липиды (жиры)
Ингредиент
Работайте вместе, чтобы помочь рекомбинантному шиповидному белку проникнуть в клетки.
Назначение
Работайте вместе, чтобы помочь рекомбинантному шиповидному белку проникнуть в клетки.
Адъювант
Тип ингредиента
Адъювант
Ингредиент
Способствует активации клеток врожденной иммунной системы.
Назначение
Способствует активации клеток врожденной иммунной системы.
Соли, сахар и кислоты
Тип ингредиента
Соли, сахара и кислоты
Ингредиент
Работайте вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту.
Вакцина может также содержать очень небольшое количество ингредиентов, оставшихся на стадии производства, которые можно найти в информационном бюллетене EUA.
Назначение
Работайте вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту.
Вакцина также может содержать очень небольшое количество ингредиентов, оставшихся на стадии производства, которые можно найти в информационном бюллетене EUA.
Информационный бюллетень для реципиентов - Ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:
Белок:
Рекомбинантный шиповидный белок SARS-CoV-2
Назначение
Вызывает иммунный ответ, помогающий защитить организм от заражения COVID-19 в будущем.
Липиды (жиры):
Цель
Совместная работа поможет рекомбинантному шиповидному белку проникнуть в клетки.
Адъювант:
Фракция-А и Фракция-С Quillaja saponaria Экстракт Молины
Назначение Способствует активации клеток врожденной иммунной системы.
Соли, сахар и кислоты:
Цель
Работать вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Вакцина также может содержать очень небольшое количество ингредиентов, оставшихся на стадии производства, которые можно найти в информационном бюллетене EUA.
Информационный бюллетень для реципиентов - Ингредиенты, способ введения вакцины и другие подробности от FDA:
Прочая клиническая информация:
В вакцинах против вирусного вектора используется безвредная модифицированная версия другого вируса (вирус-переносчик), а не вирус, вызывающий COVID-19. Вирус-переносчик дает нашим клеткам важные инструкции о том, как распознавать вирус, вызывающий COVID-19, и бороться с ним.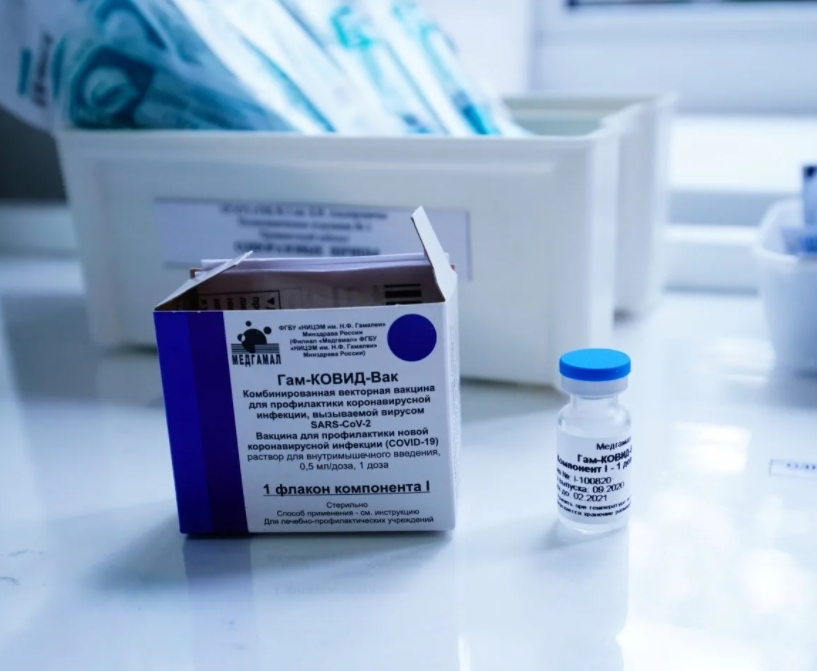
Узнайте о рекомендуемом времени между вакцинацией J&J/Janssen COVID-19 и бустерами для людей:
18 лет и старше
3 В большинстве случаев вакцины Pfizer-BioNTech, Moderna или Novavax COVID-19 рекомендуются вместо вакцин J&J/Janssen COVID-19.вакцины для первичной и бустерной вакцинации из-за риска серьезных побочных эффектов. Получатели вакцины должны поговорить со своим лечащим врачом о том, какая вакцина подходит именно вам. Они должны быть проинформированы о рисках и преимуществах вакцинации J&J/Janssen против COVID-19. Вакцина J&J/Janssen против COVID-19 может быть рассмотрена в некоторых ситуациях, в том числе для лиц, у которых:
Вакцина J&J/Janssen против COVID-19 содержит только следующие ингредиенты:
Тип ингредиента
Тип ингредиента
Тип ингредиента
Ингредиент
Ингредиент
Состав
Назначение
Назначение
Назначение
Безвредная версия вируса, не связанного с вирусом COVID-19
Тип ингредиента
Безвредная версия вируса, не связанного с COVID-19вирус
Ингредиент
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19.в будущем.
Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19.в будущем.
Назначение
Содержит инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заражения COVID-19 в будущем.
Сахара, соли, кислоты и стабилизаторы кислот
Тип ингредиента
Сахара, соли, кислоты и стабилизаторы кислот
Ингредиент
Работайте вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту.
Назначение
Работайте вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту.
Информационные бюллетени для реципиентов и лиц, осуществляющих уход - Ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:
Безвредная версия вируса, не связанного с вирусом COVID-19:
Рекомбинантный, неспособный к репликации вектор Ad26, кодирующий стабилизированный вариант белка SARS-CoV-2 Spike (S)
Назначение
Предоставляет инструкции, которые организм использует для создания безвредного фрагмента белка из вируса, вызывающего COVID-19. Этот белок вызывает иммунный ответ, который помогает защитить организм от заболевания COVID-19 в будущем.
Этот белок вызывает иммунный ответ, который помогает защитить организм от заболевания COVID-19 в будущем.
Сахара, соли, кислоты и стабилизаторы кислот:
Цель
Работать вместе, чтобы помочь сохранить молекулы вакцины стабильными, пока вакцина производится, отгружается и хранится до тех пор, пока она не будет готова для введения реципиенту вакцины.
Информационные бюллетени для реципиентов и лиц, осуществляющих уход — Ингредиенты, способ введения вакцины и другие сведения от FDA:
Прочая клиническая информация:

Вакцины против COVID-19 прошли и будут проходить самый интенсивный мониторинг безопасности в истории США. Данные о сотнях миллионов вакцин против COVID-19, уже введенных в Соединенных Штатах, и о миллиардах вакцин, введенных во всем мире, показывают, что они безопасны и эффективны.
Побочные эффекты
 Иногда они могут повлиять на способность человека заниматься повседневными делами.
Иногда они могут повлиять на способность человека заниматься повседневными делами. Нежелательные явления
 TTS возникает со скоростью около 4 случаев на миллион доз Janssen's Johnson and Johnson и приводит к летальному исходу. Из-за этого риска вакцинация от COVID-19предпочтительны вакцины, отличные от вакцины J&J/Janssen.
TTS возникает со скоростью около 4 случаев на миллион доз Janssen's Johnson and Johnson и приводит к летальному исходу. Из-за этого риска вакцинация от COVID-19предпочтительны вакцины, отличные от вакцины J&J/Janssen. Узнайте больше о мониторинге безопасности вакцин после того, как вакцина будет одобрена или одобрена для использования.
Узнайте о получении вакцины
Получение вакцины против COVID-19
Связанные страницы
Информация о вакцине против COVID-19 в США
Comirnaty Information Информационные бюллетени Pfizer-BioNTech Информационные бюллетени Pfizer-BioNTech Переводы Información sobre las vacunas para el COVID-19
23 августа 2021 года FDA объявило о первом одобрении вакцины против COVID-19. Вакцина была известна как вакцина Pfizer-BioNTech COVID-19, а одобренная вакцина продается как Comirnaty для профилактики COVID-19.у лиц в возрасте 12 лет и старше.
Вакцина была известна как вакцина Pfizer-BioNTech COVID-19, а одобренная вакцина продается как Comirnaty для профилактики COVID-19.у лиц в возрасте 12 лет и старше.
Comirnaty — это моновалентная вакцина против COVID-19, одобренная для использования в виде двух доз первичной серии для профилактики COVID-19 у лиц в возрасте 12 лет и старше. Он также разрешен для использования в экстренных случаях для введения третьей первичной дозы лицам в возрасте 12 лет и старше с определенными видами иммунодефицита.
Вакцина Pfizer-BioNTech COVID-19 — это моновалентная вакцина против COVID-19, разрешенная для использования в экстренных случаях для профилактики COVID-19.как:
Вакцина Pfizer-BioNTech COVID-19, бивалентная, разрешена для использования для профилактики COVID-19 у лиц в возрасте 5 лет и старше в виде однократной бустерной дозы, вводимой не менее чем через 2 месяца после:
В консультации с FDA CDC обновляет инструкции по применению в экстренных случаях, чтобы предоставить информацию об основных, дополнительных и бустерных дозах вакцин Pfizer-BioNTech против COVID-19 для определенных лиц.
| Информация | Последнее обновление |
|---|---|
| Вкладыш (фиолетовая крышка) | 8 июля 2022 г. |
| Вкладыш (серая крышка) | 8 июля 2022 г. |
| Нормативная информация | 25 августа 2022 г. |
| Часто задаваемые вопросы для Comirnaty (мРНК вакцины против COVID-19) (испанский) | 8 февраля 2022 г. |
| Инструкции по применению в чрезвычайных ситуациях, выпущенные CDC (обновленные) | 11 февраля 2022 г. |
| Материал | Аудитория | Вакцина Назначение | Группа получателей вакцины | Последнее обновление |
|---|---|---|---|---|
| Pfizer-BioNTech вакцина против COVID-19 Презентации Настенная диаграмма | Поставщики медицинских услуг | Бивалентный бустер | Все | 15 ноября 2022 г. |
| Информационный бюллетень | Поставщики медицинских услуг | Основная серия | От 6 месяцев до 4 лет, темно-бордовая крышка (необходимо разбавлять) | 22 ноября 2022 г. |
| Уважаемый поставщик медицинских услуг! Письмо | Поставщики медицинских услуг | Основная серия | От 6 месяцев до 4 лет, темно-бордовая крышка (необходимо разбавлять) | 17 июня 2022 г. |
| Информационный бюллетень | Реципиенты и опекуны | Основная серия | от 6 месяцев до 4 лет | 22 ноября 2022 г. |
| Уважаемый поставщик медицинских услуг! Письмо | Поставщики медицинских услуг | Основная серия и бивалентный бустер | от 5 до 11 лет, оранжевая шапочка (необходимо разбавлять) | 12 октября 2022 г. |
| Информационный бюллетень | Поставщики медицинских услуг | Основная серия | от 5 до 11 лет, оранжевая шапочка (необходимо разбавлять) | 22 ноября 2022 г. |
| Информационный бюллетень | Поставщики медицинских услуг | Бивалентный бустер | от 5 до 11 лет, оранжевая шапочка (необходимо разбавлять) | 22 ноября 2022 г. |
| Информационный бюллетень | Реципиенты и опекуны | Основная серия и Бустер | от 5 до 11 лет | 22 ноября 2022 г. |
| Уважаемый поставщик медицинских услуг! Письмо | Поставщики медицинских услуг | Бивалентный бустер | 12 лет и старше | 31 августа 2022 г. |
| Информационный бюллетень | Поставщики медицинских услуг | Основная серия | 12 лет и старше, фиолетовая крышка (состав PBS, необходимо развести) | 22 ноября 2022 г. |
| Информационный бюллетень | Поставщики медицинских услуг | Основная серия | 12 лет и старше, серая шапочка (препарат Трис, без разбавления) | 22 ноября 2022 г. |
| Информационный бюллетень | Поставщики медицинских услуг | Бивалентный бустер | 12 лет и старше, серая рамка | 22 ноября 2022 г. |
| Информационный бюллетень | Получатели и опекуны | Основная серия и бивалентный бустер | 12 лет и старше, пурпурно-серая кайма | 22 ноября 2022 г. |
| Часто задаваемые вопросы о вакцине Pfizer-BioNTech против COVID-19 | Все | Все | Все | 16 февраля 2022 г. |
| Информация | Дата |
|---|---|
| Письмо о предоставлении поправки к EUA | 22 ноября 2022 г. |
| Меморандум о решении | 12 октября 2022 г. |
| Письмо о предоставлении поправки к EUA | 18 октября 2022 г. |
| Доверенность (переизданная) | 12 октября 2022 г. |
| Меморандум о решении | 31 августа 2022 г. |
| Письмо о предоставлении поправки к EUA | 28 июня 2022 г. |
| Меморандум о решении | 17 июня 2022 г. |
| Письмо о предоставлении поправки к EUA | 1 июня 2022 г. |
| Меморандум о решении | 17 мая 2022 г. |
| Письмо о предоставлении поправки к EUA | 26 апреля 2022 г. |
| Письмо о предоставлении поправки к EUA | 13 апреля 2022 г. |
| Меморандум о решении | 28 марта 2022 г. |
| Письмо о предоставлении поправки к EUA | 31 января 2022 г. |
| Приложение к меморандуму о решении | 6 января 2022 г. |
| Меморандум о решении | 30 декабря 2021 г. |
| Меморандум о решении | 8 декабря 2021 г. |
| Приложение к меморандуму о решении | 19 ноября 2021 г. |
| Меморандум о решении | 19 ноября 2021 г. |
| Меморандум о решении | 29 октября 2021 г. |
| Информация о заседании Консультативного комитета | 26 октября 2021 г. |
| Меморандум о решении | 20 октября 2021 г. |
| Меморандум о решении | 24 сентября 2021 г. |
| Информация о собрании Консультативного комитета | 17 сентября 2021 г. |
| Письмо о предоставлении поправки к EUA | 1 сентября 2021 г. |
| Письмо о согласовании | 22 августа 2021 г. |
| Меморандум о решении | 12 августа 2021 г. |
| Письмо о предоставлении поправки к EUA | 19 мая 2021 г. |
| Меморандум о решении FDA | 10 мая 2021 г. |
| Письмо о предоставлении поправки к EUA | 6 апреля 2021 г. |
| Письмо о предоставлении поправки к EUA | 22 января 2021 г. |
| Письмо о предоставлении поправки к EUA | 6 января 2021 г. |
| Меморандум о решении FDA | 11 декабря 2020 г. |
| Информация о заседании Консультативного комитета | 10 декабря 2020 г. |
| Информация | Дата |
|---|---|
| Пресс-релиз | 12 октября 2022 г. |
| Пресс-конференция | 31 августа 2022 г. |
| Пресс-релиз | 31 августа 2022 г. |
| Пресс-конференция | 17 июня 2022 г. |
| Пресс-релиз | 17 июня 2022 г. |
| Интернет-трансляция Консультативного комитета | 15 июня 2022 г. |
| Пресс-релиз | 17 мая 2022 г. |
| Звонок для прессы | 29 марта 2022 г. |
| Пресс-релиз | 29 марта 2022 г. |
| Пресс-релиз | 3 января 2022 г. |
| Пресс-релиз | 19 ноября 2021 г. |
| Пресс-релиз | 29 октября 2021 г. |
| Пресс-конференция | 29 октября 2021 г. |
| Интернет-трансляция Консультативного комитета | 26 октября 2021 г. |
| Пресс-релиз | 20 октября 2021 г. |
| Звонок для прессы | 20 октября 2021 г. |
| Пресс-релиз | 22 сентября 2021 г. |
| Интернет-трансляция Консультативного комитета | 17 сентября 2021 г. |
| Пресс-релиз | 23 августа 2021 г. |
| Пресс-релиз | 12 августа 2021 г. |
| Коротко о FDA | 19 мая 2021 г. |
| Пресс-релиз | 10 мая 2021 г. |
| Пресс-конференция | 10 мая 2021 г. |
| Пресс-релиз | 25 февраля 2021 г. |
| Пресс-релиз | 11 декабря 2020 г. |
| Пресс-конференция | 11 декабря 2020 г. |
| Интернет-трансляция Консультативного комитета | 10 декабря 2020 г. |
| Информационный бюллетень | Группа получателей вакцины | Язык |
|---|---|---|
| HOJA INFORMATIVA PARA RECEPTORES Y CUIDADORES SOBRE LA VACUNA CONTRA EL COVID-19 DE PFIZER-BIONTECH PARA PREVENIR LA ENFERMEDAD DEL CORONAVIRUS 2019 (COVID-19) PARA USO EN NIÑOS DE 6 MESES A 4 2007 | 6 месяцев - 4 года | Español (испанский) |
| 面向 6 个 至 至 4 岁 的 个体 使用 的 用 于 预防 2019 年冠状 病 病 (Covid-19) 的 生物 技术 技术 Covid-19 疫苗 受种者 和 人员 情况 说明书 | 6 месяцев - 4 года | 中文 (китайский, упрощенный) |
| 6 개월 에서 4 세 사이 의 에 사용 하기 위한 위한 위한 2019 코로나 질병 질병 (Covid-19) 예방 위한 화이자 화이자-바이오 엔텍 Covid-19 백신 대한 수혜자 간병인 을 위한 팩트 시트 | 6 месяцев - 4 года | 한국어 (корейский) |
| ИНФОРМАЦИОННЫЙ БЮЛЛЕТЕНЬ PARA SA MGA TATANGGAP AT MGA NAG-AALAGA TUNGKOL SA BAKUNANG PFIZER-BIONTECH COVID-19 UPANG MAIWASAN ANG CORONAVIRUS DISEASE 2019(COVID-19) PARA SA PAGGAMIT SA MGA INDIBIDWAL 6 NA BUWAN HANGGANG 4 NA TAONG GULANG | 6 месяцев - 4 года | Тагальский (тагальский) |
| PHIẾU THỰC TẾ DÀNH CHO NGƯỜI NHẬN VÀ NGƯỜI CHĂM SÓC VỀ THUỐC CHỮA BỆNH PFIZER-BIONTECH COVID-19 ĐỂ PHÒNG NGỪA BỆNH HẠI LÃO HÓA 2019 (COVID-19) ĐỂ SỬ DỤNG CHO CÁ NHÂN 6 THÁNG QUA 4 TUỔI | 6 месяцев - 4 года | Тионг Вьет (вьетнамский) |
| Информационный бюллетень | Группа получателей вакцины | Язык |
|---|---|---|
| HOJA INFORMATIVA DE VACUNAS PARA RECEPTORES Y CUIDADORES SOBRE LA VACUNA DE PFIZER-BIONTECH CONTRA EL COVID-19 PARA PREVENIR LA ENFERMEDAD DEL CORONAVIRUS 2019 (COVID-19) PARA USO EN PERSONAS DE 5 A 11 AÑOS | 5–11 лет | Español (испанский) |
| 为 和 护理者 提供 的 关于 用 于 预防 2019 新冠肺炎 (Covid-19) 辉瑞 生物 技术 公司 公司 2019 新 冠肺炎 疫苗 个人 使用 的 信息 概况 5 岁 至 11 岁 | 5–11 лет | 中文 (китайский, упрощенный) |
| 5 세 에서 11 세 에 하는 사람들 사람들 에게 바이러스감염증 바이러스감염증 2019 (Covid-19) 를 예방 하기 위한 화 이저 (Pfizer)-바이오 엔텍 (Biontech) 코비드 -19 백신 대한 환자 와 의료진 을 백신 정보지 | 5–11 лет | 한국어 (корейский) |
| BAKUNA IMPORMASYON FACT SHEET PARA SA MGA TUMANGGAP AT MGA TAGAPAG-ALAGA TUNGKOL SA PFIZER-BIONTECH COVID-19 BAKUNA UPANG MAIWASAN ANG CORONAVIRUS DEASEASE 2019 (COVID-19) PARA SA PAGGAMIT SA MGA INDIBIDWAL 5 1002 GULANGGANG 11 2022) | 5–11 лет | Тагальский (тагальский) |
| bảng thông tin về vắc xin dành cho người nhận và người chăm sóc vềc xin pfizer-biontech covid-19 nhằm phòng ngừa bệnh coronavirus 2019 (covid-19). | 5-11 лет | Тионг Вьет (вьетнамский) |
| Информационный бюллетень | Группа получателей вакцины | Язык |
|---|---|---|
| HOJA INFORMATIVA DE VACUNAS PARA RECEPTORES Y CUIDADORES SOBRE COMIRNATY (VACUNA DE ARNm CONTRA EL COVID-19) Y LA VACUNA DE PFIZER-BIONTECH CONTRA EL COVID-19 PARA PREVENIR-19RUA ENFERMEDAD USO EN PERSONAS DE 12 AÑOS O MÁS (31 августа 2022 г.) | 12 лет и старше | Español (испанский) |
| 关于 复必泰 (2019 核糖 核酸 新 冠肺炎 疫苗) 以及 辉瑞 -Biontech3019 新 疫苗 预防 预防 预防 新冠肺炎 接受者 和 和 须知 须知 (31 августа 2022 г.) | 12 лет и старше | 中文 (китайский, упрощенный) |
| 코로나 바이러스감염증 2019 (Covid-19) 를 하기 위한 코멀나티 (코비드 -19 백신, 메신저 РНК) 와 화이저 (Pfizer)-바이오 엔텍 (Biontech) 코비드 -19 백신 에 환자 와 의료진 을 위한 백신 정보지 (31 августа 2022 г.  |