2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Исследование для выявления в крови специфических антител класса IgG, которые вырабатываются в ответ на инфекцию, вызванную простейшим Trichomonas vaginalis. Данные антитела являются маркером протекающего либо перенесенного трихомониаза.
Синонимы русские
Антитела класса IgG к Trichomonas vaginalis, иммуноглобулины класса G к влагалищной трихомонаде.
Синонимы английские
Anti-Trichomonas vaginalis IgG, T. vaginalis Antibodies, IgG.
Метод исследования
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Trichomonas vaginalis – это вид простейших, которые вызывают у человека трихомониаз. Эта болезнь передается половым путем. Трихомонады могут некоторое время (как правило, не более часа) выживать вне организма человека (во влажной среде), поэтому полностью исключить неполовой путь заражения нельзя, однако он встречается редко.
Мужчины и женщины инфицируются одинаково часто, но проявляется заболевание чаще у женщин. Симптомов нет примерно у половины инфицированных женщин и почти у всех инфицированных мужчин. Кроме того, есть данные о том, что в организме мужчины трихомонады часто исчезают и без лечения. Инкубационный период составляет 5-28 дней.
Симптомы трихомониаза
Кроме того, трихомониаз может приводить к осложнениям во время беременности (независимо от того, сопровождается ли инфекция внешними проявлениями): к преждевременным родам, сниженному весу новорождённого.
Есть данные, что трихомониаз увеличивает вероятность рака шейки матки
и рака простаты. Хотя, вообще, вопрос о том, насколько вероятны осложнения при трихомониазе, еще недостаточно изучен.
Трихомониаз диагностируют с помощью микроскопии, ПЦР или посева (культивирования). В последнее время часто применяются серологические методы (основанные на определении антител), в частности иммуноферментный анализ (ИФА). Чувствительность ИФА оценивается в 94-95 %, специфичность – в 77-85 %.
После того, как в организм попадают болезнетворные микроорганизмы, он начинает с ними бороться. Один из способов борьбы – это выработка антител (специальных белков иммуноглобулинов). Существует несколько их типов: IgG, IgM, IgA и др.
Антитела класса G (IgG) присутствуют в крови в наибольшем количестве по сравнению с другими типами. Как правило, при заражении IgG появляются не самыми первыми (позднее, чем IgM), зато их уровень остается высоким долгое время (месяцы и годы).
Как правило, при заражении IgG появляются не самыми первыми (позднее, чем IgM), зато их уровень остается высоким долгое время (месяцы и годы).
Как известно, антитела IgG обеспечивают вторичный иммунный ответ (который и называют иммунитетом). Если человек, который уже однажды переболел этой болезнью, заразится еще раз, то IgG появятся быстрее и в большем количестве, чем прежде. Однако при трихомониазе иммунитет часто не формируется, поэтому в течение жизни человек может заражаться несколько раз.
Уровень IgG не обязательно отражает тяжесть заболевания. Вероятность обнаружить антитела IgG не зависит от того, сопровождается ли трихомониаз болезненными проявлениями. Иммуноглобулины M являются в этом смысле более информативными (они реже встречаются при бессимптомном носительстве трихомонад).
Количество антител выражают в виде титра. Титр – это максимальное разбавление раствора, при котором в нем еще обнаруживаются антитела. Например, титр антител 1:16 означает, что, если сыворотку крови разбавить в 16 раз, в ней еще можно обнаружить антитела (а если сильнее – то они уже не детектируются).
Титр называют высоким (например, 1:612) или низким (например, 1: 4), конкретное его значение зависит от чувствительности метода. То есть такая оценка является полуколичественной.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Референсные значения
Результат: отрицательный.
Титр: менее 1:5.
Значение титра выдается только в случае положительного результата.
Отрицательный результат
 Если заражение произошло недавно (несколько дней назад), то антитела против T. vaginalis еще не выявляются. При необходимости анализ следует сдать позднее.
Если заражение произошло недавно (несколько дней назад), то антитела против T. vaginalis еще не выявляются. При необходимости анализ следует сдать позднее.Положительный результат
Также рекомендуется
Кто назначает исследование?
Врач общей практики, терапевт, уролог, венеролог, гинеколог, инфекционист.
Литература
 24th ed. Goldman L, Schafer A.I., eds. Saunders Elsevier; 2011.
24th ed. Goldman L, Schafer A.I., eds. Saunders Elsevier; 2011.Антитела класса IgG к возбудителю урогенитального уреаплазмоза (Ureaplasma urealyticum) – специфические иммуноглобулины, вырабатывающиеся в организме человека в период выраженных клинических проявлений уреаплазмоза и являющиеся серологическим маркером этого заболевания.
Синонимы русские
Антитела класса IgG к Ureaplasma urealyticum, иммуноглобулины класса G к уреаплазме.
Синонимы английские
Anti-Ureaplasma urealyticum IgG, U. urealyticum antibodies, IgG.
Метод исследования
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
Не курить в течение 30 минут до исследования.
Общая информация об исследовании
U. urealyticum – это микроорганизм, относящийся к группе микоплазм.
В медицине обращают внимание на два вида уреаплазм: U. urealyticum и U. parvum, т. к. именно они способны вызывать заболевания. Однако в большинстве случаев наличие у пациента уреаплазм не сопровождается никакими симптомами, т. е. эти бактерии могут присутствовать в микрофлоре здорового человека.
Уреаплазмы есть у 40-70 % женщин, ведущих половую жизнь. У мужчин они встречаются реже. Передача уреаплазм возможна половым путем или при родах.
Иногда эти бактерии могут быть причиной уретрита – воспаления мочеиспускательного канала. Причем U. urealyticum – это только один из возможных возбудителей уретрита, который вызывается также гонококками (Neisseria gonorrhoeae), хламидиями (Chlamydia trachomatis), трихомонадами (Trichomonas vaginalis), микоплазмами (Mycoplasma genitalium) и другими микроорганизмами. По внешним симптомам возбудителя определить невозможно, поэтому для точного диагноза (и выбора правильного метода лечения) нужны лабораторные тесты.
По внешним симптомам возбудителя определить невозможно, поэтому для точного диагноза (и выбора правильного метода лечения) нужны лабораторные тесты.
Симптомы уретрита
Некоторые исследователи считают, что существует связь между уреаплазмами и осложнениями при беременности, однако это не доказано, поэтому анализ на уреаплазму при беременности необязателен.
Предполагаемые последствия уреаплазменной инфекции:
После того как в организм попадают болезнетворные микроорганизмы, он начинает с ними бороться. Один из способов борьбы – это выработка антител – специальных белков-иммуноглобулинов. Существует несколько типов иммуноглобулинов: IgG, IgM, IgA и др.
Один из способов борьбы – это выработка антител – специальных белков-иммуноглобулинов. Существует несколько типов иммуноглобулинов: IgG, IgM, IgA и др.
Антитела класса IgG присутствуют в крови в наибольшем количестве (по сравнению с другими типами иммуноглобулинов). Как правило, при заражении они появляются не самыми первыми (позднее, чем IgM), зато их уровень остается высоким долгое время (месяцы и даже годы).
Кроме того, антитела IgG обеспечивают вторичный иммунный ответ (который и называют иммунитетом). Если человек, который уже однажды переболел этой болезнью, заразится еще раз, то IgG появятся быстрее и в большем количестве, чем прежде.
Связь между присутствием бактерий и развитием заболевания недостаточно изучена, так что выявление антител против уреаплазм является скорее дополнительным фактором для постановки диагноза, а не решающим.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Референсные значения
Результат: отрицательный.
Титр: менее 1:5.
Значение титра выдается только в случае положительного результата.
Отрицательный результат
Положительный результат
Также рекомендуется
Кто назначает исследование?
Врач общей практики, терапевт, инфекционист, уролог, венеролог.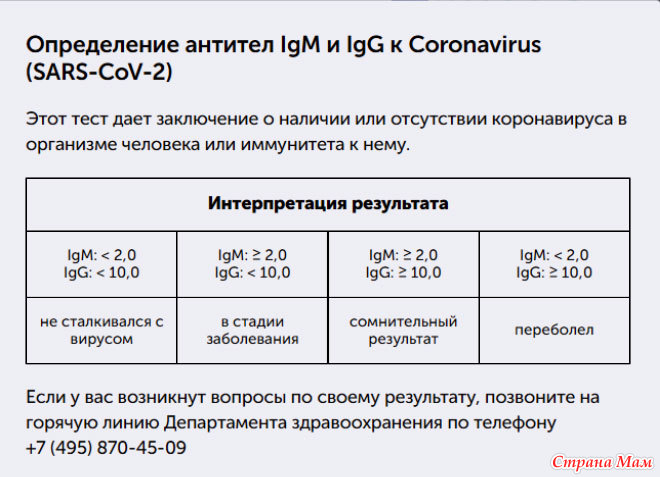
Литература
Дефицит IgG — это проблема со здоровьем, при которой ваш организм не вырабатывает достаточное количество иммуноглобулина G (IgG). Люди с дефицитом IgG более склонны к инфекциям.
Люди с дефицитом IgG более склонны к инфекциям.
Когда ваше тело чувствует, что его атакуют, оно вырабатывает специальные белки, называемые иммуноглобулинами или антителами. Эти антитела вырабатываются плазматическими клетками. Они высвобождаются по всему телу, чтобы помочь убить бактерии, вирусы и другие микробы. Организм вырабатывает 5 основных типов иммуноглобулинов:
Иммуноглобулин A
Иммуноглобулин G
Иммуноглобулин M
Иммуноглобулин D
Immunoglobulin E
Immunoglobulin E
. IgG имеет 4 разных подкласса, IgG1 — 4. IgG всегда рядом, чтобы помочь предотвратить инфекции. Он также готов размножаться и атаковать при попадании в организм чужеродных веществ. Когда вам не хватает, у вас больше шансов заразиться.
Неизвестно, что вызывает дефицит IgG. Однако генетика может сыграть свою роль. Это состояние также считается связанным с дефицитом другого иммуноглобулина.
Инфекции, которые чаще всего поражают людей с дефицитом IgG:
Инфекции носовых пазух и другие респираторные инфекции
Желудочно-кишечные инфекции
ушные инфекции
Pneumonia
Бронхит
Инфекции, которые приводят к боль в горле
Rely, тяжелые и опасные для жизни инфляции
в некоторых людях, которые подвергаются опасности, инфляции. дыхательных путей и функции легких. Это может повлиять на дыхание. Люди с дефицитом IgG также часто обнаруживают, что пневмония и вакцины против гриппа не защищают их от заражения этими инфекциями.
Анализ крови, который измеряет уровень иммуноглобулина, может диагностировать дефицит IgG. Уровень общего IgG может быть нормальным, поэтому важно тестирование подклассов IgG. Также можно провести анализ слюны и спинномозговой жидкости.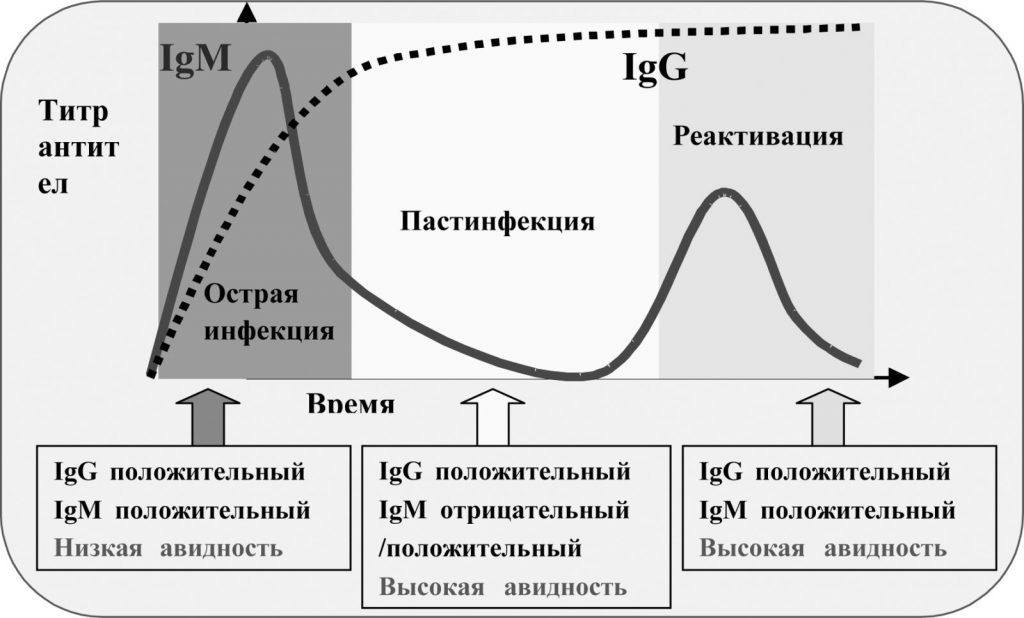 Но наиболее распространенным является анализ крови.
Но наиболее распространенным является анализ крови.
Лечение зависит от тяжести ваших симптомов и инфекций. Когда симптомы появляются в более позднем возрасте, справиться с проблемой со здоровьем становится труднее. Человек также склонен к большему количеству инфекций.
Если инфекции не мешают вашей повседневной жизни, может быть достаточно немедленного лечения. Если вы болеете частыми или тяжелыми инфекциями, которые продолжают возвращаться, вам может помочь продолжающееся лечение. Это поможет предотвратить заболевание или уменьшить симптомы или частоту. Это может означать ежедневный прием антибиотика для предотвращения инфекций. Возможно, вам придется чередовать другие антибиотики, если инфекция и симптомы все еще возникают.
Некоторые люди, страдающие тяжелыми инфекциями, могут быть устойчивы к лечению антибиотиками. Им может потребоваться терапия иммуноглобулином, чтобы помочь укрепить иммунную систему организма, а не полагаться на антибиотики для предотвращения инфекций.
Если у вас диагностирован дефицит IgG, звоните своему лечащему врачу при появлении признаков инфекции. Это верно, даже если вы просто простудились.
Иммуноглобулин G, также известный как IgG, является наиболее распространенным типом дефицита IgG.
Люди с дефицитом IgG более подвержены инфекциям.
Хотя неизвестно, что вызывает дефицит IgG, определенную роль может играть генетика.
Анализ крови, измеряющий иммуноглобулин, может диагностировать это состояние.
Когда симптомы появляются в более позднем возрасте, проблему со здоровьем труднее решить, и человек, как правило, более подвержен инфекциям.
Лечение зависит от тяжести ваших симптомов и инфекций.
Советы, которые помогут вам получить максимальную отдачу от посещения вашего поставщика медицинских услуг:
Знайте причину вашего визита и то, что вы хотите, чтобы произошло.
Перед посещением запишите вопросы, на которые вы хотите получить ответы.
Возьмите с собой кого-нибудь, кто поможет вам задавать вопросы и помнить, что говорит вам ваш врач.
При посещении запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Кроме того, запишите все новые инструкции, которые дает вам ваш врач.
Знайте, почему назначено новое лекарство или лечение и как оно вам поможет. Кроме того, знайте, каковы побочные эффекты.
Спросите, можно ли вылечить ваше заболевание другими способами.
Узнайте, почему рекомендуется тест или процедура и что могут означать результаты.
Знайте, чего ожидать, если вы не примете лекарство или не пройдете тест или процедуру.
Если у вас запланирована повторная встреча, запишите дату, время и цель этой встречи.
Знайте, как вы можете связаться со своим поставщиком медицинских услуг, если у вас есть вопросы. 9
9
Матас А., Хэллоран П.Ф.: Понимание причин отказа трансплантата почки: доминирующая роль опосредованного антителами отторжения и несоблюдения режима. Am J трансплантат 12: 388–399, 2012 [PubMed] [Google Scholar]
2. Meier-Kriesche HU, Schold JD, Srinivas TR, Kaplan B: отсутствие улучшения выживаемости почечных аллотрансплантатов, несмотря на заметное снижение частоты острого отторжения в течение недавняя эпоха. Am J трансплантат 4: 378–383, 2004 [PubMed] [Google Scholar]
3. Matas AJ, Smith JM, Skeans MA, Thompson B, Gustafson SK, Schnitzler MA, Stewart DE, Cherikh WS, Wainright JL, Snyder JJ, Israni AK, Kasiske BL: Годовой отчет OPTN/SRTR 2012: почки. Am J трансплантат 14 [Suppl 1]: 11–44, 2014 [PubMed] [Google Scholar]
-organes.htm)
5. Nankivell BJ, Alexander SI: Отторжение аллотрансплантата почки. N Engl J Med 363: 1451–1462, 2010 [PubMed] [Google Scholar]
6. Papadimitriou JC, Drachenberg CB, Ramos E, Kukuruga D, Klassen DK, Ugarte R, Nogueira J, Cangro C, Weir MR, Haririan A: Опосредованное антителами отторжение аллотрансплантата: морфологический спектр и серологические корреляции при наблюдении и по причине биопсии. Трансплантация 95: 128–136, 2013 [PubMed] [Google Scholar]
Трансплантация 95: 128–136, 2013 [PubMed] [Google Scholar]
7. Lefaucheur C, Loupy A, Hill GS, Andrade J, Nochy D, Antoine C, Gautreau C, Charron D, Glotz D, Suberbielle-Boissel C: Существующие ранее донор-специфические HLA-антитела предсказывают исход трансплантации почки. J Am Soc Нефрол 21: 1398–1406, 2010 [бесплатная статья PMC] [PubMed] [Google Scholar]
8. Chen G, Sequeira F, Tyan DB: новый анализ C1q выявляет клинически значимую подгруппу антител к лейкоцитарному антигену человека, не зависящую от силы иммуноглобулина G, на одиночной пробе. шарики антигена. Хум Иммунол 72: 849–858, 2011 [PubMed] [Google Scholar]
9. Yabu JM, Higgins JP, Chen G, Sequeira F, Busque S, Tyan DB: C1q-фиксирующие антитела к лейкоцитарному антигену человека специфичны для прогнозирования гломерулопатии трансплантата и поздняя недостаточность трансплантата после трансплантации почки. Трансплантация 91: 342–347, 2011 [PubMed] [Google Scholar]
10. Loupy A, Lefaucheur C, Vernerey D, Prugger C, Duong van Huyen JP, Mooney N, Suberbielle C, Frémeaux-Bacchi V, Méjean A, Desgrandchamps F, Anglicheau D, Nochy D, Charron D, Empana JP, Delahousse M, Legendre C, Glotz D, Hill GS, Zeevi A, Jouven X: Связывающие комплемент антитела против HLA и выживаемость почечного аллотрансплантата. N Engl J Med 369: 1215–1226, 2013 [PubMed] [Google Scholar]
N Engl J Med 369: 1215–1226, 2013 [PubMed] [Google Scholar]
11. Tao MH, Smith RI, Morrison SL: Структурные особенности человеческого иммуноглобулина G, которые определяют изотип-специфические различия в активации комплемента. J Эксперт Мед 178: 661–667, 1993 [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Шауб С., Хёнгер Г., Коллер М.Т., Ливски Р., Амико П.: Детерминанты связывания C1q в анализе с одним антигеном. Трансплантация 98: 387–393, 2014 [PubMed] [Google Scholar]
13. Woof JM, Burton DR: Взаимодействие человеческого антитела с рецептором Fc, освещенное кристаллическими структурами. Нат Рев Иммунол 4: 89–99, 2004 [PubMed] [Google Scholar]
14. van Zelm MC: В-клетки не торопятся: последовательное переключение класса IgG в ходе иммунного ответа? Иммунол Селл Биол 92: 645–646, 2014 [PubMed] [Google Scholar]
15. Sitaru C, Mihai S, Zillikens D: Актуальность подкласса IgG аутоантител для индукции пузырей при аутоиммунных буллезных заболеваниях кожи. Арка Дерматол Рез 299: 1–8, 2007 [бесплатная статья PMC] [PubMed] [Google Scholar]
16. Azevedo CD, Bruña-Romero O, Marques SG, Nascimento FR, Pinto MC, Silva LA, Bouillet LE, Azevedo FS, Stoianoff MA: Ассоциация уровня иммуноглобулина IgG и подклассов с тяжестью хромобластомикоза, вызванного Fonsecaea pedrosoi, и терапевтическим ответом на итраконазол. Eur J Clin Microbiol Infect Dis 33: 1791–1797, 2014 [PubMed] [Google Scholar]
17. Bijl M, Dijstelbloem HM, Oost WW, Bootsma H, Derksen RH, Aten J, Limburg PC, Kallenberg CG: распределение аутоантител подкласса IgG различается между почечными и внеклеточными -почечные рецидивы у больных системной красной волчанкой. Ревматология (Оксфорд) 41: 62–67, 2002 [PubMed] [Google Scholar]
18. Noël LH, Aucouturier P, Monteiro RC, Preud'Homme JL, Lesavre P: Подклассы гломерулярного и сывороточного иммуноглобулина G при мембранозной нефропатии и антигломерулярной базальной мембране нефрит. Клин Иммунол Иммунопатол 46: 186–194, 1988 [PubMed] [Google Scholar]
19. Imai H, Hamai K, Komatsuda A, Ohtani H, Miura AB: подклассы IgG у пациентов с мембранопролиферативным гломерулонефритом, мембранозной нефропатией и волчаночным нефритом. почки инт 51: 270–276, 1997 [PubMed] [Google Scholar]
Imai H, Hamai K, Komatsuda A, Ohtani H, Miura AB: подклассы IgG у пациентов с мембранопролиферативным гломерулонефритом, мембранозной нефропатией и волчаночным нефритом. почки инт 51: 270–276, 1997 [PubMed] [Google Scholar]
20. Qu Z, Liu G, Li J, Wu LH, Tan Y, Zheng X, Ao J, Zhao MH: Отсутствие гломерулярного отложения IgG4 у пациентов с мембранозная нефропатия может указывать на злокачественное новообразование. Трансплантация нефролового циферблата 27: 1931–1937, 2012 [PubMed] [Google Scholar]
21. Хаас М.: Отложения подкласса IgG в клубочках волчаночной и неволчаночной мембранозной нефропатии. Am J почек Dis 23: 358–364, 1994 [PubMed] [Google Scholar]
22. Kaneku H, O'Leary JG, Taniguchi M, Susskind BM, Terasaki PI, Klintmalm GB: Донор-специфические человеческие лейкоцитарные антигенные антитела подкласса иммуноглобулина G3 связаны с хроническим отторжением и потерей трансплантата после трансплантации печени. Трансплантация печени 18: 984–992, 2012 [PubMed] [Google Scholar]
23. Hönger G, Hopfer H, Arnold ML, Spriewald BM, Schaub S, Amico P: Pretransplant IgG подклассы донор-специфических антигенных антител человека и разработка антителоопосредованное отторжение. Трансплантация 92: 41–47, 2011 [PubMed] [Google Scholar]
Hönger G, Hopfer H, Arnold ML, Spriewald BM, Schaub S, Amico P: Pretransplant IgG подклассы донор-специфических антигенных антител человека и разработка антителоопосредованное отторжение. Трансплантация 92: 41–47, 2011 [PubMed] [Google Scholar]
24. Arnold ML, Ntokou IS, Doxiadis II, Spriewald BM, Boletis JN, Iniotaki AG: Донор-специфические HLA-антитела: оценка риска потери трансплантата при почечной недостаточности. реципиенты трансплантата с изотипом переключаются с IgG1/IgG3, связывающих комплемент, на анти-HLA-аллоантитела IgG2/IgG4, не связывающие комплемент. Транспл Интерн. 27: 253–261, 2014 [PubMed] [Google Scholar]
25. Кушихата Ф., Ватанабэ Дж., Малдер А., Клаас Ф., Скорник Дж. К.: Антитела к антигенам лейкоцитов человека и активация комплемента человека: роль подкласса IgG, специфичность и цитотоксический потенциал. Трансплантация 78: 995–1001, 2004 [PubMed] [Google Scholar]
26. Karuppan SS, Ohlman S, Möller E: Наличие цитотоксических и не связывающих комплемент антител в перекрестной сыворотке пациентов с ранними эпизодами острого отторжения.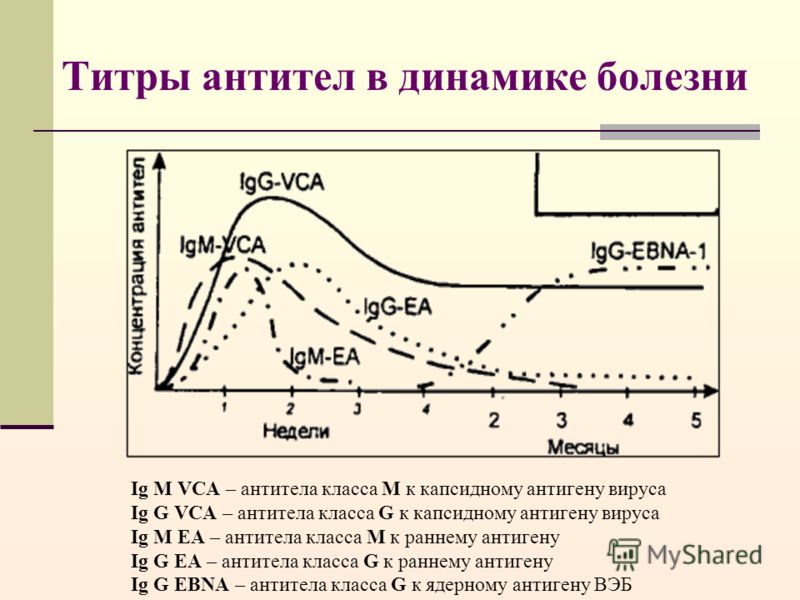 Трансплантация 54: 839–844, 1992 [PubMed] [Google Scholar]
Трансплантация 54: 839–844, 1992 [PubMed] [Google Scholar]
27. Griffiths EJ, Nelson RE, Dupont PJ, Warrens AN: Перекос предтрансплантационных анти-HLA антител класса I изотипа G иммуноглобулина исключительно в сторону иммуноглобулина G1 подкласса связан с худшей выживаемостью почечного аллотрансплантата. Трансплантация 77: 1771–1773, 2004 [PubMed] [Google Scholar]
28. Bartel G, Warmann M, Exner M, Regele H, Schillinger M, Hörl WH, Böhmig GA: Детерминанты связывающей комплемент способности пресенсибилизации реципиента против антигенов HLA. Трансплантация 83: 727–733, 2007 [PubMed] [Google Scholar]
29. Schaub S, Hönger G, Amico P: Сложность гуморального иммунного ответа против антигенов HLA. Транспл Интерн. 27: 249–250, 2014 [PubMed] [Google Scholar]
30. Monteiro F, Mineiro C, Rodrigues H, de Paula FJ, Kalil J: Мониторинг анти-HLA IgG1 класса I до и после трансплантации с помощью ELISA идентифицирует пациентов при высоком риске потери трансплантата. Процедура трансплантации 29: 1433–1434, 1997 [PubMed] [Google Scholar]
31. Regan J, Monteiro F, Speiser D, Kalil J, Pouletty P, Buelow R: Оценка риска отторжения перед трансплантацией с помощью иммуноферментного анализа анти-HLA антитела I класса. Am J почек Dis 28: 92–98, 1996 [PubMed] [Google Scholar]
Regan J, Monteiro F, Speiser D, Kalil J, Pouletty P, Buelow R: Оценка риска отторжения перед трансплантацией с помощью иммуноферментного анализа анти-HLA антитела I класса. Am J почек Dis 28: 92–98, 1996 [PubMed] [Google Scholar]
32. Arnold ML, Zacher T, Dechant M, Kalden JR, Doxiadis II, Spriewald BM: Обнаружение и спецификация аллоантител против HLA, не связывающихся комплементом. Хум Иммунол 65: 1288–1296, 2004 [PubMed] [Google Scholar]
33. Gao ZH, McAlister VC, Wright JR, Jr, McAlister CC, Peltekian K, MacDonald AS: Антидонорская реактивность подкласса иммуноглобулина-G у реципиентов трансплантата. Трансплантация печени 10: 1055–1059, 2004 [PubMed] [Google Scholar]
34. Лобашевский А., Рознер К., Гоггинс В., Хиггинс Н. Подтипы иммуноглобулина (Ig)-G антител против HLA класса II донора и результаты перекрестной совместимости в три кандидата на трансплантацию почки. Транспл Иммунол 23: 81–85, 2010 [PubMed] [Google Scholar]
35. Haas M, Sis B, Racusen LC, Solez K, Glotz D, Colvin RB, Castro MC, David DS, David-Neto E, Bagnasco SM, Cendales LC, Cornell LD, Demetris AJ, Drachenberg CB, Farver CF, Farris AB, 3rd, Gibson IW, Kraus E, Liapis H, Loupy A, Nickeleit V, Randhawa P, Rodriguez ER, Rush D, Smith RN, Tan CD, Wallace WD, Mengel M, комитет по составлению отчета о встрече в Банфе: отчет о встрече в Банфе в 2013 г. : включение C4d-негативного отторжения, опосредованного антителами, и связанных с антителами поражений артерий. Am J трансплантат 14: 272–283, 2014 [PubMed] [Google Scholar]
: включение C4d-негативного отторжения, опосредованного антителами, и связанных с антителами поражений артерий. Am J трансплантат 14: 272–283, 2014 [PubMed] [Google Scholar]
36. Kamisawa T, Zen Y, Pillai S, Stone JH: заболевание, связанное с IgG4. Lancet: 2014 [PubMed] [Google Scholar]
37. Stegall MD, Diwan T, Raghavaiah S, Cornell LD, Burns J, Dean PG, Cosio FG, Gandhi MJ, Kremers W, Gloor JM: ингибирование терминального комплемента снижает уровень антител. опосредованное отторжение у сенсибилизированных реципиентов почечного трансплантата. Am J трансплантат 11: 2405–2413, 2011 [PubMed] [Google Scholar]
. спасительное лечение рефрактерного опосредованного антителами отторжения у пациентов с трансплантацией почки: отчеты о клинических случаях. Процедура трансплантации 45: 1022–1025, 2013 [PubMed] [Google Scholar]
39. Burbach M, Suberbielle C, Brochériou I, Ridel C, Mesnard L, Dahan K, Rondeau E, Hertig A: Отчет о неэффективности экулизумаба в двух случаях тяжелого опосредованного антителами отторжения почечных трансплантатов. Трансплантация 98: 1056–1059, 2014 [PubMed] [Google Scholar]
Трансплантация 98: 1056–1059, 2014 [PubMed] [Google Scholar]
40. Lowe D, Higgins R, Zehnder D, Briggs DC: значительная гетерогенность подкласса IgG в HLA-специфических антителах: последствия для патогенности, прогноза и реакции отторжения . Хум Иммунол 74: 666–672, 2013 [PubMed] [Google Scholar]
41. Дебиек Х., Наута Дж., Куле Ф., Ван дер Бург М., Гигонис В., Шурманс Т., де Хеер Э., Субрие Ф., Янссен Ф., Ронко П.: Роль укороченных мутаций в гене MME в фетоматеринской аллоиммунизации и антенатальных гломерулопатиях . Ланцет 364: 1252–1259, 2004 [PubMed] [Google Scholar]
42. Ronco P, Debec H: Молекулярная диссекция антигенов-мишеней и нефритогенных антител при мембранозной нефропатии: на пути к терапии, управляемой эпитопом. J Am Soc Нефрол 17: 1772–1774, 2006 [PubMed] [Google Scholar]
43. Идальго Л.Г., Сис Б., Селларес Дж., Кэмпбелл П.М., Менгель М., Айнеке Г., Чанг Дж., Халлоран П.Ф.: Транскрипты NK-клеток и NK-клетки в биоптатах почек пациентов с донор-специфическими антителами: доказательства участия NK-клеток при антителоопосредованном отторжении. Am J трансплантат 10: 1812–1822, 2010 [PubMed] [Google Scholar]
Am J трансплантат 10: 1812–1822, 2010 [PubMed] [Google Scholar]
44. Рахими С., Цянь З., Лейтон Дж., Фокс-Талбот К., Болдуин В.М., 3-й, Васовска Б.А.: Антитела, не активирующие комплемент, и антитела, активирующие комплемент, синергируют друг с другом. вызвать отторжение сердечных аллотрансплантатов. Am J трансплантат 4: 326–334, 2004 [PubMed] [Google Scholar]
45. Stegall MD, Chedid MF, Cornell LD: Роль комплемента в опосредованном антителами отторжении при трансплантации почки. Нат Рев Нефрол 8: 670–678, 2012 [PubMed] [Google Scholar]
46. Леви А.С., Бош Дж.П., Льюис Дж.Б., Грин Т., Роджерс Н., Рот Д., Модификация диеты при заболеваниях почек. оценка скорости клубочковой фильтрации по креатинину сыворотки: новое уравнение прогноза. Энн Интерн Мед 130: 461–470, 1999 [PubMed] [Google Scholar]
47. Racusen LC, Solez K, Colvin RB, Bonsib SM, Castro MC, Cavallo T, Croker BP, Demetris AJ, Drachenberg CB, Fogo AB, Furness P , Габер Л.В., Гибсон И.В., Глотц Д. , Голдберг Дж.К., Гранде Дж., Халлоран П.Ф., Хансен Х.Э., Хартли Б., Хейри П.Дж., Хилл К.М., Хоффман Э.О., Хансикер Л.Г., Линдблад А.С., Ямагути Ю., Михач М.Дж., Надасди Т., Никерсон P, Olsen TS, Papadimitriou JC, Randhawa PS, Salinas-Madrigal L, Salomon DR, Sund S, Taskinen E, Trpkov K, Yamaguchi Y: The Banff 97 рабочая классификация патологии почечного аллотрансплантата. почки инт 55: 713–723, 1999 [PubMed] [Google Scholar]
, Голдберг Дж.К., Гранде Дж., Халлоран П.Ф., Хансен Х.Э., Хартли Б., Хейри П.Дж., Хилл К.М., Хоффман Э.О., Хансикер Л.Г., Линдблад А.С., Ямагути Ю., Михач М.Дж., Надасди Т., Никерсон P, Olsen TS, Papadimitriou JC, Randhawa PS, Salinas-Madrigal L, Salomon DR, Sund S, Taskinen E, Trpkov K, Yamaguchi Y: The Banff 97 рабочая классификация патологии почечного аллотрансплантата. почки инт 55: 713–723, 1999 [PubMed] [Google Scholar]
48. Racusen LC, Colvin RB, Solez K, Mihatsch MJ, Halloran PF, Campbell PM, Cecka MJ, Cosyns JP, Demetris AJ, Fishbein MC, Fogo A , Фернесс П., Гибсон И.В., Глотц Д., Хейри П., Хансикерн Л., Кашгарян М., Керман Р., Магил А.Дж., Монтгомери Р., Морозуми К., Никелеит В., Рандхава П., Регеле Х., Серон Д., Сешан С., Сунд С., Трпков K: Антитело-опосредованные критерии отторжения - дополнение к Banff 97 классификация отторжения почечного аллотрансплантата. Am J трансплантат 3: 708–714, 2003 [PubMed] [Google Scholar]
49. Solez K, Colvin RB, Racusen LC, Haas M, Sis B, Mengel M, Halloran PF, Baldwin W, Banfi G, Collins AB, Cosio F , Дэвид Д.