2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Основатель платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
Каждый год рак прямой кишки диагностируют у 746,000 пациентов. Лучше всего этот вид рака лечится на 0 и 1 стадиях. Но и на более поздних этапах есть шанс избавиться от болезни или улучшить качество жизни. В этой статье мы расскажем, какие методы лечения рака прямой кишки используют в ведущих клиниках мира.
Выбор метода терапии зависит от стадии болезни. План лечения рака прямой кишки у женщин и мужчин одинаковый. Различия могут быть только на последних стадиях и связаны они с местом локализации метастазов. Рассмотрим схемы лечения при разных степенях равития рака прямой кишки:
0 стадия. На этом этапе рак толстой кишки удаляют в ходе операции. Чаще всего это эндоскопическая операция и проводят ее во время колоноскопии. Если раковая опухоль большая, назначают частичную колэктомию — удаление пораженной части кишки.
1 стадия. На этой стадии рак прорастает в глубокие слои кишки, но не распространяется на лимфоузлы. Основной метод лечения — частичная колэктомия или колоноскопия с удалением опухоли. Второй метод применяют для опухолей в виде полипа.
2 стадия. Рак прорастает в соседние с кишкой ткани, но еще не затрагивает лимфоузлы. Врачи рекомендуют частичную колэктомию с удалением лимфоузлов. Если есть вероятность рецидива, назначают химиотерапию.
3 стадия. На этом этапе рак прорастает в глубокие ткани органа и лимфоузлы. Основной метод лечения — операция и химиотерапия. Врачи делают частичную колэктомию с удалением лимфоузлов, а затем проводят химию. Если пациент не операбельный, доктора рекомендуют лучевую терапию.
4 стадия. Рак характеризуется метастазами в отдаленные органы и ткани. Цель лечения — улучшить качество жизни и снять болезненные симптомы. В зависимости от места локализации метастазов, применяют операцию или лучевую терапию. Дополнительно врачи назначают таргетную терапию, иммунотерапию и химию.
Операция — это основной метод лечения рака прямой кишки. Он помогает убрать опухоль из организма. Благодаря этому дальнейшее лечение проходит проще и эффективнее. На ранних стадиях онкологии делают эндоскопическую операцию. Это иссечение ракового полипа или небольшой опухоли прямо во время колоноскопии. После такого вмешательства пациент восстанавливается за 1-2 дня. Операцию проводят в амбулаторном режиме.
На более поздних стадиях применяют колэктомию — полное или частичное удаление кишки. После оперативного лечения рака прямой кишки, части органа сшиваются. В некоторых случаях пациенту устанавливают колостому, то есть часть кишки выводят через брюшную полость наружу. Как правило — это временная мера на период восстановления.
Хирургическое лечение рака прямой кишки проводят открытым или лапароскопическим способами. В первом случае хирург делает разрез в брюшной полости и удаляет опухоль. Во втором — операцию проводят через несколько небольших проколов в брюшине. Благодаря этому уход за послеоперационной раной проще, а пациент восстанавливается быстрее.
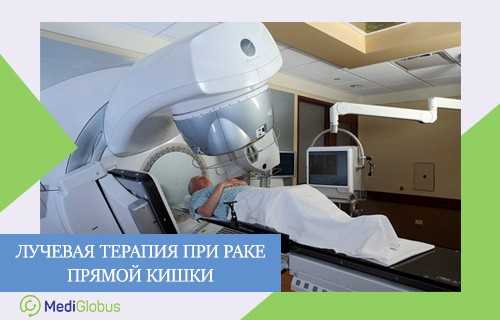
Радиотерапия — это лечение рака прямой кишки без операции, с помощью радиоактивного облучения. Этот метод не является основным. Облучение назначают для неоперабельных опухолей или для уменьшения новообразования перед операцией. На 4 стадии рака прямой кишки радиотерапию применяют для борьбы с метастазами и облегчения симптомов болезни.
При лечения рака прямой кишки применяют внешнюю лучевую терапию и интраоперационное облучение. Внешнее облучение проходит на аппаратах КиберНож и Гамма-нож.
В современных клиниках применяют технологию IMRT — радиотерапию с модулированной интенсивностью. Она помогает точно подобрать дозу облучения и настроить луч так, чтобы не повредить здоровые ткани.
Интраоперационное облучения проводят прямо во время операции по удалению опухоли. Оно помогает убить раковые клетки в соседних тканях и снизить риск рецидива.
Получить бесплатную консультацию
Абляция и эмболизация — одни из методов безоперационного лечения рака прямой кишки. Они применяются для небольших (до 4 см) опухолей на 0-1 стадиях болезни. Абляция — это удаление опухоли с помощью ультразвука или радиоволн. Они нагревают и разрушают злокачественные клетки, опухоль погибает.
Процесс эмболизации заключается в разрушении или закупоривании сосудов, которые снабжают опухоль кровью. Метод применяют для лечения метастазов в легких, мочевом пузыре, печени. В последнем случае в печеночную артерию вводят препарат, который блокирует сосуд, опухоль не может расти и погибает. Кровь для клеток печени поставляется через портальную вену, поэтому блокировка артерии не влияет на нормальную работу органа.

Химиотерапия — вспомогательный метод лечения опухолей прямой кишки. Доктора применяют адъювантную химию для борьбы с раковыми клетками после операции и неоадъювантную для уменьшения опухоли перед операцией. Большинство препаратов химии вводят системно, они действуют на раковые клетки во всем организме. Для лечения локальных метастазов, например в печени, применяют региональную химию — лекарства вводят в печеночную артерию. Для лечения рака прямой кишки применяют 5-фторурацил, оксоплатин, трифлуридин и другие препараты. Длительность химиотерапии и количество курсов назначают индивидуально, исходя из стадии болезни и состояния пациента.
Таргетные и иммунотерапевтические препараты используются для лечения рака кишечника на последних стадиях, а также в терапии рецидивов. Цель таргетной терапии — направленное воздействие на раковые клетки. Есть два подхода. В первом случае лекарства блокируют рост новых кровеносных сосудов опухоли, из-за недостатка питательных веществ новообразование погибает. Во втором случае происходит остановка роста самих раковых клеток. В таргетной терапии используют препараты Авастин, Цетуксимаб.
Иммунотерапия рака толстого кишечника направлена на активацию иммунной системы организма. Иммунные препараты помогают защитным клеткам находить рак и уничтожать его. В таком лечении используют препараты Кейтруда и Опдиво.
Прогноз при раке прямой кишки характеризуется показателем “5-летняя выживаемость”. Он обозначает вероятность того, что человек проживет 5 и больше лет после установки диагноза или лечения.
При поиске вариантов терапии рака прямой кишки важно подобрать клинику, которая работает согласно международным онкологическим протоколам. Это гарантирует качество лечения и правильный подбор процедур. Большинство пациентов Mediglobus выбирает лечение рака прямой кишки в Турции, Германии, Израиле, Австрии и Испании.
Рак прямой кишки — один из самых распространенных видов онкологии у мужчин и женщин. При выявлении болезни важно немедленно приступить к лечению, это увеличит шансы полностью выздороветь. Чтобы получить консультацию в подборе клиники и доктора для лечения рака прямой кишки обратитесь к специалистам Mediglobus.
Получить бесплатную консультацию
Основатель платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
Editor
Более 2 лет пишет медицинские тексты. Опыт работы в сфере копирайтинга превышает 6 лет. Имеет образование по направлению “Социально-правовая защита”. Освоила программу медицинских курсов. Изучает коммуникативные техники ведения переговоров с пациентами. В свободное время посещает тренинги и семинары по медицинской психологии.
Метастазы при раке молочной железы - что делать пациентам?
Читать дальшеЕсли у вас или ваших близких диагностирован рак прямой кишки, очень важно понимать как можно больше о сути болезни. Это поможет вам правильно вести диалог с лечащим врачом и принять наилучшее решение. В этом разделе мы подготовили максимально подробную информацию как о самой болезни, так и способах ее диагностики и лечения для всех, кто столкнулся с этим серьезным заболеванием.
Рак прямой кишки - это разновидность колоректального рака или рака кишечника, локализованный в прямой кишке. Обычно рак прямой кишки появляется из полипов – это небольшие разрастания на слизистой оболочке, являющейся внутренним покрытием нашего кишечника. Процесс перерождения полипа в раковую опухоль занимает несколько лет. Однако после появления рака в полипе рост опухоли принимает стремительный характер и становится угрозой для жизни заболевшего.
Профессор Петр Владимирович Царьков рассказывает об особенностях лечения рака прямой кишки
Прямая кишка является конечным отрезком кишечника и располагается непосредственно перед анусом - в узком, глубоком и ограниченном пространстве малого таза. Непосредственно вокруг прямой кишки располагаются другие органы и структуры полости малого таза. Благодаря этому тесному соседству удаление прямой кишки при раковой опухоли представляет сложную задачу даже для опытных онкохирургов, которые блестяще оперируют на других органах брюшной полости.
Еще несколько лет назад долгая продолжительность жизни, не говоря о выздоровлении, были редкостью для людей, заболевших раком прямой кишки, даже после комбинированного интенсивного лечения. Благодаря достижениям медицины за последние 30 лет, на сегодняшний день рак прямой кишки может быть успешно вылечен у большинства заболевших.
Основным методом лечения является хирургическая операция. Однако для снижения вероятности возобновления роста опухоли на месте удаленной кишки (рецидив) или появления ее отсевов в других органах и тканях (метастазов) вместе с хирургическим используются дополнительные методы лечения.
Чтобы лучше понять все последствия, которые несет в себе рак прямой кишки, вначале будет полезно точнее узнать, какая часть кишечника поражена и как она работает в нормальном состоянии.
Толстая кишка – это часть кишечника, соединяющая тонкую кишку с заднепроходным отверстием (анусом). Толстая кишка состоит из ободочной и прямой кишок.
Ободочная кишка представляет собой приблизительно 1,5-1,8 м трубку, которая соединяет тонкую кишку с прямой кишкой.
Ободочная кишка «специализируется» на окончательной переработке пищи, извлечения из нее полезных составляющих, в основном воды и солей. Оставшийся от пищевого комка кал проталкивается в прямую кишку.
Прямая кишка представляет собой заключительные 16-18 см кишечной трубки, которая соединяет ободочную кишку и анус и имеет мешкообразную форму. Ее работа заключается в накоплении кала и периодическом выведении его через задний проход наружу.
Рак прямой кишки возникает, когда в ДНК здоровых клеток слизистой оболочки прямой кишки начинают систематически вырабатываться ошибки (мутации). Конкретные причины появления этих ошибок неизвестны. Известны лишь факторы риска, увеличивающие вероятность возникновения этих ошибок.
Здоровые клетки прямой кишки растут и делятся соответствии с программой, чтобы обеспечивать ее нормальную функцию. За реализацию этой программы отвечает клеточная ДНК. В случае ее повреждения клетка становится раковой и продолжает делиться, даже в том случае, когда новые клетки не нужны, то есть бесконтрольно. Поврежденные клетки накапливаются и в итоге образуют раковую опухоль.
Плохой новостью является то, что, по мере роста, клетки переходят сначала на соседние слои стенки прямой кишки (подслизистый, мышечный и жировую ткань, окружающую орган), а также могут распространяться на соседние органы и структуры. Со временем раковые клетки могут перемещаться в другие части тела.
Петр Владимирович Царьков в эфире Mediametrics подробно и доступно рассказывает о причинах, симптомах, диагностике и эффективных методах лечения рака прямой кишки.
Хорошей новостью является точно установленный факт, что раковая опухоль прямой кишки на протяжении длительного времени растет лишь в пределах самой прямой кишки, что дает шанс на излечение большинству заболевших. Поэтому рак прямой кишки относится к относительно благоприятно протекающим ракам, которые могут развиться у человека.
У незначительного числа людей встречаются наследственные изменения (мутации) генов, которые повышают риск появления рака ободочной и прямой кишки. В этих случаях причиной развития рака прямой кишки является наследственность.
Характерным для них является то, что они передаются от родителей к детям, что увеличивает риск развития колоректального рака. Следует помнить, что в ряде случаев, некоторые гены значительно повышают риск развития раком прямой кишки, но не делают его появление неизбежным.
Сегодня определены несколько видов наследственного рака толстой кишки, из которых выделяются два синдрома, имеющих четко выраженный генетический характер:
Эти и другие, более редкие, синдромы наследственно передающегося колоректального рака могут быть обнаружены посредством генетического тестирования. Если в истории вашей семьи (прямые родственники) регистрировались случаи рака толстой кишки, желудка или женских половых органов, то вам обязательно необходимо обсудить с врачом возможный риск наследственной предрасположенности к развитию рака прямой кишки
Подавляющее большинство людей, у которых выявлен рак прямой кишки - старше 50 лет. Более того, в каждые последующие 10 лет жизни после 50-ти риск заболевание раком прямой кишки возрастает. Злокачественная опухоль прямой кишки может возникнуть и у молодых людей, но это происходит гораздо реже. Существует мнение, что рак прямой кишки молодеет. Однако это не так. Просто отмечается увеличение заболеваемости раком прямой кишки, в том числе и в России, что сказывается на пропорциональном росте абсолютного числа заболевших в возрасте младше 50 лет.
Если у вас в прошлом находили полипы или вы лечились по поводу рака толстой кишки, вы имеете большой риск заболеть раком прямой кишки в будущем.
Хронические воспалительные заболевания ободочной и прямой кишки, такие как язвенный колит и болезнь Крона, повышают риск возникновения рака прямой кишки. При этом каждый последующий год жизни с диагнозом болезни Крона или неспецифического язвенного колита увеличивают вероятность развития рака прямой.
Если у членов вашей семьи (родителей или их родителей, брата, сестры или вашего ребенка) ранее выявляли заболевания, которые передаются по наследству из поколения в поколение, это серьезно повышает риск возникновения рака прямой кишки у вас. Эти заболевания включают семейный аденоматозный полипоз и наследственный неполипозный колоректальный рак. Если у кого-то из вышеперечисленных родственников уже развился колоректальный рак, то это еще более повышает ваш риск заболеть раком прямой кишки.
Диета с низким содержанием овощей и высоким содержанием красного, сильно прожаренного или проваренного мяса (более 350 гр. в неделю) увеличивает риски развития рака прямой кишки
Физически малоактивный образ жизни увеличивает риск развития рака прямой кишки, особенно если это сочетается с другими факторами риска. Напротив, высокая физическая активность (прогулки, гимнастика, плавание) снижают вероятность заболевания раком прямой кишки.
Люди с плохо контролируемым сахарным диабетом 2 типа и резистентностью к инсулину могут иметь повышенный риск развития колоректального рака и рака прямой кишки в частности.
Повышенный вес тела или ожирение является серьезным фактором, увеличивающим риск заболевания раком прямой и ободочной кишки, а также риск смерти в результате данного заболевания в сравнении с людьми с нормальным весом тела.
Курение любых видов изделий из табака является одним из серьезнейших факторов риска заболеть раком прямой или ободочной кишки. Кроме того, курение одновременно увеличивает вероятность развития серьезных осложнений во время лечения рака прямой кишки, которые могут приводить к смертельному исходу или значительно ухудшать качество жизни после проведенного лечения.
Необходимо помнить, что отказ от курения на любом этапе жизни, даже после того, как вам был установлен диагноз рака прямой кишки, увеличит ваши шансы на благополучный исход лечения и выздоровление от рака.
Употребление даже одного алкоголь содержащего напитка более трех раз в неделю существенно повышает риск развития рака прямой кишки. Напротив, отказ от приема алкоголя снижают вероятность заболевания раком прямой и ободочной кишок.
Существуют данные о том, что ранее перенесенная лучевая терапия на область малого таза по поводу рака других органов, расположенных в этой области (рак предстательной железы, мочевого пузыря, шейки матки, матки или влагалища) увеличивает вероятность развития рака в прямой кишке. Людям, перенесшим подобное лечение в прошлом необходимо регулярное (не реже одного раза в год) обследование прямой кишки.
Симптомы рака прямой кишки можно разделить на две группы:
Относительно характерные симптомы для рака прямой кишки:
Общие:
Рак прямой кишки часто диагностируется, когда врач назначает обследование, чтобы выяснить причину ректального кровотечения или железодефицитной анемии. Колоноскопия является самым точным из диагностических методов. Для опухолей, расположенных близко к заднему проходу - до 10 см от ануса, опытному колопроктологу достаточно выполнить пальцевое исследование, чтобы заподозрить рак прямой кишки. При колоноскопии используется тонкая и гибкая трубка с ламой и камерой на конце, которые позволяют с разрешением высокого качества осмотреть просвет вашей прямой и ободочной кишки изнутри и при необходимости взять кусок ткани из подозрительного участка (биопсию), чтобы в последующем со 100% уверенностью установить диагноз рака прямой кишки.
Внимание
Только результат биопсии может служить 100% основанием для установки диагноза рака прямой кишки.Исходя из того, что рак прямой кишки является относительно медленно растущей опухолью, первые симптомы этого заболевания часто появляются на поздних стадиях развития болезни, когда возможности лечения ограничены. Именно поэтому так важна роль ранней диагностики рака прямой кишки, когда человека еще ничто не беспокоит. Этого можно добиться, если по достижении 50-летнего возраста проходить так называемое скрининговое обследование – сдавать анализ кала на скрытую кровь и регулярно выполнять колоноскопию для лиц с высоким или средним риском развития рака прямой кишки.
Внимание
Необходимо как можно быстрее обратиться к колопроктологу, если у вас появилась кровь в стуле, устойчиво изменилась привычная работа кишечника или отмечается необъяснимая потеря веса. Эти симптомы указывают на высокий риск того, что у вас может быть диагностирован рак прямой кишки.

Выявление рака прямой кишки - это необходимый, но всего лишь первый шаг на пути определения того, какое оптимальное лечение требуется выбрать и каковы его перспективы. Для этого необходимо установить стадию и другие характеристики злокачественности опухоли прямой кишки. Говоря другими словами, врач должен определить, распространен ли рак, и если да, то насколько далеко и каков его потенциал агрессивности.
Для этого врачу необходимо найти ответы на следующие вопросы:
Определение стадии рака прямой кишки базируется на результатах осмотра врача, включающего обязательное пальцевое исследование прямой кишки через задний проход (а у женщин еще и через влагалище), биопсию и инструментальные методы обследования (КТ или МРТ, рентгенографию, томографию и другие).
В связи с этим обязательными и необходимыми для выбора правильного метода лечения являются следующие анализы и инструментальные методы исследования:
Этот тест позволяет оценить число разных типов клеток в крови. Например, эритроцитов, низкий уровень которых может свидетельствовать о потере крови через опухоль, или высокий уровень лейкоцитов, позволяющий заподозрить воспаление в зоне опухоли, что усугубляет течение заболевания.
Наличие в организме раковой опухоли прямой кишки особенно на поздних стадиях, когда злокачественные клетки попадают в лимфу или кровь, сопровождается появлением в организме специфических белков-антигенов, которые могут быть обнаружены при выполнении специального анализа - определения онкомаркеров. Тестирование на этот маркер позволяет отследить ответ на лечение или заподозрить возврат заболевания при неуклонном росте его значений в процессе наблюдения после проведенного лечения.
Этот тест измеряет количество различных химических веществ в крови. Аномальные уровни некоторых из этих химических веществ могут указывать на то, что рак распространился на другие органы в частности на печень. Высокие уровни других химических веществ может указывать на проблемы с другими органами, такими как почки.
Эти два исследования, как правило, выполняющиеся одновременно, помогают определить распространение рака прямой кишки на другие органы - печень и легкие, а также установить вовлеченность в процесс отдаленных от прямой кишки групп лимфатических узлов.
МРТ крайне важное для определения распространенности рака прямой кишки исследование. Оно обеспечивает детальное изображение всех деталей строения прямой кишки и вовлеченности в злокачественный процесс слоев стенки кишки и окружающей ее брыжейки, поражение лимфатических узлов рядом с прямой кишкой, прорастание опухоли в мышцы запирательного аппарата, соседние органы и структуры.
Благодаря своей сверхвысокой точности (более 95%) МРТ используется врачами для установления стадии ракового новообразования и правильного планирования лечения. Кроме того, благодаря получению первоначальных данных о раке прямой кишки в последующем можно точно оценить эффективность проводимого лечения, что крайне важно при использовании лучевой терапии до операции, поскольку проводимое лечение может в корне изменить ситуацию в пользу проведения более благоприятных для пациента функционально и органосохраняющих операций.
Ознакомившись с результатами обследования, врач должен проинформировать Вас о стадии Вашего заболевания. Чтобы говорить на одном понятном для всех специалистов во всех странах мира языке в повседневной практике используют систему буквенных (T, N и М, а также a, b, и c) и цифровых (от 0 до 4) символов для обозначения стадии рака любой локализации, в том числе и рака прямой кишки.
Символ Т (tumor) характеризует саму опухоль прямой кишки и показывает насколько она распространилась по стенке прямой кишки и на близлежащие ткани и органы.
Символ N (node) показывает состояние лимфатических узлов, расположенных как в прямой кишке рядом с опухолью, так и в других частях организма человека. Это очень важный показатель, так как лимфатические узлы - это небольшие скопления клеток вашей иммунной системы круглой или бобовидной формы, по которым рак часто распространяется в самую первую очередь.
Символ М (metastasis) характеризует наличие или отсутствие распространения рака на другие органы и обозначает отдаленные метастазы. Рак прямой кишки в принципе может поражать любой орган человеческого тела, но наиболее часто метастазы обнаруживаются в печени или легких.
Цифры и буквы после обозначенных символов дают более подробную информацию, поскольку указывают на степень распространения опухолевого процесса в соответствии с этими тремя направлениями. Общий принцип заключается в том, что чем больше распространен рак, тем выше порядок используемой цифры или буквы после символа.
| T | N | M |
|---|---|---|
| is – рост опухоли в пределах слизистой | 0 – нет данных за поражение лимфатических узлов | 0 – нет данных за наличие отдаленных метастазов |
1 опухоль врастает, но не прорастает подслизистый слой кишки | 1 поражение от 1 до 3 лимфатических узлов | 1 наличие отдаленных метастазов опухоли |
2 опухоль врастает, но не прорастает мышечный слой кишки | 2 поражение больше, чем 3 лимфатических узлов | х неизвестно, имеются ли метастазы |
3 опухоль прорастает через мышечный слой в окружающие ткани | х неизвестно, поражены ли лимфатические узлы | |
4 опухоль врастает в окружающие органы |
После того, как врач ознакомится с результатами вашего обследования, он получает возможность сгруппировать все три символа с их обозначениями в единое целое. Совокупность этих обозначений позволяет ему определить клиническую стадию конкретно вашего рака прямой кишки.
Все раки прямой кишки попадают в одну из пяти возможных стадий (от стадии 0 до стадии 4). Стадия рака прямой кишки определяется на основании суммы данных о глубине прорастания кишечной стенки опухолью, вовлеченности в процесс соседних с прямой кишкой тканей и органов, лимфатических узлов, а также распространением на отдаленные органы (печень, легкие и др.). Описанное ранее для символов правило действует и при обозначении стадий - чем выше цифра, тем более поздней и запущенной является стадия заболевания.
Ниже описаны стадии заболевания и варианты их лечения. В большинстве случаев при лечении необходимо выполнять хирургическое вмешательство, заключающееся в резекции (удалении) участка кишки с опухолью. Однако целому ряду заболевших для достижения лучших результатов требуется проведение дополнительных методов лечения, таких как лучевая или химиотерапия.
Для неспециалистов, каковыми являются большинство заболевших раком прямой кишки, понять все нюансы бывает не просто, поэтому не стесняйтесь задавать любые волнующие вас вопросы лечащему врачу.
В упрощенной форме стадии можно представить следующим образом:
Раковые клетки обнаруживаются лишь на слизистой оболочке, чаще на слизистой выстилающей поверхность полипа. Эта стадия известна как неинвазивный или интраэпителиальный рак и обозначается как рак insitu (символ Tis). Поэтому полипэктомия при колоноскопии или операции через задний проход (анус), если очаг поражения слишком велик, чаще всего представляют из себя окончательный вариант лечения.
Рак распространяется по слизистой оболочке, переходит на подслизистый слой прямой кишки, иногда проникая в ее стенку, но не выходит за пределы мышечного слоя. Стандартным лечением 1 стадии рака прямой кишки обычно является ее резекция, при которой пораженная часть кишки и ее лимфатические узлы, располагающиеся в брыжейке, удаляются. В зависимости от места расположения опухоли применяется передняя резекция или низкая передняя резекция, реже - брюшно-промежностная экстирпация прямой кишки. Исключительно редко в условиях специализированных центров возможен отказ от резекции прямой кишки в пользу полностенной полипэктомии или местного иссечения с оставлением большей части кишки, однако этот вопрос всегда находится в рамках совместного решения врача и пациента, ознакомленного с повышенным риском возврата болезни с неблагоприятным в последующем исходом в результате такого подхода.
Рак проник за пределы мышечного слоя толстой кишки (стадия 2а) и даже смог распространиться окружающую ее на жировую ткань (стадия 2b) и даже прорасти в соседние органы (2c). Однако он еще не достиг лимфатических узлов. Как правило, лучшим решением является выполнение хирургической резекции прямой кишки (передняя резекция или экстирпация). В некоторых случаях возможно применение дополнительной химиотерапии после операции.
Опухоль вовлекает лимфатические узлы рядом с прямой кишкой, а также ткани и соседние органы за пределами стенки прямой кишки. Хотя большинство национальных руководств призывает начинать лечение 3 стадии с химиолучевой терапии, в ряде стран Европы, где достигнуты наилучшие результаты лечения, рекомендуют выделять среди больных этой стадии группу с низким риском местного возврата заболевания. Данная группа выделяется на основании совместного решения МРТ-специалиста и оперирующего хирурга о том, возможно ли достичь негативного края резекции при удалении опухоли, то есть не соприкоснувшись с ее поверхностью. В этом случае целесообразно отказаться от проведения лучевой терапии до операции, поскольку она часто ухудшает функциональные результаты лечения, вызывая расстройства мочеиспускания, импотенцию, недержание кала). Если признается, что достичь негативного края резекции невозможно или есть надежда на уменьшение опухоли, что может существенно изменить первоначальный план хирургического лечения, то решение принимается в пользу проведения перед операцией химиолучевой терапии.
Опухоль распространилась на отдаленные органы и лимфатические узлы, лежащие на значительном расстоянии от прямой кишки. Вся группа пациентов 4 стадией рака очень неоднородна, и в целом характеризуется плохим прогнозом, однако следует сказать, что в их лечении за последние 10-15 лет достигнут значительный прогресс. При определенном стечении обстоятельств возможно добиться даже выздоровления или более чем 5-летней продолжительности жизни с момента установки диагноза. Как правило, этого удается достичь среди части больных с единичными (не более 3) метастазами в печени, реже - в легкие. Для остальных пациентов с 4 стадией рака прямой кишки стандартом является проведение различных вариантов химиотерапии с подключением таргетных препаратов (усиливающих эффект химиолечения) с целью максимального продления жизни и уменьшения симптомов проявления заболевания. Хирургическое лечение кроме первой группы с благоприятным течением метастатической формы рака прямой кишки применяется лишь для устранения симптомов, связанных с прогрессией первичной опухоли в прямой кишке. В последние годы в ряде стран Востока в лечении больных, которым невозможно удалить метастазы с успехом используется удаление первичной опухоли до начала химиотерапии. Опыт этих центров, наряду с опытом нашей клиники, свидетельствует о продлении жизни таким больным от 6 до 12 месяцев дополнительно к химиотерапии при лучшем качестве жизни из-за отсутствия проявлений, связанных с ростом первичной опухоли прямой кишки. Иногда с паллиативной целью могут быть использованы радиочастотная абляция и криодеструкция, а также высокоточная терапия опухолевых метастатических очагов.
До начала лечения стадия устанавливается с помощью магнитно-резонансной томографии малого таза (МРТ), которая сегодня является “золотым стандартом” диагностики рака прямой кишки, компьютерной томографии грудной клетки и органов брюшной полости. Кроме того, ваш врач должен принять во внимание выполненные анализы крови и отклонения в них.
Кроме стадии заболевания для правильного выбора метода лечения врачу необходимо знать - насколько агрессивна опухоль в прямой кишке. Об агрессивности судят по степени дифференцировки опухоли при изучении биопсии. Выделены три степени, располагающиеся от менее к более агрессивной: хорошо или высоко дифференцированная аденокарцинома, средне или умеренно дифференцированная и низко или плохо дифференцированная аденокарцинома. Высокодифференцированные опухоли имеют тенденцию к медленному росту и распространению на другие органы. В отличие от них, низкодифференцированные раки отличаются быстрым ростом и более частым поражением отдаленных органов (печень, легкие), поэтому им часто требуется более агрессивное лечение.
Дополнительно об агрессивности опухоли и о возможности возврата рака прямой кишки могут свидетельствовать выявление в удаленном участке кишки отдельно лежащих от очагов опухоли, называемых опухолевыми депозитами, а также признаков вовлечения в злокачественный процесс окружающих опухоль кровеносных (венозных) или лимфатических сосудов, которые обозначаются как лимфо-венозная инвазия. Присутствие любого из вышеперечисленных признаков агрессивного характера опухолевого процесса является поводом для обсуждения с врачом необходимости назначения химиотерапевтического лечения в послеоперационном периоде.
В том случае, если вы, по рекомендации лечащего врача, приняли решение о необходимости проведения химиотерапии, на повестку дня встает вопрос об оптимальном выборе препаратов, режимов их введения и дополнительной терапии, усиливающей эффект от химиолечения - таргетной терапии. Здесь главным помощником выступает молекулярно-генетическая диагностика опухоли. Прежде всего это исследование видов мутаций генов Kras и Braf и маркеров механизмов, направленных на восстановление поврежденных участков генов - MMR и MSI. Комплексный анализ полученных данных позволит врачу оптимизировать проводимое лечение, а в некоторых случаях отказаться от него в виду заведомой неэффективности.
В заключении следует сказать, что до операции врач устанавливает стадию рака прямой кишки исключительно по данным инструментальных методов исследования, которая с высокой степенью вероятности, в зависимости от опыта врачей их проводивших, позволяет правильно разработать программу вашего лечения. В этом случае определяется КЛИНИЧЕСКАЯ стадия заболевания. Она является лишь предварительной.
Окончательно стадия заболевания устанавливается на основании данных исследования удаленного участка кишечника врачом-морфологом в отделении патоморфологии, поэтому она носит название ПАТОМОРФОЛОГИЧЕСКОЙ.
Только после получения патоморфологического заключения врач получает возможность обсудить с вами прогноз течения болезни и наметить шаги дальнейшего лечения и наблюдения.
Для того чтобы вам было проще представить себе общие правила, которыми должен руководствоваться лечащий врач при принятии решения на основании установленной клинической стадии заболевания, мы свели все вышеизложенное в таблицу, которая позволит вам легче ориентироваться в получаемой информации
| Стадия | Лечение |
|---|---|
| Стадия 0 |
|
| Стадия 1 |
|
| Стадия 2 |
|
| Стадия 3 |
|
| Стадия 4 |
|
Ведущую роль в лечении рака прямой кишки играет хирургическое лечение. Однако для более эффективного воздействия на опухоль прямой кишки, также, как и на большинство других онкологических заболеваний, часто требуется применение более чем одного вида лечения. Другими словами, для лечения рака прямой кишки в ряде случаев требуется комбинированное лечение - применение комбинаций из двух или даже трех методов лечения.
Также как и во всей онкологии для лечения рака прямой кишки используются следующие методы лечения:
* - у больных раком прямой кишки, химиотерапия часто используется вместе с лучевой терапией до операции.
Выбор вида операции зависит от целого ряда факторов, к числу которых относятся факторы, связанные с болезнью, с общим состоянием организма заболевшего человека, с лечебным учреждением, в котором будет проводиться лечение и, возможно, один из главных фактов – квалификацией врачей, принимающих непосредственное участие в лечении.
Первые две категории факторов, определяющих выбор метода лечения рака прямой кишки можно изменить лишь в незначительной степени, тогда как анализ факторов, связанных с учреждением, в котором вы собираетесь проходить лечение и выбор хирурга - являются целиком вашей прерогативой.
Хорошо известна история с одним из основателей современной классификации рака прямой кишки по стадиям Гутбертом Дюксом. Всю свою жизнь этот выдающийся морфолог посвятил изучению факторов, влияющих на исход хирургического лечения (других видов в начале 20-го века просто не было).
В конце жизни ему задали вопрос, надеясь получить чудесный рецепт избавления от рака прямой кишки от этого экстраординарного человека:
«Что бы вы сделали, если бы у вас обнаружили рак прямой кишки?»
Последовал на удивление краткий, но практически всеобъемлющий ответ:
«Я бы нашел самого лучшего хирурга, попросил бы его лечь пораньше спать накануне моей операции и …. вверил бы свою судьбу Богу!»
В этом на первый взгляд ироничном ответе заложено все то, о чем мы говорили с вами выше. Есть вещи, которые при этом заболевании мы изменить не можем, а можем лишь уповать на провидение.
В то же время есть самое главное, что находится в руках заболевшего рака прямой кишки – это выбор хирурга и учреждения, в котором он может выполнить вам операцию. Помните, что невозможно для хорошего хирурга работать в среднем или слабом учреждении.
И еще. Рак прямой кишки относится к категории хирургически зависимых заболеваний (от качества хирургии зависит и факт выздоровления и качество жизни после операции), поэтому не торопитесь делать свой выбор, возьмите второе мнение, поинтересуйтесь результатами - не забудьте про факторы, которые влияют на результат.
После того, как вы определитесь с местом, где будете лечиться и врачом, который будет вас оперировать, вам предстоит узнать о том, какая операция будет выполнена, какие изменения она принесет в вашу жизнь и каков вероятный прогноз после ее выполнения. При раке прямой кишки, хотя и редко, но случаются ситуации, когда при одной и той же опухоли в разных учреждениях и даже разными хирургами вам могу предложить различные варианты операции. Поэтому внимательно ознакомьтесь с кратким описанием каждой из приведенных ниже операций, чтобы подробно обсудить с врачом все возможные варианты.
Перед каждым хирургом, готовящимся к операции по поводу рака прямой кишки, стоит необходимость удалить опухоль и минимизировать возможные негативные последствия, которыми сопровождается это удаление. Применительно к хирургии рака прямой кишки эти цели достигаются в процессе решения следующих задач:
Достижениями последних десятилетий в хирургии и хирургии рака прямой кишки в частности является то, что наряду с традиционной хирургией, в которой для удаления новообразования используются разрезы передней брюшной стенки или промежности, появилась возможность использовать малоинвазивные методы. К ним относятся:
Сегодня нет данных о преимуществах какого-либо из этих методов с точки зрения онкологического исхода лечения, однако имеется ряд данных свидетельствующих о преимуществах малоинвазивных методов (лапароскопического или роботического) с точки зрения течения раннего и позднего послеоперационного периода.
Операции по удалению рака прямой кишки в Клинике колопроктологии и малоинвазивной хирургии ПМГМУ им. И.М.Сеченова
В начале 20-го века эта операция открыла путь к успешному лечению рака прямой кишки. Она заключается в удалении не только прямой кишки, но и заднего прохода (анального сфинктера) с выведением противоестественного ануса (колостомы) на переднюю брюшную стенку слева от пупка. На протяжении почти всего прошлого столетия эта операция рассматривалась как самая радикальная по отношению к опухоли. Однако, неконтролируемое выделение кишечного содержимого через не естественное отверстие на протяжении всей последующей, пусть и спасенной жизни, было и остается главным недостатком этой операции.
Появление специальных приспособлений для сбора кала и газов, выделяющихся через стому, в значительной степени изменили ситуацию к лучшему, сделали жизнь после экстирпации прямой кишки социально и физиологически более удобной. Однако страх перед последствиями этой операции все еще присутствует у людей, которым впервые сообщили о необходимости дальнейшей жизни со стомой.
Широкое использование операций с сохранением естественного хода кишечника почти вытеснило брюшно-промежностную экстирпацию прямой кишки из арсенала хирургических вмешательств, однако она все еще остается наиболее эффективным вмешательством в ситуации, когда раковая опухоль проросла большую или значительную часть сфинктера. В таких случаях только полное удаление ануса позволит хирургу избежать фатального для больного контакта с опухолью во время операции.
Альтернативой экстирпации прямой кишки при расположении опухоли не менее 1 см выше уровня анального сфинктера является брюшно-анальная резекция прямой кишки с последующим соединением вышележащего отдела ободочной кишки (как правило, сигмовидной с анальным каналом). При этом хирург использует комбинированный доступ для резекции участка прямой кишки несущего опухоль – со стороны брюшной полости и со стороны анального канала. Именно отсюда данная операция получила свое название – брюшно-анальная резекция.
Соединение резецированных участков кишечника производят со стороны анального канала путем наложения отдельных швов. Поскольку при этой операции удаляется вся прямая кишка, в процессе последующей жизни и наиболее остро в первый год после операции человек остро ощущает ее утрату, так как другие участки ободочной кишки, в том числе и сигмовидная, не обладают способностью к накоплению кишечного содержимого, что проявляется частыми и порой мучительными опорожнениями. С целью компенсации этого явления, хирурги часто формируют мешкообразное расширение из сигмовидной кишки, чтобы увеличить накопительную способность последней. Такое расширение обозначается как резервуар.
Еще одним непременным атрибутом этой операции является формирование временной стомы на вышерасположенные отделы кишечника с целью отведения каловой струи от зоны сформированного анастомоза и создания для него благоприятных условий для заживления. Связано это с тем, что в случае прохождения кала в послеоперационном периоде из-за подвижности ануса возникает высокая вероятность расхождения наложенных хирургом швов и разрушения линии анастомоза.
Такое осложнение кроме непосредственной угрозы жизни может привести к тяжелым функциональным расстройствам в течение всей последующей жизни человека. Поэтому хирургами всего мира принята тактика формирования защитной (протективной или превентивной) стомы. Такая стома носит сугубо временный характер и, как правило, закрывается в течение ближайших 1,5 – 2-х месяцев после первой операции, возвращая оперированному человеку привычный способ опорожнения кишечника через естественный задний проход.
Данная операция во многом похожа на вышеописанную брюшно-анальную резекцию. Отличием является то, что формирование анастомоза осуществляется при помощи специальных сшивающих аппаратов, используя для удаления прямой кишки доступ со стороны брюшной полости, то есть спереди от прямой кишки. Отсюда и название операции – передняя резекция. Кроме того, появление в названии термина «низкая» означает, что также, как и при брюшно-анальной резекции прямой кишки, удалению подлежит практически вся прямая кишка, а анастомоз формируется непосредственно над уровнем заднего прохода. Это, в свою очередь, означает необходимость формирования резервуара на конце сигмовидной кишки и создание временной стомы на передней брюшной стенки.
Отличительной особенностью этой операции от предыдущих двух является то, что она выполняется для более высоко расположенных раков прямой кишки – выше 10 см от края заднего прохода. Онкологические правила позволяют хирургу при таком расположении опухоли оставить нижнюю часть прямой кишки (не менее 3см), удаляя при этом все возможно пораженные отсевы опухоли. Сохранение части прямой кишки дает значительные преимущества по сравнению с полным ее удалением. Первое – это сохраняется первоначальная способность оставшейся части кишки к накоплению калового содержимого, а значит, отпадает необходимость в формировании резервуара. Второе – в связи с отдаленностью линии швов анастомоза от анального отверстия, вероятность его разрушения в послеоперационном периоде резко уменьшается, хотя и не исчезает совсем. Поэтому большинство хирургов предпочитают обходится без формирования временной стомы для защиты этого анастомоза. Данная операции является таким образом одноэтапной. Следует также сказать, что операция выполняется со стороны брюшной полости, а концы кишечника соединяются как с помощью специальных сшивающих аппаратов, так и швами, которые накладывает непосредственно хирург.
Этот относительно молодой вид операций, разработанный в мире в конце 20-го века, в том числе при огромном вкладе проф. Царькова П.В., который одним из первых в мире обосновал правомерность такого рода операции с онкологических позиций. Она используется при раках прямой кишки в относительно ранних стадиях с расположением в зоне запирательного аппарата, но лишь частичным его поражением. Техника выполнения ее в целом аналогичная брюшно-анальной резекции прямой кишки, однако, линия резекции со стороны анального канала проходит на уровне его середины и сопровождается частичным или полным удалением внутреннего сфинктера анального канала, который отвечает за непроизвольное (неконтролируемое человеком) держание кишечного содержимого. Несмотря на сохранение части внутреннего сфинктера и наружного сфинктера, которым человек может целенаправленно контролировать процесс сжатия анального канала, функциональные исходы операции далеки от идеальных (недержание газов и жидкого кала), поскольку в верхней части анального канала расположена зона, где располагаются нервные окончания, которыми человек может регулировать процесс нормального опорожнения. В связи со сложностью выполнения этапа операции через задний проход без нарушения принципов онкологического радикализма, эта операция остается прерогативной лишь узкого круга специализированных учреждений и имеет ограниченные показания.
Это самый молодой вид хирургического вмешательства при раке прямой кишки, когда для выделения дистальной части прямой кишки, которая у ряда людей представляет определенные анатомические трудности, используется специальная эндоскопическая трансанально устанавливаемая платформа, позволяющая выполнить данный этап операции, снизив вероятность повреждения прямой кишки и контакта с ее краем. Следует сказать, что в настоящий момент данный вид операций при раке прямой кишки проходит стадию клинической апробации в клиниках экспертного уровня и еще не рекомендован ни в одной стране мира, как метод выбора лечения рака прямой кишки.
Эта операция при раке прямой кишки предполагает удаление всей толстой кишки вплоть до анального канала или вместе с ним при прорастании последнего опухолью. Тотальная колэктомия используется крайне редко и только в тех случаях, когда одновременно с раковой опухолью прямой кишки выявляются другие опухоли в ободочной кишке, которые не позволяют сохранить хотя бы небольшой участок последней. Кроме того, эта операция выполняется людям с наследственными заболеваниями, при которых уже выявлена или раковая опухоль, или же риск ее появления крайне высок. В последнем случае диагноз должен быть подтвержден генетическими анализами.
Операция заключается в резекции участка прямой кишки, ушивании ее культи наглухо и выведении вышележащего отдела сигмовидной кишки на переднюю брюшную стенку в виде колостомы. Выполняется достаточно редко в специализированных учреждениях, поскольку повторная операция по восстановлению естественного хода кишечника представляется собой технически сложное и травматичное вмешательство с высокой вероятностью осложнений как во время самой повторной операции, так и после нее. Самым частым показанием к ее проведению, является кишечная непроходимость, обусловленная сужением просвета кишки опухолью, которая многократно увеличивает риск разрушения анастомоза в послеоперационном периоде, которое может повлечь серьезные осложнения вплоть до гибели. Реже операцию Гартмана выполняют пациентам с тяжелыми сопутствующими заболеваниями или при частичном удалении опухоли.
Местное иссечение представляет из себя операцию через задний проход (крайне редко через параректальный доступ), когда опухоль удаляется в пределах здоровых тканей (отступ не менее 0,5 см во все стороны от нее, в том числе и вглубь кишечной стенки). Местное иссечение вынимает опухоль прямой кишки вместе с запасом здоровой ткани и разрез стенки прямой кишки ниже опухоли. Особенностью применения данной операции является необходимость тщательного обследования на экспертном уровне до операции, чтобы решить вопрос о возможности удаления опухоли в пределах здоровых тканей и быть уверенным в отсутствии поражения лимфатического аппарата вне зоны удаления. Присутствие метастазов в лимфатических узлах или неполностью удаленная опухоль неизбежно станут причиной возврата заболевания и с большой степенью вероятности приведут к гибели. И это несмотря на то, что правильное использование вышеописанных резекций почти на 100% может гарантировать выздоровление. Поэтому большинство центров экспертного уровня расценивает местное удаление опухоли, как способ окончательной диагностики стадии процесса и после выполнения интра- или послеоперационной биопсии уже принимается окончательное решение – остановиться на этом и наблюдать или резецировать прямую кишку одним из вышеописанных способов.
Преимуществами местных операций является их малая травматичность и хорошие функциональные исходы. К числу неудобств после местного удаления опухоли можно отнести более тщательный (более частый) режим послеоперационного наблюдения, с практически ежемесячными обследованиями в течение первого года после операции.
Это разновидность местного иссечения опухоли с использованием специальной эндовидеохирургической платформы, позволяющей удалять и восстанавливать целостность стенки кишки более точно и с хорошей визуализацией.
Чаще всего является этапом выполнения стандартных резекций прямой кишки по поводу рака, описанных выше. Включает три вида лимфодиссекций:
В том случае, когда опухоль близко подходит к какому-либо органу малого таза или брюшной полости или прорастает в него, для обеспечения радикального ее удаления необходимо выполнять их одновременные резекции. Спереди от прямой кишки это могут быть влагалище, матка, яичники у женщин и предстательная железа, смененные пузырьки и мочевой пузырь с мочеточниками и уретрой у мужчин. Максимальный объем оперативного вмешательства в такой ситуации обозначается как Эвисцерация таза или удаление органов таза. Более часто используются резекции указанных органов. Следует отметить, что выполнение таких операций сопряжено с более высоким риском развития послеоперационных осложнений и более длительного периода послеоперационного восстановления.
В тех ситуациях, когда до операции выявляются отдаленные метастазы (в печени, легких, селезенке, почках, по брюшине) может быть выполнено одномоментное вмешательство на прямой кишке и органе, несущем метастаз. Следует сказать, что это решение всегда принимается индивидуально и подлежит тщательному обсуждению с больным для понимания возникающих преимуществ и недостатков такого рода подхода к лечению рака 4 стадии.
Люди с раком прямой кишки, ассоциированных с болезнью Крона, язвенным колитом или генетическая предрасположенность к колоректального рака, как правило, необходима операция, которая является более обширной, чем описанные здесь. Химиотерапия тоже нужно до или после операции.
Это этап хирургического вмешательства при 4 стадии рака прямой кишки, когда метастазы опухоли распространяются по поверхности брюшины, которая покрывает как стенки брюшной полости, так и все органы в ней расположенные. Удаление участков брюшины, пораженных раковыми клетками, направлено на удаление очагов, которые видимы хирургу. Раствором химиопрепарата (Митомицин) нагретым до 40°C, который с помощью специальной аппаратуры либо распыляют под давлением в брюшной полости, либо заставляют циркулировать в ней на протяжении 2-х часов, воздействуют на клетки, которые остаются на поверхности брюшины, но невидимы глазу хирурга или не могут быть удалены в силу объективных причин.
После операции
В зависимости от тяжести оперативного вмешательства и общего состояния вашего здоровья пребывание в палате интенсивной терапии продолжается от нескольких часов до нескольких дней.
Особого внимания в этот период требуют пациенты старческой возрастной группы (старше 75 лет) и с тяжелыми сопутствующими заболеваниями (инфаркт миокарда или инсульт в прошлом и т.п.). Участие родственников на данном этапе для таких людей становится критически важным и крайне полезным.
Обычный срок пребывания пациента в стационаре колеблется от 5-7 дней (после эндоскопических или роботических операций) до 10-12 дней после традиционных вмешательств. На протяжении этого периода оперирующий хирург, врач и медсестры посоветуют вам, как правильно питаться, принимать медикаменты и проводить процедуры, определят оптимальный режим физических нагрузок.
Как правило, прием жидкостей или пищи начинается в конце первого дня или на следующий день после операции и одновременно начинается постепенно возрастающая физическая активность. Такой подход позволит предупредить целый ряд осложнений в послеоперационном периоде и снизить отрицательные последствия оперативного вмешательства.
После выписки вы можете продолжить наблюдение и лечение как с участием врачей клиники, так и с участием врачей поликлиники по месту жительства.
Согласно большинству мировых национальных и общеевропейских рекомендаций, стандартом лечения рака прямой кишки 3 стадии является сочетание химиотерапии и лучевой (химиолучевой терапии),проводимой до хирургической операции. При этом подчеркивается, что данный подход предпочтительнее использовать при раках, имеющих высокую вероятность возникнуть повторно в месте, где находилась удаленная опухоль. Целый ряд исследований, проведенных в Европе в конце 90-х и начале 00-х годов, а также появление в арсенале диагностических методов магнитно-резонансной томографии (МРТ) высокого разрешения, позволили прийти к заключению, что 3 стадия до операции может быть разделена на опухоли высокого и низкого риска развития местного рецидива. Это позволило в ряде стран северной Европы успешно реализовать селективный подход к проведению химиолучевой терапии на дооперационном этапе, подвергая ей только пациентов с высоким риском местного возврата заболевания. Такой подход позволяет исключить негативные последствия проведения химиолучевой терапии.
Преимущества предоперационной химиолучевой терапии включают в себя:
Нежелательные последствия предоперационной химиолучевой терапии:
Обычный период между предоперационной химиолучевой терапии и хирургии составляет от 6 недель до 12 недель в зависимости от эффекта проведенного лечения.
Стратегия «наблюдай и жди» после полного исчезновения опухоли в результате проведения химиолучевой терапии.
У ряда людей результатом проведения химиолучевой терапии является полное исчезновение опухоли в просвете кишечника. В случае с высоким расположением опухоли, когда она первоначально располагалась вне зоны сфинктера, рекомендуется выполнение резекции прямой кишки, поскольку на сегодня нет методов обследования, включая МРТ и ПЭТ-КТ, позволяющих полностью исключить поражение прежде всего лимфатических узлов вокруг опухоли и на отдалении от нее. Это неизбежно приведет к возврату заболевания.
В случаях, когда опухоль располагалась и вовлекала в процесс анальный сфинктер, сегодня признается возможным наблюдение опухоли в случае ее полного исчезновения по данным МРТ через 12-16 недель после химиолучевой терапии. Это отличие от предыдущего подхода для более высокорасположенных раков определяется тем, что больным с такой локализацией необходимо выполнять операцию с удалением заднего прохода и формированием стомы на передней брюшной стенке. С учетом желания пациентов сохранить естественный путь опорожнения и вероятностью полного выздоровления из (20-30%) врачебное сообщество допускает в исключительных случаях продолжить тщательное наблюдение за больными (в течение первых 2-3 лет с интервалами 1-3 месяца с частым МРТ и КТ контролем). При этом пациент должен четко осознавать и подписать информированное согласие о том, что повышенный риск продолжения заболевания означает более частое обследование по сравнению с людьми, перенесшими традиционное лечение, а потеря времени на переход к традиционной хирургии может означать потерю контроля за течение заболевания и привести к гибели, которой можно было бы избежать, выполнив операцию в обычные для лечебной тактики рака прямой кишки сроки.
Стандартно ведущим методом лечения рака прямой кишки с диагностированными метастазами в другие органы является химиотерапия, которая в большинстве случаев позволяет продлить жизнь и уменьшить тягостные симптомы, связанные с ростом опухоли. Однако в тех ситуациях, когда имеются такие осложнения опухоли, как непроходимость, воспаление в зоне опухоли, образование свищей или кровотечение, целесообразно начинать лечение с ее удаления одним из описанных выше методов. Такой подход позволяет не только предупредить фатальные последствия этих осложнений, но и продлить жизнь, улучшив условия для проведения химиотерапии и ее эффективность.
Последнее обстоятельство и наблюдение за больными, перенесшими удаление первичной опухоли, позволили целому ряду ведущих мировых центров, в том числе и Клинике Колопроктологии и Малоинвазивной Хирургии, реализовать концепцию предпочтительного и радикального удаления опухоли прямой кишки при метастатическом колоректальном раке. Результаты, полученные в ходе наблюдения за оперированными больными, получавшими впоследствии современную химиотерапию, показали, что операция сама по себе позволяет больным дополнительно прожить еще год без тягостных проявлений прогрессии первичного опухолевого очага. При этом у ряда пациентов после проведения химиотерапии появляется возможность удаления метастатических очагов, что может привести к выздоровлению 20-30% людей.
Химиотерапия является средством лекарственного воздействия на опухолевый процесс. Принцип ее действия основан на способности целого ряда химиопрепаратов уничтожать раковые клетки, обладающие способностью к более быстрому делению, чем здоровые клетки организма. Лекарства воздействую на клетки, находящиеся в фазе активного деления и убивают их. Следует понимать, что опухолевые клетки крайне разнородны и поразному отвечают на химиотерапевтические препараты. Вот почему случаев излечения после применения только химиотерапии при раке прямой кишки нет, и она должна быть использована в совокупности с хирургическим или лучевым лечением, усиливая эффект последних.
Кроме использования химиотерапии в качестве средства усиливающего эффективность лучевой терапии опухоли, она может также применяться в послеоперационном периоде у больных с высоким риском появления отделенных метастазов, у которых выявлены поражение лимфатических узлов, опухолевые депозиты, лимфоваскулярная инвазия, прорастание в соседние органы или ткани.
Также обязательным (при отсутствии противопоказаний) является использование химиолечения у больных 4 стадией рака.
Для проведения химиотерапии сегодня доступен целый ряд химиопрепаратов и наилучшим выбором является их различные сочетания, поскольку они по-разному воздействуют на раковые клетки. По разным оценкам проведение химиотерапии у больных 3 стадии заболевания, перенесших радикальное удаление опухоли, позволяет снизить риск возврата заболевания на 3 – 10% по сравнению с людьми, которым в дополнение к операции не проводилось такого лечения.
Перед назначением химиотерапии необходимо учитывать риски побочных эффектов, которые она в себе несет. Некоторые из них имею обратимый и не выраженный характер и могут быть вылечены, в то время как другие могут привести к серьезным последствиям и даже повлечь за собой гибель. Поэтому назначение химиотерапии всегда остается прерогативой команды врачей, которая занимается вашим лечением.
Кроме химиопрепаратов в арсенале лечения рака прямой кишки в последние годы появились специальные биологические препараты, которые воздействуют на различные факторы роста опухолевых клеток, блокируя их, но не убивая саму клетку. Совместное использование таких лекарств, получивших название таргетные препараты, с химиопрепаратами позволяет более эффективно воздействовать на опухолевые клетки метастатических очагов, особенно печеночные метастазы.
Следует признать, что из-за поздней обращаемости или в результате неэффективности проводимого лечения в целом ряде случаев отсутствует реальная возможность предпринять попытка радикального воздействия на опухоль. Отсутствие возможности излечить заболевание не означает, что больному нельзя помочь. В данных ситуациях человеку оказывается паллиативная помощь, которая направлена на облегчение болей и других серьезных и порой угрожающих жизни симптомов болезни. Специалисты паллиативной помощи призваны работать как с самим пациентом, так и с его семьей и другими врачами, чтобы обеспечить дополнительный уровень поддержки.
Примером паллиативной помощи может быть хирургическое вмешательство по формированию стомы, чтобы ликвидировать непроходимость, вызванную сужением кишки в зоне опухоли, или отвести каловую струю от места образования свища между прямой кишкой и мочевым пузырем.
Паллиативный уход предоставляется группой врачей, медсестер и других специально обученных специалистов, которые объединяются в отделения паллиативной помощи или хосписы и призваны улучшить качество жизни людей страдающих раком и их семей.
Перечисленная группа врачей на постоянной основе (еженедельно) обсуждает все важнейшие этапы вашего лечения. Важным фактором успеха лечения является высокая квалификация каждого участника, обладание определенным опытом работы в прошлом и способность к высокой степени взаимодействия внутри этой группы. Только эти факторы помогут правильно, без субъективных предпочтений каждого из участников команды предложить вам для обсуждения все самые современные методы лечения и помочь вам и вашим родным принять верное решение о пути лечения заболевания. Этот выбор должен быть основан на точном понимании особенностей течения вашего заболевания, включая данные о стадии рака, его биологических и генетических особенностях персонализируя лечебную тактику и программу последующего наблюдения.
Кроме перечисленных специалистов в ситуациях, когда опухоль прорастает в соседние органы или ткани, могут быть привлечены уролог, гинеколог, сосудистый хирург, вертеброг (специалист по операциям на позвоночнике), гепато-билиарный хирург, нейрохирург, торакальный хирург, эндокринолог, психиатр, психолог, кардиолог, эндокринолог, гастроэнтрологи т.д.
Рак прямой кишки относится к категории раков с относительно благоприятным течением. Это означает, что большинство заболевших имеют шанс навсегда избавиться от болезни, хотя порой лечение будет достаточно продолжительным и нелегким. Несмотря на то, что после получения результатов морфологичесого анлиза и других исследований врач в целом может описать возможные варианты развития событий, следует признать, что точное составление индивидуального прогноза на сегодняшний день невозможно. Это значит, в течение как минимум ближайшего времени вам предстоит жить в состоянии неопределенности относительно своей дальнейшей судьбы, лучшим лекарством от которой будет время, прожитое вне заболевания и постепенное обретение уверенности в благоприятном исходе. Всегда помните, что это состояние присуще любому человеку, прошедшему лечение по поводу рака.
Следует также признать, что, несмотря на проводимое лечение, у части заболевших не удается полностью излечить рак прямой кишки. В этой ситуации часто приходится прибегать к проведению химио- или лучевой терапии, чтобы попытаться взять под контроль течение заболевания. Такое лечение может быть трудным и потребует концентрации всех ваших сил. Кроме физических сил, вам будет необходимо научиться жить со своей болезнью, что является трудной задачей. И здесь вам потребуется не только помощь специалистов медиков, но и поддержка окружающих вас близких людей.
Уже в стационаре и конечно сразу после выписки вам необходимо шаг за шагом предпринимать усилия для того, чтобы возвратиться к привычным для себя вещам. Иногда этого удается достичь в полной мере, хотя нередко после лечения рака прямой кишки приходится сталкиваться с необходимостью изменений в части своих привычек и предпочтений.
Обязательно обратитесь к лечащему врачу перед тем как покинете стационар, для того чтобы детально обсудить план действий в ближайшей и отдаленной перспективе. Этот план должен обязательно включать в себя график ваших дальнейших визитов к врачу и обследования, чтобы уловить едва заметные признаки продолжения болезни, побочные эффекты лечения или появление других заболеваний, которые могут существенно ухудшить состояние здоровья. Следует сразу сказать, что если вы закончили лечение по поводу рака прямой кишки, то следующие несколько лет вы должны находится под бдительным наблюдением врача и лучше, если это будет врач проводивший лечение. В течение первых двух лет после окончания лечения частота визитов оставляет от 3 до 6 месяцев. В последующем встречи с врачом могут носить ежегодный характер.
К обязательным процедурам можно отнести осмотр врача и обсуждение с ним появившихся изменений в состоянии, исследование им прямой кишки, исследование крови на онкомаркеры, колоноскопию, МРТ таза и компьютерную томографию брюшной полости и грудной клетки. При невозможности регулярного выполнения последних двух исследований они могут быть заменены ультразвуковым исследованием брюшной полости и рентгенографией грудной клетки.
Карциноэмбриональный антиген (РЭА) - это определение опухолевого маркера, который может быть найден в крови некоторых людей с раком прямой кишки. Изучение уровня этого маркера начинается еще до начала лечения и продолжается после операции с интервалами от 1 до 3 месяцев. Если его уровень повышен до начала лечения, а затем снижается до нормального после операции, он должен быть проверен с особой тщательностью. Медленное или стремительное повышение уровня маркера по сравнению с предыдущими показателями, как правило, свидетельствует о возврате заболевания, признаки которого с помощью других методов могут быть еще не уловимы. Следует сказать, что у ряда людей возврат заболевания может быть выявлен с нормальными значениями РЭА.
Внимание
Всегда сохраняйте копии выписок и заключений исследований, которые проходите. В случае, если вы столкнетесь с необходимостью визита к врачу ранее не знакомому с историй вашей болезни, именно медицинские документы помогут специалисту быстрее и точнее определиться с тем, какие действия ему необходимо предпринять, чтобы помочь Вам.Несмотря на то, что данная информация содержится в выписке, лабораторных анализах и заключениях различных методов обследования, наиболее важным из которых является патоморфологическое заключение, вам необходимо детальное обсуждение всей этой информации со своим лечащим врачом и хирургом. Попытайтесь узнать до этой встречи как можно больше информации о значении каждого из вышеобозначеннных вопросов. Это сделает вашу беседу максимально эффективной.
Основным методом лечения рака кишечника является хурургическая операция, которую часто комбинируют с химиотерапией и новой таргетной (с англ. target – цель) терапией при помощи антител. Лучевую терапию при раке кишечника используют значительно реже, чем при других видах рака. Лучевую терапию используют в случаях, когда пучок лучей можно очень точно сфокусировать на место локализации уничтожаемых клеток. Но кишечник является подвижным, поэтому этот метод терапии в основном используют при раке прямой кишки.
Хирургическое лечение является наиболее часто применяемым методом лечения на всех стадиях рака кишечника.
Существует три основных вида хирургической помощи при лечении колоректального рака:
Если рак удаётся диагностировать на очень ранней стадии, его можно удалить во время колоноскопии через колоноскоп без вскрытия брюшной полости. Если рак находится в полипе, производят полипэктомию или удаление полипа.
Если опухоль большая – производят удаление части кишечника. Это включает удаление самой опухоли и части окружающих здоровых тканей, затем соединяют оба края кишечнка (т.е.образуют анастомоз). Обычно также удаляются ближайшие лимфатические узлы и проверяются на наличие раковых клеток.
Если соединение оставшихся частей кишечника является затруднительным, приводящий край кишечника выводят на переднюю стенку живота, где образуют искуственное отверстие (стому), через которое в специальный мешочек выводятся испражнения. Эта процедура называется колостомия. Чаще всего колостому делают только на время, пока достаточно заживут стенки оперированного кишечника, после этого при повторной операции края кишечника сшивают и искуственное отверстие закрывают. Однако, если соединение кишечника не является возможным, отверстие на передней стенке живота останется постоянным.
Иногда сразу после хирургической операции назначают профилактическую химиотерапию, чтобы уничтожить возможно оставшиеся в организме раковые клетки.
Древнейшим химиотерапевтическим препаратом, до сих пор применяемым для лечения рака кишечника, является фторурацил (5-ФУ). Это - вводимое в вену производное фторпиримидина, которое с момента его синтезирования в 1957. году используется для лечения рака, в т.ч. рака груди и кишечника. Во вспомогательной терапии его часто назначают совместно с другим медикаментом – лейковорином, усиливающим действие фторурацила. Обычно комбинация 5-ФУ/лейковорин применяется 6‑8 месяцев. Фактически в последнии годы существенно увеличилось применение не только этих средств, но и комбинированной терапии вообще.
При использовании новейших комбинаций увеличивается частота успешной терапии, основным показателем которой является увеличение продолжительности жизни.
В последнее десятилетие значительое место занимает капецитабин, который имеет ряд преимуществ: он более прост в применении, так как выпускается в виде таблеток; имеет меньше побочных эффектов., часто применятся в комбинации с другими химиотерапевтическими препаратами.
Иринотекан является химиотерапевтическим препаратом, широко используемым для лечения рака кишечника в комбинации с другими медикаментами.
Ещё одним препаратом, используемым в комбинированной терапии колоректального рака является оксилиплатин.
Большинство химиотерапевтических препаратов вводят в вену, но есть также и перорально применяемые средства.
Восемь из десяти пациентов отдают предпочтение пероральной химиотерапии.*
В исследованиях обнаружено, что 8 из 10 пациентов предпочли бы получать химиотерапевтические препараты в виде таблеток, а не в виде внутривенных инъекций. Основной причиной такого выбора является возможность получения такого лечения дома. Пероральная химиотерапия позволяет пациентам намного больше времени проводить дома – совместно с семьёй и друзьями - а не в больнице. В одном из исследований 9 из 10 пациентов предпочли бы принимать таблетки вместо внутривенной инфузии, если бы была возможность выбора. В другом исследовании обнаружено, что 84% пациентов, получавших оба вида лечения, лучшим признали употребление таблеток. Эти исследования подтверждают как то, насколько необходимы эффективные пероральные химиотерапевтические средства, так и то, насколько важным является такой способ получение химиотерапевтических средств, которой существенно улучшает качество жизни.
*1) Patient Preferences for Oral versus Intravenous Palliative Chemotherapy. Liu G, Franssen E, Fitch M, Warner E. J Clin Oncol 1997; 15: 110–115. 2) Patient preference and pharmacokinetics of oral modulated UFT versus intravenous fluorouracil and leucovorin: a randomised crossover trial in advanced colorectal cancer. Borner M, Schöffski P, de Wit R et al. J Clin Oncol 1997;15:110–115
Очень важно информировать врачей и медсестёр, вовлечённых в ваше лечение, о любых других, употребляемых параллельно с химиотерапией, средствах, не зависимо от того, являются ли они лечебными растениями, пищевыми добавками, витаминами или даже – особенностями диеты. Не зависимо от того, разделяет ли ваше мнение врач, пожалуйста, информируйте его о вашем решении или привычках! Это может повлиять на действие химиотерапевтических препаратов или других медикаментов, применяемых для вашего лечения. Вы же не хотите снизить эффективность лечения или увеличить частоту побочных эффектов по незнанию!
Клетки не могут нормально и достаточно эффективно воспринимать химиотерапевтические средства, если им не хватает воды. Не снижайте эффективность терапии из-за недостаточного употребления жидкости!
Проконсультируйтесь у своего стоматолога перед началом химиотерапии! Зубы рекомендуется покрыть специальным, защитным средством. Усиленное образование кариеса вызывает сухость ротовой полости. В свою очередь, одним из самых частых побочных эффектов большинства химиотерапевтических препаратов является сухость во рту.
Эрозии в ротовой полости, язвенный стоматит, изменения вкуса, металлический привкус, понос, тошнота, рвота, жжение в глазах, затуманивание взора, повышенный риск развития инфекции (которую вызывает нейтропения или пониженное количество лейкоцитов), пониженное количество тромбоцитов, анемия, слабость, выпадение волос, ломкость ногтей, чувствительность к свету, зуд кожи, оттёк стоп и кистей и/или покраснение (так наз. Синдром стоп и кистей), слезоточивость глаз.
Моноклональные антитела - специальные вещества, полученные методом генной инженерии, специально предназначенные для лечения рака.
Ангиогенез – образование новых кровеносных сосудов в организме. Быстро растущие опухоли выделяют особые вещества, вызывающие рост новых кровеносных сосудов, для того, чтобы обеспечить себя необходимыми питательными веществами и кислородом. Новейшим достижением науки, которое в лечении рака дошло до практического применения, является, созданное методом генной инженерии, антитело, которое присоединяется к рецептору фактора роста, расположенному на внутренней стенке или эндотелия кровеносного сосуда ( Vascular Endothelial Growth Factor Receptor- VEGFR), и тормозит его биологическую активность, т.е. не позволяет расти новым кровеносным сосудам. Рост и деление раковых клеток значительно замедляется, если они не получают питательные вещества и кислород. На зрелые кровеносные сосуды антитела не влияют, поэтому нормальное кровообращение организма не нарушается. Поэтому антитела применяют совместно с химиотерапевтическими препаратами.
В Латвии такие антитела зарегистрированы для применения в комбинации с химиотерапией, содержащей5-фторурацил для лечения рака ободочной и прямой кишки.
Подробнее
Рак прямой кишки – распространенное онкологическое заболевание. Точных причин роста заболеваемости ученые не называют, но обращают внимание, что...
...в группе риска находится население экономически развитых стран и жители больших городов. Среди основных причин, ведущих к заболеванию, статисты и онкологи выделяют два главных фактора: характер питания и наследственность.
При наличии в семье родственников в разных поколениях с онкологическим заболеванием прямой кишки говорят о наследственной предрасположенности к колоректальному раку. Но неправильное питание и наличие хронических болезней конечных отделов кишечника даже без отягощенной наследственности могут стать причиной появления злокачественной опухоли.
Пищевой рацион, бедный клетчаткой, но с избытком красного мяса, животных жиров, жареного, мучного и сладкого приводит к накоплению в кишечнике жирных кислот, превращающихся в канцерогены. Малоподвижный и сидячий образ жизни в свою очередь способствует застою крови в венах таза и приводит к нарушению функций слизистой оболочки прямой кишки. В толстом кишечнике возникают хронические воспалительные процессы, провоцируя мутации клеток.
Рак прямой кишки – это злокачественное новообразование, развивающееся в слизистой оболочке конечной части сегмента толстой кишки, заканчивающейся анусом. Опухоль развивается, расширяет свои границы на слизистой и со временем выходит за ее пределы.
Появляются вторичные патологические очаги (метастазы), которые в первую очередь поражают лимфоузлы и органы малого таза, и постепенно распространяются по всему организму. Раковая опухоль в прямой кишке может также развиваться на фоне предраковых заболеваний: полипов, трещин, свищей, проктитов.
Даже незначительное, но затянувшееся отклонение от привычного состояния кишечника должно насторожить человека и стать поводом обращения к врачу. Лучше сказать себе: «боюсь, что у меня рак прямой кишки», чем беспечно отмахнуться от проблемы, и услышать этот диагноз на 3-4 стадии заболевания.
Первые признаки рака прямой кишки проявляются нарушением стула в виде запоров или диареи, дискомфортом, ощущением тяжести, состоянием слабости. С увеличением размеров опухоли появляются небольшие кровотечения, которые нередко принимаются пациентом за геморроидальные, а появившиеся боли он относит на обострившиеся проблемы с печенью и желчным пузырем.
Постоянный дискомфорт, боли, ложные частые позывы к дефекации вынуждают его посетить вначале гастроэнтеролога или проктолога, и если у доктора возникает подозрение на рак, то пациента перенаправляют к онкологу. К онкологу-колопроктологу больной чаще всего попадает через 3-5 месяцев от начала проявления заболевания.
Современная онкология имеет высокотехнологичную аппаратуру и позволяет выявить заболевание на любой стадии развития:
Онкомаркеры – это белки, которые вырабатываются злокачественными образованиями в процессе их жизнедеятельности. Наибольшая их концентрация в крови, по увеличенному количеству этих своеобразных меток можно выявить участок кишечника с онкологией.
Для этого используют специфические маркеры – СА 242, РЭА и неспецифические – АФП.
Раковая опухоль прямой кишки развивается медленно, на протяжении нескольких лет, чаще всего бессимптомно на первых порах, и проходит 4 стадии развития:
Рак прямой кишки может быть излечен только оперативным путем, его также нельзя вылечить народными средствами. Хирургическая операция является основным методом лечения рака толстой и прямой кишки.
Лучевая терапия и химиотерапия используются как дополнение к хирургическому лечению, и имеют второстепенное значение в комплексном лечении. Но, чем раньше диагностирована опухоль, и чем выше она расположена, тем проще операция, лучше результаты и полнее реабилитация.
Сложные операции с удалением прямой кишки, анального канала и мышц сфинктера требуют формирования у пациента постоянной колостомы на передней брюшной стенке. К ней крепится калоприемник, который надо периодически заменять по утрам или перед сном. За стомой и кожей вокруг отверстия нужно тщательно ухаживать, чтобы не было раздражения.
Прогноз продолжительности жизни после удаления опухоли на прямой кишке будет зависеть от стадии онкологического поражения, возраста и характера проведенного лечения. Недуг, выявленный на 1-2 этапе поражения, и операция на ранних стадиях, дают хирургу возможность удалить опухоль и первые незначительные метастазы, не затрагивающие жизненно важные органы. В этих случаях 65-85 % молодых пациентов выздоравливают полностью, а остальные имеют от 2 до 5 лет полноценной жизни.
Резко снижается вероятность появления рецидива рака по прошествии 5 лет после операции, поэтому этот период считается критическим. При поражении более 5 лимфатических узлов или при метастазах в соседних органах, в тканях печени и легких шансов продлить больному жизнь очень мало. В этих случаях не доживают до года.
Послеоперационный восстановительный период также занимает важное место в выживаемости пациента. В краткие сроки нужно восстановить организм больного после хирургического вмешательства и химиотерапии с помощью лечебного питания, и не допустить рецидивов заболевания.
Хорошей профилактикой рака прямой кишки служит правильное питание: употребление продуктов, богатых клетчаткой, овощей и фруктов, каш из злаков, орехов, которые способствуют эффективному очищению кишечника, до 2 литров чистой питьевой воды в день. Кроме этого следует придерживаться следующих правил:
Во всем мире онкологи отмечают возрастание частоты заболеваний раком прямой кишки, а с возрастом человека риск заболеть увеличивается. С целью своевременной диагностики рака Американское общество рака и Национальный раковый институт США рекомендуют населению всех стран проходить скрининг на рак прямой кишки по следующей методике:
В Украине с учетом повышенной радиологической ситуацией фиброколоноскопию нужно проводить каждые 2 года.
Провести диагностику, чтобы заблаговременно выявить заболевание, может каждый житель Украины. Для этого нужно записаться на обследование к проктологу в своем городе.
Запомните! Своевременно диагностированный рак поддается результативному лечению.
Рейтинг статьи:
4.5 из 5 на основе 4 оценки

«ОН Клиник»
Колоректальный рак в России занимает в настоящее время 2-3-е место в структуре онкологических заболеваний и включает рак ободочной кишки, рак прямой кишки, а также рак анального канала (плоскоклеточный или железистый), подходы к лечению которых в силу анатомических и патоморфологических особенностей могут несколько различаться. Так, если при аденоматозном раке (аденокарциноме) различных локализаций основным методом лечения остается хирургический, то при плоскоклеточном анальном раке приоритет отдается консервативному лечению с включением химиолучевой терапии, позволяющей в ряде наблюдений достигнуть стойкой ремиссии, не прибегая к калечащим оперативным вмешательствам. Лишь в небольшом числе наблюдений при лечении плоскоклеточного рака онкологи вынуждены выполнять оперативные вмешательства - при недостаточной эффективности консервативного лечения или при возникновении рецидива заболевания после ранее проведенной консервативной химиолучевой терапии.
Несмотря на успехи использования хирургического метода в лечении рака ободочной и прямой кишок, результаты только хирургического лечения вряд ли можно считать удовлетворительными, что связано со значительным числом возникающих впоследствии локорегионарных рецидивов и отдаленных метастазов [11]. Наибольшего прогресса в лечении колоректальных аденокарционом удалось достигнуть, применяя комбинированные методы лечения, включающие, кроме хирургического вмешательства, различные варианты лучевой и химиотерапии [3, 11, 14, 17, 18]. Наибольшее значение приобрела лучевая терапия как эффективный метод локального контроля за процессом диссеминации клеток опухоли в процессе операции и подавления роста резидуальных комплексов раковых клеток в зоне операционного поля после оперативного вмешательства [12]. Наибольшую эффективность в лечении колоректального рака лучевая терапия показала при комбинированном лечении рака прямой кишки [11, 14]. При этом первоначально изучались режимы предоперационного, послеоперационного, а также сочетанного пред- и послеоперационного применения лучевой терапии в программе комбинированного лечения рака прямой кишки [11, 14, 15, 17, 19].
Проведенные исследования показали, что с точки зрения профилактики локорегионарных рецидивов при лечении первично операбельного рака прямой кишки наиболее эффективно применение короткого крупнофракционного курса предоперационной лучевой терапии с ежедневным облучением разовой очаговой дозой (РОД) 5 Гр в течение 5 дней до суммарной очаговой дозы (СОД) 25 Гр, позволяющее достоверно снизить количество рецидивов с 22,0-23,0% при хирургическом лечении до 9,0-10,0% при комбинированном [11]. При этом больший эффект был отмечен при наличии таких прогностически неблагоприятных факторов, как высокая степень опухолевой инвазии или наличие метастатического поражения регионарных лимфатических узлов, не оказывающего существенного влияния на частоту возникновения отдаленных метастазов.
По нашим данным, применение послеоперационного облучения мелкими фракциями (РОД 2 Гр при ежедневном облучении) по радикальной программе (до СОД 50-60 Гр) при выявлении регионарных метастазов способствовало такому же улучшению результатов лечения, как и проведение предоперационного облучения. Это происходило за счет уменьшения возникновения локорегионарных рецидивов [4]. Однако у трети больных послеоперационное облучение либо невозможно было провести из-за возникших послеоперационных осложнений, либо лечение было прервано на дозах до 30 Гр из-за развившихся осложнений лучевой терапии, что приводило к полному отсутствию эффекта по сравнению с чисто хирургическим лечением.
Применение сочетанного пред- и послеоперационного облучения также не привело к значимому улучшению результатов по сравнению с использованием только предоперационной лучевой терапии. По нашему мнению, вероятнее всего, это было связано с нечувствительностью остающихся в пределах операционного поля раковых комплексов к послеоперационному лучевому воздействию вследствие тканевой гипоксии и постлучевого фиброза в тканях после проведения предоперационного облучения. В результате проведенного исследования приоритет в комбинированном лечении рака прямой кишки отдан предоперационной крупнофракционной лучевой терапии. Вместе с тем применение данной методики не приводило к достоверному уменьшению частоты локорегионарных рецидивов по сравнению с этим показателем в хирургической группе при нижнеампулярной локализации опухоли в прямой кишке [11].
Одним из возможных направлений в поиске путей повышения эффективности лучевого воздействия на опухоли нижнеампулярной локализации стало увеличение дозы ионизирующего облучения. Однако по ряду причин, главной из которых являлось возможное увеличение послеоперационных осложнений вследствие усиления лучевых повреждений здоровых тканей, от данного способа повышения эффективности канцерицидного воздействия решено было отказаться. Вторым направлением было использование физических или химических радиомодификаторов, повышающих противоопухолевую эффективность лучевой терапии без увеличения дозы облучения. Один из таких агентов - локальная СВЧ-гипертермия, усиливающая лучевые повреждения в гипоксических глубоко расположенных опухолевых клетках [18], ее использование позволило достоверно по сравнению с хирургическим лечением снизить частоту возникновения локорегионарных рецидивов до уровня 4,5-5,5%, а также достоверно уменьшить количество рецидивов при раке нижнеампулярной локализации [1]. Реализованные за последние годы программы комплексного лечения рака прямой кишки с применением предоперационной химиолучевой терапии и одновременным использованием нескольких радиомодулирующих агентов позволили еще более значительно снизить уровень локорегионарных рецидивов, а также достоверно по сравнению с хирургическим лечением уменьшить частоту отдаленных метастазов и достигнуть уровня безрецидивной 5-летней выживаемости, превышающего 85,0% [2, 3].
Таким образом, использование предоперационной лучевой терапии в комбинированном и комплексном лечении рака прямой кишки на сегодняшний день стало общепризнанным стандартом. Объемы оперативных вмешательств при раке прямой кишки стандартны и определяются локализацией опухоли в прямой кишке и степенью ее местного распространения. Так, при значительных размерах опухоли, особенно в сочетании с низкой локализацией, хирурги с целью достижения приемлемой радикальности оперативного вмешательства бывают вынуждены выполнять операцию в объеме брюшно-промежностной экстирпации прямой кишки. При такой операции необратимо удаляют сфинктерный замыкательный аппарат прямой кишки, всю параректальную клетчатку в пределах фасциального футляра прямой кишки и значительную часть сигмовидной кишки вместе с брыжейкой. При этом высоко перевязывают и пересекают у места отхождения от нижних брыжеечных сосудов верхние прямокишечные сосуды, а также формируют постоянную одноствольную колостому из остающейся дистальной части сигмовидной кишки.
При локализации опухоли средних размеров в верхнеампулярном отделе прямой кишки (на расстоянии 11 см и более от переходной складки анального канала) технически осуществима операция в объеме чрезбрюшной резекции прямой кишки. При этом дистальная граница резекции стенки кишки должна находиться не ближе 2 см от видимого края опухоли, а околопрямокишечная жировая клетчатка в пределах параректальной фасции должна быть удалена не менее чем на 5 см от дистальной границы опухоли (мезоректумэктомия). Межкишечный анастомоз может быть сформирован как аппаратным швом, так и отдельными узловыми швами (двухрядный узловой шов).
При значительных размерах опухоли и верхнеампулярной локализации возможно увеличение объема операции до брюшно-анальной резекции и даже брюшно-промежностной экстирпации прямой кишки.
При локализации опухоли в среднеампулярном отделе прямой кишки (на расстоянии от 6 до 10 см от переходной складки анального канала) предпочтительным объ-емом оперативного вмешательства следует считать брюшно-анальную резекцию прямой кишки с низведением сигмовидной кишки в анальный канал и формированием сигмоанального анастомоза. При этом прямую кишку мобилизуют в пределах фасциального футляра до мышц тазового дна с перевязкой и пересечением верхних прямокишечных сосудов, а ткань брыжейки сигмовидной кишки удаляют до краевого аркадного сосуда, питающего низводимый ее фрагмент. Анальный канал демукозируют путем отхождения острым путем от анального сфинктера, после чего мобилизованный фрагмент прямой кишки с опухолью резецируют, а остающуюся часть сигмовидной кишки низводят в анальный канал, где формируют колоанальный анастомоз.
При значительных размерах опухоли данной локализации возможно и выполнение брюшно-промежностной экстирпации. При нижнеампулярной локализации или при инвазии опухоли в сфинктер анального канала общепринятым объемом операции является брюшно-промежностная экстирпация прямой кишки. Тем не менее следует отметить, что проведение предоперационного термолучевого и термохимиолучевого лечения с облучением 3 раза в неделю РОД 4 Гр до СОД 40 Гр способствует в ряде наблюдений значительному уменьшению размеров опухоли и перифокального воспалительного компонента. В этих ситуациях расширяются показания к выполнению сфинктеросохраняющих операций даже при низкорасположенных опухолях без ущерба для радикальности [1].
В лечении рака ободочной кишки общепризнанным стандартом является выполнение хирургического вмешательства, объем которого определяется локализацией опухоли. Так, при раке правой половины ободочной кишки, в том числе дистальной трети поперечной ободочной кишки, следует выполнять операцию в объеме правосторонней гемиколэктомии с обязательной мобилизацией и высоким пересечением средней ободочной и подвздошно-ободочной артерии с целью удаления всех лимфатических узлов, расположенных вдоль этих сосудов вплоть до их устья.
При раке левой половины ободочной кишки, в том числе дистальной трети поперечной ободочной кишки, максимальным объемом оперативного вмешательства является левосторонняя гемиколэктомия с высокой перевязкой нижней брыжеечной артерии и удалением лимфатических узлов, находящихся по ее ходу вплоть до устья.
При локализации опухоли в нижней трети сигмовидной кишки или в ректосигмоидном отделе адекватна операция типа чрезбрюшной резекции прямой кишки.
При раке средней трети поперечной ободочной кишки адекватна субтотальная колэктомия с высокой перевязкой всех сосудов, питающих ободочную кишку, и формированием илеосигмо- или илеоректоанастомоза. Однако при наличии относительных противопоказаний к такому обширному объему оперативного вмешательства (старческий возраст, наличие серьезных сопутствующих заболеваний) в ряде наблюдений приходится ограничиваться выполнением резекции поперечной ободочной кишки с высокой перевязкой и пересечением средней ободочной артерии. При этом следует учитывать, что операция данного объема выполняется вынужденно и является условно радикальной.
Рядом отечественных авторов были получены положительные показатели выживаемости больных раком ободочной кишки, которым в предоперационном периоде применяли лучевую терапию в различных режимах облучения [5, 7, 8]. При этом достигались сублетальные и летальные повреждения опухолевых клеток, большая часть которых расположена в хорошо оксигенированных периферических участках опухоли и в зонах ее роста как в первичном очаге, так и в регионарных метастазах [12]. Однако применение предоперационного облучения при раке ободочной кишки несколько лимитируется попаданием в зоны облучения здоровых участков тонкой кишки. Это послужило основанием применения радиопротекторов, обеспечивающих защиту здоровых окружающих тканей в сочетании с подведением к опухоли большей дозы ионизирующего излучения [13]. К числу таких радиопротекторов можно отнести гипоксические газовые смеси, содержащие 9-10% кислорода. При этом установлено, что использование предоперационной лучевой терапии СОД 25 Гр на фоне гипоксических газовых смесей позволило достоверно увеличить общую кумулятивную выживаемость до 87,5% по сравнению с 55,7% в хирургической группе больных, имевших регионарные метастазы [10]. Такое снижение было достигнуто за счет уменьшения почти в 2,5 раза частоты отдаленных метастазов (до 5,26% по сравнению с 12,5% в контрольной хирургической группе). Что касается общих лучевых реакций, то при использовании гипоксирадиотерапии они отмечались в 2,5 раза реже, чем при обычном предоперационном облучении. По нашим данным, послеоперационных энтеритов не было зарегистрировано ни у одного больного.
Таким образом, предоперационная лучевая терапия рака ободочной кишки, особенно при наличии регионарных метастазов, также может служить дополнительным фактором, обеспечивающим улучшение отдаленных результатов. Помимо этого, прорастание опухолью серозной оболочки ободочной кишки и наличие метастазов в регионарных лимфатических узлах диктуют необходимость обязательного проведения адъювантной химиотерапии [6].
Особой нозологической формой колоректального рака следует считать плоскоклеточный рак анального канала, который характеризуется крайне неблагоприятным течением и негативными отдаленными результатами при обычном хирургическом лечении. В настоящее время общепризнана нецелесообразность использования чисто хирургического лечения при данной нозологии. Это обстоятельство обусловлено не только высокой злокачественностью плоскоклеточного рака и склонностью к рецидивированию, но и его высокой чувствительностью к лучевой и лекарственной терапии. Применение современной методики терморадиохимиотерапии с ежедневным облучением РОД 2 Гр до СОД 40-44 Гр в сочетании с облучением паховых регионарных зон метастазирования на фоне введения препаратов цисплатина и блеомицина дает возможность у 80% больных достигнуть полной резорбции опухоли, а при последующем проведении второго этапа лучевой терапии методом внутриполостного или дистанционного облучения СОД 20 Гр - стойкой ремиссии.
Эти данные открывают путь к сфинктеросохраняющему лечению, позволяя избежать калечащей операции [9]. Лишь в 20% наблюдений при невозможности достигнуть резорбции опухоли приходится выполнять брюшно-промежностную экстирпацию прямой кишки. Тем не менее и у таких больных предшествующее химиолучевое лечение способствует улучшению отдаленных результатов по сравнению с таковыми при обычном хирургическом лечении. Большинство авторов сходятся во мнении, что выполнение при плоскоклеточном раке анального канала профилактической паховой лимфаденэктомии нецелесообразно, показанием к ней может быть лишь наличие верифицированного метастатического поражения паховых лимфатических узлов [16].
Таким образом, понятие «колоректальный рак» представляет собой широкий спектр нозологических форм, и лечение каждой из них имеет свои особенности. Несмотря на то что хирургический метод и по сей день остается ведущим в лечении колоректального рака различных форм и локализаций, результаты только этого метода лечения вряд ли можно считать удовлетворительными. Современные подходы диктуют необходимость широкого использования методов комбинированного и комплексного лечения с применением лучевой терапии, радиомодулирующих агентов и противоопухолевых препаратов. В известной мере совершенствование хирургических методик в лечении колоректального рака достигло возможного предела, поэтому только использование всего комплекса современных мер противоопухолевого воздействия позволяет надеяться на дальнейший прогресс в улучшении отдаленных результатов в борьбе с этим заболеванием.
Актуальность
Рак прямой кишки является одной из наиболее распространенных онкологических причин смерти в западном мире. Людей с диагностированным раком прямой кишки лечат преимущественно хирургически. Однако, сохраняется риск рецидива рака прямой кишки после хирургического лечения. Курс лучевой терапии перед операцией может снизить риск местного рецидива, так как лучевая терапия может разрушить небольшие остаточные опухоли и усилить эффекты операции.
Характеристика исследований
4 июня 2018 года мы провели поиск рандомизированных испытаний (экспериментальных исследований, в которых людей случайным образом распределяют по двум или более группам лечения) в медицинских базах данных, чтобы определить, есть ли у людей с раком прямой кишки польза от лучевой терапии перед операцией с точки зрения снижения риска смерти от любой причины, риска смерти от рака и риска рецидива рака в полости таза. Мы рассматривали лучевую терапию в высоких дозах с последующим хирургическим вмешательством любого типа для удаления рака прямой кишки.
Результаты
Мы нашли четыре испытания с участием 4 663 человек с операбельным раком прямой кишки. Наши результаты свидетельствуют о том, что проведение короткого курса лучевой терапии перед операцией, вероятно, снижает смертность. Однако, когда наш анализ ограничивался современным типом хирургического вмешательства (тотальная мезоректальная эксцизия), доказательств разницы между группой, получавшей лучевую терапию до операции, и группой, которой проводили только операцию, не было. При проведении короткого курса лучевой терапии различия между группами в смертности, связанной с раком, могли быть небольшими или вовсе отсутствовать.
Мы нашли доказательства среднего качества в пользу того, что в сравнении с хирургическим вмешательством предоперационная лучевая терапия может принести существенную пользу в плане снижения вероятности местного рецидива рака.
Предоперационная лучевая терапия мало или вовсе не влияла на радикальную резекцию или щадящие сфинктер операции.
Мы обнаружили более высокую частоту сепсиса, а также хирургических и половых осложнений у участников, получавших лучевую терапию, в сравнении с теми, кому проводили только операцию.
Качество доказательств
В целом дизайн исследований был хорошим. Мы посчитали качество доказательств средним для рецидивов рака и общей смертности, поскольку были серьезные опасения касательно применимости результатов к современному лечению рака прямой кишки.
Мы снизили оценку качества доказательств по остальным исходам из-за неточных результатов и/или различий между испытаниями по критериям определения рака прямой кишки, стадии рака у участников, предоперационной визуализации для оценки стадии, типам проводившихся операций, дозам и фракционированию излучения, времени между лучевой терапией и операцией, а также по применению адъювантной или послеоперационной терапии.
Колоректальный рак (рак прямой кишки и толстого кишечника) – это заболевание, которое характеризуется появлением злокачественной опухоли в области толстого кишечника или прямой кишки. Объединение опухолей прямой, сигмовидной, ободочной и слепой кишки в одну статистическую единицу не случайно. Опухоли перечисленных отделов пищеварительного тракта имеют сходные причины и механизм развития, проявления и осложнения, методы диагностики и лечения.
Преимущественно раком прямой кишки страдают пожилые люди, которые находятся в возрасте от 50 лет. Каждый год в мире регистрируется до полумиллиона людей, заболевшим раком толстой кишки.
Причины развития рака толстого кишечника в настоящее время окончательно не известны, однако существуют факторы, которые повышают риск развития данного заболевания, к ним относятся:
Каковы же симптомы и признаки рака толстого кишечника и прямой кишки?
Колоректальный рак развивается медленно и длительное время не проявляется никакими симптомами. Основные признаки рака толстого кишечника и прямой кишки зависят от типа рака толстого кишечника и степени распространения.
Различают основные симптомы рака толстого кишечника:
Распространение рака толстого кишечника в другие органы (метастазы) может проявляться различными симптомами, которые зависят от места появления метастазов (в печени, головном мозге, легких, яичниках и т.д.): желтуха, головные боли, боли в груди, головокружения и пр.
На поздних стадиях рака толстого кишечника может развиться кишечная непроходимость, которая характеризуется закупоркой просвета кишечника растущей опухолью. Она может проявляться проявляется отсутствием кала и газов, сильнейшим вздутием живота, сильными коликообразными болями в животе, сильной тошнотой, многократной рвотой, выраженной слабостью и т.д. Кишечная непроходимость является смертельно опасным осложнением рака толстого кишечника и требует экстренного обращения к врачу.
Диагностика рака толстого кишечника
Анализ кала на скрытую кровь является простым методом диагностики колоректального рака. С помощью этого анализа могут быть обнаружены даже небольшие потери с калом, которые встречаются на ранних стадиях рака толстого кишечника.
Определение уровня опухолевых маркеров в сыворотке крови больного. Наиболее известным маркером рака толстой кишки является раковоэмбриональный антиген (РЭА). Повышение уровня РЭА отмечается в запущенных стадиях опухолевого процесса. Другой широко определяемый маркер СА – 19-9 – имеет при раке толстой кишки прогностическое значение.
Пальцевое исследование прямой кишки осуществляется с целью обнаружения опухоли в нижних отделах прямой кишки. Этот метод позволяет определить наличие опухоли в случае ее расположения в нескольких сантиметрах от анального отверстия.
Ректороманоскопия – это метод диагностики рака нижних отделов толстого кишечника ( прямой и сигмовидной кишки). С помощью ректороманоскопии удается обследовать участки кишки длиной 20 см. В ходе ректороманоскопии можно сделать биопсию – отщипнуть небольшой кусочек опухоли для подробного исследования под микроскопом (гистологическое исследование). Только гистологическое исследование позволяет понять, какая опухоль – доброкачественная или злокачественная.
Колоноскопия – это метод диагностики колоректального рака, который позволяет выявить опухоль практически в любом отделе толстого кишечника. В ходе этого исследования также представляется возможность осуществить биопсию. Ведущие мировые эксперты на основании результатов проведенных исследований определили колоноскопию самым эффективным методом скрининга колоректального рака, который позволяет проводить не только диагностику с биопсией, но и удаление предраковых состояний (аденоматозных полипов).
Компьютерно-томографическая колоноскопия (КТ) – компьютерная реконструкция внутренней поверхности кишки без эндоскопического исследования.
Трансректальное ультразвуковое исследование (ТРУЗИ) – метод определения глубины опухолевой инвазии стенки кишки и поражения региональных лимфатических узлов.
Лечение рака прямой кишки и толстого кишечника
Лечение колоректального рака зависит от стадии рака, общего состояния человека, наличия других тяжелых заболеваний и включает хирургическое лечение, радиотерапию и химиотерапию.
Хирургическое лечение – операция по удалению опухоли и ближайших лимфатических узлов.
Радиотерапия уничтожает, либо препятствует размножению раковых клеток, которые не были удалены во время операции.
Химиотерапия – это метод лекарственного лечения рака толстого кишечника. Лекарства, применяемые в химиотерапии, уничтожают, либо прекращают деление раковых клеток. Химиотерапия способна продлить жизнь человека, даже при наличии метастазов в других органах.
Врач-хирург Большакова Е. Н.
Возврат к списку
Хирургическое лечение играет важную роль в лечении рака толстой кишки. Дополнительная химиотерапия у пациентов с высоким риском рецидива увеличивает частоту излечения и продолжительность жизни. В выбранной группе химиотерапия при паллиативном лечении значительно продлевает жизнь пациентам с отдаленными метастазами. При локализации рака прямой кишки обращают внимание на роль предоперационной лучевой терапии (уменьшение массы опухоли, возможность резекции R0 после неоадъювантной лучевой терапии), тогда как при лечении больных раком толстой кишки она имеет второстепенное значение.
Согласно данным исследования EUROCARE-4, 5-летняя выживаемость больных раком толстой кишки, диагностированных в период с 1995 по 1999 год, в Польше составила 39% (в среднем по Европе - 55%). По данным SEER (Surveillance Epidemiology and End Results) показатели 5-летней выживаемости (%) в зависимости от стадии опухоли составляют: I 74,0; ИИА 66,5; ИИБ 58,6; ИИК 37.3; IIIА 73,1; IIIБ 46,3; IIIС 28,0; IV (наличие отдаленных метастазов) 5,7%.
У больных с новообразованиями желудочно-кишечного тракта во многих случаях выявляются признаки гипотрофии, обусловленные как прогрессированием заболевания (непроходимость, диарея, рвота), так и метаболическими изменениями, вызванными стрессом, связанным с тяжелым заболеванием.
Состояние питания является одним из факторов, определяющих выбор метода лечения. Плохой статус питания может привести к невозможности пройти операцию или химиотерапию. Это также напрямую влияет на результаты проведенного лечения, возможность осложнений и дальнейший прогноз.
Важно, чтобы каждый пациент был должным образом подготовлен к лечению, особенно к хирургическому вмешательству. Пациентам с плохим нутритивным статусом перед процедурой следует проводить нутритивную поддержку (белковые, высококалорийные препараты).Диетотерапия должна быть неотъемлемой частью правильного лечебного процесса.
Дополнительная информация в разделе Диетотерапия.
Метод хирургического лечения индивидуально адаптирован к стадии прогрессирования и техническим возможностям резекции. Хирургическое вмешательство заключается в резекции соответствующего фрагмента кишки с регионарными лимфатическими узлами (блоком - при раке толстой кишки без отдаленных метастазов - сегментарная резекция с анастомозом, гемиколэктомия, расширенная гемиколэктомия, панколэктомия).
В патологическом препарате необходимо оценить не менее 12 лимфатических узлов из местного лимфооттока, кроме резекции единым блоком, также удаляются все подозрительные лимфатические узлы и другие видимые изменения, выходящие за рамки стандартной резекции. При наличии синхронных метастазов в печень или легкие - оценивают их резектабельность, а также производят сегментарное иссечение кишки с одномоментной или последующей резекцией метастатического поражения (печень - хирургически, термоабляция).
В случае далеко зашедшего - метастатического заболевания, но при наличии нерезектабельных вторичных изменений в печени или легких рассматривается индукционная химиотерапия и через 2-3 месяца следует оценить объективный ответ и пересмотреть вопрос о радикальном хирургическом вмешательстве. Иногда в случае первичной опухоли, если существует реальная угроза стриктуры кишечника или значительного кровотечения из опухоли, необходимо провести хирургическое лечение первичной опухоли и после операции осуществить химиотерапию для уменьшения метастатических изменений.
Значительные стадии прогрессирования рака, т. е. перманентно неоперабельные поражения, подлежат паллиативным вмешательствам (резекция кишки, обход анастомозов, декомпрессивная колостомия, эндоскопическое протезирование стеноза).
В случае экстренных операций - в связи с подозрением на неопластическую непроходимость и риском перфорации - чаще всего выполняются декомпрессионные колостомы. Колоректальная непроходимость, вызванная раком, чаще всего возникает при опухолях сигмовидной кишки (где находится физиологически наиболее узкий просвет) или при опухолях селезеночной складки.В экстренном случае выполняется искусственное соединение просвета кишки со слизистой оболочкой живота (стома).
Наложение стомы существенно влияет на качество жизни пациента, особенно на психическое состояние и возможность психосоциальной адаптации после операции, требует изменения режима питания, соблюдения соответствующих правил гигиены и повседневной жизнедеятельности. Поэтому перед каждой процедурой на кишечнике пациента следует информировать о возможности создания стомы.Отверстие стомы должно быть хорошо спланировано: оно должно проходить через прямую мышцу живота, вдали от линии операционного разреза (чтобы не привести к контаминации), рубцов и деформаций кожи, располагаться на кожной складке (важно у людей с ожирением). ).
Планово выполняются следующие виды резекций:
Рис. Колоректальный рак. Опухоль, расположенная в слепой кишке.
Основным показанием к адъювантной терапии является рак III стадии (опухоль Т1-Т4 с метастазами в лимфатические узлы). В этой группе больных всегда назначают адъювантную химиотерапию, если нет противопоказаний к назначению цитостатиков (сопутствующая патология).При II стадии применение адъювантной терапии является предметом споров — наличие Т4, и особенно Т4b (стадия IIC), может быть самостоятельным показанием к ней.
Кроме того, адъювантное лечение может быть рассмотрено при наличии факторов с более высоким риском рецидива, таких как: признак T4a, высокая гистологическая злокачественность, небольшое количество удаленных лимфатических узлов, перфорация опухоли во время хирургического вмешательства, экстренное хирургическое вмешательство (обструкция , перфорация), инвазия сосудов вокруг опухоли.
При паллиативном лечении метастатического колоректального рака (стадия IV) успешно применяются схемы, содержащие фторурацил - по сравнению с чисто симптоматическим лечением он снижает относительный риск смерти на 35% и увеличивает 1-летнюю выживаемость на 16% и медиану время выживания на 3,7 месяца.
В настоящее время у пациентов с хорошим общим самочувствием и отсутствием противопоказаний, связанных со стрессом, предпочтительно использовать схемы, содержащие иринотекан в дополнение к фторпиримидину (например,FOLFIRI) или оксалиплатин (например, FOLFOX-4 или CAPOX). Выбор конкретной схемы производится в индивидуальном порядке в зависимости от наличия противопоказаний к назначению иринотекана или оксалиплатина, обусловленных сопутствующими заболеваниями и ожидаемыми синдромами токсичности, и планируемой последовательной лечебной тактики. Представляется, что химиотерапию не обязательно продолжать до прогрессирования или неприемлемой токсичности - рациональным ведением в случае отсутствия динамики опухолевых изменений может быть прекращение лечения и его возобновление в момент прогрессирования.
У пациентов, перенесших метастазэктомию по поводу метастазов в печень, предпочтительны схемы, содержащие оксалиплатин (например, FOLFOX-4, возможно, более токсичный FOLFOXIRI), а работоспособность должна быть повторно оценена не позднее чем через 12 недель после начала лечения. Не установлено, может ли добавление к классическим схемам молекулярно-направленных препаратов, таких как антитела против EGFR, повысить эффективность начальной терапии. Продолжительность системного лечения как первичной метастазэктомии с последующей химиотерапией, так и химиотерапии до метастазэктомии не должна превышать шести месяцев.
Внутрибрюшинная перфузионная химиотерапия при гипертермии (DCPH) рекомендуется при наличии перитонеальных метастазов при колоректальном раке. Условием эффективности данной процедуры является радикальное иссечение первичной опухоли до степени отсутствия перитонеальных метастазов и максимально возможная циторедукция перитонеальных метастазов. Чем он больше, тем лучше результаты лечения ДКПГ.
Внутрибрюшинная перфузионная химиотерапия при гипертермии - метод лечения метастатического поражения брюшины колоректальным раком, раком желудка, мезотелиомой брюшины, псевдомиксомой.Он заключается во введении цитостатиков в перфузионную жидкость, подогретую до 42°С, что позволяет обеспечить синергетический эффект высоких доз этих препаратов и повышенной температуры.
Подробнее по этой теме:
"Методы лечения - HIPEC"
"Внутрибрюшинная перфузионная химиотерапия при гипертермии"
ЭГФР
Рецептор эпидермального фактора роста (EGFR) представляет собой трансмембранный гликопротеин с тирозинкиназной активностью.Повышенная экспрессия EGFR обнаруживается в 25-80% случаев колоректального рака. Активность этого рецептора приводит к образованию сосудов (ангиогенез), увеличивает способность клеток к делению (пролиферация) и защищает раковые клетки от естественных процессов клеточной гибели (апоптоз - запрограммированная гибель клеток: процесс чрезвычайно важный для правильное функционирование организма).
Таргетная терапия, основанная на молекулярном тестировании этого рецептора, состоит из препаратов, которые блокируют активность рецептора EGFR (анти-EGFR).Такие препараты включают в себя в т.ч. цетуксимаб, панитумумаб.
КРАС (к-рас)
Белок K-RAS является протоонкогеном и . Роль белка заключается в передаче сигнала роста, в основном от системы рецепторов эпидермального фактора роста (EGFR), и, следовательно, в передаче активности, связанной с EGFR.
Мутации в гене KRAS при колоректальном раке являются основным предиктором резистентности к таргетной терапии против EGFR. Наличие мутаций в опухоли связано с лекарственной устойчивостью.Мутации KRAS встречаются у 30-50% больных колоректальным раком.
Таргетная терапия основана на лекарствах, блокирующих рецептор EGFR и сигнальный путь k-ras. Эти препараты эффективны, когда белок k-ras находится в немутировавшей форме («дикий тип»). В случае мутаций в гене белка k-ras таргетные препараты, направленные против рецептора EGFR, неэффективны.
Протоонкоген - ген, присутствующий в нормальной клетке, при определенных условиях обладающий потенциальной способностью запускать неопластические изменения
Прогностические факторы - факторы, указывающие на потенциальный ответ на запланированное лечение
BRAF
BRAF представляет собой серонин-треонинкиназу, которая активирует киназы MAP/ERK.Он является частью сигнального пути MAPK , который контролирует рост раковых клеток. Ген влияет на пролиферацию, созревание и апоптоз клеток. Мутация BRAF обнаруживается примерно у 10% больных колоректальным раком. Нарушение этого пути в результате мутации BRAF приводит к неконтролируемой пролиферации клеток и развитию опухоли.
Таргетные препараты блокируют белок BRAF как один из компонентов пути MAPK. Эти препараты включают:в дабрафениб, вемурафениб (в основном используются для лечения меланомы).
MAPK - Митоген-активируемые протеинкиназы
Гены-мутаторы (MMR) и микросателлитная нестабильность (MSI)
Гены-мутаторы кодируют белки, ответственные за исправление ошибок, возникающих при репликации генетического материала (гены-мутаторы = гены репарации ДНК). Эта коррекция основана на удалении несовпадающих нуклеотидов.Если репарационный белок, кодируемый геном-мутатором, не удаляет неуместный нуклеотид, мутация может сохраняться, и матрица для репликации генетического материала расширяется, что можно измерить в областях, называемых микросателлитными областями. Это так называемый микросателлитная нестабильность. Микросателлитная нестабильность при колоректальном раке встречается примерно в 10-20% случаев.
ВЭФР
Фактор роста эндотелия сосудов (VEGF) — сигнальный белок, отвечающий за ангиогенез (рост кровеносных сосудов — процесс, необходимый для роста раковой ткани).Гиперэкспрессия (повышенная активность) VEGF наблюдается в 50-60% случаев колоректального рака.
Таргетная терапия в случае сверхэкспрессии VEGF заключается в назначении блокирующих препаратов (анти-VEGF), таких как, например, бевацизумаб
Больные раком толстой кишки после радикального лечения - должны находиться под наблюдением в соответствии с рекомендациями ESMO:
При рецидиве заболевания - изолированном, местном, всегда следует рассматривать возможность местной терапии - оперативное вмешательство, методы аблации, в случае рецидива в брюшине - циторедукционные процедуры с внутрибрюшинно проводимой химиотерапией.В остальных случаях применяют системное паллиативное и симптоматическое лечение.
Производство:
доктор хаб. доктор медицинских наук Томаш Ястшембски, проф. Солнце КРУЖКА
Кафедра онкологической хирургии
Университетский клинический центр в Гданьске,
MD врач Паулина Цихон
Кафедра онкологической хирургии
Университетский клинический центр в Гданьске.
«Колоректальный рак - предыдущая страница (стадирование, tnm, клиническая оценка)

Колоректальный рак является второй ведущей причиной смерти от рака в Польше. Колоректальный рак преимущественно развивается у лиц старше 40 лет, риск развития заболевания увеличивается с возрастом, достигая своего пика на 8-м десятилетии жизни.
Злокачественные новообразования толстой кишки включают в основном аденокарциномы, возникающие в толстой кишке, сигмовидном изгибе и прямой кишке. Являются одной из самых распространенных злокачественных опухолей, их количество постоянно растет . Среди женщин КРР является 2-м по частоте злокачественным новообразованием (после рака молочной железы), а у мужчин — 3-м (после рака предстательной железы и рака легкого).
Примерно в 90% случаев КРР носит спорадический характер, т. е. не является наследственным. Факторами, повышающими риск развития КРР, считаются: слишком калорийная диета, употребление в пищу термически обработанного красного мяса и насыщенных жиров, небольшая физическая активность, употребление алкоголя, диабет и курение.Существует также более высокий риск развития CRC у людей с воспалительными заболеваниями кишечника, такими как болезнь Крона или язвенный колит.
Диета с высоким содержанием клетчатки, овощей и фруктов снижает риск CRC .
Каждый пациент с диагнозом КРР нуждается в углубленной диагностике и лечении группой специалистов, состоящей из нескольких специалистов; гастроэнтеролог, хирург-онколог, клинический онколог, радиотерапевт, психоонколог, диетолог и физиотерапевт.Роль проктолога – врача, специализирующегося на лечении нижних отделов желудочно-кишечного тракта (толстой кишки, заднего прохода), также может быть важной.
Сроки развития КРР очень различны , от образования опухоли до появления клинических симптомов может пройти несколько, несколько и даже несколько десятков лет. Поэтому очень важно проводить профилактические обследования, позволяющие выявить опухолевые клетки на ранней стадии развития их заболевания.
Наиболее важный тест, который необходимо выполнить, — это колоноскопия, т. е. эндоскопическое исследование.Он заключается в осмотре толстой кишки гибким фиброскопом – колоноскопом. Он позволяет выявить ранний, еще не запущенный рак без симптомов и полипов или предраковых образований (раковые аденомы и зубчатые полипы).
В Польше на основании эпидемиологических данных рекомендуется проводить скрининговую колоноскопию всем лицам без противопоказаний и без симптомов колоректального рака в возрасте 50-65 лет, а также лицам в возрасте 40-49 лет, имеющим родственников первой степени родства с раком больших размеров кишечник.
Ранняя диагностика КРР благодаря, в частности, проведение эндоскопических скрининговых обследований (колоноскопия) позволяет не только полностью восстановиться, но и чаще всего предотвращает необходимость потенциально травмирующих процедур.
Симптомы колоректального рака, которые должны побудить к постановке диагноза: анемия, положительный анализ кала на скрытую кровь, макроскопически видимое кровотечение из желудочно-кишечного тракта и изменения дефекации (запор или диарея, стул в виде карандаша).Кроме того, запущенный колоректальный рак может сопровождаться такими симптомами, как потеря веса, боль в животе и анемия.
У некоторых людей колоректальный рак диагностируется при полном закрытии опухолью просвета кишечника, что приводит к симптомам желудочно-кишечной непроходимости и необходимости срочного хирургического лечения.
Золотым стандартом в диагностике колоректального рака является вышеупомянутая колоноскопия (эндоскопия).Обследование позволяет осмотреть всю толстую кишку, визуализировать опухоль, определить ее локализацию, оценить размеры видимого из просвета кишки образования, а главное, позволяет взять образцы для гистопатологического исследования, что является необходимым элемент окончательного диагноза колоректального рака со степенью его злокачественности.
Колоноскопия также позволяет обнаружить синхронные изменения (т. е. происходящие в толстой кишке одновременно с обнаруженной опухолью), такие как предраковые изменения (полипы, большинство из которых можно удалить малоинвазивными эндоскопическими методами), обнаруживаемые примерно у 30% пациентов или вторая опухоль появляется примерно у 3% пациентов.
Небольшие полипы (до 10-15 мм) размером обычно можно удалить сразу во время первой колоноскопии даже в амбулаторных условиях. Более крупные (даже несколько сантиметров) подлежат эндоскопическому удалению (полипэктомия, мукозэктомия, рассечение подслизистого слоя) во время колоноскопии в условиях стационара. Все удаленные полипы исследуют микроскопически для определения размеров, степени дисплазии и полного удаления. На основании этого может быть установлена рекомендуемая программа эндоскопического наблюдения.
Перед проведением колоноскопии необходима подготовка толстой кишки путем очищения кишечника специальными препаратами полиэтиленгликоля (макроголы, ПЭГ), которые выпивают накануне или за несколько часов до исследования. Хорошая очистка позволяет безопасно проводить осмотр и обеспечивает необходимую видимость для детальной оценки поверхности слизистой оболочки и является чрезвычайно важным фактором в определении качества колоноскопии. Обследование может проводиться без анестезии, а у лиц, нуждающихся в ней, под кратковременной общей анестезией, проводимой анестезиологом .
Другими важными диагностическими процедурами, которые проводятся при диагностике колоректальных новообразований, являются визуализирующие исследования: компьютерная томография, магнитно-резонансная томография, УЗИ, трансректальное УЗИ. Они важны для определения стадии заболевания и выявления возможных метастазов.
На основании информации, полученной в результате колоноскопии и визуализирующих исследований , клинический онколог и онкологический хирург планируют дальнейшее ведение и лечение .
В случае диагноза КРР необходимо лечение, вид которого зависит от способа постановки диагноза и стадии, на которой было диагностировано заболевание.
Распространение эндоскопической диагностики, т.е. неинвазивной диагностики, проводимой с использованием гибких зеркал, применяемых в процедурах методом осмотра «внутренней части» толстой кишки (колоноскопия), означает, что опухоли выявляются все раньше и раньше.
Нередко опухоль может быть полностью удалена во время колоноскопии , и обычно дальнейшее лечение, такое как хирургическое вмешательство или химиотерапия, больше не требуется.
Не все колоректальные опухоли можно удалить с помощью эндоскопии .В таких ситуациях применяют другие методы лечения, например, хирургическое вмешательство, системное лечение.
Хирургическое лечение колоректального рака является старейшим из используемых методов . Это также основной и наиболее эффективный метод лечения этого состояния. Долгие годы это был единственный метод, но последующие открытия в области онкологии, такие как химиотерапия, лучевая терапия и биологические препараты — так называемая «таргетная терапия» значительно улучшили результаты оперативного лечения.
Хирургическое лечение подразделяется на:
Хирургическое лечение с годами не изменилось, но изменились методы его выполнения. В прошлом преобладали обширные операции, связанные с необходимостью выполнения разреза на животе. Часто из-за боязни инфекции пациенту накладывали стому (искусственный задний проход, вынесенный за пределы брюшной стенки). В настоящее время те же операции выполняются малоинвазивными методами с использованием лапароскопии или хирургических роботов.
Независимо от метода, правила онкологической хирургии годами остаются неизменными: опухоль толстой кишки должна быть удалена с адекватным краем здоровой кишки, чтобы не осталось раковой ткани . Также необходимо удалить лимфатические узлы в области опухоли. Это особенно важно, поскольку правильно проведенная онкологическая операция повышает шансы пациента на выздоровление и позволяет клиническим онкологам принять решение о проведении дополнительного лечения в зависимости от стадии прогрессирования: лучевой и химиотерапии.
Классическое открытое лечение, правильно выполненное, имеет такую же эффективность в лечении рака, как и малоинвазивное лечение , но современные методы намного комфортнее для пациента.
Лапароскопическая операция при колоректальном раке проводится с помощью камеры (так называемый «лапароскоп»), вводимой в брюшную полость через небольшой разрез (10-12 мм, чаще вокруг пупка), благодаря которой хирург просматривает увеличенные органы брюшной полости на высококлассном цифровом мониторе, а затем благодаря специальным инструментам (4-5 небольших разрезов, каждый из них не больше 8 мм) может точно вырезать пораженные ткани и зафиксировать кишки с помощью механических швов, так называемыхстеплеры.
В некоторых случаях один из разрезов удлиняется на 5-7 см. Это позволяет удалить из брюшной полости иссеченный орган, например фрагмент кишки с опухолью, и завершить операцию. Это гораздо меньшая травма для пациента, чем в случае необходимости выполнения обширного разреза брюшной полости.
Колоректальные новообразования выявляют также, когда опухоль настолько велика, что ее первым признаком является закрытие просвета кишки, т. е. так называемая «непроходимость». CRC затем диагностируется после операции.Обычно в такой ситуации необходимо лечение у клинического онколога, особенно если при этом обнаруживается наличие метастазов опухоли кишечника в другие органы.
Основным методом консервативного лечения при уже удаленной опухоли является так называемая системная терапия, которая заключается во введении больному препаратов системного действия. Затем химиотерапия (лечение с низкой специфичностью) или молекулярно-направленные биологические/таргетные препараты (которые разрушают раковые клетки определенным образом - что можно сравнить с молекулой лекарства, внедряющейся в раковую клетку, чтобы уничтожить ее, с сопоставлением ключа и замка - только определенный ключ <не каждый> подходит для определенного замка).Применяются также комбинации этих методов и их совместное введение, т.е. химиотерапия в сочетании с таргетной терапией одновременно или в последовательной последовательности.
Также иммунологическая терапия рака – прорыв в онкологии, за открытие которого в 2018 году была присуждена Нобелевская премия, является ценным системным методом лечения, применяемым при лечении отдельных пациентов с диагнозом КРР.
Препараты, уничтожающие рак при КРР, могут назначаться больным в виде перорально - таблеток/капсул, в виде внутривенных инъекций или внутривенных вливаний различной продолжительности.
Пероральная химиотерапия позволяет лечить больного дома - 1 раз в 2-4 недели необходимо посещение онколога, который после проведения лабораторных исследований и оценки безопасности и переносимости лечения и оценки его эффективности назначает таблетки, выдаваемые пациенту. Лекарства принимаются дома до тех пор, пока их запасы не будут исчерпаны и не потребуется следующий визит к врачу. Вы по-прежнему можете активно проводить время, принимая домашние лекарства - работая или занимаясь домашним хозяйством практически так же, как и до лечения.
Введение препаратов путем инъекций или инфузий требует госпитализации, повторяемой с интервалом в 2,3 или 4 недели. Только в некоторых случаях эти периодические госпитализации требуют пребывания в стационаре, как правило, не более 3 дней.
В настоящее время возможно лечение в режиме так называемой госпитализации на один день , когда больной поступает в отделение ежедневной химиотерапии утром, имеет анализы и медицинскую квалификацию для следующего курса химиотерапии, после которой он получает вливания и инъекции наркотиков и в тот же день, когда он приходит домой.Благодаря этому многие пациенты могут продолжать свою профессиональную деятельность и нормально функционировать в своей среде.
Для удобного введения при повторных циклах инъекций или внутривенных вливаний можно вставлять длительные проколы, так называемые «Сосудистые порты». Это невидимые камеры, размещаемые под кожей (чаще всего в области под правой ключицей), в которые вместо периферической вены вводится игла перед забором крови для анализа или введения лекарств. Это повышает как безопасность введения, т.е.химиотерапии, а также комфорт пациента.
После завершения лечения устройство удаляется. Процедура установки и удаления «порта» длится от нескольких до нескольких минут и безболезненна. Требуется только местная анестезия.
Лучевая терапия в отдельных случаях КРР является признанным и эффективным методом, но предназначенным в основном для лечения рака прямой кишки и заднего прохода, то есть рака конца толстой кишки. Освещение дополняет или предшествует хирургическим процедурам.Иногда его можно использовать как единственный местный метод лечения.
5-дневная лучевая терапия - за неделю до удаления рака прямой кишки - было доказано, что значительно улучшает выживаемость по сравнению с только хирургическим вмешательством . Лучевую терапию в ряде случаев можно сочетать с одновременным назначением химиотерапии как метода, повышающего ее эффективность.
Максимизация эффективности и безопасности при минимальном риске осложнений — один из основных принципов современной медицины.Клиническая онкология также постоянно развивается в этом направлении. В результате системное онкологическое лечение становится более эффективным и вызывает все меньше побочных эффектов или минимизирует их выраженность.
Запоры могут возникать у некоторых пациентов при заболеваниях кишечника, а также при системной терапии в результате приема противорвотных препаратов. Также может быть диарея, обычно временная. Пациентам, использующим системную терапию, всегда назначают специальные препараты в случае возникновения симптомов. Эти препараты также можно использовать дома и помочь в таких ситуациях, предотвращая или останавливая диарею.
Применение системного лечения может, наконец, у некоторых больных вызвать снижение иммунитета , инфекцию иногда с лихорадкой. Онкологи используют препараты для предотвращения снижения иммунитета, а также препараты, лечащие последствия снижения резистентности. Такая процедура является стандартной в современном лечении КРР и сводит к минимуму риск и последствия таких осложнений.
Эффективность лечения КРР во многом зависит от стадии прогрессирования заболевания .Также это зависит от того, удалось ли хирургу-онкологу или гастроэнтерологу удалить всю опухоль и удалось ли удалить метастазы рака, если они были.
В случае КРР с метастазами на момент постановки диагноза очень часто удается их удалить, если они расположены в печени или легких. Метастазы в печени можно уничтожить и без операции рассечения покровов и их иссечения.
С этой целью применяют так называемые «малоинвазивные» методы, заключающиеся во введении в область опухоли очень тонкого катетера или зонда под контролем компьютерно-томографического изображения (реже ультразвукового сканера) и вызвать его распад с помощью высокой температуры или инъекции специального вещества.В большинстве случаев дополнительно следует проводить системное лечение, задача которого – устранение микроскопических размеров, невидимых остатков болезни.
Чаще всего весь курс лечения ранней стадии заболевания составляет от 6 до 8 месяцев . Желательно, чтобы оно проводилось в учреждениях, имеющих в своей структуре всех необходимых специалистов и методик и необходимое оборудование, которые в онкологии называются мультидисциплинарными процедурами. Такая командная работа (отсюда и название – мультидисциплинарная команда) улучшает результаты лечения и скорость излечения КРР, является хорошим эталоном диагностических и лечебных мероприятий.
Его использование должно соблюдаться во всех центрах лечения колоректального рака. Колоректальный рак, диагностированный с удаляемыми/деструктируемыми метастазами в печень и/или легкие, также в значительной части случаев излечим.
.Рак толстой кишки вызывается неконтролируемым ростом клеток в одном отделе толстой кишки (слепая кишка, восходящая ободочная кишка, поперечная ободочная кишка, ободочная или прямая кишка). Симптомы и методы лечения рака различных отделов толстой кишки могут значительно различаться. Подавляющее большинство (90%) случаев колоректального рака составляют колоректальный рак (аденокарцинома).
Чаще встречается у мужчин, чем у женщин.Редко встречается в возрасте до 40 лет, пик заболеваемости приходится на 7-е десятилетие жизни. В Польше это вторая ведущая причина смерти от рака. Изменения в пищевых привычках, происходящие в Польше с 1990-х годов, привели к неуклонному увеличению числа случаев колоректального рака.
Повышенный риск развития колоректального рака касается людей с этим же заболеванием, а также пациентов с болезнью Крона и язвенным колитом, курильщиков, людей с ожирением, людей с полипами в толстой кишке и людей, которые ранее лечились по поводу рака толстой кишки.
Следует различать две группы заболеваемости колоректальным раком: спорадические случаи (не связанные с известным генетическим/семейным бременем) и семейные (возникающие в результате известного дефекта [мутации] некоторых генов или неизвестной причины, проявляющиеся повышенным риск развития этого рака в данной семье). Подавляющее большинство случаев можно отнести к первой группе, а доля семейных/генетических заболеваний, по разным оценкам, не превышает 15–30% всех случаев заболевания.
Симптомы колоректального рака зависят от тяжести заболевания и локализации заболевания в кишечнике. Общие ранние симптомы включают:
К числу поздних симптомов относятся типичные симптомы распространенного рака: прогрессирующее похудание, потеря аппетита, слабость, анемия и др.
Существует множество исследований по диагностике колоректального рака. В зависимости от типа симптомов, о которых сообщил пациент, врач решит, какие анализы следует провести и в каком порядке для подтверждения диагноза колоректального рака или для их исключения.Некоторые тесты также используются в скрининговых тестах, то есть проводятся у здоровых людей, не сообщающих о каких-либо симптомах, для выявления рака толстой кишки на очень ранней стадии развития.
Метод лечения колоректального рака зависит от стадии заболевания на момент постановки диагноза. Основным методом лечения колоректальных новообразований всегда является и операция и ее выполнение следует учитывать во всех случаях.Вместе с тем следует подчеркнуть, что оперативное вмешательство возможно не всегда, а иногда его выполнение приходится откладывать - после окончания других, начальных (так называемых неоадъювантных) методов лечения.
Если опухоль толстой кишки очень мала или ограничена небольшим полипом, возможно локальное иссечение опухоли/полипа без иссечения фрагмента кишки . Такая процедура может быть выполнена, в зависимости от локализации и типа поражения, либо лапароскопически, либо эндоскопически (с помощью колоноскопии или хирургического ректоскопа).
Однако в большинстве случаев колоректального рака необходима резекция опухоли вместе с фрагментом толстой кишки . Такая процедура проводится под общим наркозом. Обычно его делают, вырезая на коже живота надрез длиной 15-30 см. Существует несколько видов стандартной операции: при раке правого отдела толстой кишки (слепая кишка, восходящая ободочная кишка, правая часть предка) — так называемая правосторонняя гемиколэктомия. С другой стороны, в случае поражения левой части поперечно-ободочной кишки, нисходящей ободочной кишки и верхней части сигмовидной кишки обычно выполняется «левосторонняя гемиколэктомия».Иногда сигмовидную тоже иссекают с верхушкой прямой кишки, если опухоль расположена в этих отделах толстой кишки. Наконец, при опухолях прямой кишки иссекают нижний отдел сигмовидной кишки с прямой кишкой (иногда приходится иссекать и задний проход). Если по разным причинам оба свободных конца кишки не могут быть сшиты между собой («кишечный анастомоз»), верхний конец следует трансформировать в так наз. фекальный свищ или «искусственный задний проход».
В последние годы были предприняты попытки иссечь участки толстой кишки при раке с помощью лапароскопа, но это еще не процедура, принятая во всех центрах, хотя она, по-видимому, не связана с худшими отдаленными результатами в плане эффективности.С другой стороны, следует подчеркнуть, что даже наличие в том или ином хирургическом отделении соответствующего оборудования и обучение персонала этому виду хирургии не означает, что все операции на толстой кишке будут выполняться лапароскопически. Решение о проведении такой операции зависит от размера и локализации опухоли, сопутствующих заболеваний и предпочтений пациента.
В некоторых случаях необходимо наложение стомы ("каловый свищ", "искусственная прямая кишка", "колостома") при операциях на толстой кишке. Это отверстие в брюшной стенке, к которому проходит концевой отдел кишечника и через которое кал выходит в пластиковый резервуар (стомический мешок), расположенный над отверстием. Фистула может быть временной, но может быть и последним средством. Иногда так наз. «защитный» кишечный свищ, чтобы кишечное содержимое не проходило через ушитый (анастомозный) участок кишки в течение нескольких месяцев (на период, необходимый для заживления анастомоза).Такой свищ (еюноанастомоз) устанавливается временно, т.е. планируется закрыть стому и восстановить естественный путь дефекации в более поздние сроки (от нескольких недель до нескольких месяцев).
У пациентов с очень распространенным колоректальным раком может потребоваться полиорганная хирургия . Это тот случай, когда рак проник в соседние органы и для его полного удаления необходимо иссечение частично или полностью пораженного органа (напр.желудок, печень, селезенка, почки, брюшная стенка, мочевой пузырь и др.).
Химиотерапия (и современная таргетная молекулярная терапия) используются при лечении колоректального рака как до, так и после операции. Применение химиотерапии перед операцией может в ряде случаев уменьшить массу опухоли и тем самым облегчить работу хирурга и повысить эффективность операции, выражающуюся в шансах на полное выздоровление. В свою очередь, применение химиотерапии после хирургического вмешательства заключается в повышении выживаемости пациентов за счет уничтожения любых опухолевых клеток, которые могут циркулировать в организме.
Лучевая терапия (лучевая терапия) чаще всего используется для лечения рака прямой кишки, которая является частью толстой кишки непосредственно перед анусом. Применяется либо до операции (самая распространенная), либо после нее. Перед операцией он направлен на уменьшение опухоли, что позволяет или облегчает операцию, а после операции он предназначен для уничтожения любой остаточной опухоли. Облучение также может быть использовано для лечения симптомов колоректального рака, т.е.боль.
В последние годы было разработано множество препаратов, т.н. молекулярно-таргетная терапия . Это препараты, способные «распознавать» раковые клетки и уничтожать их, как правило, без особого вреда для большинства здоровых клеток. В настоящее время эти препараты используются у некоторых пациентов в качестве дополнения к описанным выше классическим методам лечения. Следует подчеркнуть, что не во всех случаях можно использовать препараты из этой группы, поскольку условием их применения является чувствительность раковых клеток к данному препарату.Эффективность этих препаратов также существенно ограничена.
Около 80% всех случаев колоректальных новообразований являются новообразованиями без семейного происхождения, т.е. это новообразования, возникшие у людей, у которых у ближайших родственников не диагностирован этот тип заболевания. Остальные 20% больных колоректальным раком — это люди с семейными заболеваниями, то есть те, у близких родственников которых диагностирован этот вид рака.Около 5% всех случаев колоректального рака составляют онкологические заболевания с семейным анамнезом синдрома Линча (неполипозный колоректальный рак — HNPCC). Приблизительно 0,5–1% случаев колоректального рака вызваны мутациями в гене APC, вызывающими синдром семейного полипоза. Люди, имеющие родственников первой степени родства с колоректальным раком, имеют более высокий риск развития этих заболеваний.
Ко всем членам семьи с повышенным риском развития колоректального рака следует применять различные правила наблюдения и возможные профилактические операции.
Среди факторов риска развития колоректального рака есть несколько, которые можно изменить, изменив свое поведение на более здоровое. Действия по снижению риска развития колоректального рака включают:
Вышеуказанные меры снижают риск развития колоректального рака, но не устраняют его полностью. Поэтому всем людям старше 50 лет рекомендуется проходить хотя бы одно периодическое обследование, позволяющее своевременно выявить колоректальный рак, что дает шанс на получение очень хороших результатов лечения. Существуют различные схемы скрининга для раннего выявления колоректального рака. Наиболее часто рекомендуются:
Просмотреть полный текст ...
.90 000 Как лапароскопия изменила лечение колоректального рака 90 001
Лукаш Антчак / Agencja Gazeta
Источник: Kurier Mediczny / KL
Автор: Ивона Казимерска Дата: 07.01.2021
- Лапароскопическая хирургия занимает бесспорное место в лечении рака толстой кишки. В нашем центре целых 30 процентов. операции выполняются с использованием этой малоинвазивной техники, - говорит проф.доктор хаб. доктор медицинских наук Войцех Зегарский, заведующий отделением онкологической хирургии Collegium Medicum в Быдгоще Университета Николая Коперника в Торуни и клинического отделения онкологической хирургии Онкологического центра в Быдгоще.
Лапароскопическая хирургия стала новым стандартом лечения. Доказано, что использование этого метода может быть безопасным опытными хирургами (тесты COLOR II, COLOR III, CLASSIC, COREAN, ACOSOG).- Наши пациенты становятся бенефициарами этого лечения.Малоинвазивным способом мы можем вырезать практически 70-80 процентов. опухоли. Мы признаем, что пациентов с колоректальным раком без инвазии других органов можно безопасно и качественно оперировать с помощью лапароскопической техники, — говорит проф. Войцех Зегарский.
Лапароскопический доступ способствует уменьшению кровопотери во время операции, более быстрому восстановлению перистальтики кишечника и боли в периоперационном периоде, что в целом приводит к сокращению пребывания в стационаре. Исследование COLOR II показало, что лапароскопия приводила к более быстрому выздоровлению, лучшему трехлетнему безрецидивному исходу у пациентов с 3-й стадией и меньшей частоте поражения края шейки матки при низком раке прямой кишки.В лапароскопической хирургии локальные рецидивы встречаются значительно реже, чем в открытой хирургии, а время выживания значительно больше.
Первые лапароскопические операции по поводу колоректального рака были проведены в 1991 году. Сегодня они проводятся в десятках стран мира. Исследование, проведенное несколько лет назад (данные за 2016-2017 годы), показывает, что целых 37 процентов. хирургия рака толстой кишки и 38 процентов. рак прямой кишки выполняется с использованием лапароскопической техники. К сожалению, в Польше лапароскопические операции при колоректальном раке все еще слишком редки.
Из исследования PSSO_01 известно, что в 2018 году из 500 случаев, зарегистрированных в более чем дюжине польских больниц, только 11 процентов. были оперированы лапароскопически. 2020 год принес некоторое улучшение, потому что во всей колоректальной хирургии 15 процентов. операции (более 200) выполнены лапароскопическим методом. Большинство из них выполняются этим методом в Южной Корее, Нидерландах, Австралии - более 50%, а в Великобритании даже 70%. В других странах Европы этот процент составляет 7-35 процентов. Лапароскопическая хирургия толстой кишки является практически золотым стандартом, как и лапароскопическая резекция рака толстой кишки.
Методика HIPEC связана с лапароскопической техникой и желательна, когда брюшина вовлечена в колоректальный рак. Применяется в случае ограниченного продвижения перитонеальных метастазов, что позволяет провести радикальную операцию с последующей внутрибрюшинной перфузионной химиотерапией в условиях гипертермии. - Адъювантную ГИПХ целесообразно проводить у пациентов, ранее перенесших неотложные операции по поводу обструкции или перфорации, и у которых диагностированы опухолевые клетки в лаваже из брюшной полости.HIPEC с митомицином, выполненная через 4-8 недель, значительно улучшает 5-летнюю выживаемость, - комментирует проф. Войцех Зегарский.
- Лапароскопическая трансректальная мезоректальная резекция (ТА ТМЭ) все еще находится на стадии оценки. Ведутся исследования, например COLOR III, чтобы оценить, является ли этот метод более ценным, чем классические операции, которые мы выполняли до сих пор. На данный момент группа норвежских исследователей приняла решение временно приостановить выполнение операций ТА ТМЭ в своей стране до завершения собственных и чужих исследований, так как их беспокоил высокий процент местных рецидивов, почти 10%.- поясняет проф. Заводной.
- Следует подчеркнуть огромные преимущества лапароскопической хирургии у пациентов, которым необходимо выполнить брюшно-промежностную резекцию прямой кишки с окончательной стомой из-за низко расположенных опухолей нижнего отдела прямой кишки. Пациент с такой обширной и калечащей операцией избегает ненужных травм и страданий, риска образования грыжи живота и возвращается домой 3–5 числа. в сутки без типичных осложнений и проблем, которые часто возникают у пациентов после брюшно-промежностной ректальной ампутации классическим методом, - говорит специалист.
Больные с диагнозом колоректальный рак, нуждающиеся в оперативном лечении, обращаются в хорошие центры, где проводится соответствующее количество операций, что дает шанс добиться хороших результатов лечения. Именно поэтому хирургов, особенно молодого поколения, обучают лапароскопическим методам. В 2018 году была реализована программа LAPCO Poland – польская версия британской программы аккредитации и обучения в области лапароскопической колоректальной хирургии, считающаяся образцом.В Польше есть пять учебных центров LAPCO.
- В настоящее время в Великобритании целых 70 процентов. Хирургическое лечение колоректального рака проводится лапароскопическим методом. Еще 10 лет назад, до введения программы LAPCO, она составляла всего около 20 процентов. Эти операции, благодаря постоянному контролю со стороны LAPCO, соответствуют самым высоким онкологическим стандартам, — резюмирует проф. Заводной.
Текст опубликован в "Kurier Medyczny" 8/2020. Журнал можно заказать по адресу: www.termedia.пл/км/подписка .
Мы рекомендуем вам поставить лайк профилю Health Manager на Facebook: www.facebook.com/MenedzerZdrowia и подписаться на аккаунты в Twitter и LinkedIn: www.twitter.com/MenedzerZdrowia и www.linkedin. com/MenedzerZdrowia .
.Введение
Рак прямой кишки является одной из наиболее частых причин смерти от рака в западном мире. Людей, у которых диагностирован рак прямой кишки, лечат в основном хирургическим путем. Однако существует риск рецидива рака после операции. Цикл лучевой терапии перед операцией может снизить риск местного рецидива, поскольку лучевая терапия может разрушить остаточные опухоли меньшего размера и усилить эффект самой операции.
Тестовые характеристики
4 июня 2018 г. мы провели поиск в медицинских базах данных на предмет рандомизированных контролируемых испытаний (экспериментальных исследований, в которых участников случайным образом распределяют в одну из двух или более групп лечения), чтобы определить, есть ли какие-либо преимущества предоперационной лучевой терапии у людей с раком прямой кишки. для снижения риска смерти от любой причины, смерти от рака и рецидива рака малого таза.Мы рассмотрели высокодозную лучевую терапию с последующим любым типом хирургического лечения для удаления рака прямой кишки.
Результаты
Мы нашли 4 исследования, в которых приняли участие 4663 человека с операбельным раком прямой кишки. Наши результаты показывают, что проведение коротких курсов лучевой терапии перед операцией, вероятно, снижает смертность. Однако когда наш анализ ограничился используемой в настоящее время методикой оперативного лечения (полное иссечение мезоректума [удаление опухоли и окружающей жирово-лимфатической ткани; прим.]), мы не обнаружили различий между группой предоперационной лучевой терапии и группой только хирургического лечения. Различия между исследуемыми группами могут быть незначительными или отсутствовать вообще с точки зрения риска смерти от рака во время коротких циклов лучевой терапии.
Мы нашли доказательства среднего качества, что могут быть значительные преимущества в снижении риска рецидива рака с помощью предоперационной лучевой терапии по сравнению с только хирургическим вмешательством.
Мы обнаружили незначительное влияние предоперационной лучевой терапии на резекцию или хирургическое вмешательство с сохранением сфинктера или его отсутствие.
Мы обнаружили более высокую частоту сепсиса, послеоперационных осложнений и сексуальной дисфункции у субъектов, получивших предоперационную лучевую терапию, по сравнению с теми, кто получил только хирургическое вмешательство.
Качество научных данных
В целом исследования были хорошо спланированы.Мы оценили качество доказательств как умеренное в отношении рецидива опухоли и общей смертности, поскольку были серьезные опасения по поводу применимости результатов к современному лечению рака прямой кишки.
Затем мы снизили качество доказательств для остальных конечных точек из-за неточных результатов и/или различий между исследованиями в критериях, используемых для диагностики рака прямой кишки, стадии заболевания у участников, предоперационной визуализации, используемой для оценки стадии, типа операции выполненная доза облучения и фракционирование, время между лучевой терапией и операцией, а также использование адъювантной терапии (адъювантной химиотерапии).перев.) или послеоперационный.
.© Borgis - New Medicine 4/1999, стр. 15-18
Януш Олендски, Марек П. Новацкий
Колоректальные новообразования - радикальное хирургическое лечение
Опухоли толстой кишки - хирургия колоректального рака
от Клиники рака толстой кишки Онкологического центра - НИИ им. Мария Склодовская-Кюри в Варшаве
Заведующий клиникой: проф.доктор хаб. Марек П. Новацки, MD 9000 3
Хирургическое лечение остается методом выбора при большинстве случаев колоректального рака. Результаты лечения зависят в основном от клинико-патологической стадии. Однако оказывается, что хирург является вторым по важности прогностическим фактором в случае колоректального рака, особенно прямой кишки, и, таким образом, его мотивация, опыт и взгляды, привитые во время обучения. Современные правила поведения, на которых основана операционная стратегия, вытекают из многолетних экспериментальных исследований и опыта нескольких поколений хирургов.Знание принципов онкологического лечения, факторов риска и прогностических факторов, а также возможностей комбинированного лечения в сочетании с опытом и технической подготовкой, несомненно, облегчают выбор наилучшего лечения в конкретном случае. Самый низкий процент послеоперационных смертей и осложнений и, в конечном итоге, самый низкий возможный процент местных рецидивов и отдаленных метастазов, а также самый высокий возможный процент постоянных излечений, помимо прогрессирования рака, в значительной степени зависят от оператора.В этой статье мы попытались обрисовать технические принципы хирургической процедуры.
1. Для оперативного вмешательства по поводу патологии толстой кишки больных обычно помещают в т. н. Позиция Ллойда-Дэвиса. Наиболее распространенным хирургическим разрезом в нашей Клинике является длинный разрез по средней линии тела, который в большинстве случаев дает наилучший обзор всей брюшной полости и позволяет оптимально выбрать место возможной колостомы. В интраоперационную оценку органов брюшной полости следует включить:
- макроскопическое состояние печени, подтвержденное по возможности интраоперационным ультразвуковым исследованием,
- состояние париетальной и висцеральной брюшины при особо тщательном осмотре большой сетки,
- объем свободной жидкости в брюшной полости.Асцит и обсеменение серозной оболочкой являются противопоказанием к резекции, и процедура должна ограничиваться декомпрессией кишечника. В случае сомнений может быть рекомендовано провести экстренный мазок Папаниколау,
.- оценка забрюшинных лимфатических узлов (пальпация и, возможно, интраоперационное УЗИ),
- обследование всей толстой кишки в поисках синхронных изменений, типов кровоснабжения, соотношения опухоли с окружающими органами и ее подвижности. Ограничение подвижности как первичной опухоли, так и лимфатических узлов не всегда является синонимом опухолевой инфильтрации.Это может быть результатом воспалительной реакции.
Все выявленные изменения должны быть задокументированы в рабочем протоколе. Предоперационная оценка наряду со знанием всех особенностей конкретного случая, наряду с интраоперационной оценкой, используются для принятия окончательного решения. Отказ от намерения провести радикальную операцию равносилен невозможности излечения, а принятие решения о проведении операции с намерением выздоровления равносильно неизбежному риску осложнений (35-40%), и даже послеоперационной смерти. (1-6%).
Очень хорошее знание анатомии сосудистой и лимфатической систем толстой кишки является необходимым условием для выбора правильного объема резекции. Артериовенозная васкуляризация, путь лимфооттока и расположение лимфатических узлов определяют объем резекции соответствующего отдела толстой кишки, включая ее мезоректум, в случае прямой кишки.
2. Есть много способов составить ассоциативный ряд. Несостоятельность анастомоза определяется не столько методом, сколько технической правильностью наложения анастомоза.Лишь при необходимости наложения «низкого» анастомоза с забрюшинным отделом прямой кишки механический анастомоз является своего рода выбором. Он не обременен более высоким процентом несостоятельности или местных рецидивов по сравнению с традиционным анастомозом, наложенным вручную. Многие исследования явно поддерживают механические анастомозы, поскольку процент осложнений в виде несостоятельности статистически значимо ниже, а значит, ниже также процент местных рецидивов и увеличивается процент отдаленной выживаемости (1).
Анастомики должны стать повседневным инструментом хирургов, потому что: они практически надежны, позволяют быстро и безопасно накладывать анастомоз, а количество операций на сфинктерах и их эффективность увеличились за последнее десятилетие значительно, даже во много раз. Процент ректальных ампутаций, выполняемых брюшно-промежностным методом, в настоящее время в специализированных центрах колеблется от 20 до 30%, а показанием к данному виду операции является расположение рака в ректальном канале или инфильтрация сфинктеров.Количество всегда серьезных несостоятельностей анастомозов значительно уменьшилось и при интраоперационной оценке не превышает 10%, а послеоперационно - от 5% до <20%, в зависимости от метода оценки (клинически, эндоскопически и/или рентгенологически), высоты анастомоз, опыт оператора и способ выполнения.
Иногда, особенно при самых нижних анастомозах, т.е. на высоте зубчатой линии или чуть выше нее, технически проще и одновременно безопаснее использовать ручной анастомоз одинарными рассасывающимися швами.
Следует, однако, помнить, что незнание принципов лечения онкологических заболеваний и недостаточная общехирургическая техническая квалификация не могут быть заменены увлечением сшивающими аппаратами. Показанием к наложению механического анастомоза может быть любой вид колоректальной резекции и любой вид анастомоза, однако по медицинским и экономическим причинам наиболее важными показаниями являются:
- низкая передняя резекция прямой кишки по поводу локализованного рака: у женщин на расстоянии <8 см от ануса, а у мужчин <10 см, если удается обеспечить макроскопический дистальный край (ниже пальпируемого края опухоли) не менее 2 см для среднезрелых и зрелых раков около 5 см для низкодифференцированных,
- восстановление непрерывности толстой кишки после операции Гартмана,
- паллиативные резекции (также удалить большую сетку и яичники!).
3. До сих пор остается нерешенным вопрос о том, выполнять ли «профилактическую» фистулу, и если да, то в каких случаях. Большинство хирургов не выполняют профилактические фистулы. Следует подчеркнуть, что профилактическая фистула не влияет на герметичность анастомоза и может значительно уменьшить последствия несостоятельности. Поэтому следует учитывать целесообразность создания профилактического свища, особенно в случае так называемого низкий «ненадежный» анастомоз у пациентов пожилого возраста, с высоким периоперационным риском из-за легочно-циркуляторных нагрузок, так как такой менеджмент может снизить вероятность повторного вмешательства для лечения несостоятельности анастомоза и его последствий.
4. Другой часто обсуждаемой проблемой является дренирование зоны анастомоза. Число ярых сторонников и противников слива вроде бы примерно одинаковое. По нашему мнению, обильный рутинный интраоперационный лаваж брюшной полости является все более частой причиной дренирования брюшины. Обычно достаточно пассивного дренирования в течение 24 часов после операции. Клинический опыт показывает, что большинство «профилактических» дренажей через это время засоряются. Другой, тем не менее, обсуждаемый вопрос заключается в том, должен ли дренаж быть активным или пассивным (осадки).Мы разделяем мнение, что активный дренаж не только не нужен, но и может быть опасен. Длительное «профилактическое» дренирование брюшины в области анастомоза не снижает вероятности осложнений, а при возникновении таких осложнений оказывается недостаточным для эффективного удаления гноя и/или каловых масс. Использование дренажа не может служить дополнением к небрежной хирургической технике или средством успокоения совести оператора. Безусловно, оценка фактической пользы или вреда дренирования требует окончательного решения посредством дальнейших проспективных рандомизированных клинических испытаний.
5. Перитонизация малого таза после передней резекции или ректальной ампутации методом тотальной мезоректальной эксцизии (ТМЭ) просто невозможна и в настоящее время с этим согласны подавляющее большинство хирургов.
6. Во всех случаях внутрибрюшинного рака толстой кишки с инфильтрацией серозной оболочки следует проводить профилактическое иссечение толстой кишки. Большая сеть, часто называемая «хранителем брюшины», в этих случаях может оказаться удобным местом для имплантации опухолевых клеток, присутствующих на поверхности серозной оболочки или отслоившихся в брюшную полость во время операции.
7. Подсчитано, что метастазы в яичники встречаются в крайних пределах от 1,4 до 28%, в среднем у 6% женщин, получающих лечение по поводу распространенного колоректального рака. Вероятность поражения яичников увеличивается по мере прогрессирования рака. Гормональный статус пациенток, по-видимому, не играет большой роли, хотя некоторые авторы считают, что вероятность метастазов в яичники выше у молодых женщин в пременопаузе. Метастазы чаще всего встречаются с обеих сторон (50-70), поэтому односторонняя аднексэктомия представляется оправданной только в случае непрерывности инфильтрата.В свете современных знаний потенциальными показаниями для одновременной овариэктомии с резекцией колоректального рака могут быть:
- все случаи у женщин в менопаузе,
- случаи инфильтрации серозной оболочки, массивного поражения лимфатических узлов, макроскопически измененных (подозрение) яичников у женщин в пременопаузе,
- Семейный анамнез рака яичников,
- спайки между яичником и очагом рака,
- паллиативные процедуры (диагностированные отдаленные метастазы, инфильтрация или распространение в пределах париетальной или висцеральной брюшины).
Окончательная роль профилактической овариэктомии требует проведения проспективных рандомизированных клинических испытаний.
Мы загрузили отрывок из статьи выше, к которой вы можете получить полный доступ.
У меня есть код доступа
90 069 19 90 070
злотых я выбираюполученный код необходимо ввести на странице статьи, на которую он был погашен
49 90 070
злотых я выбираю119
зл. я выбираюСсылки
1. Nowacki M.P.: Колоректальные новообразования. Коллективный труд под редакцией М.П. Nowackiego, Wiedza i Życie, Warsaw 1996, 206. 2. Nogueras J.J., Jagelman D.G.: Принципы хирургической резекции. Влияние хирургической техники на исход лечения. Surg. клин. Север Ам. 1993, 73: 103-116.
.