2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Получают соляную кислоту растворением в воде хлористого водорода, который синтезируют или непосредственно из водорода и хлора или получают действием серной кислоты на хлорид натрия.
Выпускаемая техническая соляная кислота имеет крепость не менее 31% HCl (синтетическая) и 27,5% HCl (из NaCI). Торговую кислоту называют концентрированной, если она содержит 24% и больше HCl, если содержание HCl меньше, то кислота называется разбавленной.
Соляную кислоту применяют для получения хлоридов различных металлов, органических полупродуктов и синтетических красителей, уксусной кислоты, активированного угля, различных клеев, гидролизного спирта, в гальванопластике. Ее применяют для травления металлов, для очистки различных сосудов, обсадных труб буровых скважин от карбонатов, окислов и др. осадков и загрязнений. В металлургии кислотой обрабатывают руды, в кожевенной промышленности – кожу перед дублением и крашением. Соляную кислоту применяют в текстильной, пищевой промышленности, в медицине и т. д.
Соляная кислота играет важную роль в процессах пищеварения, она является составной частью желудочного сока. Разведенную соляную кислоту назначают внутрь главным образом при заболеваниях, связанных с недостаточной кислотностью желудочного сока.
Транспортируют соляную кислоту в стеклянных бутылях или гуммированных (покрытых слоем резины) металлических сосудах, а также в полиэтиленовой посуде.
Соляная кислота очень опасна для здоровья человека. При попадании на кожу вызывает сильные ожоги. Особенно опасно попадание в глаза.
При попадании соляной кислоты на кожные покрытия ее необходимо немедленно смыть обильной струей воды.
Очень опасны туман и пары хлороводорода, образующиеся при взаимодействии с воздухом концентрированной кислоты. Они раздражают слизистые оболочки и дыхательные пути. Длительная работа в атмосфере HCl вызывает катары дыхательных путей, разрушение зубов, помутнение роговицы глаз, изъязвление слизистой оболочки носа, желудочно-кишечные расстройства.
Острое отравление сопровождается охриплостью голоса, удушьем, насморком, кашлем.
В случае утечки или разлива соляная кислота может нанести существенный ущерб окружающей среде. Во-первых, это приводит к выделению паров вещества в атмосферный воздух в количествах превышающих санитарно-гигиенические нормативы, что может повлечь отравление всего живого, а также появлению кислотных осадков, которые могут привести к изменению химических свойств почвы и воды.
Во-вторых, она может просочиться в грунтовые воды, в результате чего может произойти загрязнение внутренних вод.
Там, где вода в реках и озерах стала довольно кислой (рН менее 5) исчезает рыба. При нарушении трофических цепей сокращается число видов водных животных, водорослей и бактерий.
В городах кислотные осадки ускоряют процессы разрушения сооружений из мрамора и бетона, памятников и скульптур. При попадании на металлы соляная кислота вызывает их коррозию, а, реагируя с такими веществами, как хлорная известь, диоксид марганца, или перманганат калия, образует токсичный газообразный хлор.
В случае разлива соляную кислоту смывают с поверхностей большим количеством воды или щелочного раствора, который нейтрализует кислоту.
Материал подготовлен на основе информации открытых источников
Соляная кислота представляет собой жидкую форму своего газового аналога (гидрохлорид или HCl) и является результатом добавления воды к гидрохлориду. Он от слегка желтого до бесцветного, негорючий, но вызывает сильную коррозию.
Соляная кислота имеет множество применений в различных отраслях промышленности. Он обычно используется в качестве компонента при производстве батарей и фейерверков, а также для регулирования уровня pH в бассейнах. Его можно использовать для удаления ржавчины и окалины со стали.
Соляная кислота также используется в производстве питьевой воды (для дезинфекции воды), других напитков и пищевых продуктов (для улучшения вкуса и уменьшения порчи), а также в фармацевтических препаратах.
 Соляная кислота защищает бассейны от водорослей
Соляная кислота защищает бассейны от водорослей Основные пути воздействия соляной кислоты - через рот и попадание на кожу или в глаза, при этом также возможен вдыхание.
Отравление соляной кислотой повлияет на покровы человека (волосы, кожа и ногти) и дыхательную систему (дыхательные пути и легкие).
Серьезность ваших симптомов будет зависеть от уровня и типа воздействия химического вещества.
Они могут включать;
Длительное воздействие соляной кислоты может вызвать дерматит, воспаление кожи, хронический бронхит и гастрит. Продолжительное воздействие низких концентраций кислоты, например, содержащихся в обычных продуктах питания и напитках, может привести к кариесу и обесцвечиванию зубов.
Если вы проглотили соляную кислоту, немедленно обратитесь за медицинской помощью и не вызывайте рвоту, если не рекомендовано или не более чем в 15 минутах от больницы (вызывайте рвоту только у человека, который находится в сознании).
В случае контакта с кожей; снимите всю загрязненную одежду, обувь и аксессуары и немедленно промойте пораженный участок большим количеством воды с мылом. Перед повторным ношением загрязненную одежду необходимо выстирать. Если симптомы не исчезнут, обратитесь к врачу.
При попадании в глаза промойте глаза водой не менее 15 минут (не забудьте под веками). Снять контактные линзы должен только опытный профессионал.
Если человек вдохнул химическое вещество, отнесите его из зараженной зоны к ближайшему источнику свежего воздуха и следите за его дыханием. Если они не дышат, вы можете выполнить СЛР (при наличии соответствующей квалификации) с помощью одностороннего клапана или защитной маски, чтобы обезопасить себя от остаточных химических веществ, которые могут присутствовать в дыхательных путях пациента.
 Кислоты особенно вредны для глаз, поэтому необходимо надевать защитные очки.
Кислоты особенно вредны для глаз, поэтому необходимо надевать защитные очки. Безопасный душ и фонтанчики для аварийной промывки глаз должны быть доступны в непосредственной близости от потенциального воздействия химического вещества, и всегда должна быть соответствующая вентиляция.
СИЗ, такие как защитные очки с боковыми щитками, пыленепроницаемая одежда, перчатки, фартуки и маски / респираторы, необходимы при работе с химическими веществами. Также следует избегать ношения контактных линз.
Chemwatch имеет самую большую коллекцию паспортов безопасности (SDS) в мире. Для свободный копию SDS для соляной кислоты, созданного Chemwatch, нажмите кнопку ниже.
1. Общие требования безопасности
1.1. На основе настоящей Инструкции разрабатываются инструкции по охране труда для работников, занятых в процессах нанесения металлопокрытий, при работе с кислотами и щелочами (далее - работники, занятые работами с кислотами и щелочами).
1.2. К выполнению работ с кислотами и щелочами допускаются работники в возрасте не моложе 18 лет, освоившие безопасные методы и приемы выполнения работ, методы и приемы правильного обращения с механизмами, приспособлениями, инструментами, а также с грузами.
1.3. К работе на грузоподъемных машинах, управляемых с пола, по подвешиванию груза на крюк таких машин допускаются работники не моложе 18 лет, обученные по специальной программе, аттестованные экзаменационной комиссией организации и имеющие удостоверение на право пользования грузоподъемными машинами и зацепку грузов.
1.4. При выполнении работ необходимо соблюдать принятую технологию. Не допускается применять способы, ведущие к нарушению требований безопасности труда.
1.5. В случае возникновения в процессе работы каких-либо вопросов, связанных с ее безопасным выполнением, необходимо обратиться к своему непосредственному или вышестоящему руководителю.
1.6. Работники, занятые работами с кислотами и щелочами, обязаны соблюдать правила внутреннего трудового распорядка организации.
1.7. При работе с кислотами и щелочами на работника могут воздействовать опасные и вредные производственные факторы:
повышенная загазованность парами вредных химических веществ;
пожаровзрывоопасность;
движущиеся механизмы и машины;
брызги кислот и щелочей токсичных электролитов и растворов.
В связи с этим невыполнение настоящей Инструкции может привести к отравлению и химическим ожогам.
1.8. Работники, занятые на работах с кислотами и щелочами, должны обеспечиваться средствами индивидуальной защиты.
1.9. Порядок и условия хранения и выдачи каждого химического вещества должны быть установлены соответствующими инструкциями, утверждаемыми работодателем.
1.10. Условия хранения кислот и щелочей необходимо выбирать в зависимости от их физико-химических свойств и классификации опасных веществ.
1.11. Хранить кислоты в цехе необходимо в специальном помещении с кислотоупорными полами и стенами в закрытых кислотостойких резервуарах или в таре завода-поставщика. Не допускается хранить кислоты в подвальных помещениях. В кислотохранилищах необходимо постоянно следить за исправным состоянием емкостей и трубопроводов, своевременным ремонтом и заменой арматуры, качеством уплотнения фланцев. Запас кислот в цеховых расходных кладовых не должен превышать двухсуточной потребности цеха.
1.12. При входе в помещение, где хранятся кислоты, должен быть устроен пандус или порог, предотвращающий растекание жидкости в случае аварии.
1.13. Кислоты должны храниться в следующей таре:
азотная кислота всех концентраций - в алюминиевых бочках и цистернах;
азотная кислота средней агрессивности - в бочках и цистернах из коррозионностойкой стали марки Х18Н9Т и других;
серная кислота всех концентраций - в бочках и цистернах из коррозионностойкой стали марки 06ХН28МДТ;
серная кислота низких концентраций (до 20%) - в бочках и цистернах из коррозионностойкой стали марки 06ХН28МТ;
соляная кислота - в стальных гуммированных бочках и цистернах;
плавиковая (фтористоводородная) кислота - в эбонитовых бидонах емкостью 20 л и в полиэтиленовых баллонах емкостью до 50 л.
Азотная и серная кислота в количестве до 40 л могут храниться в стеклянных бутылях.
1.14. Внутренняя поверхность тары, предназначенной для хранения и транспортировки агрессивных жидкостей, способных вступать в химические соединения с материалами, из которых сделана тара, должна быть гуммирована или футерована материалами, устойчивыми к воздействию агрессивных жидкостей.
1.15. Не допускается хранение кислот в помещении, где хранятся или применяются цианистые соединения.
1.16. На складах хранения и в местах применения кислот должны быть:
резервные емкости для аварийного слива кислот;
кислотостойкие насосы;
передвижные фильтры и резиновый шланг со специальным наконечником, создающим напор воды для смывания кислоты;
растворы извести или соды для нейтрализации пролитых кислот;
средства индивидуальной защиты и первой помощи (очки, противокислотный костюм с капюшоном, резиновые сапоги, фартук, перчатки, респиратор, противогаз и аптечка).
1.17. Емкости для транспортировки кислот должны быть окрашены кислотостойкой краской и иметь надпись "Опасно! Кислота" и наименование кислот, выполненное устойчивой краской.
1.18. Бутыли с кислотами, поставленные в плетеные корзины с прочными ручками или в деревянные обрешетки, должны устанавливаться в местах хранения группами (одного наименования) в 2 - 4 ряда и не более 100 шт. в каждой группе. Ширина проходов между рядами бутылей должна быть не менее 1 м. Пространство между бутылью и корзиной должно быть заполнено прокладочными материалами, пропитанными раствором хлористого кальция, во избежание воспламенения. Бутыли с кислотой должны защищаться от воздействия на них солнечных лучей.
1.19. В емкости для кислот не допускается попадание бензина, керосина, масла и спирта.
1.20. Во избежание пожара, взрыва или выделения ядовитых газов не допускается хранение кислот и щелочей в помещении, где производится обработка изделий из магния и титана.
1.21. Твердый едкий натр должен храниться в железных барабанах; жидкий едкий натр - в железных банках, бочках и баках. Сосуды с едким натром должны иметь надпись "Опасно - едкий натр".
КонсультантПлюс: примечание.
Нумерация пунктов дана в соответствии с официальным текстом документа.
1.25. При переливании кислот и щелочей должны применяться специальные приспособления из кислотостойких материалов (сифоны и другие). При пользовании сифонами для переливания кислот, щелочей и рабочих растворов сифоны заполняют, засасывая жидкость путем создания вакуума или при помощи сжатого газа. Засасывать воздух ртом не допускается.
1.26. При опорожнении бутылей не допускается оставлять в них кислоту.
1.27. Слив из бочек и цистерн следует производить, создавая разрежение или специальными кислотостойкими насосами. Все трубопроводы необходимо выполнять из винипласта или равноценного материала. Цистерна должна находиться выше уровня слива.
1.28. При большом потреблении кислот опасные и трудоемкие работы по сливу и выдаче кислот должны быть механизированы путем устройства трубопроводов из кислотостойких материалов и установки в отдельных помещениях специальных насосов для перекачки кислот. Насосы для перекачки кислот должны иметь дистанционное включение. Двери насосной должны быть закрыты. При расходе менее 400 кг кислоты в смену допускается подача их в плотно закрытой небьющейся таре.
1.29. Насосы, помпы, емкости, трубопроводы, арматура и другое оборудование для перелива кислот должны периодически, не реже 1 раза в квартал, а резиновые шланги - ежемесячно спрессовываться давлением, превышающим в 1,5 раза рабочее давление, с последующим нанесением клейма о проведенном испытании.
1.30. Каждый работающий на сливных и транспортных операциях обязан пользоваться спецодеждой, спецобувью и индивидуальными защитными приспособлениями. Сливные работы должны производиться в противогазе, при этом работник должен находиться с наветренной стороны.
1.31. При сливе кислот из железнодорожной цистерны в стационарную емкость нагнетательный шланг от центробежного насоса должен быть спущен в верхнюю горловину емкости, а не присоединен к сливному патрубку во избежание гидравлического удара при включении насоса. Не допускается работать с концентрированными кислотами на открытом воздухе в дождь, метель и при сильном ветре.
1.32. Барабаны с каустической содой необходимо перевозить на специальных тележках.
1.33. Жидкий каустик следует переливать при помощи насоса осторожно, не брызгая, а желеобразный каустик - ковшом на длинной деревянной или металлической рукоятке.
1.34. Бутыли, резервуары и другую тару следует заполнять кислотой или другими химическими растворами не более чем на 0,9 их емкости.
1.35. На участках работ, где применяется азотная кислота, не должно быть горючих веществ, материалов и отходов (стружка, опилки и другие материалы).
1.36. При несчастном случае работник, занятый на работах с кислотами и щелочами, должен прекратить работу, известить об этом своего непосредственного или вышестоящего руководителя и обратиться за медицинской помощью.
1.37. Работник, занятый на работах с кислотами и щелочами, обязан соблюдать правила личной гигиены: перед приемом пищи и после окончания работы вымыть руки теплой водой с мылом. Пищу необходимо принимать в специально оборудованных для этой цели помещениях.
1.38. Работники, занятые на работах с кислотами и щелочами, должны уметь оказывать доврачебную помощь пострадавшему.
1.39. Работники, занятые на работах с кислотами и щелочами, не выполняющие требования настоящей Инструкции, привлекаются к ответственности согласно действующему законодательству.
Кислотностью желудка называется концентрация кислоты в просвете органа или желудочном соке. Главную роль в формировании кислотности желудка играет соляная кислота. В норме кислотность в просвете желудка натощак – 1,5-2,0 рН3.
В течение суток и в разных отделах органа кислотность может меняться. Она повышается во время еды, так как кислота активирует ферменты, которые отвечают за переваривание пищи. Кислотность, которая возникает в ответ на прием пищи, называется стимулированной. Постоянная продукция кислоты, не связанная с едой, называется базальной кислотностью3.
В механизме развития изжоги важна не только кислотность желудка, но и среда пищевода. В этом органе кислотность значительно ниже, из-за чего его стенки не имеют дополнительной защиты от воздействия кислоты, как стенки желудка. Поэтому при гастроэзофагеальном рефлюксе кислота желудка оказывает раздражающее действие на стенки пищевода, что может приводить к развитию жжения за грудиной2.
Существует два варианта нарушения кислотности желудка: повышение и понижение. Оба варианта могут провоцировать неприятные симптомы и болезни пищеварительного тракта.
Основные проявления3:
Стойкое повышение выработки соляной кислоты может приводить к развитию кислотозависимых болезней. Самой распространенной проблемой, проявления которой – изжога и кислая отрыжка, является гастроэзофагеальная рефлюксная болезнь2,3. Она характеризуется частыми забросами пищи из желудка в пищевод и хроническим ослаблением пищеводного сфинктера2.
Также повышенная кислотность может провоцировать развитие гиперацидного гастрита, чаще всего ассоциированного с бактерией Helicobacter Pylori или язвенной болезни желудка3. Поставить точный диагноз при частом, длительном возникновении симптомов повышенной кислотности может только врач после комплексного обследования.
Понижение кислотности желудка возникает при развитии гастрита со снижением выработки соляной кислоты. При недостатке кислоты могут развиваться инфекционные процессы в пищеварительном тракте. Кроме того, переваривание пищи тоже ухудшается из-за недостатка ферментов, которые активировались соляной кислотой3.
Проявления состояния3:
Точно установить тип кислотности желудка можно только с помощью специального исследования – внутрижелудочной рН-метрии3.
Омез® 10 мг с действующим веществом омепразол относится к группе ингибиторов протонной помпы и применяется для лечения изжоги и кислой отрыжки1. Омез® 10 мг понижает кислотность желудка, подавляя выработку соляной кислоты1. Таким образом, он влияет непосредственно на причину развития изжоги, а не только на симптом.
Омез® 10 мг – удобный для применения препарат. Его рекомендуется принимать 1 раз в сутки1. Лекарство выпускается в кишечнорастворимых капсулах, поэтому действующее вещество даже при высокой кислотности дойдет до кишечника, где происходит всасывание в кровь.
Омез® 10 мг при пониженной кислотности желудка еще больше снижает продукцию кислоты. Поэтому при данном расстройстве работы пищеварительного тракта лучше воспользоваться другими препаратами. В частности, при развитии гастритов с пониженной кислотностью может применяться заместительная терапия непосредственно соляной кислотой3.

Muriatic acid представляет собой несколько разбавленную версию соляной кислоты. Как и большинство других форм кислоты, соляная кислота обладает высокой коррозионной активностью, а это означает, что вы должны быть очень осторожны при ее использовании. Если у вас есть бассейн на заднем дворе, соляная кислота может быть неотъемлемой частью поддержания надлежащего химического состава воды. Основная причина, по которой соляную кислоту необходимо добавлять в воду в бассейне, заключается в том, что она может помочь снизить уровень pH, который стал слишком высоким. Известно, что высокие уровни pH приводят к образованию накипи.
Наряду с балансировкой уровня pH воды в бассейне, соляная кислота достаточно сильна, чтобы убить плесень, удалить пятна ржавчины, избавиться от отложений кальция и очистить поверхности вашего бассейна. Если вы хотите, чтобы вода в вашем бассейне была чистой и полезной для плавания, очень важно, чтобы вы постоянно принимали меры по очистке бассейна. Из-за того, насколько агрессивной может быть соляная кислота, вы должны точно знать, как ее использовать, прежде чем добавлять ее в воду в бассейне.
В этой статье подробно рассказывается о том, что нужно для безопасного добавления соляной кислоты в бассейн.
Что такое соляная кислота?
Muriatic acid — это особый тип кислоты, который считается менее чистой и несколько разбавленной версией соляной кислоты. Эта кислота полезна из-за ее очень коррозионных свойств. Например, соляная кислота может разъедать все, от одежды и ковров до металлов и пластмасс. Таким образом, он эффективен для снижения pH воды. Однако коррозионная природа соляной кислоты также делает ее опасной для использования, если вы не уверены в том, что делаете. Если эта кислота попадет на кожу, она вызовет сильные ожоги.
Почему вы должны добавлять соляную кислоту в свой бассейн?

Важно добавлять соляную кислоту в бассейн, потому что она может помочь вам сбалансировать уровни pH, когда они достигли слишком высокого уровня. Правильный уровень pH колеблется в пределах 7,2-7,8, что означает, что вода эффективно сбалансирована. Если уровень pH падает ниже этого значения, вода стала кислой, что может привести к целому ряду проблем с водой в вашем бассейне. Однако слишком щелочная вода может быть еще более проблематичной.
Если уровень pH воды в вашем бассейне превышает 7,8, это означает, что вода стала слишком щелочной. Хотя щелочная вода не так опасна для вашего здоровья, как сильнокислая вода, она может создавать проблемы, которых вам следует избегать, если это возможно. Например, вода в вашем бассейне может стать мутной, если она имеет высокое значение pH.
Хлор в воде также будет менее эффективен, а это значит, что поддерживать чистоту бассейна будет сложнее. Высокий уровень pH также может вызвать образование накипи, что связано с накоплением отложений кальция в воде бассейна. Эти отложения могут повредить оборудование вокруг вашего бассейна, что может привести к дорогостоящему ремонту. Балансировка уровня pH в воде вашего бассейна должна дать вам уверенность в том, что ваш бассейн чист.
Шаги по добавлению соляной кислоты в бассейн

Если вы считаете, что химический состав воды в вашем бассейне неправильно сбалансирован, вам может потребоваться добавить немного соляной кислоты, чтобы снизить уровень pH. Прежде чем сделать это, рекомендуется внимательно прочитать следующие шаги, необходимые для правильного добавления соляной кислоты в бассейн. Следуя этим шагам, вы сможете безопасно добавлять кислоту. Свяжитесь со специалистами, если вам нужна помощь.
Шаг 1. Проверьте параметры воды вашего бассейна
Шаг 2. Наденьте защитное снаряжение
Шаг 3. Разбавьте кислоту
Шаг 4. Включите свой бассейн
Шаг 5. Медленно добавьте кислоту в воду
Шаг 6. Снова проверьте уровень pH

Шаг 1. Проверьте параметры воды вашего бассейна
Первый шаг в этом процессе включает в себя проверку уровня химического состава воды в вашем бассейне, что можно сделать с помощью нескольких различных тестеров качества воды (TDS метры, кондуктометры, pH метры, ОВП метры, фотометры и рефрактометры). Хотя можно использовать тест-полоски для определения уровня pH воды в вашем бассейне, эти полоски могут быть неточными. Вместо этого вы должны использовать pH метр, который может обеспечить точные показания pH. Здесь, в МоемГород, мы предлагаем широкий спектр pH метров, контроллеров и датчиков, которые могут выдержать строгие испытания.
Если вы обнаружите, что показания pH слишком высоки, возможно, пришло время добавить в бассейн немного соляной кислоты. Имейте в виду, что идеальные показания для воды в бассейне находятся в пределах 7,2-7,8, а это означает, что все, что выше, может потребовать кислоты.
Шаг 2. Наденьте защитное снаряжение
Прежде чем вы начнете добавлять соляную кислоту в свой бассейн, очень важно надеть защитное снаряжение. Даже кратковременное воздействие на кожу может привести к развитию тяжелых ожогов на пораженных участках, поэтому необходимо защитное снаряжение. Во-первых, убедитесь, что одежда, которую вы носите при добавлении соляной кислоты в бассейн, способна полностью покрыть ваши ноги и руки.
Если у вас есть очки, используйте их, чтобы защитить глаза от возможных брызг. Также важно носить прочные перчатки, полностью устойчивые к кислоте. На этикетке, которую можно найти на ваших перчатках, должно быть указано, к чему перчатки устойчивы. Если когда-нибудь брызги кислоты попадут на вашу кожу, вам нужно немедленно обдать это место прохладной водой, которая может смягчить воздействие кислоты.
Шаг 3. Разбавьте кислоту
Разбавление кислоты является следующим и наиболее важным шагом в безопасном добавлении кислоты в бассейн. Если вы добавите кислоту в воду в бассейне, не разбавив ее предварительно, раствор будет слишком сильнодействующим. Разбавление кислоты позволяет достичь нужного химического состава до того, как кислота будет добавлена в воду бассейна.
Прежде чем начать разбавлять кислоту, убедитесь, что вы никогда не добавляете воду в кислоту. Это приведет к сильной реакции, которая заставит кислоту выплеснуться из контейнера на вас. Чтобы правильно разбавить кислоту, вы должны сначала заполнить ведро на 4-5 галлонов водой. Эта вода должна быть чистой, а не водой из бассейна. Кислота, которую вы добавляете в воду, должна составлять около 10 процентов воды в ведре, что соответствует соотношению кислоты/воды 1/10.
Шаг 4. Включите свой бассейн
Убедитесь, что вы включили свой бассейн, прежде чем добавлять кислоту в воду. Вода должна быть проточной и полностью циркулирующей, прежде чем вы поместите кислоту в бассейн.
Шаг 5. Медленно добавьте кислоту в воду
Теперь пришло время, наконец, добавить кислоту в воду. Полученную смесь кислоты и воды следует распределить по периметру бассейна, что позволит ей правильно распределиться по всем частям бассейна. Убедитесь, что вы не входите в бассейн в течение как минимум 30 минут. Когда вы добавляете кислоту в воду, рекомендуется делать это очень медленно. Любые брызги могут вызвать ожог кожи, поэтому важны дополнительные меры предосторожности.
Шаг 6. Снова проверьте уровень pH
Теперь, когда вы добавили соляную кислоту в свой бассейн, пришло время снова проверить уровень pH. Имейте в виду, что это тестирование должно проводиться только по прошествии нескольких часов. В случае, если показания датчика все еще слишком высоки, вы можете добавить очень небольшое количество соляной кислоты в воду бассейна, пока не достигнете желаемого pH. Обязательно проводите повторное тестирование воды каждые 3-4 часа, пока не получите правильные показания pH, которые могут быть где-то в диапазоне 7,2-7,8.
Muriatic Acid и Соляная кислота и Серная кислота
Есть три очень распространенных типа кислоты, которые можно использовать в воде, включая Muriatic Acid, соляную кислоту и серную кислоту. Muriatic Acid и соляная кислота очень похожи по составу. В общем, Muriatic Acid представляет собой менее чистую форму соляной кислоты. Чтобы получить его эффективность, загрязняющие вещества добавляются непосредственно в соляную кислоту. Что касается соляной кислоты, она обычно используется в лабораториях. Поскольку Muriatic Acid не такая чистая, как соляная кислота, она также дешевле.
Если смотреть конкретно на серную кислоту, это форма кислоты, которую можно использовать вместе с соляной кислотой для снижения уровня pH воды в вашем бассейне. Тем не менее, соляная кислота дешевле и не имеет побочных эффектов, которые возникают при использовании серной кислоты. Хотя можно использовать серную кислоту для снижения уровня pH воды в бассейне, эта кислота сильнее и вреднее, чем соляная кислота. При использовании в воде бассейна серная кислота образует пары и может добавлять в воду все растворенные твердые вещества, что увеличивает вероятность коррозии. Вероятно, лучшим вариантом для снижения уровня pH воды в бассейне является соляная кислота.
Достигните идеального баланса pH с помощью соляной кислоты

При правильном использовании соляная кислота может снизить уровень pH воды в бассейне. Эффективность соляной кислоты делает ее полезной при избавлении от затвердевшей воды, которая стала слишком щелочной. Она также намного более доступна по сравнению с соляной кислотой, поэтому рекомендуется использовать его для очистки бассейнов.
Если вам нужна помощь в понимании правильного состава воды или в том, как проверить уровень pH, свяжитесь с МоемГород сегодня!
Таблицы DPVA.ru - Инженерный Справочник | Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Рабочие среды / / Хлороводород HCl, он же - Cоляная кислота. / / Химические, физические и тепловые свойства хлороводорода HCl (соляная кислота) Поделиться:
| ||||||||||||||||||||||||||||||||||||||||||||||
| Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. Вложите в письмо ссылку на страницу с ошибкой, пожалуйста. | |||||||||||||||||||||||||||||||||||||||||||||||
| Коды баннеров проекта DPVA.ru Начинка: KJR Publisiers Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | ||||||||||||||||||||||||||||||||||||||||||||||
Сообщите нам свой адрес электронной почты, чтобы подписаться на рассылку новостного бюллетеня. Предоставление адреса электронной почты является добровольным, но, если Вы этого не сделаете, мы не сможем отправить Вам информационный бюллетень. Администратором Ваших персональных данных является Акционерное Общество PCC Rokita, находящееся в Бжег-Дольном (ул. Сенкевича 4, 56-120 Бжег-Дольный, Польша ). Вы можете связаться с нашим инспектором по защите личных данных по электронной почте: .
Мы обрабатываем Ваши данные для того, чтобы отправить Вам информационный бюллетень - основанием для обработки является реализация нашей законодательно обоснованной заинтересованности или законодательно обоснованная заинтересованность третьей стороны – непосредственный маркетинг наших продуктов / продуктов группы PCC .
Как правило, Ваши данные мы будем обрабатывать до окончания нашего с Вами общения или же до момента, пока Вы не выразите свои возражения, либо если правовые нормы будут обязывать нас продолжать обработку этих данных, либо мы будем сохранять их дольше в случае потенциальных претензий, до истечения срока их хранения, регулируемого законом, в частности Гражданским кодексом.
В любое время Вы имеете право:
Получателями Ваших данных могут быть компании, которые поддерживают нас в общении с Вами и помогают нам в ведении веб-сайта, внешние консалтинговые компании (такие как юридические, маркетинговые и бухгалтерские) или внешние специалисты в области IT, включая компанию Группы PCC .
Больше о том, как мы обрабатываем Ваши данные Вы можете узнать из нашего Полиса конфиденциальности.
Люди с желудочными расстройствами, такими как изжога и кислотный рефлюкс, обычно думают, что страдают от избытка соляной кислоты. Мы начинаем принимать препараты, подавляющие его выработку, но проблема не решается, что еще хуже, через какое-то время прекратить прием препаратов становится практически невозможно. Начинают появляться дополнительные недомогания, связанные с дефицитом соляной кислоты.
К сожалению, фармацевтические препараты не могут вылечить изжогу или кислотный рефлюкс, они только маскируют симптомы.Речь идет об ингибиторах протонной помпы – препаратах, быстро убирающих изжогу или рефлюкс, но приводящих ко многим вредным эффектам при длительном приеме. Как можно уменьшить побочные эффекты? Ознакомьтесь с митохондриальным раствором. Но давайте начнем с самого начала.
Желудочная кислота необходима для правильного пищеварения и усвоения питательных веществ, а также является неотъемлемой частью нашей иммунной системы.Это первая линия защиты от потенциально вредных бактерий и паразитов.
Соляная кислота – природный стимулятор пищеварительных процессов.
Если в желудке слишком мало кислоты, возрастает опасность недостаточного пищеварения и, следовательно, нехватки питательных веществ и витаминов. Поэтому соляная кислота очень важна не только для пищеварительной системы, но и для здоровья всего организма.
Соляная кислота, хотя и выделяется только в желудке, необходима для всего процесса пищеварения. Гипохлоргидрия, или дефицит соляной кислоты, может иметь множество причин:
У здоровых людей в клетках слизистой оболочки желудка работают протонные помпы, которые переносят протоны в желудочный сок, поддерживая его нормальный рН.
Использование ингибиторов протонной помпы (препаратов, таких как омепразол или пантопразол) или антацидов рекомендуется при традиционном лечении изжоги и кислотного рефлюкса. Антациды представляют собой соли, нейтрализующие желудочную кислоту, тогда как ингибиторы протонной помпы (ИПП) деактивируют протонную помпу и предотвращают образование соляной кислоты в клетках желудка.Что еще хуже, эти фармацевтические препараты наносят вред митохондриям, поскольку они также повреждают насосы, присутствующие в митохондриях. Поэтому эти препараты не подходят для длительной терапии, так как неизбежно приводят к дальнейшим проблемам со здоровьем.
Некоторых удивляет, что дефицит кислоты в желудке может привести к кислотному рефлюксу. Гипохлоргидрия способствует недостаточному усвоению белков и углеводов. Неразложившаяся пища, попав в кишечник, меняет в нем рН, поэтому ферменты не выделяются должным образом.Непереваренные углеводы создают газы, которые повышают давление, вызывая даже открытие сфинктера желудка и рефлюкс.
Что еще хуже, слишком мало кислоты в желудке препятствует усвоению важных питательных веществ из пищи: магния, кальция, цинка, железа, фолиевой кислоты и витаминов B12, C и D 2-4 . Следствием этого являются многочисленные недостатки, несмотря на правильное питание, что увеличивает проблемы с митохондриями. Кроме того, уменьшенное количество соляной кислоты подвергает вас риску бактериальных инфекций.Непереваренная пища способствует росту бактерий и может привести к скрытому воспалению.
В отличие от антацидов, действующих непосредственно в желудке, ИПП вмешиваются в метаболизм клеток слизистой оболочки желудка. Таким образом, они также нарушают производство так называемого внутренний фактор IF (фактор Кастля). Это небольшое количество белка необходимо для усвоения витамина B12 из пищи.Если клетки блокируются лекарствами, они не производят достаточно внутреннего фактора. Витамин В12 из пищи не усваивается и находится в дефиците.
В 2013 году было опубликовано исследование влияния ИПП на формирование дефицита витамина B12. В исследовании приняли участие 26 000 пациентов, у которых был диагностирован дефицит витамина B12 в период с 1997 по 2011 год, по сравнению с более чем 180 000 человек, у которых не было дефицита витамина B12 5 . Они обнаружили, что в группе людей с дефицитом витамина B12 было значительно больше пациентов, принимавших ИПП или антагонисты h3-рецепторов (антигистаминные препараты, подавляющие секрецию желудочного сока).Дефицит витамина B12 был на 65% выше у людей, принимавших ИПП.
Кроме того, чем выше доза ИПП, тем выше риск дефицита. Например, у пациентов, принимавших более 1,5 таблеток в день, дефицит витамина B12 был в два раза выше. Однако у тех, кто принимал только одну таблетку в день, риск не был столь высоким, но все же риск был намного выше, чем у тех, кто не принимал свои лекарства.
1.Как это ни парадоксально, желудочно-кишечный дискомфорт является одним из наиболее частых побочных эффектов ИПП. Они устраняют проблему изжоги, но на их место приходят новые: головные боли, нарушения сна, утомляемость, пищеварительный дискомфорт, метеоризм, нарушения всасывания.
2. ИПП может способствовать развитию пищевой аллергии. Если в желудке вырабатывается слишком мало кислоты, пища плохо переваривается. Это, в свою очередь, увеличивает риск попадания непереваренных белковых частиц (которые могут действовать как аллергены) в кровоток через слизистую оболочку кишечника.Там организм защищается от них, вырабатывая против них антитела. Когда аллергены (непереваренные частицы) снова попадают в кровь, возникает аллергическая реакция.
3. Кроме того, ИПП подавляют всасывание железа, магния и кальция, что приводит к анемии или потере костной массы, остеопорозу (и всем другим последствиям дефицита минералов).
4. Если выработка желудочной кислоты снижается лекарственными препаратами, это приводит, как упоминалось в начале, к недостаточной иммунной защите желудка.В результате никого не должно удивлять, что люди, принимающие ИПП, гораздо более восприимчивы к бактериальным кишечным инфекциям (например, Helicobacter pylori, сальмонеллезным инфекциям), чем люди, не принимающие ИПП.
5. Поскольку париетальные клетки продуцируют внутренний фактор всасывания витамина B12, очевидно, что ингибирование их действия ИПП может привести к дефициту внутреннего фактора, за которым следует дефицит витамина B12.
Гастрина – это гормон, выделяемый клетками желудка, который стимулирует секрецию желудочного сока.Слишком много гастрина может вызвать стойкую повышенную кислотность, которая повреждает слизистую оболочку желудка, а также образование язв. Его повышенный уровень опасен и увеличивает риск нейроэндокринных клеток и опухолей.
Когда стоит проверять уровень гастрина:
Тест следует проводить натощак, материал - сыворотка, результат не должен превышать 90 нг/л.
Ингибиторы протонной помпы повышают риск злокачественных новообразований желудка и нейроэндокринной системы. В далеко зашедших стадиях желудочных заболеваний стоит исследовать уровень нейрональной енолазы – это показатель нейроэндокринных новообразований, возникающих в цитоплазме клеток. Может быть маркером рака желудка. Проводим тест с сывороткой, норматив ниже 6 мкг/л.
У людей, у которых изжога сохраняется, несмотря на прием витамина В12, следует определить уровень хромогранина А (CgA) – еще одного гормона, являющегося маркером нейроэндокринных новообразований.Материал сыворотки - референсный диапазон: 19-100 нг/мл.
К сожалению, чем больше времени требуется на прием ИПП, тем труднее их отложить. Поэтому не прекращайте их использование на ночь, а только после консультации с врачом. Существует множество стратегий безопасного и постепенного отказа от этих препаратов, например, путем замены их соляной кислотой и соответствующей терапией витамином B12.При использовании ИПП может потребоваться парентеральное введение витамина В12. Такая терапия может длиться до нескольких недель, но без побочных эффектов и приводит к полному выздоровлению.
Натуральные средства: магний, кальций, железо, цинк, витамины: B12, C, D3 и полезные бактериальные культуры могут помочь вам восстановить правильную секрецию соляной кислоты и устранить негативные побочные эффекты ИПП.
Одним из наиболее эффективных витаминов для борьбы со стрессом нитрозирования является витамин B12.Его уровень может быть снижен у людей, принимающих ингибиторы протонной помпы и блокаторы соляной кислоты и имеющих нарушения всасывания. Железо, цинк, кальций и витамин D3 также являются ингредиентами, которых часто не хватает людям, принимающим препараты ИПП. Кроме того, хорошо подействуют витамин С, который поддерживает выработку соляной кислоты, и пробиотики, поддерживающие правильное функционирование кишечника и усвоение питательных веществ. В свою очередь микроэлементы, такие как магний и калий, обеспечивают электролитный баланс.
Дополнение этих ингредиентов предотвращает дефицит, связанный с использованием ингибиторов протонной помпы, и помогает устранить последствия окислительного и нитрозативного стресса, восстанавливая нормальные механизмы в клетках желудка.
Паулина Журек
Презентация
.Химические ожоги глаз — неотложное состояние, требующее немедленных действий. Их выраженность зависит от вида действующего вещества, его рН и концентрации, а также способности проникать вглубь тканей и длительности его контакта с поверхностью глаза. Чем более щелочным или более кислым является средство, тем большего ущерба можно ожидать.
Основания особенно опасны, потому что они легче проникают в ткани. Основания обладают высоким сродством к жирам, они омыляют жирные кислоты клеточных мембран, вызывая разрушение и гибель клеток. Кроме того, ион гидроксида разрушает межклеточные структуры коллагена. Поврежденные ткани вызывают воспалительную реакцию, которая сочетается с выделением протеолитических ферментов. В совокупности он вызывает дренажный некроз, который быстро (в течение 5–15 минут) распространяется на глубокие структуры глазного яблока.Следствием ожогов глазной поверхности основаниями также может быть повышение внутриглазного давления и развитие катаракты.
Кислоты денатурируют белки поверхностных слоев роговицы, что ограничивает их проникновение в ткани, но тем не менее повреждают роговицу, что также может вызвать слепоту. Исключение составляет слабая плавиковая кислота, которая быстро проникает через клеточные мембраны и, действуя подобно сильным основаниям, вызывает распространенный некроз. Кроме того, ионы фтора, выделяющиеся внутрь клеток, нарушают действие гликолитических ферментов и образуют нерастворимые связи в связи с кальцием и магнием.Эти ожоги особенно болезненны и, если они не ограничиваются глазами, могут быть связаны с тяжелой гипокальциемией.
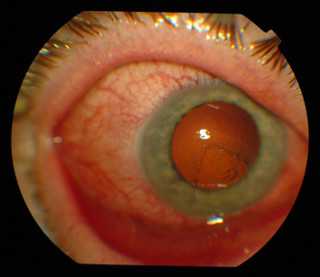
Следующую группу составляют раздражающие соединения, которые, однако, обычно имеют нейтральный pH и хотя их действие очень неприятно, они не вызывают необратимых повреждений.
Большинство химических ожогов глаз происходит на промышленных и ремесленных предприятиях, а также в домашних условиях.Наиболее распространенными щелочными веществами являются гидроксид аммония, то есть аммиак, щелочи, гидроксид калия, магний, оксид и гидроксид кальция. Они содержатся в таких продуктах, как удобрения для растений, чистящие средства (аммиак), средства для очистки канализации (щелочи), средства для чистки духовок и средства для удаления сильных загрязнений, а также в гипсе, гипсе и бетоне.Относительно распространенными кислотами являются серная, сернистая, соляная, азотная, уксусная, хромовая и плавиковая. Последний входит в состав многих полировальных веществ.Одной из причин ожогов является взрыв автомобильного аккумулятора с серной кислотой. Уксусная кислота присутствует в уксусах, а также в жидкости для снятия лака.
К раздражителям также относятся бытовые моющие средства и репелленты, содержащие перцовую кислоту.
Ожоги глаз составляют 7–18% травм, леченных в отделениях неотложной помощи больниц. Более 80% из них составляют химические ожоги. Кислотные ожоги почти так же распространены, как и щелочные.
Ранние симптомы ожога глаза включают боль, покраснение, ощущение инородного тела, слезотечение, трудности с удержанием век открытыми, отек и нечеткость зрения. В случае особо тяжелых химических ожогов, когда возникает выраженная ишемия и быстрый некроз тканей, вместо покраснения обожженный глаз может стать совсем бледным, конъюнктива может напоминать «рыбье мясо», а роговица - «фарфор».
Если предполагается, что глаз подвергся воздействию химических веществ, не относитесь к этому легкомысленно и не думайте, что это «пройдет само».
Самое главное знать или подозревать, что химическое вещество попало в глаза. Важно начать лечение сразу после события, а не откладывать его до медицинского осмотра, ведь дорога каждая минута. Специализированное обследование заключается в осмотре глаза (например, в щелевой лампе) и, в частности, рН-тест на поверхности глазного яблока.
Самое главное быстро вымыть раздражитель из конъюнктивального мешка.Лучшим решением является буферный раствор Рингера (мультиэлектролитная жидкость). Если он недоступен, используется изотонический раствор (0,9% NaCl). Однако, если он не доступен немедленно, промойте чистой (питьевой) холодной водой как можно скорее. Струю жидкости следует направить к медиальному углу глаза так, чтобы вытекающая жидкость не попала на другой глаз, и промыть осторожной струей большого количества жидкости. Душ может быть отличным вариантом, даже не снимая одежду.Можно также аккуратно побрызгать глаз из открытой бутылочки и, в крайнем случае, окунуть лицо больного в миску с водой. Минимальное время промывания глаз составляет 5 минут, но чем дольше промывание, тем лучше. Если в глаз попали твердые частицы, необходимо вывернуть веко и удалить их промыванием или смоченным ватным тампоном. Промывание в течение не менее 20 минут требуется перед транспортировкой в больницу и продолжается во время транспортировки. Транспортировка в специализированный центр без предварительной промывки является ошибкой.
Не следует также забывать, что химический ожог лица, особенно щелочью, может быть связан с ожогом трахеи и пищевода и тогда, как всегда, в первую очередь необходимо оценить дыхание.
Дальнейшее специализированное лечение зависит от степени поражения глазного яблока и включает продолжение промывания глаз, контроль рН, снижение внутриглазного давления, противовоспалительное лечение и профилактику бактериальной суперинфекции. Лечение может потребовать хирургического вмешательства, включая реконструкцию поверхности глаза, трансплантацию роговицы и конъюнктивы, инокуляцию амниотической мембраны и удаление спаек конъюнктивы.
При незначительных поверхностных ожогах прогноз благоприятный, если стук начинается немедленно. При тяжелых ожогах, особенно при задержке промывания, прогноз для сохранения зрения серьезный. У 1/3 обожженных может быть инвалидность, а у ~15% риск слепоты.
После завершения лечения вы должны регулярно посещать специалиста, так как некоторые последствия химических ожогов глаз могут быть отсрочены.
Около 90% химических ожогов глаз можно избежать, если принять надлежащие меры предосторожности. К ним, в первую очередь, относится ношение защитных очков при работе с опасными веществами. Важно держать жидкости, содержащие такие вещества, в пределах досягаемости, не снимая их с высоких полок, иначе они могут опрокинуться. Контейнеры должны быть тщательно закрыты. Помните, что вы можете обжечь глаза при использовании многих домашних средств.Крайне важно защитить их от доступа детей, а детей следует предупреждать об опасностях с раннего возраста.
.  Каждый из нас знает, какой на вкус кислый апельсиновый или лимонный сок. Термин кислый относится к вкусам в повседневной жизни, но имеет и другое значение. В химии кислым раствором считается раствор с низким pH. Существуют также некоторые щелочные растворы с высоким pH.
Каждый из нас знает, какой на вкус кислый апельсиновый или лимонный сок. Термин кислый относится к вкусам в повседневной жизни, но имеет и другое значение. В химии кислым раствором считается раствор с низким pH. Существуют также некоторые щелочные растворы с высоким pH.
Шкала рН позволяет количественно (числово) определить кислотность и щелочность водных растворов. Например, апельсиновый сок имеет pH 3,5, а более кислый лимонный сок имеет pH 2,4.Чем кислее что-то, тем ниже у него pH.
Значение pH может быть от 0 до 14. Ноль — это очень сильная кислота (например, очень агрессивная соляная кислота), а 14 — очень сильное основание (например, гидроксид натрия). Наше тело в значительной степени состоит из воды, рН которой не является ни кислым, ни щелочным — он находится в середине шкалы на уровне 7. Конечно, это не означает, что все части нашего тела имеют одинаковый рН. В желудке есть кислоты с pH всего около 2, в то время как кровь слабощелочная с pH около 7,4.
У большинства людей кислота ассоциируется с чем-то опасным. Однако не все осознают, что сильные принципы не менее, а то и более опасны для человека. Например, концентрированный раствор гидроксида натрия (щелочь) вызывает коррозию и чрезвычайно опасен.
Физические законы измерения pH сложны, но измерение pH очень просто. Одним из инструментов для измерения pH являются лакмусовые бумажки, которые меняют свой цвет при воздействии кислоты или щелочи.Они становятся более красными для кислот и синими для оснований. Вы можете проверить это по шкале pH, прилагаемой к набору Invisibility.
. Номера ООН опасных веществ
|
| | |
| л.с. в IBB | |
| | |
| Паспорта безопасности материалов: | |
| КАРТОЧКИ являются основным источником информации об опасных свойствах химических веществ, видах и размерах их опасности для человека и окружающей среды, а также о принципах и рекомендациях по их безопасному использованию.ПАСПОРТ БЕЗОПАСНОСТИ предназначен в первую очередь для профессиональных пользователей, чтобы дать им возможность принимать необходимые меры на рабочем месте для обеспечения безопасности и защиты здоровья человека и окружающей среды. Применение опасных веществ и препаратов в профессиональной деятельности без наличия паспорта безопасности недопустимо! Его свойства определяют, является ли данное вещество или препарат опасным.Перечень опасных веществ с их классификацией и маркировкой можно найти в приложении к Постановлению министра здравоохранения от 28 сентября 2005 г. о перечне опасных веществ с их классификацией и маркировкой, а для препаратов необходимо проводить такие классификация (Приказ министра здравоохранения от 2 сентября 2003 г. о критериях и методах классификации химических веществ и препаратов). | |
| | |
| 3-аминотриазол (pdf 127kB) | |
| 3-амино-5-меркаптотриазол (pdf 125kB) | |
| 5-азацитидин (pdf 190kB) | |
| AZTTP (3-азидо-3-дезокситимидин) (pdf 163kB) | |
| ацетон (pdf 53kB) | |
| ацетонитрил (pdf 54kB) | |
| ацетонитрил для синтеза ДНК (pdf 31kB) | |
| Ацетосирингон (АС) (pdf 136kB) | |
| ацетилхлорид (pdf 143kB) | |
| акриламид (pdf 54kB) | |
| акриламид: N, N-метилбисакриламид (24 к 1) (pdf 54kB) | |
| хлоруксусный альдегид (pdf 158kB) | |
| Амфотерицин В (Фунгизон) (pdf 125kB) | |
| аммиак (pdf 54kB) | |
| хлорид аммония (pdf 54kB) | |
| персульфат аммония (pdf 22kB) | |
| ампициллин (pdf 127kB) | |
| амиламин (pdf 149kB) | |
| Антимицин А (pdf 147kB) | |
| Нитрат аммония (pdf 136kB) | |
| нитрат лантана (pdf 55kB) | |
| нитрат свинца (pdf 138kB) | |
| нитрат калия (pdf 145kB) | |
| нитрат серебра (pdf 334kB) | |
| нитрат кальция (pdf 136kB) | |
| APS (персульфат аммония) (pdf 125kB) | |
| BCP (1-бром-3-хлорпропан) (pdf 140kB) | |
| BNT (2-бром-6-нитротолуол) (pdf 130kB) | |
| беномил (pdf 194kB) | |
| бензол (pdf 265kB) | |
| блеомицин (флеомицин) (pdf 145kB) | |
| бура (pdf 138kB) | |
| Реагент Брэдфорда (pdf, 142 КБ) | |
| бензилбромид (pdf 125kB) | |
| этидий бромид (pdf 21kB) | |
| бромид меди (pdf 127kB) | |
| цианоген бромид (pdf 142kB) | |
| Calcofluor White (pdf 139kB) | |
| CCCP (pdf 141kB) | |
| хлоралгидрат (pdf 54kB) | |
| хлорамфеникол (pdf 53kB) | |
| тетраметиламмония хлорид (pdf 130kB) | |
| хлорид олова (pdf 130kB) | |
| хлорид марганца (pdf 127kB) | |
| Мезилхлорид (pdf 140kB) | |
| пиридинхлорхромат (pdf 139kB) | |
| хлорфенилаланин (pdf 140kB) | |
| хлороформ (pdf 53kB) | |
| бензамидина гидрохлорид (pdf 131kB) | |
| гуанидина гидрохлорид (pdf 138kB) | |
| хромянка (pdf 54kB) | |
| Оксид хрома (pdf 56kB) | |
| конканавалина А (pdf 131kB) | |
| Красный Конго (pdf 130kB) | |
| CPT (камптотецин) (pdf 152kB) | |
| циклогексимид (pdf 130kB) | |
| циклогексан (pdf 56kB) | |
| Циклопентан (pdf 130kB) | |
| цинк (цинковая пыль) (pdf 333kB) | |
| цитохалазин E (pdf 145kB) | |
| DAB (диаминобензидин) (pdf 140kB) | |
| DAPI (4', 6-диамидино-2-фенилиндола дигидрохлорид) (pdf 137kB) | |
| DAST (трифторид диэтиламиносеры) (pdf 22kB) | |
| ДБУ (1,8-диазабицикло(5.4.0) UNDEC-7-ENE (1,5-5) (pdf 143kB) | |
| DEPC (ROTH) (pdf 54kB) | |
| DEPC (Sigma) (pdf 54kB) | |
| ДИК (N, N'-диизопропилкарбодиимид) (pdf 127kB) | |
| дихромат калия (pdf 57kB) | |
| 1,3-дихлорацетон (pdf 150kB) | |
| 1,2-дихлорбензол (pdf 133kB) | |
| 2,4-дихлорфенол (pdf 133kB) | |
| дихлорметан (метиленхлорид) (pdf 54kB) | |
| дигитонин (pdf 122kB) | |
| диоксан (pdf 54kB) | |
| ДМАП (4-диметиламинопиридин).pdf (pdf 20kB) | |
| ДМЭ (1,2-диметоксиэтан) (pdf 159kB) | |
| ДМФА (N, N-диметилформамид) (pdf 54kB) | |
| ДМС (диметилсульфат) (pdf 54kB) | |
| DOX (доксорубицин гидрохлорид) (pdf 122kB) | |
| DTNB (реагент Эллманса) (pdf 122kB) | |
| DTSP (реагент Ломанца) (pdf 125kB) | |
| ДТТ (дитиотреитол) (pdf 122kB) | |
| EDAC (pdf 120kB) | |
| этанол 96% (pdf 53kB) | |
| этанол 99.8% (pdf 53kB) | |
| этаноламин (pdf 55kB) | |
| диэтиловый эфир (pdf 56kB) | |
| петролейный эфир (pdf 56kB) | |
| этионин (pdf 165kB) | |
| этилацетат (pdf 56kB) | |
| фенол (pdf 54kB) | |
| фенилендиамин (pdf 54kB) | |
| 5-фторурацил (pdf 237kB) | |
| формальдегид 40% (pdf 53kB) | |
| формамид (pdf 53kB) | |
| пикоксид фосфора (pdf 55kB) | |
| Гентамицин (pdf 122kB) | |
| глицидол (pdf 171kB) | |
| глутаровый альдегид (pdf 140kB) | |
| гексан (pdf 55kB) | |
| HNE (4-гидрокси-2-ноненаль) (pdf 144kB) | |
| гептан (pdf 56kB) | |
| Гигромицин B (pdf 143kB) | |
| гидрохинон (pdf 135kB) | |
| 8-гидроксихинолин (pdf 52kB) | |
| гидроксимочевина (pdf 122kB) | |
| имидазол (pdf 127kB) | |
| IPTG (изопропил-бета-D-тиогалактопиранозид) (pdf 177kB) | |
| ISOPAC (N-нитрозо-N-метилмочевина) (pdf 194kB) | |
| изоамиловый спирт (pdf 53kB) | |
| йодацетамид (pdf 122kB) | |
| йодистый метил (pdf 168kB) | |
| йодид пропидия (pdf 120kB) | |
| хлорид йода (pdf 140kB) | |
| йод (pdf 133kB) | |
| Кадмий хлорид 2,5 гидрат (pdf 54kB) | |
| Ацетат кадмия (pdf 141kB) | |
| Кобальт хлорид (pdf 29kB) | |
| ксилол (pdf 55kB) | |
| Канаван (pdf 127kB) | |
| аминогексаоновая кислота (pdf 120kB) | |
| акриловая кислота (pdf 135kB) | |
| антраниловая кислота (pdf 149kB) | |
| аристохолевая кислота и ее соли (pdf 140kB) | |
| азотная кислота (pdf 55kB) | |
| бензойная кислота (pdf 54kB) | |
| Бромуксусная кислота (pdf 149kB) | |
| Бромпировиноградная кислота (pdf 127kB) | |
| коричная кислота (pdf 125kB) | |
| лимонная кислота (pdf 55kB) | |
| фталевая кислота (pdf 125kB) | |
| 5-фтороротовая кислота (pdf 125kB) | |
| Фосфоноуксусная кислота (pdf 125kB) | |
| гентизиновая кислота (DHB) (pdf 125kB) | |
| яблочная кислота (pdf 125kB) | |
| 3-йодпропионовая кислота (pdf 125kB) | |
| п-кумаровая кислота (pdf 120kB) | |
| малеиновая кислота (pdf 146kB) | |
| молочная кислота (pdf 54kB) | |
| Муравьиная кислота (pdf 55kB) | |
| хлорная кислота 60% (pdf 55kB) | |
| нафталин уксусная кислота (NAA) (pdf 125kB) | |
| налидиксовая кислота (pdf 191kB) | |
| никотиновая кислота (pdf 125kB) | |
| нитрилотриуксусная кислота (NTA) (pdf 125kB) | |
| уксусная кислота ледяная (pdf 53kB) | |
| пиколиновая кислота (pdf 125kB) | |
| ретиноевая кислота (pdf 120kB) | |
| ортофосфорная кислота (pdf 333kB) | |
| серная кислота (pdf 54kB) | |
| соляная кислота (pdf 53kB) | |
| толуиловая кислота (pdf 131kB) | |
| трифторуксусная кислота (TFA) (pdf 22kB) | |
| трихлоруксусная кислота (TCA) (pdf 55kB) | |
| LAH (тетрагидроалюминат лития) (pdf 151kB) | |
| N-лауроилсаркозин (pdf 125kB) | |
| лептомицин B (pdf 151kB) | |
| хлорид лития (pdf 52kB) | |
| люминол (pdf 120kB) | |
| сульфат марганца (pdf 333kB) | |
| МБТ (2-меркаптобензотиазол) (pdf 159kB) | |
| меркаптоэтанол (pdf 157kB) | |
| метанол (pdf 54kB) | |
| МЕСНА (pdf 140kB) | |
| митомицин С (pdf 138kB) | |
| MMS (метилметансульфонат) (pdf 301kB) | |
| MNNG (1-метил-3-нитро-1-нитрозогуанидин) (pdf 274kB) | |
| MPD (гексиленгликоль) (pdf 150kB) | |
| Смесь базальных солей Мурасиге и Скуга (pdf 138kB) | |
| нафталин (pdf 135kB) | |
| NBT (нитросиний тетразолий) (pdf 134kB) | |
| NMP (1-метил-2-пирролидинон) (pdf 125kB) | |
| нитрат никеля (pdf 55kB) | |
| Хлорид никеля (pdf 54kB) | |
| сульфат никеля (pdf 55kB) | |
| Nonidet (4-нонилфенил-полиэтиленгликоль) (pdf 127kB) | |
| 1-октен-3-ол (спирт S-мацутаке) (pdf 20kB) | |
| олигомицин А (pdf 125kB) | |
| ONCB (1-хлор-2-нитробензол) (pdf 141kB) | |
| ацетат свинца (pdf 150kB) | |
| параформальдегид (pdf 122kB) | |
| Pefabloc (pdf 122kB) | |
| пиридин (pdf 174kB) | |
| пиперидин (pdf 55kB) | |
| пирокатехол (pdf 171kB) | |
| POPOP (pdf 125kB) | |
| калий (металл, каваки) (pdf 144kB) | |
| цианид калия (pdf 133kB) | |
| Фторид калия (pdf 149kB) | |
| перманганат калия (pdf 156kB) | |
| пропанол (pdf 55kB) | |
| Протеиназа К (pdf 138kB) | |
| PMSF (фенилметилсульфонилфторид) (pdf 144kB) | |
| резорцин (pdf 133kB) | |
| рифампицин (pdf 122kB) | |
| SDS (pdf 53 КБ) | |
| арсенат натрия (V) (pdf 133kB) | |
| Азид натрия (pdf 56kB) | |
| Боргидрид натрия (pdf 154kB) | |
| дезоксихолат натрия (pdf 120kB) | |
| фторид натрия (pdf 54kB) | |
| Какодилат натрия (pdf 130kB) | |
| перхлорат натрия (pdf 137kB) | |
| гипохлорит натрия (pdf 54kB) | |
| Селенат натрия (pdf 55kB) | |
| Селенит натрия (pdf 186kB) | |
| сульфид натрия 9 гидрат (pdf 53kB) | |
| Ванадат натрия (pdf 125kB) | |
| Гидрид натрия (pdf 142kB) | |
| бисульфит натрия (pdf 54kB) | |
| гидроксид натрия (pdf 53kB) | |
| спермидин (pdf 122kB) | |
| спермина (pdf 125kB) | |
| Стеринол (pdf 332kB) | |
| TCEP (pdf 122kB) | |
| тетрациклин (pdf 125kB) | |
| тетрабутилацетат (pdf 148kB) | |
| трет-бутилдиметилсилилхлорид (pdf 142kB) | |
| тионилхлорид (pdf 122kB) | |
| ТГФ (тетрагидрофуран) (pdf 162kB) | |
| Тетразолий красный (TTC) (pdf 120kB) | |
| Тетразол-ацетонитрил (pdf 149kB) | |
| TEMED (N, N, N', N'-тетраметилэтилендиамин) (pdf 125kB) | |
| толуол (pdf 54kB) | |
| трихлорэтилен (ТХЭ) (pdf 204kB) | |
| триэтиламин (N, N-диэтилэтанамин) (pdf 31kB) | |
| TMB (pdf 153kB) | |
| ТМФ (триметилфосфат) (pdf 125kB) | |
| Реагент TRI (pdf, 150 КБ) | |
| Triton X-100 (pdf 125kB) | |
| TRIZMA BASE (pdf 137kB) | |
| Трипановый синий (Direct Blue 14) (pdf 215kB) | |
| туникамицин (pdf 127kB) | |
| уранилацетат (pdf 161kB) | |
| гипохлорит кальция (pdf 55kB) | |
| винилхлорид (pdf 200kB) | |
| винилцианид (акрилонитрил) (pdf 138kB) | |
| винилацетат (pdf 133kB) | |
| перекись водорода (перекись водорода) (pdf 55kB) | |
| Ксилолцианол (pdf 17kB) | |
| хлорид железа (II) (pdf 141kB) | |
| хлорид железа (III) (pdf 55kB) | |
| сульфат железа (II) (pdf 120kB) | |
| железный порошок (pdf 148kB) | |
| | |
| Другие ПАСПОРТ БЕЗОПАСНОСТИ можно найти на страницах: | |
ПОЧ | |
МЕРК | |
SIGMA-Aldrich Польша | |
| | |
| | |
| | |
| | |