2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Лактобактерии, ДНК Lactobacillus spp., качественный — определение ДНК Lactobacillus spp. в соскобе урогенитального тракта, методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени».
Метод ПЦР — позволяет идентифицировать в биологическом материале искомый участок генетического материала и обнаружить единичные молекулы ДНК микроорганзма, не выявляемые другими методами. Принцип метода основан на многократном увеличении числа копий специфичного для данного возбудителя участка ДНК.
С помощью ПЦР-анализа можно диагностировать инфекцию в остром периоде и выявлять случаи носительства.
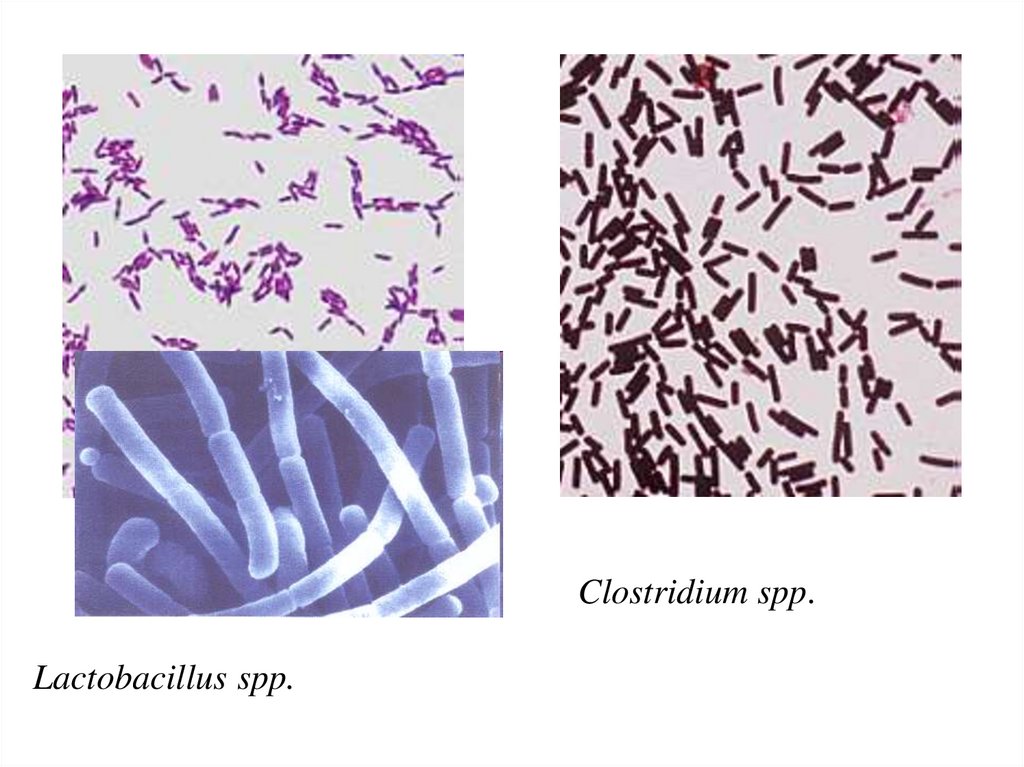
Лактобактерии — род грамположительных анаэробных неспорообразующих молочнокислых бактерий, которые являются представителями облигатного (который не могут существовать вовне) бактериоценоза здорового человека. На лактобактерии приходится около 10% нормофлоры.
Они доминируют у детей раннего возраста.
У женщин репродуктивного возраста нормофлора влагалища представлена преимущественно 5–6 видами Lactobacillus spp., которые составляют основу микробиоценоза.
Количество лактобацилл во влагалище здоровой женщины варьирует от 10*5 до 10*9 КОЕ/мл, что составляет от 90 до 99,9% всей микрофлоры влагалища.
Лактобактерии оказывают существенное влияние на процессы обмена веществ, обеспечивают организм человека витаминами группы В, С, К, никотиновой и фолиевой кислотами, биотином, вырабатывают аминокислоты, молочную, уксусную и другие органические кислоты, антибиотико- и гормоноподобные вещества, перекись водорода, L. fermentum № 90T-C4 продуцирует эндогенный лизоцим.
Дисбиоз влагалища
Выраженный дисбиоз влагалища (нарушение нормальной микрофлоры влагалища) — состояние микробиоценоза, характеризующееся значительным снижением доли лактобактерий (менее 20% от всех выделенных микроорганизмов) или полных их отсутствием.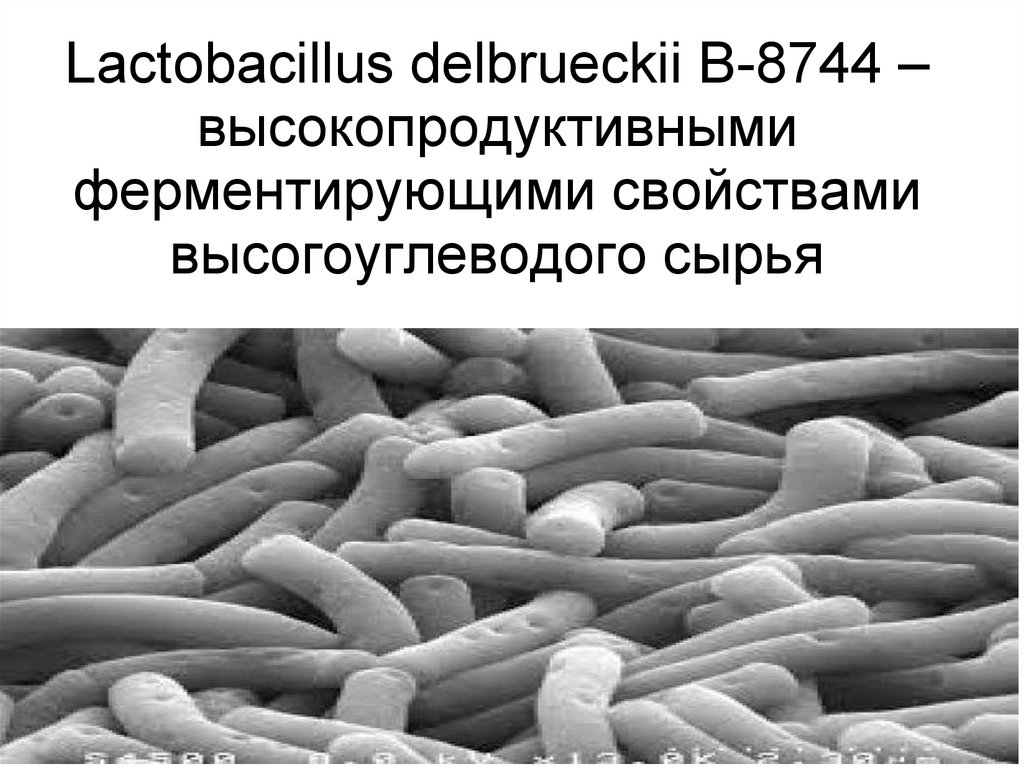 Выявление низкого содержания лактобактерий само по себе не является основанием для заключения о наличии какого-либо заболевания, ассоциированного с нарушением состава микрофлоры, однако указывает на его высокую вероятность и требует подтверждения, основанного на результатах анализа клинических данных и/или выявления условно-патогенных бактерий в концентрации, имеющей диагностическую значимость.
Выявление низкого содержания лактобактерий само по себе не является основанием для заключения о наличии какого-либо заболевания, ассоциированного с нарушением состава микрофлоры, однако указывает на его высокую вероятность и требует подтверждения, основанного на результатах анализа клинических данных и/или выявления условно-патогенных бактерий в концентрации, имеющей диагностическую значимость.
Показания:
Подготовка
Обсемененность и видовой состав исследуемого биотопа урогенитального тракта женщины зависит от фазы менструального цикла.
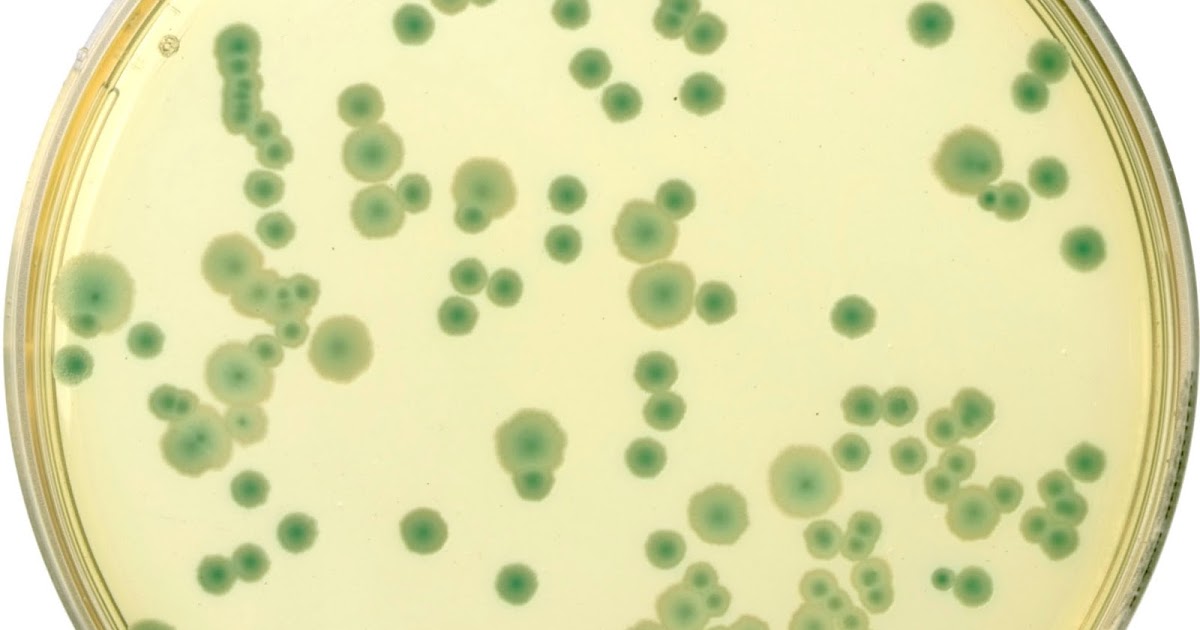
Интерпретация результатов
Ответ выдается в качественном формате: «обнаружено» или «не обнаружено».
Лактобактерии, ДНК Lactobacillus spp., количественный — количественное определение ДНК Lactobacillus spp. в соскобе урогенитального тракта, методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени».
Метод ПЦР позволяет идентифицировать в биологическом материале искомый участок генетического материала и обнаружить единичные молекулы ДНК микроорганизма, не выявляемые другими методами. Принцип метода основан на многократном увеличении числа копий, специфичных для данного возбудителя участка ДНК.
С помощью ПЦР-анализа можно диагностировать инфекцию в остром периоде и выявлять случаи носительства.
Лактобактерии — род грамположительных анаэробных неспорообразующих молочнокислых бактерий, которые являются представителями облигатного (которые не могут существовать вовне) бактериоценоза здорового человека.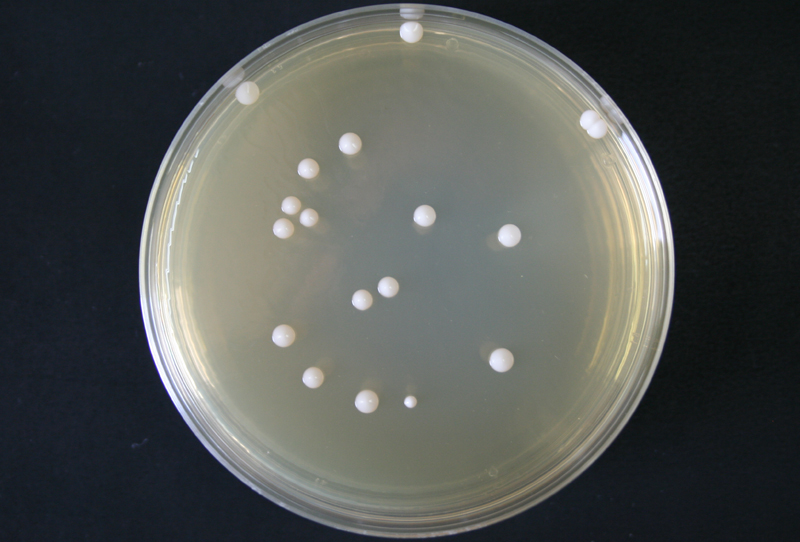 9 КОЕ/мл, что составляет от 90 до 99,9% всей микрофлоры влагалища.
9 КОЕ/мл, что составляет от 90 до 99,9% всей микрофлоры влагалища.
Лактобактерии оказывают существенное влияние на процессы обмена веществ, обеспечивают организм человека витаминами группы В, С, К, никотиновой и фолиевой кислотами, биотином, вырабатывают аминокислоты, молочную, уксусную и другие органические кислоты, антибиотико- и гормоноподобные вещества, перекись водорода, L. fermentum № 90T-C4 продуцирует эндогенный лизоцим.
Дисбиоз влагалища
Выраженный дисбиоз влагалища (нарушение нормальной микрофлоры влагалища) — состояние микробиоценоза, характеризующееся значительным снижением доли лактобактерий (менее 20% от всех выделенных микроорганизмов) или полных их отсутствием. Выявление низкого содержания лактобактерий само по себе не является основанием для заключения о наличии какого-либо заболевания, ассоциированного с нарушением состава микрофлоры, однако указывает на его высокую вероятность и требует подтверждения, основанного на результатах анализа клинических данных и/или выявления условно-патогенных бактерий в концентрации, имеющей диагностическую значимость.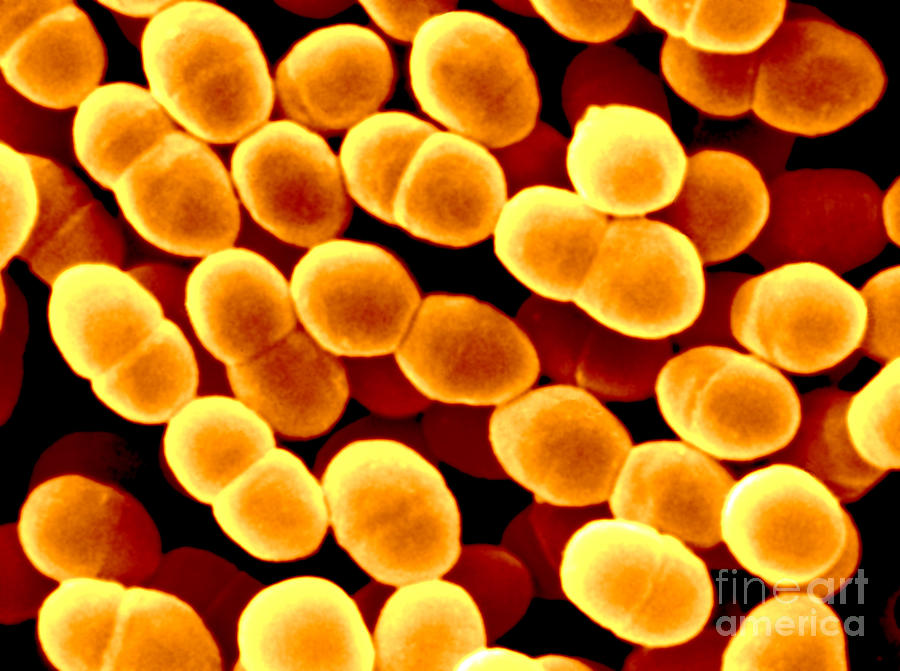
Показания:
Подготовка
Обсеменённость и видовой состав исследуемого биотопа урогенитального тракта женщины зависит от фазы менструального цикла.
Обследование женщин целесообразно проводить в первую половину менструального цикла, не ранее 5-ого дня. Допустимо обследование во второй половине цикла, не позднее, чем за 5 дней до предполагаемого начала менструации.
При наличии выраженных симптомов воспаления, взятие материала проводится в день обращения.
Накануне и в день обследования пациентке не рекомендуется выполнять спринцевание влагалища.
Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии (общей/местной), применения пробиотиков и эубиотиков, ранее 24–48 часов после полового контакта, интравагинального УЗИ и кольпоскопии.
Если для исследования берут соскоб из уретры, сбор материала проводят до или не ранее 2–3 часов после мочеиспускания.
Эякулят и секрет простаты
Пациент самостоятельно собирает в контейнер эякулят. Сбор секрета простаты выполняется подготовленным медицинским персоналом. Контейнер для сбора секрета простаты, эякулята плотно закрыть крышкой для предотвращения протекания. Не проводить сбор биоматериала при наличии обильных гнойных выделений из уретры.
Моча
Следует собирать первую утреннюю порцию мочи в количестве 20–30 мл в стерильный флакон. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии.
Слюна
Сбор слюны должен проводиться строго до начала применения антибактериальных и химиотерапевтических препаратов или не ранее, чем через 10–14 дней после их отмены (для местных антибиотиков), и не ранее, чем через один месяц после применения антибиотиков рer os (перорально). Перед сбором слюны рекомендуется провести трёхкратное полоскание полости рта физиологическим раствором или кипячёной водой. Сбор слюны у детей можно проводить стерильным шприцем объёмом 2–5 мл (без иглы!) из защёчного пространства в эппендорф. Следует собрать не менее 1 мл слюны. Плотно закрыть контейнер крышкой для предотвращения вытекания биоматериала.
Сбор слюны у детей можно проводить стерильным шприцем объёмом 2–5 мл (без иглы!) из защёчного пространства в эппендорф. Следует собрать не менее 1 мл слюны. Плотно закрыть контейнер крышкой для предотвращения вытекания биоматериала.
Интерпретация результатов
Ответ предоставляется в количественном формате.
Виды Lactobacillus — это тип бактерий. Существует множество различных видов лактобацилл.
Бактерии Lactobacillus обычно обнаруживаются в кишечнике, рту и влагалище человека. Их обычно считают «хорошими бактериями», и на самом деле они могут способствовать хорошему здоровью, часто их включают в пробиотические добавки. Эти бактерии характеризуются способностью продуцировать молочную кислоту как побочный продукт метаболизма глюкозы.
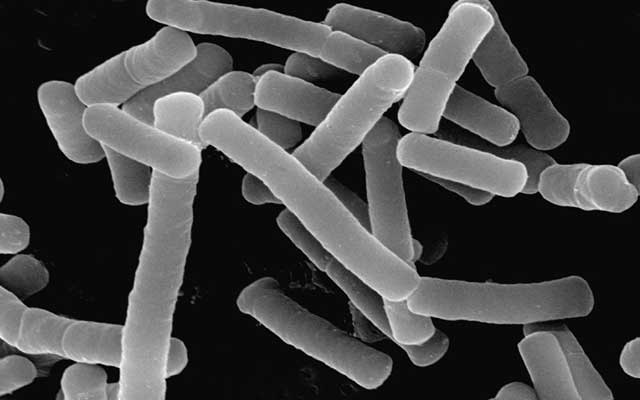
Lactobacillus считаются грамположительными, что означает, что они имеют толстую клеточную стенку, состоящую из пептидогликана (= состоящего из сахаров и аминокислот).
Lactobacillus — это группа бактерий, насчитывающая более 200 видов. Бактерии Lactobacillus исторически использовались для производства ферментированных молочных продуктов.
Лактобациллы важны для работы желудочно-кишечного тракта, так как они участвуют в синтезе витаминов, производстве природных антибиотиков, иммунной защите, пищеварении, детоксикации проканцерогенов и множестве других действий. В идеале уровень Lactobacillus должен быть 2+ или выше.
Для женщин виды Lactobacillus также можно рассматривать как биомаркеры и агенты, которые могут способствовать различным аспектам вагинального здоровья.
Лактобактерии Характеристики:
- грамположительные неспорообразующие палочки или коккобациллы
- Гомоферментативные (преимущественно молочнокислые)
- Гетероферментативный (молочная кислота, CO2, этанол и уксусная кислота)
- Переваривать и метаболизировать белки и углеводы
- Синтезировать витамины группы В и витамин К
- Катаболизирует соли желчных кислот
- Повышение врожденного и приобретенного иммунитета
- Ингибируют провоспалительные медиаторы
- Антимикробная активность в отношении множества патогенов:
Ссылки:
- Противоинфекционная активность штаммов лактобацилл в кишечной микробиоте человека: от пробиотиков до желудочно-кишечных противоинфекционных биотерапевтических средств. [L]
[L]
- Виды Lactobacillus в качестве биомаркеров и агентов, которые могут способствовать различным аспектам вагинального здоровья [L]
- Lactobacillus acidophilus: характеристика видов и применение в производстве пищевых продуктов. [L]
- Экологическая роль лактобацилл в желудочно-кишечном тракте: значение для фундаментальных и биомедицинских исследований [L]
- Низкий уровень фекальных лактобацилл у женщин с железодефицитной анемией на юге Индии [L]
- Виды Lactobacillus : таксономическая сложность и противоречивая восприимчивость. [L]
Более низкие уровни наблюдались при синдроме раздраженного кишечника (СРК):
– Снижение Lactobacillus , Collinsella
– Повышение Clostridium, Ruminococcus, Veilonella
- Если вы принимали пробиотики, уменьшите дозу Lactobacillus spp. пробиотики
пробиотики
- Высокие уровни в кишечнике Lactobacillus sp. были положительно связаны с повышенными концентрациями жирных кислот с короткой цепью в фекалиях, лактата и незаменимых аминокислот. [L]
- Некоторые Lactobacillus spp. геномы тесно связаны с высоким ИМТ. [L] Мир. Было показано, что старение увеличивает жизнеспособность 9 0009 Lactobacillus со значительными изменениями в распространенности видов [L,L].
10 000+ довольные клиенты
100% удовлетворение
★ ★ ★ ★ ★ поддержка клиентов
Мы в HealthMatters стремимся обеспечивать безопасность и конфиденциальность вашей личной информации. Мы внедрили передовые стандарты безопасности, чтобы защитить от потери, неправильного использования или изменения информации, находящейся под нашим контролем. Мы используем процедурные, физические и электронные методы безопасности, предназначенные для предотвращения доступа посторонних лиц к этой информации.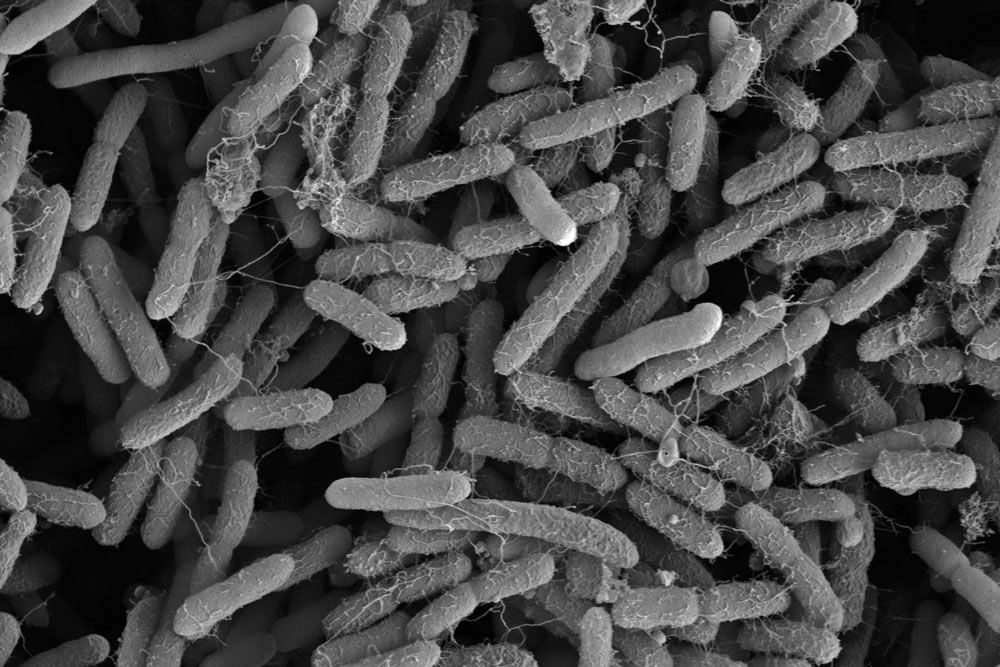 Наш внутренний кодекс поведения обеспечивает дополнительную защиту конфиденциальности. Все данные резервируются несколько раз в день и шифруются с использованием SSL-сертификатов. Подробнее см. в нашей Политике конфиденциальности.
Наш внутренний кодекс поведения обеспечивает дополнительную защиту конфиденциальности. Все данные резервируются несколько раз в день и шифруются с использованием SSL-сертификатов. Подробнее см. в нашей Политике конфиденциальности.
1. Бен Тахёр Ф., Куиди Б., Фдхила К., и др. Антибактериальная и антибиопленочная активность пробиотических бактерий в отношении оральных патогенов. Микроб Патог. 2016; 97: 213–20. [PubMed] [Google Scholar]
2. Мэтьюз MJ, Мэтьюз EH, Мэтьюз GE. Здоровье полости рта и ишемическая болезнь сердца. Здоровье полости рта BMC. 2016; 16: 1–10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Дитрих Т., Уэбб И., Стенхаус Л., и др. Резюме доказательств: взаимосвязь между оральными и сердечно-сосудистыми заболеваниями. Бр Дент Дж. 2017; 222: 381–5. [PubMed] [Google Scholar]
4. Такахаши Н.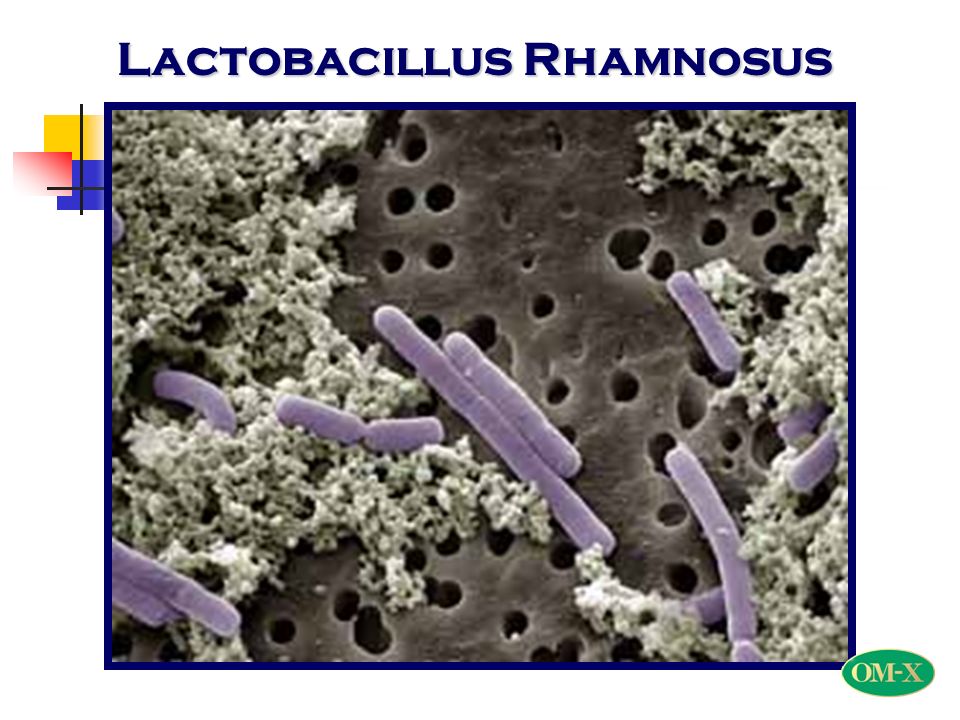 , Нивад Б. Новый взгляд на экологию кариеса: микробная динамика и процесс кариеса. Кариес рез. 2008 г.; 42: 409–18. [PubMed] [Google Scholar]
, Нивад Б. Новый взгляд на экологию кариеса: микробная динамика и процесс кариеса. Кариес рез. 2008 г.; 42: 409–18. [PubMed] [Google Scholar]
5. Тонг З., Чжоу Л., Ли Дж., и др. Исследование in vitro Lactococcus lactis , противодействующего кариесогенным бактериям Streptococcus mutans. Arch Oral Biol. 2012 г.; 57: 376–82. [PubMed] [Академия Google]
6. Абранчес Дж., Миллер Дж. Х., Мартинес А. Р., и др. Коллаген-связывающий белок Cnm необходим для прикрепления Streptococcus mutans и внутриклеточной инвазии эндотелиальных клеток коронарных артерий человека. Заразить иммун. 2011 г.; 79: 2277–84. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Kreth J, Merritt J, Qi F. Взаимодействие оральных стрептококков с бактериями и хозяином. ДНК-клеточная биол. 2009 г.; 28: 397–403. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Форсстен С.Д., Бьёрклунд М., Оувеханд АС. Streptococcus mutans, кариес и имитационные модели. Питательные вещества. 2010 г.; 2:290–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Питательные вещества. 2010 г.; 2:290–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Безерра Д.С., Стипп Р.Н., Невес Б.Г., и др. Изучение особенностей вирулентности стрептококков mutans при кариозных поражениях дентина у детей с ранним кариесом. Кариес рез. 2016; 50: 279–87. [PubMed] [Google Scholar]
10. Нгуен П.Т., Фальсетта М.Л., Хван Г., и др. Альфа-Мангостин нарушает развитие биопленок Streptococcus mutans и облегчает их механическое удаление. ПЛОС ОДИН. 2014; 9: e111312. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Ку Х., Сяо Дж., Кляйн М.И., и др. Экзополисахариды, продуцируемые глюкозилтрансферазами Streptococcus mutans, модулируют образование микроколоний в многовидовых биопленках. J Бактериол. 2010 г.; 192: 3024–32. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Сяо Дж., Кляйн М.И., Фальсетта М.Л., и др. Экзополисахаридная матрица модулирует взаимодействие между трехмерной архитектурой и вирулентностью ротовой биопленки смешанного вида.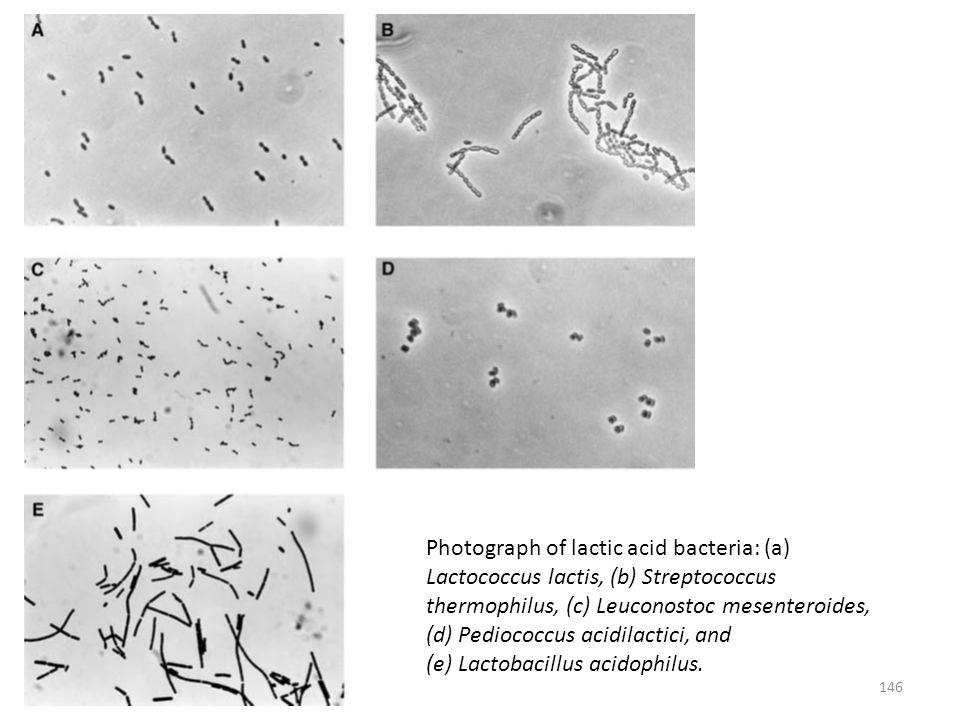 PLoS Патог. 2012 г.; 8: e1002623. [Бесплатная статья PMC] [PubMed] [Google Scholar]
PLoS Патог. 2012 г.; 8: e1002623. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Сенадира Д., Крастел К., Майр Р., и др. Инактивация VicK влияет на выработку кислоты и выживаемость Streptococcus mutans в кислоте. J Бактериол. 2009 г.; 191: 6415–24. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Смит Э.Г., Спатафора Г.А. Генная регуляция у S. mutans: сложный контроль в сложной среде. Джей Дент Рез. 2012 г.; 91: 133–41. [PubMed] [Google Scholar]
15. Кагетти М.Г., Мастроберардино С., Милия Э., и др. Использование пробиотических штаммов для профилактики кариеса: систематический обзор. Питательные вещества. 2013; 5: 2530–50. [Бесплатная статья PMC] [PubMed] [Google Scholar]
16. ФАО/ВОЗ . Руководство по оценке пробиотиков в пищевых продуктах. Отчет совместной рабочей группы ФАО/ВОЗ по составлению руководства по оценке пробиотиков в пищевых продуктах. Онтарио, Канада, 2002 г.
17. Vuotto C, Longo F, Donelli G. Пробиотики для противодействия инфекциям, связанным с биопленкой: многообещающие и противоречивые данные. Int J Oral Sci. 2014; 6: 189–94. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Int J Oral Sci. 2014; 6: 189–94. [Бесплатная статья PMC] [PubMed] [Google Scholar]
18. Баде С, Тебо Н.Б. Экология лактобацилл в полости рта: обзор литературы. Открытый Microbiol J. 2008; 2: 38–48. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Марш П., Мартин М.В., Льюис М. Микробиология полости рта. Китай: Черчилль Ливингстон; 2009. [Google Scholar]
20. Twetman S, Stecksen-Blicks C. Пробиотики и влияние на здоровье полости рта у детей. Int J Paediatr Dent. 2008 г.; 18: 3–10. [PubMed] [Google Scholar]
21. Теанпайсан Р., Пиват С., Тианвиват С., и др. Влияние длительного потребления Lactobacillus paracasei SD1 на снижение риска возникновения мутантных стрептококков и кариеса: рандомизированное плацебо-контролируемое исследование. Дент Дж. 2015; 3: 43–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Сидху Г.К., Манта С., Мурти С., и др. Оценка Lactobacillus и Streptococcus mutans при добавлении пробиотиков в виде творога в рацион.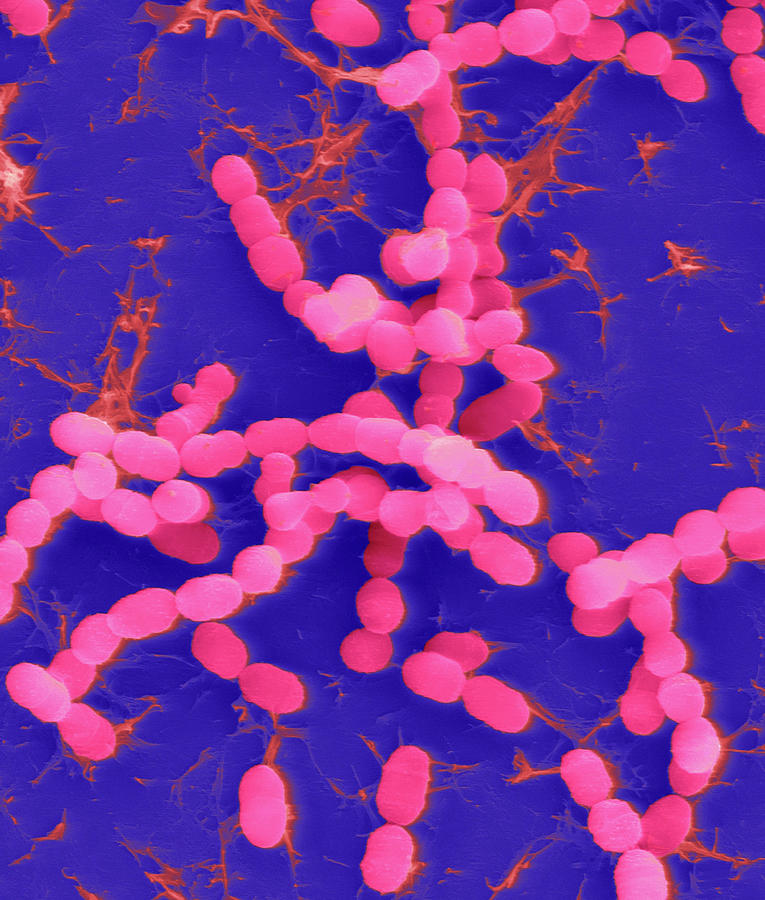 J Int Здоровье полости рта. 2015 г.; 7: 85–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Int Здоровье полости рта. 2015 г.; 7: 85–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Стаматова И, Меурман Ю.Х. Пробиотики: польза для здоровья во рту. Эм Джей Дент. 2009 г.; 22: 329–38. [PubMed] [Google Scholar]
24. Сравните D, Rocco A, Coccoli P, и др. . Lactobacillus casei DG и его постбиотик уменьшают воспалительную реакцию слизистой:0009 ex-vivo модель культуры органов постинфекционного синдрома раздраженного кишечника. БМК Гастроэнтерол. 2017; 17: 1–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Линь X, Чен X, Чен Y, и др. Влияние пяти пробиотических штаммов лактобацилл на рост и образование биопленок Streptococcus mutans. Оральный Дис. 2015 г.; 21: e128–34. [PubMed] [Google Scholar]
26. Шокряздан П., Сиео К.С., Калавати Р., и др. Пробиотический потенциал штаммов Lactobacillus с антимикробной активностью в отношении некоторых патогенных для человека штаммов. Биомед Рез Инт. 2014; 927268: 1–16.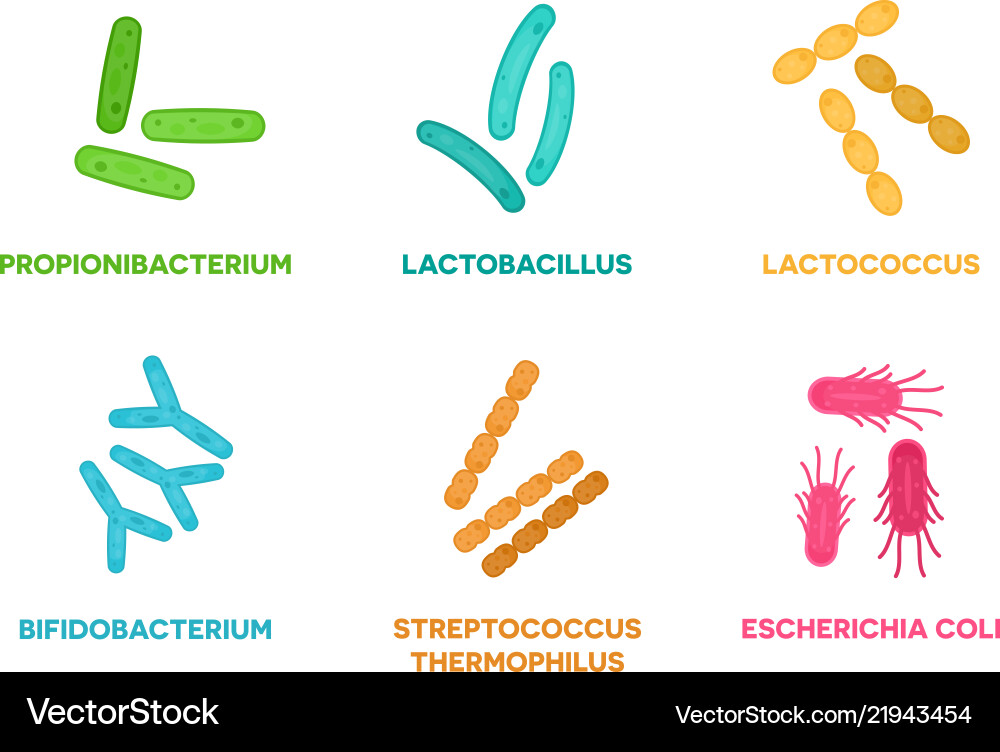 [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Cadirci BH, Citak S. Сравнение двух методов, используемых для измерения антагонистической активности молочнокислых бактерий. Пак Дж Нутр. 2005 г.; 4: 237–41. [Google Scholar]
28. Chew SY, Cheah YK, Seow HF, и др. Пробиотики Lactobacillus rhamnosus GR-1 и Lactobacillus reuteri RC-14 проявляют сильное противогрибковое действие в отношении изолятов Candida glabrata, вызывающих вульвовагинальный кандидоз. J Appl Microbiol. 2015 г.; 118: 1180–11890. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Васфи Р., Абд Эль-Рахман О.А., Мансур Л.Е., и др. Антимикробная активность в отношении биопленки, образованной изолятами Proteus mirabilis при инфекциях ран и мочевыводящих путей. Индийская J Med Microbiol. 2012 г.; 30: 76–80. [PubMed] [Google Scholar]
30. Ву CC, Лин CT, Ву CY, и др. Ингибирующее действие Lactobacillus salivarius на образование биопленок Streptococcus mutans. Мол Оральный микробиол. 2015 г.; 30: 16–26. [PubMed] [Академия Google]
Мол Оральный микробиол. 2015 г.; 30: 16–26. [PubMed] [Академия Google]
31. Pfaffl MW, Tichopad A, Prgomet C, и др. Определение стабильных генов домашнего хозяйства, дифференциально регулируемых генов-мишеней и целостности образца: инструмент на основе BestKeeper–Excel с использованием парных корреляций. Биотехнологическая лат. 2004 г.; 26: 509–515. [PubMed] [Google Scholar]
32. Пфаффл МВт. Относительная количественная оценка В: Дорак Т., редактор. ПЦР в реальном времени. International University Line 2004. [Google Scholar]
33. Килиан М., Чаппл ILC, Ханниг М., и др. Микробиом полости рта — обновленная информация для специалистов по уходу за полостью рта. Бр Дент Дж. 2016; 221: 657–66. [PubMed] [Google Scholar]
34. Петрова М.И., Ливенс Э., Малик С., и др. Виды Lactobacillus в качестве биомаркеров и агентов, которые могут способствовать различным аспектам вагинального здоровья. Фронт Физиол. 2015 г.; 6: 1–18. [Бесплатная статья PMC] [PubMed] [Google Scholar]
35. Флох М.Х., Уокер В.А., Мэдсен К., и др. Рекомендации по использованию пробиотиков, обновление 2011 г. Дж. Клин Гастроэнтерол. 2011 г.; 45 (Прил.): S168–71. [PubMed] [Академия Google]
Флох М.Х., Уокер В.А., Мэдсен К., и др. Рекомендации по использованию пробиотиков, обновление 2011 г. Дж. Клин Гастроэнтерол. 2011 г.; 45 (Прил.): S168–71. [PubMed] [Академия Google]
36. Донелли Г. Активность пробиотиков в отношении биопленочных патогенов полости рта. Microb Ecol Health Дис. 2013; 24: 6. [Google Scholar]
37. Линь Y-TJ, Чжоу C-C, Хсу C-YS. Влияние приема Lactobacillus casei Shirota на риск развития кариеса у детей. J Dent Sci. 2017; 12: 179–84. [Google Scholar]
38. Имран Ф., Дас С., Падманабхан С., и др. Оценка эффективности пробиотического напитка, содержащего Lactobacillus casei , на уровни пародонтопатогенных бактерий при пародонтите: клинико-микробиологическое исследование. Индиан Джей Дент Рез. 2015 г.; 26: 462–8. [PubMed] [Академия Google]
39. Чаглар Э., Чилдир С.К., Эргенели С., и др. Уровни стрептококков и лактобацилл в слюне после приема пробиотических бактерий Lactobacillus reuteri ATCC 55730 через соломинку и таблетки. Акта Одонтол Сканд. 2006 г.; 64(5): 314–318. [PubMed] [Google Scholar]
Акта Одонтол Сканд. 2006 г.; 64(5): 314–318. [PubMed] [Google Scholar]
40. Саха С., Томаро-Дюшено С., Родес Л., и др. Исследование пробиотических бактерий в качестве биотерапевтических средств для лечения кариеса и заболеваний пародонта. Польза микробов. 2014; 5: 447–60. [PubMed] [Академия Google]
41. Baca-Castanon ML, De la Garza-Ramos MA, Alcazar-Pizana AG, и др. Противомикробное действие Lactobacillus reuteri на кариесогенные бактерии Streptococcus gordonii, Streptococcus mutans и заболевания пародонта Actinomyces naeslundii и Tannerella forsythia. Пробиотики Антимикробные белки. 2015 г.; 7: 1–8. [PubMed] [Google Scholar]
42. Hasslöf P. Пробиотические Lactobacilli в контексте кариеса зубов как заболевания, опосредованного биопленкой [Докторская диссертация, исчерпывающее резюме]. Умео: Университет Умео; 2013. [Google Академия]
43. Исикава Х., Айба Ю., Наканиши М., и др. Подавление пародонтальных патогенных бактерий в слюне человека путем введения Lactobacillus salivarius TI 2711. Nihon Shishubyo Gakkai Kaishi (J Japanese Soc Periodontol). 2003 г.; 45: 105–12. [Google Scholar]
Nihon Shishubyo Gakkai Kaishi (J Japanese Soc Periodontol). 2003 г.; 45: 105–12. [Google Scholar]
44. Нишихара Т., Сузуки Н., Йонеда М., и др. Влияние таблеток, содержащих Lactobacillus salivarius, на факторы риска кариеса: рандомизированное открытое клиническое исследование. Здоровье полости рта BMC. 2014; 14: 1–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
45. Олдак А., Зелинска Д., Жепковска А., и др. Сравнение антибактериальной активности штаммов Lactobacillus plantarum, выделенных из двух разных видов региональных сыров из Польши: сыра Осцыпек и Корычинского. Биомед Рез Инт. 2017; 6820369: 1–10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46. Тахери П., Самади Н., Эхсани М.Р., и др. Оценка и частичная характеристика бактериоцина, продуцируемого Lactococcus lactis subsp lactis ST1, выделенного из козьего молока. Браз Дж Микробиол. 2012 г.; 43: 1452–1462. [Бесплатная статья PMC] [PubMed] [Google Scholar]
47. Го Л., Маклин Дж. С., Люкс Р., и др. Хорошо скоординированная связь между ацидогенностью и кислотностью через нерастворимых глюканов на поверхности Streptococcus mutans. Научный представитель 2015 г.; 5: 1–11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Го Л., Маклин Дж. С., Люкс Р., и др. Хорошо скоординированная связь между ацидогенностью и кислотностью через нерастворимых глюканов на поверхности Streptococcus mutans. Научный представитель 2015 г.; 5: 1–11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Лю Ю, Бёрн Р.А. Множественные двухкомпонентные системы Streptococcus mutans регулируют экспрессию гена агматиндезиминазы и стрессоустойчивость. J Бактериол. 2009 г.; 191: 7363–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Dalié DKD, Deschamps AM, Richard-Forget F. Молочнокислые бактерии – потенциал для контроля роста плесени и микотоксинов: обзор. Пищевой контроль. 2010 г.; 21: 370–80. [Google Академия]
50. Сюй Х, Чжоу XD, Ву CD. Галлат эпигаллокатехина катехина чая подавляет кариесогенные факторы вирулентности Streptococcus mutans. Противомикробные агенты Chemother. 2011 г.; 55: 1229–1236. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Дасари С., Шоури Р.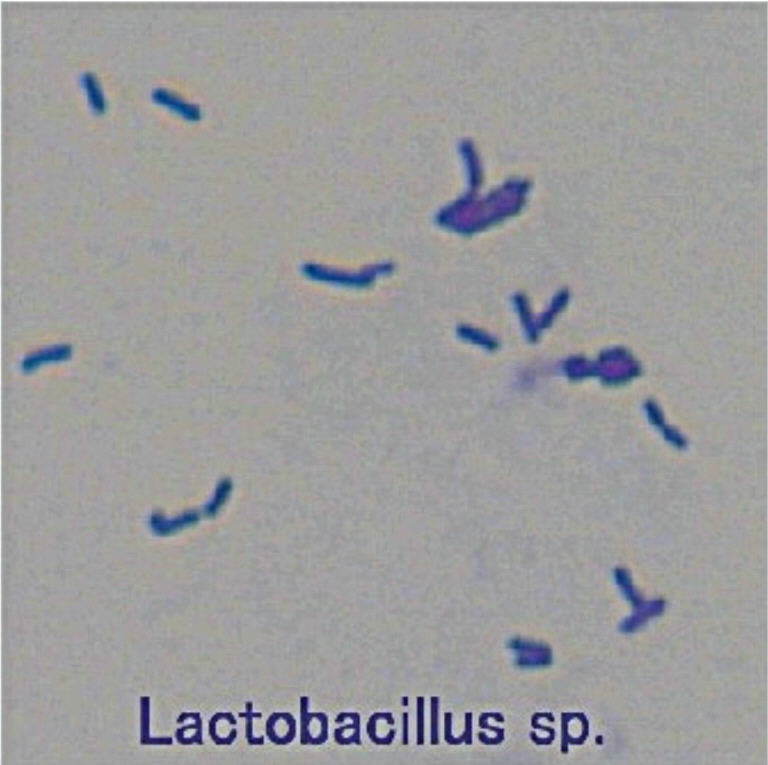 Д., Вудаягири Р., и др. Антимикробная активность Lactobacillus в отношении микробной флоры цервиковагинальных инфекций. Азиатский Pac J Trop Dis. 2014; 4: 18–24. [Google Scholar]
Д., Вудаягири Р., и др. Антимикробная активность Lactobacillus в отношении микробной флоры цервиковагинальных инфекций. Азиатский Pac J Trop Dis. 2014; 4: 18–24. [Google Scholar]
52. Тахмуреспур А., Салехи Р., Касра К.Р. Влияние биосурфактанта, полученного из Lactobacillus Acidophilus, на уровень экспрессии GTFB и GTFC в клетках биопленки Streptococcus mutans. Браз Дж Микробиол. 2011 г.; 42: 330–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Хасслёф П., Хедберг М., Тветман С., и др. Ингибирование роста пероральных стрептококков mutans и Candida коммерческими пробиотическими лактобациллами — исследование in vitro . Здоровье полости рта BMC. 2010 г.; 10: 1–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
54. Леунг В., Дюфур Д., Левеск К.М. Смерть и выживание у Streptococcus mutans: разные результаты сигнального пептида, чувствительного к кворуму. Фронт микробиол. 2015 г.; 6: 1–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Бану ЛД. Экспрессия генов в биопленках Streptococcus mutans. Университет Цюриха, 2010 г.
Бану ЛД. Экспрессия генов в биопленках Streptococcus mutans. Университет Цюриха, 2010 г.
56. Лю С, Ху П, Данг Ю, и др. Очистка и частичная характеристика нового бактериоцина, продуцируемого Lactobacillus casei TN-2, выделенного из ферментированного верблюжьего молока (Шубат) Синьцзян-Уйгурского автономного района, Китай. Пищевой контроль. 2014; 43: 276–83. [Академия Google]
57. Морита Х., Тох Х., Фукуда С., и др. Сравнительный анализ генома Lactobacillus reuteri и Lactobacillus fermentum выявил геномный остров для производства реутерина и кобаламина. Рез. ДНК 2008 г.; 15: 151–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. да Силва С.С., Витоло М., Гонсалес Х.М.Д. Оливейра RPdS. Обзор Lactobacillus plantarum как перспективного продуцента бактериоцинов среди молочнокислых бактерий. Фуд Рез Инт. 2014; 64: 527–36. [Академия Google]
59. О'Ши Э.Ф., О'Коннор П.М., О'Салливан О., и др. Бактофенцин А, новый тип катионного бактериоцина с необычным иммунитетом.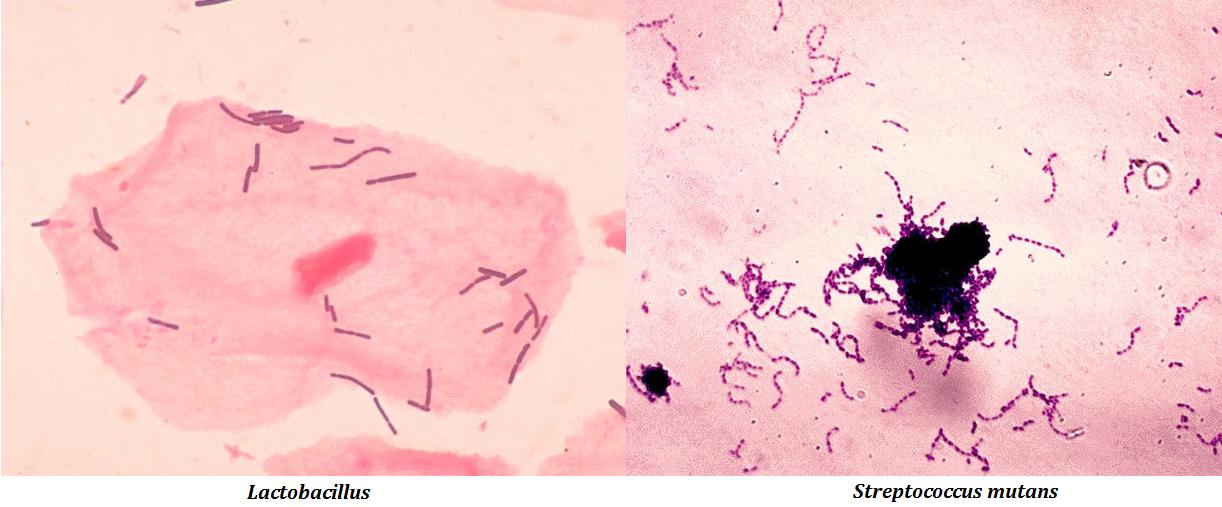 МБио. 2013; 4: e00498–13. [Бесплатная статья PMC] [PubMed] [Google Scholar]
МБио. 2013; 4: e00498–13. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Декер Э.-М., Кляйн С., Швиндт Д., и др. Метаболическая активность биопленок Streptococcus mutans и экспрессия генов при воздействии ксилита и сахарозы. Int J Oral Sci. 2014; 6: 195–204. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61. Шемеш М., Там А., Фельдман М., и др. Профили дифференциальной экспрессии генов Streptococcus mutans ftf, gtf и vicR в присутствии пищевых углеводов на ранней и поздней фазах экспоненциального роста. Карбогид Рез. 2006 г.; 341: 2090-7. [PubMed] [Google Scholar]
62. Нарисава Н., Кавараи Т., Судзуки Н., и др. Компетентно-зависимая перестройка эндогенной ДНК и поглощение внеклеточной ДНК дают естественный вариант Streptococcus mutans без образования биопленки. J Бактериол. 2011 г.; 193: 5147–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Чон Дж. Г., Кляйн М. И., Сяо Дж., и др. Влияние встречающихся в природе агентов в сочетании с фтором на экспрессию генов и структурную организацию Streptococcus mutans в биопленках. БМС микробиол. 2009 г.; 9: 228. [Бесплатная статья PMC] [PubMed] [Google Scholar]
БМС микробиол. 2009 г.; 9: 228. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Велин-Нейландс Дж., Свенсатер Г. Кислотоустойчивость клеток биопленки Streptococcus mutans. Appl Environ Microbiol. 2007 г.; 73: 5633–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
65. Сенадхира, доктор медицины, Гуггенхайм Б., Спатафора Г.А., и др. Система передачи сигнала VicRK у Streptococcus mutans влияет на экспрессию gtfBCD, gbpB и ftf, образование биопленки и развитие генетической компетентности. J Бактериол. 2005 г.; 187: 4064–76. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Кшищак В., Юрчак А., Косельняк Д., и др. Вирулентность Streptococcus mutans и способность образовывать биопленки. Eur J Clin Microbiol Infect Dis. 2014; 33: 499–515. [Бесплатная статья PMC] [PubMed] [Google Scholar]
67. Bowen WH, Koo H. Биология глюкозилтрансфераз, полученных из Streptococcus mutans: роль в формировании внеклеточного матрикса кариесогенных биопленок. Кариес рез. 2011 г.; 45: 69–86. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Кариес рез. 2011 г.; 45: 69–86. [Бесплатная статья PMC] [PubMed] [Google Scholar]
68. Саваби О., Каземи М., Камали С., и др. Влияние биосурфактанта, продуцируемого Lactobacillus casei , на уровень экспрессии генов gtfB , gtfC и ftf у S. mutans с помощью RT-PCR в реальном времени. Adv Biomed Res. 2014; 3: 1–16. [Бесплатная статья PMC] [PubMed] [Google Scholar]
69. Xiao J, Koo H. Структурная организация и динамика образования экзополисахаридного матрикса и микроколоний Streptococcus mutans в биопленках. J Appl Microbiol. 2010 г.; 108: 2103–13. [PubMed] [Google Scholar]
70. Yamashita Y, Bowen WH, Burne RA, и др. Роль генов Streptococcus mutans gtf в индукции кариеса в модели крыс без специфических патогенов. Заразить иммун. 1993 год; 61: 3811–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Ульрих М. Бактериальный полисахарид: текущие инновации и будущие тенденции. Норфолк, Великобритания: Caister Academic Press; 2009 г.