2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Подтверждаю Подробнее
Ветряная оспа
Краснуха
Корь
Подагра
Энцефалит
Гепатит
Ревматизм
14658 06 Октября
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
С-реактивный белок (СРБ, CRP): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
С-реактивный белок (СРБ) – наиболее высокочувствительный показатель повреждения тканей при воспалении, некрозе, травме. В крови здорового человека СРБ отсутствует или выявляется в минимальных количествах. Вырабатывается он преимущественно клетками печени (гепатоцитами), как реакция на попадание в организм человека возбудителей инфекций, на травму, а также при системных заболеваниях соединительной ткани (ревматических заболеваниях).
В крови здорового человека СРБ отсутствует или выявляется в минимальных количествах. Вырабатывается он преимущественно клетками печени (гепатоцитами), как реакция на попадание в организм человека возбудителей инфекций, на травму, а также при системных заболеваниях соединительной ткани (ревматических заболеваниях).
СРБ стимулирует иммунные реакции в организме, активирует его защитные системы и имеет высокую корреляцию с активностью заболевания и стадией процесса, то есть его концентрация становится тем выше, чем активнее воспаление (инфекционное или аутоиммунное) и более обширна зона повреждения тканей при некрозе или травме. Поэтому С-реактивный белок называют белком «острой фазы».
Еще одним показателем острого воспаления является СОЭ (скорость оседания эритроцитов).
СОЭ (Cкорость Оседания Эритроцитов, ESR)
СОЭ – неспецифичный маркер воспаления.
Синонимы: Реакция оседания эритроцитов; РОЭ.2007/ST19/Untitled-1.gif) Westergren sedimentation rate; Erythrocyte Sedimentation Rate; ESR; Sed Rate; Sedimentation Rate.
Крат...
Westergren sedimentation rate; Erythrocyte Sedimentation Rate; ESR; Sed Rate; Sedimentation Rate.
Крат...
До 1 рабочего дня
Доступно с выездом на дом
295 руб
В корзину
Однако СРБ более информативен, поскольку его уровень начинает расти раньше, а снижаться быстрее (при правильном лечении СРБ снижается на 6-10-е сутки, в то время как СОЭ – только на 14-28-е). Кроме того, на результаты СОЭ оказывает влияние пол пациента (у женщин показатель СОЭ выше, чем у мужчин), время суток, число эритроцитов, а на значениях СРБ это никак не отражается. Таким образом, для оценки воспалительного процесса анализ на С-реактивный белок выглядит более оправданным.
Уровень СРБ при вирусных заболеваниях повышается незначительно, поэтому его существенный рост в сочетании с повышенной температурой тела с большой долей вероятности свидетельствует о наличии бактериальной инфекции.
На короткое время С-реактивный белок может повышаться после оперативных вмешательств из-за повреждения тканей, но при отсутствии бактериального воспаления в послеоперационном периоде быстро снижается.
Тогда как присоединение бактериальной инфекции, будь то локальный процесс или сепсис, сопровождается ростом СРБ или отсутствием его снижения.
Существует высокочувствительный метод определения СРБ – высокочувствительный С-реактивный белок (кардио). Исследование позволяет выявить повышение СРБ при вялотекущем, низкой степени активности воспалении внутренней поверхности сосудистой стенки, которое чревато образованием атеросклеротических бляшек. Анализ назначают только в отсутствии острых заболеваний и травм (при них повышение СРБ выявляется стандартным методом). Увеличение значений высокочувствительного С-реактивного белка может свидетельствовать о риске сердечно-сосудистых заболеваний: инфаркта миокарда, инсульта.
Таким образом, анализ на С-реактивный белок в комплексе с исследованием некоторых показателей клинического анализа крови (уровня лейкоцитов, лейкоцитарной формулы и СОЭ) обычно назначают в случае повышения температуры тела, чтобы по степени их увеличения предположить вирусное или бактериальное воспаление.
СРБ определяют при болях в суставах, не связанных с травмой, для дифференциальной диагностики дегенеративных и воспалительных заболеваний – артроза и артрита. При ревматических заболеваниях СРБ исследуют для оценки активности процесса и контроля эффективности лечения.
Сдавать кровь предпочтительно утром натощак, после 8-14-часового перерыва в приеме пищи. Нельзя пить соки, чай и кофе. Воду пить разрешается.
При необходимости можно сдавать анализ на СРБ через 4-6 часов после легкого приема пищи.
За 2-3 дня до исследования следует исключить физические нагрузки.
Не следует курить минимум за 30 минут до забора крови.
С-реактивный белок (СРБ, CRP)
С-реактивный белок – белок острой фазы, чувствительный индикатор повреждения тканей при воспалении, некрозе, травме. Синонимы: Анализ крови на СРБ; С-реактивн...
До 1 рабочего дня
Доступно с выездом на дом
665 руб
В корзину
Анализ выполняется в течение одного рабочего дня.
На результаты исследования может повлиять целый ряд факторов:
Для исследования берется кровь из вены.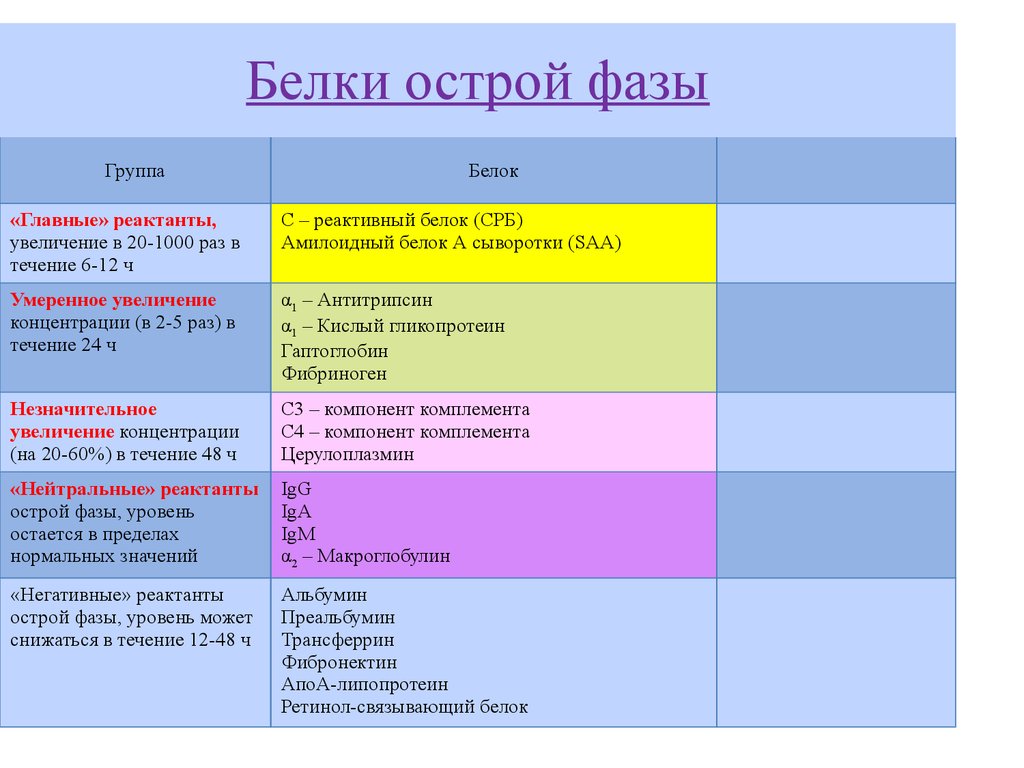
Сдать анализ крови на С-реактивный белок (СРБ, CRP) можно в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса».
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения: мг/л
Нормальным считается уровень СРБ менее 5 мг/л.
При оценке сердечно-сосудистых рисков уровень высокочувствительного СРБ менее 1,0 мг/л расценивают как низкий, 1-3 мг/л – как средний, более 3 мг/л указывает на повышенный риск развития сердечно-сосудистых заболеваний в будущем.
Уровень С-реактивного белка в крови не зависит от пола и возраста пациента, а его повышение может быть связано с повреждением различной природы любых органов и систем организма. Конкретный диагноз устанавливается путем комплексной оценки жалоб, данных осмотра, инструментальных и лабораторных методов обследования.
Поскольку в крови здорового человека С-реактивный белок или отсутствует, или выявляется в минимальных количествах, говорить о его понижении некорректно.
Степень повышения С-реактивного белка обычно коррелирует с объемом, характером и выраженностью поражения тканей.
Повышение СРБ до 30 мг/л может говорить о вирусных заболеваниях - ОРВИ, ротавирусной инфекции и др., обнаруживается при злокачественных опухолях, ревматических болезнях вне стадии обострения (системная красная волчанка, дерматомиозит, системная склеродермия, ревматоидный артрит и др. ).
).
Повышение СРБ до 100 мг/л и выше, как правило, сопутствует различным острым бактериальным инфекциям (ангине, пневмонии, аппендициту, острому холециститу, пиелонефриту и др.), обострениям хронических инфекционных заболеваний и ревматических болезней, а также различным повреждениям тканей (оперативное вмешательство, инфаркт миокарда и т.д.).
Самое значимое повышение СРБ – до 300 мг/л и более возможно при обширных ожогах и сепсисе, когда бактерии из очага поражения попадают в кровь и распространяются по всему организму.
Подъем температуры тела в сочетании с повышением уровня С-реактивного белка может сопутствовать генерализованным (распространенным) и любым локальным поражениям – инфекциям кожи и подкожной жировой клетчатки, респираторным и стоматологическим инфекциям, инфекциям глаз, ЛОР-органов, желудочно-кишечного тракта, сердечно-сосудистой системы, урологическим инфекциям, инфекциям центральной нервной системы, костей и суставов.
В зависимости от клинической картины, обследованием и лечением таких пациентов занимаются врачи разных специальностей – терапевты, хирурги, узкие специалисты, в том числе ЛОРы, стоматологи, гинекологи, урологи, ревматологи.
В качестве дополнительных исследований в каждом конкретном случае может понадобиться самый разнообразный спектр инструментальной и лабораторной диагностики.
Повышение уровня высокочувствительного СРБ влечет за собой определение других факторов риска сердечно-сосудистых заболеваний. Для этого выполняется анализ крови на липидный спектр, фибриноген, гомоцистеин, глюкозу, мочевую кислоту, а также ультразвуковое исследование сосудов шеи и сердца.
Источники
 № 1. 2013. С. 23-27.
№ 1. 2013. С. 23-27.ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Рекомендации
Анализ на ПСА (простатический специфический антиген)
7827 13 Мая
Вирус папилломы человека
12053 04 Мая
Щелочная фосфатаза
3908 16 Апреля
Показать еще
Аллергия
Простуда
Пиелонефрит
Энцефалит
Подагра
Цистит
Общий анализ крови
Общий клинический анализ крови без лейкоцитарной формулы и СОЭ: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы
Подробнее
Атеросклероз
Сахарный диабет
Артрит
Подагра
Холестерин
Холестерин: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Подробнее
Желтуха
Гепатит
Антитела к вирусу гепатита В
Антитела к вирусу гепатита В: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Подробнее
Подагра
Сахарный диабет
Атеросклероз
Мочевая кислота (в крови) (Uric acid)
Мочевая кислота в крови: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Подробнее
Аллергия
Рак шейки матки
Рак матки
Ревматизм
Артрит
Белок S100 (S100 protein)
Белок S100: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Подробнее
Введите e-mail
Даю согласие на обработку персональных данных
Подписаться
Синонимы: СРБ, CRP, C-reactive Protein
СРБ – это белок плазмы крови, концентрация которого повышается при воспалении. Основное количество белка вырабатывается в клетках печени в ответ на некоторые сигналы от макрофагов (иммунные клетки)¹.
Основное количество белка вырабатывается в клетках печени в ответ на некоторые сигналы от макрофагов (иммунные клетки)¹.
Основная функция СРБ – защитная. Он активирует систему комплемента (группа белков, обладающих антибактериальной активностью), а также некоторые клетки иммунной системы. Концентрация СРБ повышается пропорционально масштабу воспалительного процесса. Чем сильнее воспаление, тем больше вырабатывается белка в печени.
Когда воспаление переходит в хроническую стадию, то уровень СРБ снижается (иногда до нуля). Однако при обострениях он вновь повышается.
Еще одно свойство СРБ – связывание липопротеинов низкой плотности (ЛПНП)². Это так называемый «плохой холестерин». Таким образом, этот белок способствует и развитию атеросклероза. Увеличение концентрации С-реактивного белка при отсутствии острой инфекции или травм может показывать риск сердечных патологий.
 Фото: freepik.com
Фото: freepik.comКак правило, определяют C-реактивный белок в биохимическом анализе крови (CRP). Показатель измеряется в миллиграммах на литр (мг/л). Кровь для такого анализа берут из вены.
Нормальные значения СРБ могут отличаться в разных лабораториях. В большинстве случаев это до 1 мг/л. В некоторых учреждениях – до 5 мг/л. Нижнего предела для данного маркера не существует, поскольку белок определяется в острую фазу воспаления.
СРБ в крови определяют при следующих обстоятельствах:

Специальной подготовки от пациента не требуется. Нужно соблюдать стандартные требования, которые предъявляются перед сдачей крови из вены:
 После ужина и до момента сдачи крови (на следующий день) допускается только употребление чистой воды (не чая, кофе, соков или других напитков).
После ужина и до момента сдачи крови (на следующий день) допускается только употребление чистой воды (не чая, кофе, соков или других напитков). Поскольку С-реактивный белок определяется в крови в ответ на острое воспаление или инфекционный процесс, то его уровень не зависит от пола или возраста пациента. Это значит, что для мужчины, женщины и ребенка существует единые критерии оценки СРБ.
Для оценки инфекционно-воспалительных процессов в организме нормой считается уровень СРБ до 5 мг/л. Что касается оценки сердечно-сосудистых рисков, то показатели другие:
Установлено, что лица с повышенным СРБ, но нормальным уровнем ЛПНП, имеют больший риск развития сердечно-сосудистых заболеваний, чем люди с нормальным СРБ, но повышенным ЛПНП. Таким образом, показатель СРБ в прогнозе сердечно-сосудистых патологий имеет куда большую значимость, чем уровень холестерина.
К основным причинам повышения СРБ относятся:
 Например, травмы, острый инфаркт миокарда, ожоги или последствия хирургических операций.
Например, травмы, острый инфаркт миокарда, ожоги или последствия хирургических операций.Низкий или нулевой показатель СРБ может означать отсутствие воспалительного процесса. Факторами, снижающими СРБ, также являются противовоспалительные препараты (нестероидные противовоспалительные средства, глюкокортикоиды), статины или бета-блокаторы.
Если вы принимаете эти препараты, то перед проведением анализа нужно отменить их прием в течение 1-2 суток. Делать это нужно только с разрешения врача.
Само повышение уровня СРБ является следствием развития инфекционно-воспалительного процесса. Это защитный белок, который начинает продуцироваться в ответ на воспаление.
В данном случае важно верно поставить диагноз. Для этого одних значений СРБ недостаточно. Этот маркер лишь указывает на статус воспаления, а для точного диагноза нужны дополнительные исследования.
Исследование уровня СРБ во время пандемии коронавирусной болезни COVID-19 приобрело дополнительную значимость. Маркер рассматривают в качестве основного индикатора активности воспалительного процесса в легких. Определение СРБ у пациентов с COVID-19 позволяет оценить следующие показатели:
 При тяжелом течении СРБ может увеличиваться до 100 мг/л и более. При этом уровень СРБ коррелирует с объемом поражения легочной ткани.
При тяжелом течении СРБ может увеличиваться до 100 мг/л и более. При этом уровень СРБ коррелирует с объемом поражения легочной ткани.Показанием для выписки из стационара является уровень СРБ менее 10 мг/л.
У каждого второго пациента с коронавирусом С-реактивный белок повышается уже в первые дни болезни. Фото: halfpoint / DepositphotosУстранение факторов, повышающих уровень СРБ, автоматически приводит к его снижению. Это регулярные умеренные физические нагрузки, отказ от вредных привычек (курения, чрезмерного употребления спиртного) и нормализация массы тела.
Это регулярные умеренные физические нагрузки, отказ от вредных привычек (курения, чрезмерного употребления спиртного) и нормализация массы тела.
Своевременное лечение острых и хронических заболеваний также снижает уровень С-реактивного белка.
В норме у здорового человека СРБ отсутствует или определяется в крайне низких концентрациях. Повышать уровень этого маркера не нужно.
С-реактивный белок – высокочувствительный маркер воспалительного процесса. Уровень СРБ повышается при инфекциях, воспалениях, злокачественных опухолях, сахарном диабете и ряде других заболеваний и состояний.
Определяют СРБ в рамках биохимического анализа. Кровь берется из вены утром, натощак. При расшифровке анализа врач также учитывает и ряд обстоятельств, которые могут повлиять на уровень СРБ в крови. Среди таковых курение, злоупотребление алкоголем, прием некоторых лекарств и ожирение.
Нормальные уровни СРБ не зависят от пола и возраста, что делает его более точным и специфичным анализом, чем СОЭ.
1. Johnson RW. Ингибирование роста провоспалительными цитокинами; комплексный вид. J Anim Sci. 1997; 75: 1244–55. [PubMed] [Google Scholar]
2. Baumann H, Gauldie J. Регуляция генов белков острой фазы плазмы факторами, стимулирующими гепатоциты, и другими медиаторами воспаления. Мол Биол Мед. 1990; 7: 147–59. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
3. Уичер Дж. Т., Westacott CI. Реакция острой фазы. В: Уичер Дж. Т., Эванс С. В., редакторы. Биохимия воспаления. Лондон: Академик Клювера; 1992. стр. 243–71. [Google Scholar]
4. Eckersall PD, Conner JG. Белки острой фазы крупного рогатого скота и собак. Ветрез. коммун. 1988; 12: 169–78. [PubMed] [Google Scholar]
5. Габай С., Кушнер И. Белки острой фазы и другие системные реакции на воспаление. N Engl J Med. 1999; 340:448–54. [PubMed] [Google Scholar]
6. Бек Г., Хабихт Г.С. Выделение и характеристика примитивного белка, подобного интерлейкину-1, из беспозвоночного. Астериас форбези. Proc Natl Acad Sci USA. 1986;83:7429–33. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Huang H, Potter AA, Campos M, Leighton FA, Willson PJ, Haines DM, et al. Патогенез свиной Actinobacillus pleuropneumoniae, Часть II: Роль провоспалительных цитокинов. Can J Vet Res. 1999; 63: 69–78. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Schijns VE, Horzinek MC. Цитокины в ветеринарии. Уоллингфорд: CAB International; 1997. [Google Scholar]
Schijns VE, Horzinek MC. Цитокины в ветеринарии. Уоллингфорд: CAB International; 1997. [Google Scholar]
9. Bird S, Wang T, Zou J, Cunningham C, Secombes CJ. Первая последовательность цитокинов у хрящевых рыб: IL-1β у малой пятнистой кошачьей акулы (Scyliorhinus canicula) J Immunol. 2002;168:332940. [PubMed] [Google Scholar]
10. Myers M, Murtaugh MP. Цитокины в здоровье и болезнях животных. Нью-Йорк: Марсель Деккер; 1995. [Google Scholar]
11. Murtaugh MP. Цитокины свиньи. Вет Иммунол Иммунопатол. 1994; 43:37–44. [PubMed] [Google Scholar]
12. Heegaard PM, Godson DL, Toussaint MJ, Tjonehoj K, Larsen LE, Viuff B, et al. Реакция острой фазы гаптоглобина и сывороточного амилоида А (SAA) у крупного рогатого скота, подвергшегося экспериментальному заражению бычьим респираторно-синцитиальным вирусом. Вет Иммунопатол. 2000;77:9–15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Sipe JD. Белки острой фазы при хроническом воспалении. В: Кой А, редактор. Реакция острой фазы на травму и инфекцию. Амстердам: Эльзевир; 1985. стр. 273–84. [Google Scholar]
Реакция острой фазы на травму и инфекцию. Амстердам: Эльзевир; 1985. стр. 273–84. [Google Scholar]
14. Horadagoda NU, Knox KM, Gibbs HA, Reid SW, Horagoda A, Edwards SE, et al. Белки острой фазы у крупного рогатого скота: различие между острым и хроническим воспалением. Ветеринар Рек. 1999; 144:437–41. [PubMed] [Google Scholar]
15. Vegad JL. Учебник общей ветеринарной патологии. 2-е изд. Лакхнау: изд. Международная компания по распространению книг; 2007. Воспаление; стр. 105–82. [Академия Google]
16. Beutler B, Cerami A. Cahcectin Фактор некроза опухоли: эндогенный медиатор шока и воспаления. Иммунол. 1986; 5: 381–93. [PubMed] [Google Scholar]
17. Динарелло, Калифорния. Интерлейкин-1 и его биологически родственные цитокины. Ад Иммунол. 1989; 44: 153–205. [PubMed] [Google Scholar]
18. Moshage H. Цитокины и ответ острой фазы печени. Джей Патол. 1997; 181: 257–66. [PubMed] [Google Scholar]
19. Curits MJ, Butler EJ. Реакция церуплазмина на эндотоксин E. coli и гормоны надпочечников у домашних птиц. рез. вет. 1980;28:217–22. [PubMed] [Google Scholar]
coli и гормоны надпочечников у домашних птиц. рез. вет. 1980;28:217–22. [PubMed] [Google Scholar]
20. Армани Д.И., Мози-Мелиц Д., Мозессон В.М. Влияние гепатоцитостимулирующего фактора и глюкокортикоидов на уровень фибронектина. Биохим Дж. 1986; 23:365–71. [Google Scholar]
21. Gruys E, Ederen AM, Van Aslengeest SP, Kalsbeck HC, Wensing T. Показатели белков острой фазы в крови крупного рогатого скота; показатель животных с патологическими процессами. Обеспечьте гигиену Filr Lebensmittel. 1993; 44: 107–12. [Google Scholar]
22. Дженсен Л.Э., Уайтхед А.С. Регуляция экспрессии белка SAA во время острофазового ответа. Биохим Дж. 1998;334:489–503. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Petersen HH, Nielsen JP. Состояние здоровья и клинические признаки в зависимости от концентрации С-реактивного белка в сыворотке свиней. 4-й Европейский коллоквиум по белкам острой фазы, Сеговия, Испания: Коллоквиум; 2003. стр. 118–9. [Google Scholar]
24. Petersen HH, Nielsen JP, Heegard PM. Применение измерений белков острой фазы в ветеринарной клинической химии. Вет Рез. 2004; 35: 163–87. [PubMed] [Академия Google]
Petersen HH, Nielsen JP, Heegard PM. Применение измерений белков острой фазы в ветеринарной клинической химии. Вет Рез. 2004; 35: 163–87. [PubMed] [Академия Google]
25. PiOeiro M, Alava MA, Lampreave F. Белки острой фазы у разных видов: обзор. 4-й Европейский коллоквиум по белкам острой фазы: Сеговия, Испания: Коллоквиум; 2003. стр. 77–82. [Google Scholar]
26. Fritz JH, Girardin SE. Как Toll-подобные рецепторы и Nod-подобные рецепторы способствуют врожденному иммунитету у млекопитающих. J Эндотоксин Res. 2005; 11: 390–4. [PubMed] [Google Scholar]
27. Мантовани А., Гарланда С., Дони А., Боттацци Б. Пентраксины во врожденном иммунитете: от С-реактивного белка до длинного пентраксина PTX3. Дж. Клин Иммунол. 2008; 28:1–13. [PubMed] [Академия Google]
28. Deban L, Jaillon S, Garlanda C, Bottazzi B, Mantovani A. Пентраксины во врожденном иммунитете: уроки PTX3. Доступно по адресу: http://www.springerlink.com/content/15818314617t51n3/abstract/ [Последний доступ 10 июля 2010 г.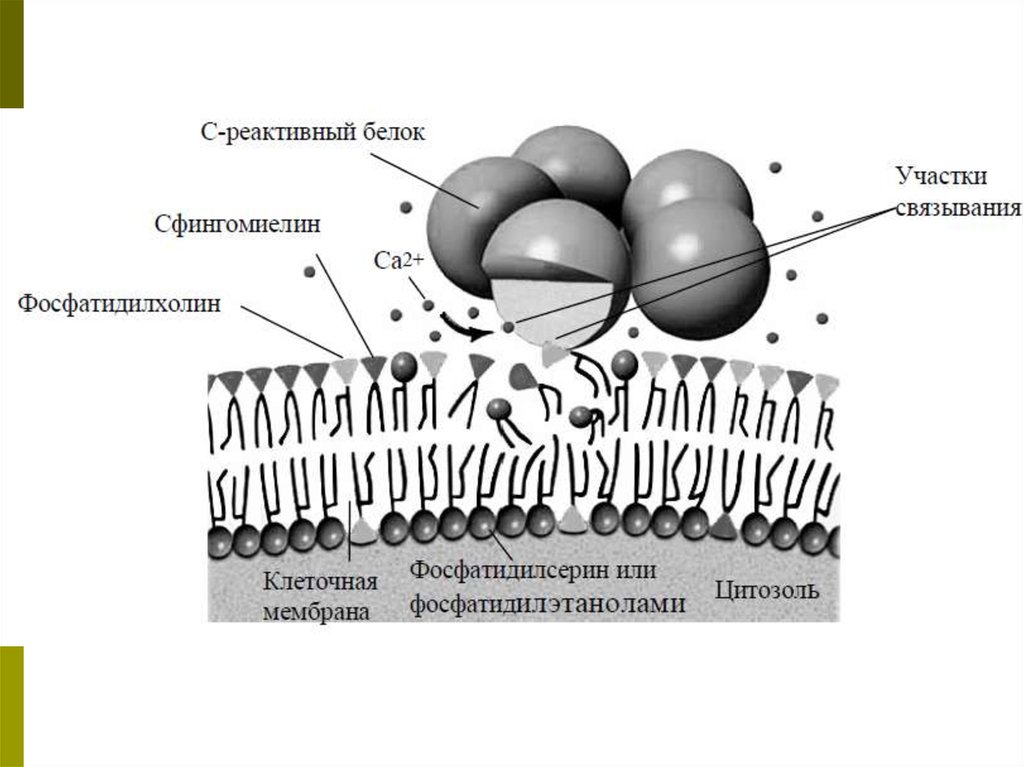 ] [PubMed]
] [PubMed]
29. Roitt IM, Delves PJ. Врожденный иммунитет: количество белков острой фазы увеличивается в ответ на инфекцию. 10-е изд. Оксфорд: Издательство Блэквелл; 1998. С. 16–7. [Google Scholar]
30. Tillet WS, Francis T. Серологические реакции при пневмонии с небелковым соматическим фрактином пневмококка. J Эксперт Мед. 1930;52:561–71. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Ridker PM. Клиническое применение С-реактивного белка для выявления и профилактики сердечно-сосудистых заболеваний. Тираж. 2003; 107: 363–9. [PubMed] [Google Scholar]
32. Danesh J, Wheeler JG, Hirschfield GM, Eda S, Eiriksdottir G, Rumley A, et al. С-реактивный белок и другие циркулирующие маркеры воспаления в прогнозе ишемической болезни сердца. N Engl J Med. 2004; 350:1387–97. [PubMed] [Академия Google]
33. Ballantyne CM, Hoogeveen RC, Bang H, Coresh J, Folsom AR, Chambless LE, et al. Липопротеин-ассоциированная фосфолипаза А2, высокочувствительный С-реактивный белок и риск развития ишемического инсульта у мужчин и женщин среднего возраста в исследовании риска атеросклероза в сообществах (ARIC). Arch Intern Med. 2005; 165: 2479–84. [PubMed] [Google Scholar]
Arch Intern Med. 2005; 165: 2479–84. [PubMed] [Google Scholar]
34. Sattar N, Murray HM, McConnachie A, Blauw GJ, Bollen EL, Buckley BM, et al. С-реактивный белок и прогнозирование ишемической болезни сердца и глобальных сосудистых событий в проспективном исследовании кровообращения правастатина у пожилых людей из группы риска (PROSPER). 2007;115:981–9. [PubMed] [Google Scholar]
35. Miller DT, Zee RY, Suk Danik J, Kozlowski P, Chasman DI, Lazarus R, et al. Ассоциация распространенных вариантов гена CRP с уровнями CRP и сердечно-сосудистыми событиями. Энн Хам Жене. 2005; 69: 623–38. [PubMed] [Google Scholar]
36. Carlson CS, Aldred SF, Lee PK, Tracy RP, Schwartz SM, Rieder M, et al. Полиморфизмы в области промотора С-реактивного белка (СРБ) связаны с уровнями СРБ в плазме. Am J Hum Genet. 2005; 77: 64–77. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Смит Г.Д., Эбрахим С. Менделевская рандомизация: перспективы, возможности и ограничения. Int J Эпидемиол. 2004; 33:30–42. [PubMed] [Google Scholar]
2004; 33:30–42. [PubMed] [Google Scholar]
38. Zacho J, Hansen AT, Jensen JS, Grande P, Sillesen H, Nordestgaard BG. Генетически повышенный уровень С-реактивного белка и ишемическая болезнь сосудов. N Engl J Med. 2008; 359:1897–908. [PubMed] [Google Scholar]
39. Yamamoto M, Katoh N, Yoshikazu A. Присутствие двух белков с низкой молекулярной массой, иммунологически связанных с амилоидом A в сыворотке 14 килодальтон, во фракции липопротеинов и их сниженные концентрации в сыворотке у телят с экспериментально индуцированным пневмония. J Vet Med Sci. 1998;60:181–187. [PubMed] [Google Scholar]
40. Хасби Г., Мархауг Г., Доутон Б., Слеттен К., Сайп Д.Д. Сывороточный амилоид А (САА): биохимия, генетика и патогенез амилоидоза АА. Амилоид: Int J Exp Clin Invest. 1994; 1:119–37. [Google Scholar]
41. Yamada T, Kluve-Beckerman B, Kuster WM, Liepnieks JJ, Benson MD. Измерение сывороточного амилоида-А4 (SAA4): его постоянное присутствие в сыворотке. Амилоид: Int J Exp Clin Invest. 1994; 1:114–8. [Google Scholar]
1994; 1:114–8. [Google Scholar]
42. Митчелл Т.И., Джеффри Дж.Дж., Палмитер Р.Д., Бринкерхофф К.Э. Реагент острой фазы сывороточного амилоида А (SAA3) является новым субстратом для деградации металлопротеиназами коллагеназой и стромелизином. Биохим Биофиз Акта. 1993;1156:245–54. [PubMed] [Google Scholar]
43. Eckersall PD, Young FJ, McComb C, Hogarth CJ, Safi S, Weber A, et al. Белки острой фазы в сыворотке и молоке молочных коров с клиническим маститом. Ветеринар Рек. 2001; 148:35–41. [PubMed] [Google Scholar]
44. McDonald TL, Larson MA, Mack DR, Weber A. Повышенная внепеченочная экспрессия и секреция связанного с молочной железой сывороточного амилоида A 3 (M-SAA3) в молозиво. Вет Иммунол Иммунопатол. 2001; 83: 203–11. [PubMed] [Академия Google]
45. Ларсон М.А., Вебер А., Вебер А.Т., Макдональд Т.Л. Дифференциальная экспрессия и секреция амилоида A3 бычьей сыворотки (SAA3) эпителиальными клетками молочной железы, стимулированными пролактином или липополисахаридом. Вет Иммунол Иммунопатол. 2005; 107: 255–64. [PubMed] [Google Scholar]
Вет Иммунол Иммунопатол. 2005; 107: 255–64. [PubMed] [Google Scholar]
46. Ларсон М.А., Вэй С.Х., Вебер А., Мак Д.Р., Макдональд Т.Л. Амилоидный пептид A3 сыворотки человека усиливает экспрессию MUC3 в кишечнике и ингибирует прилипание к EPEC. Biochem Biophys Res Commun. 2003; 300: 531–40. [PubMed] [Академия Google]
47. Ларсон М.А., Вэй С.Х., Вебер А., Макдональд Т.Л. Индукция экспрессии амилоида А3 в сыворотке молочной железы человека пролактином или липополисахаридом. Biochem Biophys Res Commun. 2003; 301:1030–7. [PubMed] [Google Scholar]
48. Mack DR, McDonald TL, Larson MA, Wei SH, Weber A. Консервативный мотив TFLK ассоциированного с молочной железой сывороточного амилоида A3 отвечает за активацию экспрессии кишечного муцина MUC3 в витро . Педиатр Рез. 2003; 53: 137–42. [PubMed] [Академия Google]
49. Ройтт И.М., Делвес П.Дж. Врожденный иммунитет: количество белков острой фазы увеличивается в ответ на инфекцию. 10-е изд. Оксфорд: Издательство Блэквелл; 2001. с. 17. [Google Scholar]
с. 17. [Google Scholar]
50. Хансен С., Холмсков Ю. Структурные аспекты коллектинов и рецепторов для них. Иммунобиология. 1998; 199: 165–89. [PubMed] [Google Scholar]
51. Отани К., Судзуки Ю., Эда С., Каваи Т., Касе Т., Ямадзаки Х. и др. Молекулярное клонирование нового человеческого коллектина из печени (CL-L1) J Biol Chem. 1999 г.;274:136–81. [PubMed] [Google Scholar]
52. Отани К., Судзуки Ю., Эда С., Каваи Т., Касе Т., Кеши Х. и др. Коллективин мембранного типа CL-P1 представляет собой рецептор-мусорщик на эндотелиальных клетках сосудов. Дж. Биол. Хим. 2001; 276:44222–8. [PubMed] [Google Scholar]
53. Korfhagen TR, LeVine AM, Whitsett JA. Ген сурфактантного белка А (SP-A) нацелен на мышей. Биохим Биофиз Акта. 1998; 1408: 296–302. [PubMed] [Google Scholar]
54. ЛеВин А.М., Гвоздз Дж., Старк Дж., Бруно М., Уитсетт Дж., Корфхаген Т. Сурфактантный белок-А усиливает клиренс респираторно-синцитиального вируса in vivo . Джей Клин Инвест. 1999; 103:1015–21. [Бесплатная статья PMC] [PubMed] [Google Scholar]
1999; 103:1015–21. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Thiel S, Jensen TV, Stover CM, Schwaeble W, Laursen SB, Poulsen K, et al. Вторая сериновая протеаза, связанная с маннан-связывающим лектином, активирует комплемент. Природа. 1997; 386: 506–10. [PubMed] [Google Scholar]
56. Aittoniemi J, Miettinen A, Laippala P, Isolauri E, Viikari J, Ruuska T, et al. Возрастные изменения концентрации маннан-связывающего белка в сыворотке крови. Акта Педиатр. 1996;85:906–9. [PubMed] [Google Scholar]
57. Gan WQ, Man SF, Senthilselvan A, Sin DD. Связь между хронической обструктивной болезнью легких и системным воспалением: системный обзор и метаанализ. грудная клетка. 2004; 59: 574–80. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Sin DD, Lacy P, York E, Man SFP. Влияние флутиказона на системные маркеры воспаления при хронической обструктивной болезни легких. Am J Respir Crit Care Med. 2004; 170:760–5. [PubMed] [Академия Google]
59. Шлеймер Р.П. Глюкокортикоиды подавляют воспаление, но щадят врожденные иммунные реакции в эпителии дыхательных путей. Proc Am Thorac Soc. 2004; 1: 222–30. [PubMed] [Google Scholar]
Шлеймер Р.П. Глюкокортикоиды подавляют воспаление, но щадят врожденные иммунные реакции в эпителии дыхательных путей. Proc Am Thorac Soc. 2004; 1: 222–30. [PubMed] [Google Scholar]
60. Walport MJ. Достижения в области иммунологии: дополнение [вторая из двух частей] N Engl J Med. 2001; 344:1140–4. [PubMed] [Google Scholar]
61. Гаджева М., Такахаши К., Тиль С. Маннан-связывающий лектин: растворимая молекула распознавания образов. Мол Иммунол. 2004;41:113–21. [PubMed] [Академия Google]
62. Ной Т.Л., Мерфи П.С., Алинк Дж.Дж., Ли М.В., Халл В.М., Сталман М.Т. и соавт. Сурфактантный белок-А и сурфактантный белок-D жидкости бронхоальвеолярного лаважа обратно пропорциональны воспалению при раннем муковисцидозе. Am J Respir Crit Care Med. 2003; 168: 685–91. [PubMed] [Google Scholar]
63. Gould JM, Weiser JN. Экспрессия С-реактивного белка в дыхательных путях человека. Заразить иммун. 2001; 69: 1747–54. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Tsuj S, Uehori J, Matsumoto M, Suzuki Y, Matsuhisa A, Toyoshima K, et al. Интелектин человека представляет собой новый растворимый лектин, который распознает галактофуранозу в углеводных цепях клеточной стенки бактерий. Дж. Биол. Хим. 2001; 276:23456–63. [PubMed] [Академия Google]
Tsuj S, Uehori J, Matsumoto M, Suzuki Y, Matsuhisa A, Toyoshima K, et al. Интелектин человека представляет собой новый растворимый лектин, который распознает галактофуранозу в углеводных цепях клеточной стенки бактерий. Дж. Биол. Хим. 2001; 276:23456–63. [PubMed] [Академия Google]
65. Le L, Chi K, Tyldesley S, Flibotte S, Diamond DL, Kuzyk MA, et al. Идентификация сывороточного амилоида А в качестве биомейкера для выявления пациентов с раком предстательной железы с поражением костей. Клин Хим. 2005; 51: 695–707. [PubMed] [Google Scholar]
66. Tecles F, Spiranelli E, Bonfanti U, Ceron JJ, Paltrileiri S. Предварительные исследования концентрации белков острой фазы в сыворотке крови при гематологических и неопластических заболеваниях у собак. J Vet Intern Med. 2005; 19: 865–70. [PubMed] [Академия Google]
67. Humblet M. Оценка белков острой фазы для раннего выбора лечения растущих луковиц, страдающих бронахопневмонией в полевых условиях. рез. вет. 2003; 77: 41–7. [PubMed] [Google Scholar]
68. Biro L, Domjan G, Falus A, Jakab L, Cseh K, Kalabay L, et al. Цитокиновая регуляция острофазовых уровней белка при множественной миеломе. Евро Джей Клин Инвест. 1998; 28: 679–86. [PubMed] [Google Scholar]
Biro L, Domjan G, Falus A, Jakab L, Cseh K, Kalabay L, et al. Цитокиновая регуляция острофазовых уровней белка при множественной миеломе. Евро Джей Клин Инвест. 1998; 28: 679–86. [PubMed] [Google Scholar]
69. Lehtolainen T, Rontvedb C, Pyrola S. Сывороточный амилоид A и TNF-α в сыворотке и молоке при экспериментальном эндотоксиновом мастите. Вет Рез. 2004; 35: 651–9.. [PubMed] [Google Scholar]
70. Пёрала С. Показатели воспаления в диагностике мастита. Вет Рез. 2003; 34: 565–78. [PubMed] [Google Scholar]
71. Mischke R, Eckersall PD. Изменения С-реактивного белка и гаптоглобина у собак с лимфатической неоплазией. 5-й Международный коллоквиум по животным белкам острой фазы Дублин: Коллоквиум; 2005. с. 35. [PubMed] [Google Scholar]
72. Gruys E, Toussaint MJ, Upragarin N, Van EA, Adewuyi AA, Candani D, et al. Острофазовые реагенты вызовут в ближайшем будущем животноводство и ветеринарию. J Zhejiang Univ Sci B. 2005; 6: 941–7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Gronlund U, Sandgren CH, Waller KP. Гаптоглобин и сывороточный амилоид А в молоке молочных коров с хроническим субклиническим маститом. Вет Рез. 2005; 36: 191–8. [PubMed] [Google Scholar]
Gronlund U, Sandgren CH, Waller KP. Гаптоглобин и сывороточный амилоид А в молоке молочных коров с хроническим субклиническим маститом. Вет Рез. 2005; 36: 191–8. [PubMed] [Google Scholar]
74. Campbella FM, Waterston M, Andersenb LO, Sorensenb NS, Heeggardb PM, Eckersella PD. Отрицательный ответ острой фазы сывороточного транстиретина после инфекции Streptocococus suis у свиней. Вет Рез. 2005; 36: 657–64. [PubMed] [Академия Google]
75. Toussaint MJ, Campbell FM, Pineiro M, Gruys E. 5 th Международный коллоквиум по белкам острой фазы животных. Дублин: Коллоквиум; 2005. Измерение отрицательных острофазовых белков для оценки острофазовых реакций при голодании; п. 14. [Google Scholar]
76. Джонсон Р.В. Ингибирование роста провоспалительными цитокинами: комплексный взгляд. J Anim Sci. 1997; 75: 1244–55. [PubMed] [Google Scholar]
77. Everett BM, Kurth T, Buring JE, Ridker PM. Относительная сила уровней С-реактивного белка и липидов как детерминант ишемического инсульта по сравнению с ишемической болезнью сердца у женщин. J Am Coll Кардиол. 2006;48:2235–42. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Am Coll Кардиол. 2006;48:2235–42. [Бесплатная статья PMC] [PubMed] [Google Scholar]
78. Джонсон Р.В., Кертис С.Е., Данцер Р., Келли К.В. Центральные и периферические простагландины вовлечены в болезненное поведение птиц. Физиол Поведение. 1993; 53: 127–31. [PubMed] [Google Scholar]
79. Джонсон Р.В., Кертис С.Е., Данцер Р., Бахр Дж.М., Келли К.В. Болезненное поведение у птиц, вызванное периферической или центральной инъекцией эндотоксина. Физиол Поведение. 1993; 53: 343–8. [PubMed] [Google Scholar]
80. Ceron JJ, Eckersall PD, Subiela SM. Белки острой фазы у собак и кошек: современные знания и перспективы на будущее. Ветеринар Клин Патол. 2005; 34: 85–9.9. [PubMed] [Google Scholar]
81. Брюинз М.Дж., Дойц Н.Е., Сотерс П.Б. Аспекты обмена белков органов, аминокислот и глюкозы в модели гиперметаболического сепсиса у свиней. Клин науч. 2003; 104: 127–41. [PubMed] [Google Scholar]
82. Ле Флок Н., Мельхиор Д., Сев Б. Важность пищевого триптофана для сохранения роста и контроля воспалительной реакции у поросят-отъемышей, подвергшихся иммунному стрессу. В: Madec F, Clement G, редакторы. Животноводство в Европе: путь вперед в меняющемся мире. Материалы промежуточного Конгресса ISAH. Сен-Мало, Франция: Коллоквиум; 2004. стр. 239.–40. [Google Scholar]
В: Madec F, Clement G, редакторы. Животноводство в Европе: путь вперед в меняющемся мире. Материалы промежуточного Конгресса ISAH. Сен-Мало, Франция: Коллоквиум; 2004. стр. 239.–40. [Google Scholar]
83. Брюинз М.Дж., Сотерс П.Б., Ламерс В.Х., Дойц Н.Е. Добавка L-аргинина у свиней снижает обмен белка в печени и увеличивает обмен белка в задней части тела как во время, так и после эндотоксемии. Am J Clin Nutr. 2002; 75: 1031–44. [PubMed] [Google Scholar]
84. Harding JC, Baarsch MJ, Murtaugh MP. Ассоциация фактора некроза опухоли и изменений реагентов острой фазы с болезнью после прибытия у свиней. J Vet Med Ser B. 1997;44:405–13. [PubMed] [Академия Google]
85. Petersen HH, Nielsen JP, Heegard PM. Применение измерений белков острой фазы в ветеринарной клинической химии. Вет Рез. 2004; 35: 163–87. [PubMed] [Google Scholar]
86. Tothova C, Nagy O, Seize H, Kovac G. Влияние хронических респираторных заболеваний на белки острой фазы и отдельные параметры белкового обмена крови у телят. Берл Мунк Tierarztl Wochenschr. 2010; 123:307–13. [PubMed] [Google Scholar]
Берл Мунк Tierarztl Wochenschr. 2010; 123:307–13. [PubMed] [Google Scholar]
87. Niewold TA, Tousaint MJ, Gruys E. 4 -й Европейский коллоквиум по белкам острой фазы. Сеговия, Испания: Коллоквиум; 2003. Мониторинг здоровья по белкам острой фазы; стр. 57–67. [Google Scholar]
1. Abdalla SA, Hiriuchi H, Furusawa S, Matsuda H. Молекулярное клонирование и характеристика лигандов надсемейства фактора некроза опухоли курицы (TNF), CD30L и TNF лиганд, индуцирующий апоптоз (TRAIL) J Vet Med Sci. 2004; 66: 643–650. doi: 10.1292/jvms.66.643. [PubMed] [CrossRef] [Академия Google]
2. Адлер К.Л., Пэн П.Х., Пэн Р.К., Класинг К.С. Кинетика уровней гемопексина и α1-кислого гликопротеина, индуцированная инъекцией воспалительных агентов у цыплят. Авиан Дис. 2001; 45: 289–296. [PubMed] [Google Scholar]
3. Алава М.А., Гонсалес-Рамон Н., Хегард П., Гузилак С., Туссен М.Дж.М., Липперхайде С., Мадек Ф., Грюйс Э. , Экерсалл П.Д., Ламприв Ф. и др. Pig-MAP, белки острой фазы свиньи и стандартизация анализов в Европе. Комп Гематол Интерн. 1997; 7: 208–213. [Академия Google]
, Экерсалл П.Д., Ламприв Ф. и др. Pig-MAP, белки острой фазы свиньи и стандартизация анализов в Европе. Комп Гематол Интерн. 1997; 7: 208–213. [Академия Google]
4. Alcorn JM, Fierer J, Chojkier M. Реакция острой фазы защищает мышей от сенсибилизации D-галактозамина к эндотоксину и фактору некроза опухоли-α Гепатология. 1992; 15: 122–129. [PubMed] [Google Scholar]
5. Alexander JW, MacMillan BG, Stinnnett JD, Ogle C, Bozian RC, Fischer JE, Oakes JB, Morris MJ, Krummel R. Благоприятные эффекты агрессивного белкового питания у детей с тяжелыми ожогами. Энн Сург. 1980; 192: 505–517. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Alsemgeest SPM. Концентрация белков острой фазы в крови крупного рогатого скота как маркеры заболевания. Утрехт, Нидерланды: Утрехтский университет; 1994. Кандидатская диссертация, ISBN: 90-3-0573-0. [Google Scholar]
7. Alsemgeest SPM, Taverne MAM, Boosman R, van der Weyden GC, Gruys E. Концентрация амилоида-А в сыворотке острой фазы перипартума в плазме крови коров и плодов. Am J Vet Res. 1993; 54: 164–167. [PubMed] [Google Scholar]
Am J Vet Res. 1993; 54: 164–167. [PubMed] [Google Scholar]
8. Alsemgeest SPM, Kalsbeek HC, Wensing T, Koeman JP, van Ederen AM, Gruys E. Концентрации сывороточного амилоида-A (SAA) и гаптоглобина (Hp) как параметры воспалительных заболеваний у крупный рогатый скот. Вет Квартал. 1994;16:21–23. [PubMed] [Google Scholar]
9. Baeten JM, Richardson BA, Bankson DD, Wener MH, Kreiss JK, Lavreys L, Mandaliya K, Bwayo JJ, McClelland RS. Использование сывороточного ретинол-связывающего белка для прогнозирования дефицита витамина А: последствия инфекции ВИЧ-1, белковая недостаточность и реакция острой фазы. Am J Clin Nutr. 2004; 79: 218–225. [PubMed] [Google Scholar]
10. Baybutt HN, Holsboer F. Ингибирование дифференцировки и функции макрофагов кортизолом. Эндокринология. 1990;127:476–480. [PubMed] [Google Scholar]
11. Blackburn WD. Валидность белков острой фазы как маркеров активности заболевания. J Ревматол. 1994; 21 (Приложение 42): 9–13. [PubMed] [Google Scholar]
12. Bonnefoy M, Ayzac L, Ingenbleek Y, Kostka T, Boisson RC, Bienvenu J. Полезность прогностического индекса воспаления и питания (PINI) у госпитализированных пожилых пациентов. Int J Vitam Nutr Res. 1998; 68: 189–195. [PubMed] [Google Scholar]
Bonnefoy M, Ayzac L, Ingenbleek Y, Kostka T, Boisson RC, Bienvenu J. Полезность прогностического индекса воспаления и питания (PINI) у госпитализированных пожилых пациентов. Int J Vitam Nutr Res. 1998; 68: 189–195. [PubMed] [Google Scholar]
13. Chamanza R, Toussaint MJM, van Ederen AM, van Veen L, Hulskamp-Koch C, Fabri TH. Сывороточный амилоид А и трансферрин у кур. Предварительное исследование использования переменных острой фазы для оценки заболеваний у цыплят. Вет Квартал. 1999;21:158–162. [PubMed] [Google Scholar]
14. Chamanza R, van Veen L, Tivapasi MT, Toussaint MJM. Белки острой фазы у домашней птицы. World's Poult Sci. 1999; 55: 61–71. doi: 10.1079/WPS199
. [CrossRef] [Google Scholar]15. Cooper EH, Ward AH. Белки-реагенты острой фазы как средства мониторинга заболевания. Инвестируйте клеточный патол. 1979; 2: 293–301. [PubMed] [Google Scholar]
16. Counotte GHM, Toussaint MJM, van Ederen AM, et al. Безопасность пищевых продуктов и реакция острой фазы. Материалы Третьего европейского колоквиума по белкам острой фазы. Каап Дорн: отделение ветеринарной патологии; 2002. ISBN: 9.0-
Материалы Третьего европейского колоквиума по белкам острой фазы. Каап Дорн: отделение ветеринарной патологии; 2002. ISBN: 9.0-
17. де Вильерс В. Дж., Лоу Дж. П., Страчан А. Ф., Эцебет С. М., Шепард EGFC, де Бир ФК. С-реактивный белок и белок амилоида А в сыворотке крови при беременности и родах. Брит Джей Обст Гинеколог. 1990; 97: 725–730. [PubMed] [Google Scholar]
18. Динарелло, Калифорния. Патогенез лихорадки при гемодиализе. Контр Нефрол. 1983; 36: 90–99. [PubMed] [Google Scholar]
19. Динарелло, Калифорния. Интерлейкин-1 и его биологически родственные цитокины. Ад Иммунол. 1989; 44: 153–205. [PubMed] [Академия Google]
20. Дисильвестро Р.А., Карлсон Г.П. Воспаление, индуктор металлотионеина, ингибирует гепатотоксичность, вызванную четыреххлористым углеродом, у крыс. Токсикол Летт. 1992; 60: 175–181. doi: 10.1016/0378-4274(92)
-L. [PubMed] [CrossRef] [Google Scholar]
21. Доутон С.Б., Колтен Х.Р. Реактанты острой фазы воспаления и инфекции. Сем Гематол. 1988; 25:84–90. [PubMed] [Google Scholar]
Сем Гематол. 1988; 25:84–90. [PubMed] [Google Scholar]
22. Даффи Л.К., Бойер Р.Т., Теста Дж.В., Фаро Дж.Б. Белки и цитокины острой фазы у млекопитающих Аляски как маркеры хронического воздействия загрязнителей окружающей среды. Am Fish Soc Symp. 1996;18:809–813. [Google Scholar]
23. Duthie S, Eckersall PD, Addie DD, Lawrence CE, Jarrett O. Значение α1-кислого гликопротеина в диагностике инфекционного перитонита кошек. Ветеринар Рек. 1997; 141: 299–303. [PubMed] [Google Scholar]
24. Eckersall PD, Harvey MJA, Ferguson JM, Renton JP, Nickson DA, Boyd JS. Белки острой фазы беременности у собак ( Canis familiaris ) J Reprod Fert. 1993; 47 (прил.): 159–164. [PubMed] [Google Scholar]
25. Eckersall PD, Young FJ, McComb C, Hogarth CJ, Safi S, Weber A, McDonald T, Nolan AM, Fitzpatrick JL. Белки острой фазы в сыворотке и молоке молочных коров с клиническим маститом. Ветеринар Рек. 2001; 148:35–41. [PubMed] [Академия Google]
26. El Beitune P, Duarte G, de Morais EN, Quintana SM, Vannucchi H. Дефицит витамина А и клинические ассоциации: обзор. Арх Латиноам Нутр. 2003; 53: 355–363. [PubMed] [Google Scholar]
Дефицит витамина А и клинические ассоциации: обзор. Арх Латиноам Нутр. 2003; 53: 355–363. [PubMed] [Google Scholar]
27. Эль Гхмати С.М., ван Хоивельд Э.М., ван Страйп Дж.Г., Сеуппенс Дж.Л., Стивенс Э.А. Идентификация гаптоглобина как альтернативного лиганда для CD11B/CD18. Дж Иммунол. 1996;156:2542–2552. [PubMed] [Google Scholar]
28. Ferard G, Gaudias J, Bourguignat A, Ingenbleek Y. Соотношение C-реактивного белка и транстиретина для ранней диагностики и последующего наблюдения за послеоперационной инфекцией. Clin Chem Lab Med. 2002;40:1334–1338. doi: 10.1515/CCLM.2002.230. [PubMed] [CrossRef] [Академия Google]
29. Функе С., Кинг Д.П., Братидж Р.М., Аделунг Д., Скотт Дж.Л. Тюлень обыкновенный ( phoca vitulina ) С-реактивный белок (C-RP): очистка, характеристика специфических моноклональных антител и разработка иммунологического анализа для измерения концентрации C-RP в сыворотке. Вет Иммунол Иммунопатол. 1997; 59: 151–162. doi: 10.1016/S0165-2427(97)00059-7. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
30. Glass EJ, Craigmile SC, Springbett A, Preston PM, Kirvar E, Wilkie GM, Eckersall PD, Hall FR, Brown CG. Протозойный паразит Theileria annulata индуцирует у крупного рогатого скота отчетливую острую белковую реакцию, связанную с патологией. Int J Паразитол. 2003;33:1409–1418. doi: 10.1016/S0020-7519(03)00166-8. [PubMed] [CrossRef] [Google Scholar]
31. Goff JP, Stabel JR. Снижение концентрации ретинола, α-токоферола и цинка в плазме в периродовой период: эффект молочной лихорадки. Дж. Молочная наука. 1990;73:3195–3199. [PubMed] [Google Scholar]
32. Гордон А.Х., Кой А. Реакция острой фазы на травму и инфекцию. Роли интерлейкина 1 и других медиаторов. Амстердам: Эльзевир; 1985. ISBN: 0444-80648-2. [Академия Google]
33. Gruys E. Белки острой фазы в медицине крупного рогатого скота; Примечания к Конвенции AVMA 2002. Труды 2002 г. Американской ветеринарной медицинской ассоциации; Нэшвилл. 2002. стр. 317–321. [Google Scholar]
34. Gruys E, Snel FWJJ. Животные модели реактивного амилоидоза. Клинический ревматолог Байьера. 1994; 8: 599–611. [PubMed] [Google Scholar]
Gruys E, Snel FWJJ. Животные модели реактивного амилоидоза. Клинический ревматолог Байьера. 1994; 8: 599–611. [PubMed] [Google Scholar]
35. Gruys E, Obwolo MJ, Toussaint MJM. Диагностическое значение основных белков острой фазы в ветеринарной клинической химии: обзор. Вет Булл. 1994;64:1009–1018. [Google Scholar]
36. Gruys E, Tooten PCJ, Kuijpers MHM. Легкие, подвздошная кишка и сердце являются местами предрасположенности к отложению амилоида AApoAII у мышей CD-1 Swiss, используемых для исследований токсичности. Легочный амилоид указывает на AApoAII. Лаборатория Аним. 1996; 30: 28–34. [PubMed] [Google Scholar]
37. Gruys E, Toussaint MJM, Landman WJM, et al. Инфекция, воспаление и стресс препятствуют росту. Механизмы и неспецифическая оценка процессов белками острой фазы. В: Венсинг Т., редактор. Производственные болезни сельскохозяйственных животных. 10-я Международная конференция, 1998. Вагенинген: Вагенинген Пресс; 1999. С. 72–87. ISBN: 90-74134-60-2. [Google Scholar]
38. Hallquist NA, Klasing KC. Уровни серотрансферрина, овотрансферрина и металлотионеина во время иммунного ответа у кур. Comp Biochem Physiol Biochem Mol Biol. 1994; 108: 375–384. doi: 10.1016/0305-0491(94)
Hallquist NA, Klasing KC. Уровни серотрансферрина, овотрансферрина и металлотионеина во время иммунного ответа у кур. Comp Biochem Physiol Biochem Mol Biol. 1994; 108: 375–384. doi: 10.1016/0305-0491(94)
39. Heinrich PC, Castell TA, Andus T. Интерлейкин-6 и ответ острой фазы. Биохим Дж. 1990; 265:621–636. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Heinrich PC, Behrmann I, Müller-Newen G, Schaper F, Graeve L. Передача сигналов цитокинов типа интерлейкина-6 через путь gp130/Jak/STAT. Биохим Дж. 1998; 334:297–314. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Höfner MC, Fosbery MW, Eckersall PD, Donaldson AI. Гаптоглобиновый ответ крупного рогатого скота, инфицированного вирусом ящура. рез. вет. 1994; 57: 125–128. [PubMed] [Google Scholar]
42. Hulten C, Sandgren B, Skioldebrand E, Klingeborn B, Marhaug G, Forsberg M. Белок острой фазы сывороточного амилоида A (SAA) как маркер воспаления при заражении вирусом гриппа лошадей. Акта Вет Сканд. 1999;40:323–333. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Акта Вет Сканд. 1999;40:323–333. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Husby G, Marhaug G, Dowton B, Sletten K, Sipe JD. Сывороточный амилоид А (САА): биохимия, генетика и патогенез АА амилоидоза. Амилоид: Int J Exp Clin Invest. 1994; 1:119–137. [Google Scholar]
44. Husebekk A, Skogen B, Husby G, Marhaug G. Трансформация предшественника амилоида SAA в белок AA и включение в амилоидные фибриллы in vivo. Сканд Дж. Иммунол. 1985; 21: 283–287. [PubMed] [Академия Google]
45. Ингенблек Ю., Карпентье Ю.А. Прогностический индекс воспаления и питания для критически больных пациентов. Int J Vit Nutrit Res. 1985; 55: 91–101. [PubMed] [Google Scholar]
46. Ingenbleek M, Young V. Транстиретин (преальбумин) в норме и болезни: последствия для питания. Энн Рев Нутр. 1994; 14: 495–533. doi: 10.1146/annurev.nu.14.070194.002431. [PubMed] [CrossRef] [Google Scholar]
47. Ingenbleek Y, Bernstein LH. Зависимая от питания адаптивная дихотомия (NDAD) и стрессовый гиперметаболизм. J Clin Lig Ass. 1999;22:259–267. [Google Scholar]
48. Ingenbleek Y, Bernstein LH. Стрессовое состояние как алиментарно-зависимая адаптивная дихотомия. Питание. 1999;15:305–320. doi: 10.1016/S0899-9007(99)00009-X. [PubMed] [CrossRef] [Google Scholar]
49. Jacquier-Sarlin MR, Fuller K, Dinx-Xuan AT, Richard MJ, Polla BS. Защитные эффекты HSP70 при воспалении. Опыт. 1994; 50:1032–1038. doi: 10.1007/BF01923458. [PubMed] [CrossRef] [Google Scholar]
50. Джонсон Р.В. Ингибирование роста провоспалительными цитокинами: комплексный взгляд. J Anim Sci. 1997;75:1244–1255. [PubMed] [Google Scholar]
51. Джонсон Р.В., Борелл Э. Болезненное поведение свиней, вызванное липополисахаридами, подавляется предварительной обработкой индометацином. J Anim Sci. 1994; 72: 309–314. [PubMed] [Google Scholar]
52. Джонсон Р.В., Кертис С.Е., Данцер Р., Келли К.В. Центральные и периферические простагландины вовлечены в болезненное поведение птиц. Физиол Поведение. 1993; 53: 127–131. doi: 10.1016/0031-9384(93)
-G. [PubMed] [CrossRef] [Google Scholar]
53. Джонсон Р.В., Кертис С.Е., Данцер Р., Бахр Дж.М., Келли К.В. Болезненное поведение у птиц, вызванное периферической или центральной инъекцией эндотоксина. Физиол Поведение. 1993;53:343–348. doi: 10.1016/0031-9384(93)
-2. [PubMed] [CrossRef] [Google Scholar]54. Kaiser P, Rothwell L, Goodchild M, Bumstead N. Куриные провоспалительные цитокины интерлейкин-1 бета и интерлейкин-6: различия в структуре генов и генетической локализации по сравнению с их млекопитающими. ортологи. Аним Жене. 2004; 35: 169–175. doi: 10.1111/j.1365-2052.2004.01121.x. [PubMed] [CrossRef] [Google Scholar]
55. Kaiser P, Poh TY, Rothwell L, Avery S, Balu S, Pathiana US, Hughes S, Goodchild M, Morrell S, Watson M, et al. Геномный анализ куриных цитокинов и хемокинов. J Интерферон Цитокин Res. 2005; 25: 467–484. дои: 10.1089/ джир. 2005.25.467. [PubMed] [CrossRef] [Google Scholar]
56. Kimura M, Toth LA, Agostini H, Cady AB, Majde JA, Krueger JM. Сравнение ответов острой фазы, индуцированных у кроликов липополисахаридом и двухцепочечной РНК. Am J Physiol Reg Int Comp Physiol. 1995; 36: 1596–1605. [PubMed] [Google Scholar]
57. Кисилевский Р., Груйс Э., Ширахама Т. Существует ли фактор усиления амилоида (AEF)? Является ли AEF единой биологической сущностью? Амилоид: Int J Exp Clin Invest. 1994; 2: 128–133. [Академия Google]
58. Knolle P, Lohr H, Treichel U, Dienes HP, Lohse A, Schlaack J, Gerken G. Паренхиматозные и непаренхиматозные клетки печени и их взаимодействие в местном иммунном ответе. Zeitschr Гастроэнтерол. 1995; 33: 613–620. [PubMed] [Google Scholar]
59. Koets AP, de Schwartz N, Tooten P, Kankofer M, Broekhuijsen-Davies JM, Rutten VPMG, van Leengoed LAMG, Taverne MAM, Gruys E. Высвобождение провоспалительных цитокинов, связанных с лютеолизом и реакция острой фазы перед родами при индуцированных простагландинами родах у коров. Териогенология. 1998;49:797–812. doi: 10.1016/S0093-691X(98)00029-6. [PubMed] [CrossRef] [Google Scholar]
60. Kraft R, Ruchti C, Burkhardt AH, Cottier H. Патогенетические принципы развития кишечного инфекционно-токсического шока (GITS) и полиорганной недостаточности. Cur Stud Haematol Blood Transfus. 1992; 59: 204–240. [PubMed] [Google Scholar]
61. Kushner I, Gewurz H, Benson MD. С-реактивный белок и острофазовый ответ. J Lab Clin Med. 1981; 97: 739–749. [PubMed] [Академия Google]
62. Landman WJM, Sletten K, Koch CAM, Tooten PCJ, Gruys E. Амилоидный белок куриного сустава относится к SAA-типу. I. Характеристика амилоидного белка. Сканд Дж. Иммунол. 1996; 43: 210–218. doi: 10.1046/j.1365-3083.1996.d01-31.x. [PubMed] [CrossRef] [Google Scholar]
63. Langhans W. Бактериальные продукты и контроль пищевого поведения: клинические последствия. Питание. 1996; 12: 303–315. doi: 10.1016/S0899-9007(96)80052-9. [PubMed] [CrossRef] [Google Scholar]
64. Ланнергард А., Ларссон А., Крагсбьерг П., Фриман Г. Корреляции между сывороточным амилоидным белком А и С-реактивным белком при инфекционных заболеваниях. Scand J Clin Lab Invest. 2003; 63: 267–272. [PubMed] [Академия Google]
65. Ларсон М.А., Вэй С.Х., Вебер А., Мак Д.Р., Макдональд Т.Л. Амилоидный пептид A3 сыворотки человека усиливает экспрессию MUC3 в кишечнике и ингибирует прилипание к EPEC. Biochem Biophys Res Commun. 2003; 300: 531–540. doi: 10.1016/S0006-291X(02)02901-7. [PubMed] [CrossRef] [Google Scholar]
66. Ларсон М.А., Вэй С.Х., Вебер А., Макдональд Т.Л. Индукция экспрессии амилоида А3 в сыворотке молочной железы человека пролактином или липополисахаридом. Biochem Biophys Res Commun. 2003; 301:1030–1037. дои: 10.1016/S0006-291Х(03)00045-7. [PubMed] [CrossRef] [Google Scholar]
67. Ларсон М.А., Вебер А., Вебер А.Т., Макдональд Т.Л. Дифференциальная экспрессия и секреция амилоида A3 бычьей сыворотки (SAA3) эпителиальными клетками молочной железы, стимулированными пролактином или липополисахаридом. Вет Иммунол Иммунопатол. 2005; 107: 255–264. doi: 10.1016/j.vetimm.2005.05.006. [PubMed] [CrossRef] [Google Scholar]
68. Le J, Vilcek J. Интерлейкин 6: многофункциональный цитокин, регулирующий иммунные реакции и белковый ответ острой фазы. Лаборатория Инвест. 1989;61:588–602. [PubMed] [Google Scholar]
69. Лещинский Т.В., Класинг К.С. Профиль куриных цитокинов, индуцированный липополисахаридом, модулируется диетическим ацетатом альфа-токоферола. наук о птицеводстве. 2003; 82: 1266–1273. [PubMed] [Google Scholar]
70. Linke RP, Bock V, Valet G, Rothe G. Ингибирование реакции окислительного взрыва нейтрофилов, стимулированных N-формилпептидом, сывороточным амилоидным белком-A. Biochem Biophys Res Commun. 1991;176:1100–1105. doi: 10.1016/0006-291X(91)
-P. [PubMed] [CrossRef] [Академия Google]71. Loyer P, Iiyin G, Razzak ZA, Banchereau J, Dezier JF, Campion JP, Guguenguillouzo C, Guillouzo A. Интерлейкин-4 ингибирует выработку некоторых белков острой фазы гепатоцитами человека в первичной культуре. Письма ФЭБС. 1993; 336: 215–220. doi: 10.1016/0014-5793(93)80806-6. [PubMed] [CrossRef] [Google Scholar]
72. Lynagh GR, Bailey M, Kaiser P. Интерлейкин-6 продуцируется как мышиными, так и птичьими инфекциями Eimeria . Вет Иммунол Иммунопатол. 2000; 76: 98–102. [PubMed] [Академия Google]
73. Mack DR, McDonald TL, Larson MA, Wei SH, Weber A. Консервативный мотив TFLK ассоциированного с молочной железой сывороточного амилоида A3 отвечает за активацию экспрессии кишечного муцина MUC3 in vitro. Педиатр Рез. 2003; 53: 137–142. doi: 10.1203/01.PDR.0000041517.15440.F3. [PubMed] [CrossRef] [Google Scholar]
74. Magnus JH, Stenstad T, Husby G. Протеогликаны, гликозаминогликаны и отложение амилоида. Клинический ревматолог Байьера. 1994; 8: 575–597. [PubMed] [Академия Google]
75. Майно Г., Йорис И. Клетки, ткани и болезни. Принципы общей патологии. Кембридж Массачусетс, США: Blackwell Science; 1996. С. 487–496. 0-86542-372-5. [Google Scholar]
76. Мазур-Гонковская Б., Концицкий А., Краснодебская-Депта А. Оценка реакции острой фазы у индеек, экспериментально зараженных Escherichia coli или вирусом геморрагического энтерита. Bull Vet Inst Pulawy. 2004; 48:19–23. [Google Scholar]
77. Макдональд Т.Л., Ларсон М.А., Мак Д.Р., Вебер А. Повышенная внепеченочная экспрессия и секреция связанного с молочной железой сывороточного амилоида A 3 (M-SAA3) в молозиво. Вет Иммунол Иммунопатол. 2001; 83: 203–211. doi: 10.1016/S0165-2427(01)00380-4. [PubMed] [CrossRef] [Академия Google]
78. McGuire W, Alessandro UD, Olaleye BO, Thomson MC, Langerock P, Greenwood BM, Kwiatkowski D. C-реактивный белок и гаптоглобин в оценке программы борьбы с малярией на базе сообщества. Transact Royal Soc Trop Med Hyg. 1996; 90:10–14. doi: 10.1016/S0035-9203(96)
-7. [PubMed] [CrossRef] [Google Scholar]79. Mitchell TI, Jeffrey JJ, Palmiter RD, Brinckerhoff CE. Реагент острой фазы сывороточного амилоида А (SAA3) является новым субстратом для деградации металлопротеиназами коллагеназой и стромелизином. Биохим Биофиз Акта. 1993;1156:245–254. [PubMed] [Google Scholar]
80. Monshouwer M, Witkamp RF, Nijmeijer SM, van Leengoed LAMG, Verheyden JHM, van Miert ASJPAM. Инфекционное ( Actinobacillus pleuropneumoniae ) опосредованное подавление окислительного метаболизма лекарств в печени и уровней мРНК цитохрома P4503A у свиней. Препарат Метабол Dispos. 1995; 23:44–47. [PubMed] [Google Scholar]
81. Monshouwer M, Witkamp RF, Nijmeijer SM, Pijpers A, Verheyden JHM, van Miert ASJPAM. Избирательные эффекты бактериальной инфекции ( Actinobacillus pleuropneumoniae ) на печеночный клиренс кофеина, антипирина, парацетамола и индоцианина зеленого у свиней. Ксенобиотика. 1995; 25: 491–499. [PubMed] [Google Scholar]
82. Monshouwer M, Witkamp RF, Nijmeijer SM, van Leengoed LAMG, Vernooy HCM, Verheyden JHM, van Miert ASJPAM. Липополисахарид-индуцированный острофазовый ответ у свиней связан со снижением печеночного цитохрома Р450-опосредованного метаболизма лекарств. J Vet Pharmacol Терапия. 1996; 19: 382–388. [PubMed] [Академия Google]
83. Monshouwer M, Witkamp RF, Nijmeijer SM, van Amsterdam JG, van Miert ASJPAM. Подавление активности цитохрома Р450- и УДФ-глюкуронозилтрансферазы-зависимых ферментов провоспалительными цитокинами и возможным оксидом азота в первичных культурах гепатоцитов свиньи. Toxicol Appl Pharmacol. 1996; 137: 237–244. doi: 10.1006/taap.1996.0077. [PubMed] [CrossRef] [Google Scholar]
84. Morgan ET. Регуляция цитохромов Р450 при воспалении и инфекции. Препарат Метабол Ред. 1997;29:1129–1188. [PubMed] [Google Scholar]
85. Morgan ET, Thomas KB, Swanson R, Vales T, Hwang J, Wright K. Избирательное подавление экспрессии гена цитохрома P-450 интерлейкинами 1 и 6 в печени крыс. Биохим Биофиз Акта. 1994;1219:475–483. [PubMed] [Google Scholar]
86. Morlese JF, Forrester T, Jahoor F. Белковая реакция острой фазы на инфекцию при тяжелом недоедании. Am J Physiol Endocrinol Metabol. 1998; 38: E112–E117. [PubMed] [Google Scholar]
87. Набуурс М. Микробиологические, структурные и функциональные изменения тонкого кишечника поросят при отъеме. Новости свиней Информ. 1995;16:93С–97С. [Google Scholar]
88. Nakamura K, Mitarai Y, Yoshioka M, Koizumi N, Shibahara T, Nakajima Y. Сывороточные уровни интерлейкина-6, α1-кислого гликопротеина и кортикостерона у двухнедельных цыплят, привитых . Липополисахарид Escherichia coli . наук о птицеводстве. 1998; 77: 908–911. [PubMed] [Google Scholar]
89. Накаяма Т., Сонода С., Урано Т., Ямада Т., Окада М. Мониторинг сывороточного белка А и С-реактивного белка как маркеров воспаления при инфекционных заболеваниях. Клин Хим. 1993;39:293–297. [PubMed] [Google Scholar]
90. Odink J, Smeets JFM, Visser IJR, Sandman H, Snijders JMA. Гематологические и клинико-химические профили здоровых свиней и свиней с воспалительными процессами. J Anim Sci. 1990; 68: 163–170. [PubMed] [Google Scholar]
91. Patterson LT, Mora EC. Появление в крови домашней птицы субсиансового аналога С-реактивного белка. Техас Rep Biol Med. 1964; 22: 716–721. [PubMed] [Google Scholar]
92. Patterson LT, Mora EC. Реакция С-реактивного белка и устойчивость к болезням домашней птицы. Техас Rep Biol Med. 1965;23:600–606. [PubMed] [Google Scholar]
93. Pepys MB. С-реактивный белок пятьдесят лет спустя. Ланцет. 1981; 21: 653–656. doi: 10. 1016/S0140-6736(81)91565-8. [PubMed] [CrossRef] [Google Scholar]
94. Petersen HH, Nielsen JP, Heegaard PMH. Применение измерений белков острой фазы в ветеринарной клинической химии. Вет Рез. 2004; 35: 163–187. doi: 10.1051/vetres:2004002. [PubMed] [CrossRef] [Google Scholar]
95. Пинелли Э. Защитные иммунные реакции против Leishmania у собак. Утрехт, Нидерланды: Утрехтский университет; 1996. Кандидатская диссертация, ISBN: 90-
02-8. [Google Scholar]96. Pue CA, Mortensen RF, Marsh CB, Pope HA, Webers MD. Уровни С-реактивного белка в острой фазе увеличивают продукцию IL-1β и IL-1ra моноцитами крови человека, но подавляют продукцию IL-1β и IL-ra альвеолярными макрофагами. Дж Иммунол. 1996; 156: 1594–1600. [PubMed] [Google Scholar]
97. Пёрала С. Университет Хельсинки; 2000. Диссертация Хирвонена об острой фазе реакции у молочного скота. ISBN: 951-45-9106-2 (Доступно по адресу: http://ethesis.helsinki.fi/julkaisut/ela/kliin/hirvonen/) [Google Scholar]
98. Reeds PJ, Fjeld CR, Jahoor F. Влияют ли различия между аминокислотным составом острофазовых и мышечных белков на потерю азота при травматических состояниях? Дж Нутр. 1994; 124:906–910. [PubMed] [Google Scholar]
99. Schindler R, Mancilla J, Endres S, Ghorbani R, Clark SC, Dinarello CA. Корреляции и взаимодействия в продукции интерлейкина-6 (ИЛ-6), ИЛ-1 и фактора некроза опухоли (ФНО) в мононуклеарных клетках крови человека: ИЛ-6 подавляет ИЛ-1 и ФНО. Кровь. 1990;75:40–47. [PubMed] [Google Scholar]
100. Schroedl W, Fuerll B, Reinhold P, Krueger M, Schuett C. Новый маркер острой фазы у крупного рогатого скота: липополисахарид-связывающий белок (LBP) J Endotoxin Res. 2001; 7: 49–52. doi: 10.1179/096805101101532530. [PubMed] [CrossRef] [Google Scholar]
101. Sehgal PB, Grieninger G, Tosato G. Регуляция острой фазы и иммунных ответов: интерлейкин-6. Энн Нью-Йоркская академия наук. 1989; 557:1–583. [PubMed] [Google Scholar]
102. Sijben JW, Klasing KC, Schrama JW, Parmentier HK, van der Poel JJ, Savelkoul HF, Kaiser P. Ранняя экспрессия генов цитокинов in vivo у цыплят после заражения Salmonalla typhymirium липополисахарид и модуляция диетическими n-3 полиненасыщенными жирными кислотами. Дев Комп Иммунол. 2003; 27: 611–619. doi: 10.1016/S0145-305X(03)00031-4. [PubMed] [CrossRef] [Google Scholar]
103. Sipe JD. Белки острой фазы при остеоартрозе. Сем Артр Реум. 1995; 25:75–86. doi: 10.1016/S0049-0172(95)80020-4. [PubMed] [CrossRef] [Google Scholar]
104. Smith DJ, Roberts D. Влияние больших объемов и/или интенсивных упражнений на отдельные параметры химии крови. Клин Биохим. 1994;27:435–440. doi: 10.1016/0009-9120(94)00055-Z. [PubMed] [CrossRef] [Google Scholar]
105. Сордилло Л.М., Пигетти Г.М., Дэвис М.Р. Повышенная продукция бычьего фактора некроза опухоли-а в периродовой период. Вет Иммунол Иммунопатол. 1995; 49: 263–270. doi: 10.1016/0165-2427(95)05465-0. [PubMed] [CrossRef] [Google Scholar]
106. Stephensen CB. Инфекционное бремя при нарушении роста. Дж Нутр. 1999; 129 (прил.): 534S–538S. [PubMed] [Google Scholar]
107. Stephensen CB. Витамин А, инфекция и иммунная функция. Анну Рев Нутр. 2001; 21: 167–19.2. doi: 10.1146/annurev.nutr.21.1.167. [PubMed] [CrossRef] [Google Scholar]
108. Stephensen CB, Gildengorin G. Ретинол в сыворотке, реакция острой фазы и очевидная неправильная классификация статуса витамина А в третьем Национальном обзоре исследований здоровья и питания. Am J Clin Nutr. 2000;72:1170–1178. [PubMed] [Google Scholar]
109. Takahashi K, Ohta N, Akiba Y. Влияние диетического метионина и цистеина на метаболические реакции на иммунологический стресс при инъекции липополисахарида Escherichia coli и митогенный ответ у цыплят-бройлеров. Бр Дж Нутр. 1997;78:815–821. doi: 10.1079/BJN19970197. [PubMed] [CrossRef] [Google Scholar]
110. Tape C, Tan R, Nesheim M, Kisilevsky R. Прямые доказательства того, что циркулирующий апоSAA является предшественником отложений амилоида AA в тканях. Сканд Дж. Иммунол. 1987; 28: 317–324. [PubMed] [Google Scholar]
111. Tillett WS, Francis T. Серологические реакции при пневмонии с небелковой соматической фракцией Pneumococcus . J Эксперт Мед. 1930; 52: 561–571. doi: 10.1084/jem.52.4.561. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
112. Tohjo H, Miyoshi F, Uchida E, Niiyama M, Syuto B, Moritsu Y, Ichikawa S, Takeauchi M. Электрофоретические модели куриной сыворотки в полиакриламидном геле при остром воспалении, вызванном внутримышечной инъекцией скипидара. наук о птицеводстве. 1995; 74: 648–655. [PubMed] [Google Scholar]
113. Tohjo H, Yadatsu M, Uchida E, Niiyama M, Syuto B, Moritsu Y, Ichikawa S, Takeuchi M. Электрофоретическая картина белков сыворотки в полиакриламидном геле при остром воспалении, вызванном внутримышечной инъекцией скипидара. у молодых цыплят-бройлеров. J Vet Med Sci. 1996;58:267–268. [PubMed] [Google Scholar]
114. Туссен MJM. Белок острой фазы у разных видов измеряется как инструмент для оценки здоровья животных. Отчет Европейского коллоквиума. 2000; 1:1–3. [Google Scholar]
115. Toussaint MJM, van Ederen AM, Gruys E. Значение клинической патологии в оценке здоровья животных, в животноводстве и проверке мяса. Комп Гематол Интерн. 1995; 5: 149–157. doi: 10.1007/BF00368037. [CrossRef] [Google Scholar]
116. Toussaint MJM, van Ederen AM, Hulskamp-Koch CAM, Gruys E. Измерение белков острой фазы в свиной крови как инструмент для клинической патологии у свиней. Комп Гематол Интерн. 1997;7:182. [Google Scholar]
117. Toussaint MJM, Eckersall PD, Alava M, Madec F, Meloen RH, Gruys E. Анализ белка в острой фазе как инструмент оценки здоровья свиней. проц. Конгресс ISACB Тулуза. Преподобный Вет Мед. 2000;151:780. [Google Scholar]
118. Toussaint MJM, Lipperheide C, Eckersall PD, et al. Оценка здоровья свиней с помощью анализа белка в острой фазе. В: Tielen MJM, Voets MT, редакторы. Материалы X -го Международного конгресса по гигиене животных. Том. 1. Бокстель, Нидерланды: Центр ветеринарных услуг; 2000. С. 139.–143. ISBN: 90-71649-04-0. [Google Scholar]
119. Учида Э., Катох Н., Такахаши К. Появление гаптоглобина в сыворотке крови коров при родах. J Vet Med Sci. 1993; 55: 893–894. [PubMed] [Google Scholar]
120. Упрагарин Н. Исследования патогенеза АА-амилоидной артропатии у кур in vitro. Утрехт, Нидерланды: 2005 г. Кандидатская диссертация, ISBN: 90-393-4038-2. [Google Scholar]
121. van Gool J, Boers W, Sala M, Ladiges NCJJ. Глюкокортикоиды и катехоламины как медиаторы белков острой фазы, особенно α-макрофетопротеина крысы. Биохим Дж. 1984;220:125–132. [Бесплатная статья PMC] [PubMed] [Google Scholar]
122. van Miert ASJPAM. Провоспалительные цитокины на модели жвачных животных: патофизиологические, фармакологические и терапевтические аспекты. Вет Квартал. 1995; 175:41–50. [PubMed] [Google Scholar]
123. van Reeth K, Nauwynck H, Pensaert M. Бронхоальвеолярный интерферон-альфа, фактор некроза опухоли-альфа, интерлейкин-1 и воспаление во время острого гриппа у свиней: возможная модель для человека? J заразить Dis. 1998; 177: 1076–1079.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
124. Верлинг Д., Саттер Ф., Арнольд М., Кун Г., Тутен П.С.Дж., Грюйс Э. Характеристика острофазового ответа телок на длительное введение низких доз липополисахарида . рез. вет. 1996; 61: 252–257. doi: 10.1016/S0034-5288(96)
-9. [PubMed] [CrossRef] [Google Scholar]125. West KP. Дефицит витамина А как предотвратимая причина материнской смертности в обществах, страдающих от недоедания: вероятность и последующие шаги. Int J Gynaecol Obstet. 2004; 85: С24–С27. doi: 10.1016/j.ijgo.2004.02.008. [PubMed] [CrossRef] [Академия Google]
126. Xie H, Huff GR, Huff WE, Balog JM, Holt P, Rath NC. Идентификация овотрансферрина как белка острой фазы у кур. наук о птицеводстве. 2002; 81: 112–120. [PubMed] [Google Scholar]
127. Yamada T, Kluve-Beckerman B, Kuster WM, Liepnieks JJ, Benson MD. Измерение сывороточного амилоида-А4 (SAA4): его постоянное присутствие в сыворотке. Амилоид: Int J Exp Clin Invest.