2011-2017 © МБУЗ ГКП № 7, г.Челябинск.
Что такое ВИЧ?
Вирус иммунодефицита человека – ВИЧ - относится к семейству ретровирусов, подсемейство лентивирусов. Как и другие лентивирусы (например, вирус гепатита С) ВИЧ вызывает в организме длительный инфекционный процесс, часто протекающий скрыто, но в то же время эти вирусы имеют выраженную наклонность к мутациям (изменение генотипа), в связи с чем на данном этапе возникают сложности в изготовлении вакцины против этих инфекций и при лечении.
Что делает ВИЧ в организме?
Размножение ВИЧ в организме связано с клетками, на поверхности которых находится рецептор СД-4. Этот рецептор имеют в основном Т-лимфоциты, циркулирующие в крови, поэтому их называют СД-4 лимфоциты (или СД-4 клетки).
Эти лимфоциты играют важную роль в иммунной системе, в защите организма от инфекций. Попав в организм человека, вирус ВИЧ, содержащий 2 нити РНК, встречает СД-4 клетки, прикрепляется к ним, после чего поверхности клетки и вируса сливаются.
РНК вируса проникает в клетку хозяина и благодаря ферменту обратная транскриптаза, превращается в ДНК – «образуется» провирус ВИЧ. Затем с помощью фермента интеграза ДНК вируса интегрирует в ДНК клетки-хозяина, формируется матрица. Благодаря ферменту протеаза с преобразованной матрицы образуется множество новых вирусных частиц.
Как возникает иммунодефицит?
Полный жизненный цикл вируса реализуется за 1-2 сутки, в день может образоваться до 1 млрд. вирусных частиц. С одной стороны, размножение вируса в клетках иммунной системы ведет постепенно к гибели этих клеток, в то же время ВИЧ-инфекция, являясь вирусной инфекцией, оказывает хроническое возбуждающее действие на иммунную систему, что ведет к истощению клеток иммунитета.
Постепенно уменьшается количество СД-4 клеток и способность иммунной системы противостоять отдельным внешним и внутренним врагам (микроорганизмам, опухолевым клеткам), развивается иммунодефицит.
Состояние иммунитета показывает иммунный статус, который определяется количеством СД-4 лимфоцитов в 1 мл.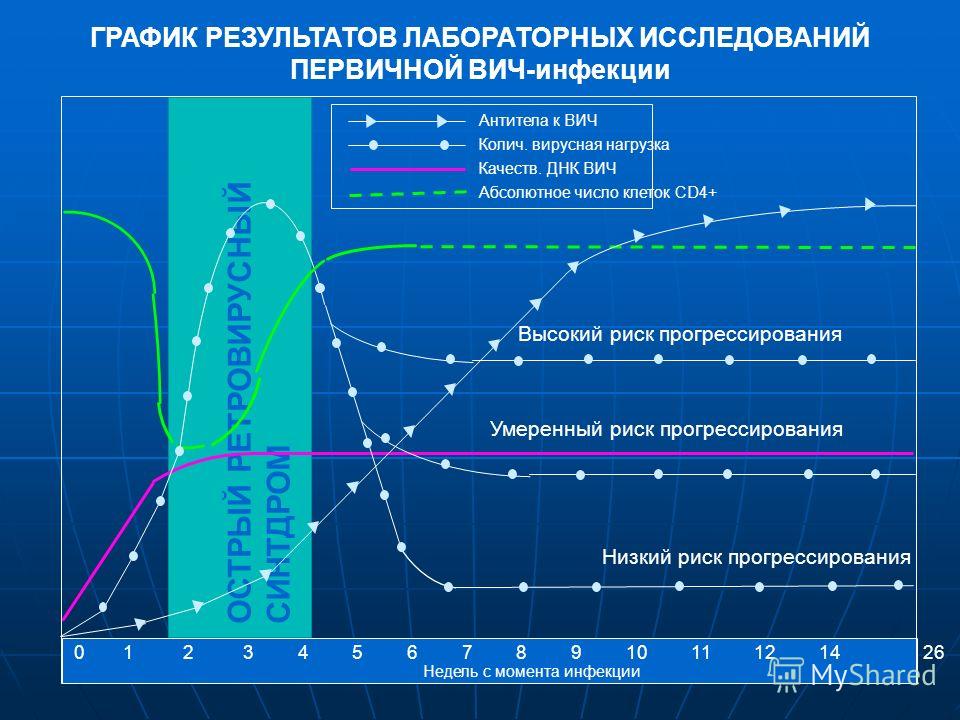 крови. У здорового человека в 1 мл содержится 800-1200 СД-4 клеток. У ВИЧ-инфицированных пациентов при благоприятном течении заболевания уровень СД-4 лимфоцитов более 500 в 1 мл. Снижение иммунного статуса до 200 клеток и ниже создает опасность развития |угрожающих жизни заболеваний – оппортунистических инфекций.
крови. У здорового человека в 1 мл содержится 800-1200 СД-4 клеток. У ВИЧ-инфицированных пациентов при благоприятном течении заболевания уровень СД-4 лимфоцитов более 500 в 1 мл. Снижение иммунного статуса до 200 клеток и ниже создает опасность развития |угрожающих жизни заболеваний – оппортунистических инфекций.
Как развивается ВИЧ-инфекция?
ВИЧ-инфекция характеризуется многолетним течением, клинически связанным с прогрессирующим снижением иммунитета, приводящим к развитию оппортунистических заболеваний и опухолей.
Выделяют несколько стадий в развитии ВИЧ-инфекции:
 В этот период антитела к ВИЧ, как правило, отсутствуют. Но диагноз ВИЧ-инфекция можно установить, обнаружив сам вирус в крови, его генный материал и антигены. Через 2 недели от начала острых проявлений в крови начинают появляться антитела.
В этот период антитела к ВИЧ, как правило, отсутствуют. Но диагноз ВИЧ-инфекция можно установить, обнаружив сам вирус в крови, его генный материал и антигены. Через 2 недели от начала острых проявлений в крови начинают появляться антитела.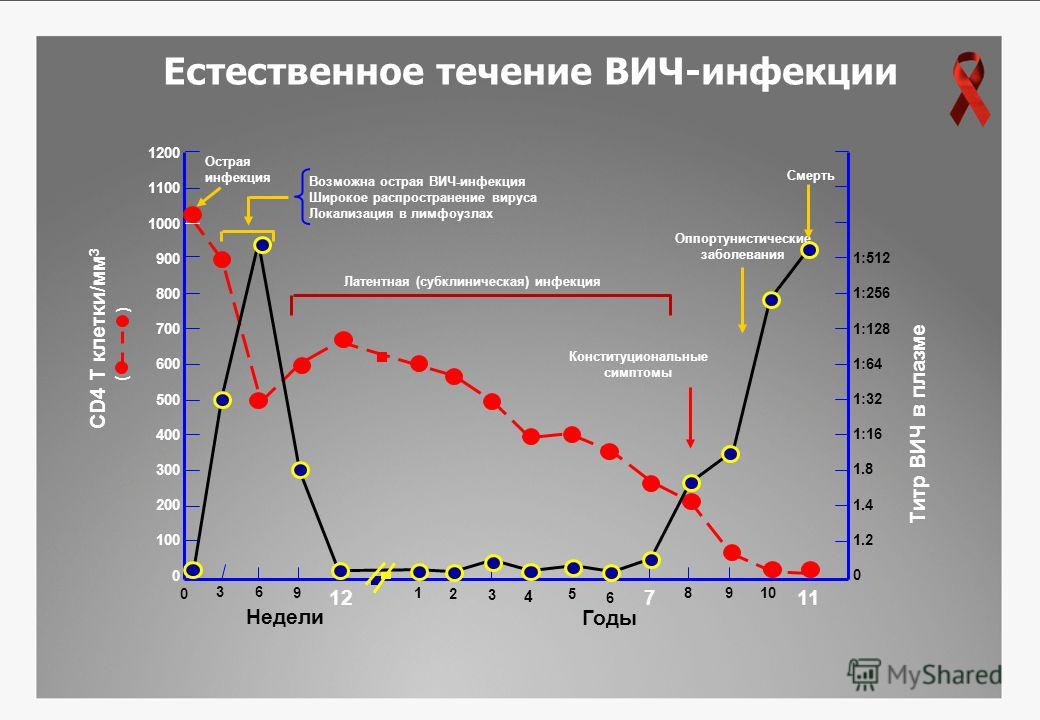 Оппортунистические заболевания и оппортунистические инфекции (Opportunity - удачная возможность) – это заболевания, которые вызываются возбудителями, окружающими нас ежедневно и обитающими в нашем организме, но их развитие подавляется адекватным иммунным ответом. А при снижении иммунитета эти условно-патогенные микроорганизмы вызывают развитие инфекций и заболеваний. Наступает период вторичных заболеваний при ВИЧ-инфекции. При снижении уровня СД-4 клеток до 200 возникает угроза для жизни.
Оппортунистические заболевания и оппортунистические инфекции (Opportunity - удачная возможность) – это заболевания, которые вызываются возбудителями, окружающими нас ежедневно и обитающими в нашем организме, но их развитие подавляется адекватным иммунным ответом. А при снижении иммунитета эти условно-патогенные микроорганизмы вызывают развитие инфекций и заболеваний. Наступает период вторичных заболеваний при ВИЧ-инфекции. При снижении уровня СД-4 клеток до 200 возникает угроза для жизни.
Иммунная система нашего организма представлена органами и клетками, расположенными по всему телу. Лимфоциты, являясь частью иммунной системы и обладая специфичностью, способны создавать и хранить иммунную память о возбудителе инфекционной болезни. Лимфоциты-Т4 (или CD4 Т-клетки) распознают чужеродные вещества или микроорганизмы, проникающие в наш организм, при этом запоминая их.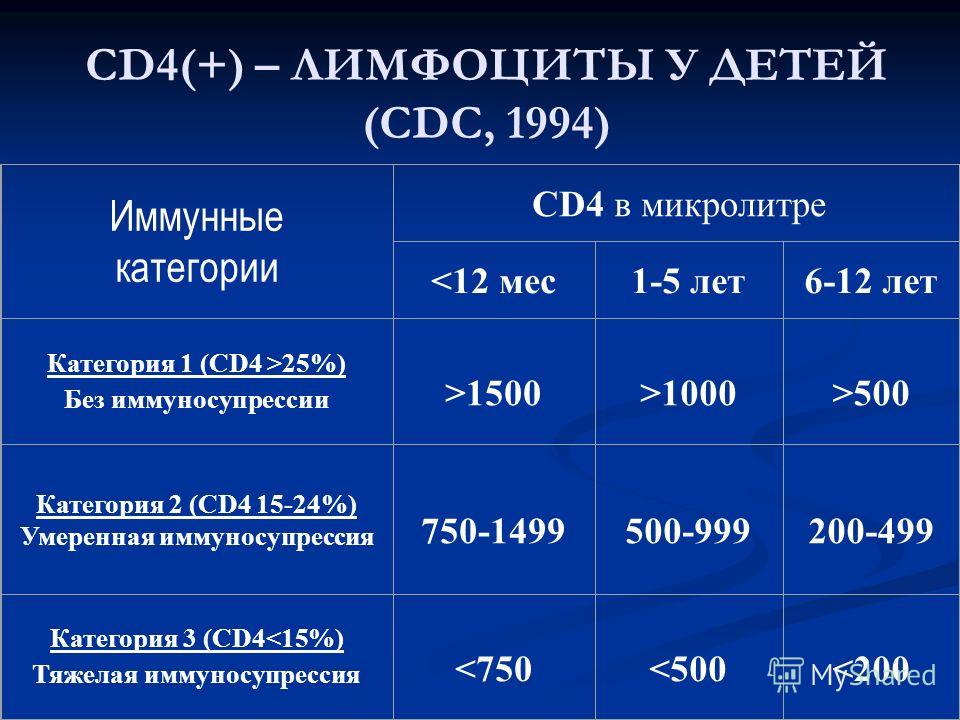 При повторном попадании в наш организм этих чужеродных субстанций, белые клетки крови способны их распознавать, блокируя их разрушительное воздействие и уничтожать.
При повторном попадании в наш организм этих чужеродных субстанций, белые клетки крови способны их распознавать, блокируя их разрушительное воздействие и уничтожать.
Поражение иммунной системы ВИЧ начинает именно с разрушения лимфоцитов-Т4. Также иммунная система содержит клетки, называемые Т8 (СВ8 Т-клетки). Эти лимфоциты «выключают» иммунную систему человека после того, как она завершила работу по борьбе с инфекцией. Обычно у здорового человека клеток СD4 в два раза больше, чем клеток CD8. И соотношение этих клеток (CD4/CD8) в норме превышает 1. У больного СПИДом часто соотношение этих клеток бывает противоположным. Это значит, что в организме содержится слишком мало клеток CD4 для того, чтобы победить инфекцию, и слишком много клеток, которые заставляют борющуюся с инфекцией иммунную систему прекратить свою работу (CD4/CD8 менее 1). Это одна из главных причин, почему у больных СПИДом развивается так много других инфекций и болезней.
В течение первых нескольких недель после проникновения в организм, ВИЧ стремительно размножается. В ответ на внедрение вируса в организм, у человека начинают вырабатываться антитела к ВИЧ. Ранние антитела появляются к концу первого месяца, поздние к концу 3-го, реже к 6-му месяцу. Этот период называется «периодом окна», а точнее "периодом серонегативного окна", потому что в этот период (в среднем до 3-х месяцев) тест на ВИЧ будет отрицательный.
В ответ на внедрение вируса в организм, у человека начинают вырабатываться антитела к ВИЧ. Ранние антитела появляются к концу первого месяца, поздние к концу 3-го, реже к 6-му месяцу. Этот период называется «периодом окна», а точнее "периодом серонегативного окна", потому что в этот период (в среднем до 3-х месяцев) тест на ВИЧ будет отрицательный.
Тест на ВИЧ проводится методом ИФА и ориентирован на выявление антител и антигена. Отрицательный или негативный результат говорит о том, что антител не обнаружено. При этом ВИЧ очень быстро размножается в организме человека. И риск передать ВИЧ при сексуальном контакте или через кровь очень высокий.
У многих людей в первый год после заражения развивается острое заболевание с повышением температуры, увеличением лимфатических узлов. Иногда острая ВИЧ-инфекция может протекать как бронхит или пневмония, краснуха или в виде высыпаний на коже. Такое состояние у ВИЧ-инфицированного может продолжаться около двух недель, а затем состояние на фоне лечения основных симптомов нормализуется. Но на основании этих признаков нельзя сказать, что человек ВИЧ-инфицированный, т.к. перечисленные симптомы являются общими для многих заболеваний, например - обычной простуды.
Но на основании этих признаков нельзя сказать, что человек ВИЧ-инфицированный, т.к. перечисленные симптомы являются общими для многих заболеваний, например - обычной простуды.
В следующие месяцы или даже годы у большинства ВИЧ-инфицированных не проявляется никаких симптомов; этот «спокойный» период инфекции называется латентным или бессимптомным. Позже число CD4-клеток уменьшается, и инфицированные люди становятся восприимчивыми к целому ряду различных инфекций из-за поражения их иммунной системы. Бессимптомный период продолжается достаточно долго и протекает по-разному, а длительность его у разных людей колеблется от 4 месяцев до 12 лет и более. Длительность его зависит от индивидуальных особенностей человека, от образа жизни, который он ведет и от многих других факторов. Обычно продолжительность бессимптомного периода составляет около 5-7 лет.
Если в этот период не было начато лечение ВИЧ-инфекции, то у человека с ВИЧ наступает период, когда подавленный вирусом иммунитет больше не может выполнять свою защитную функцию.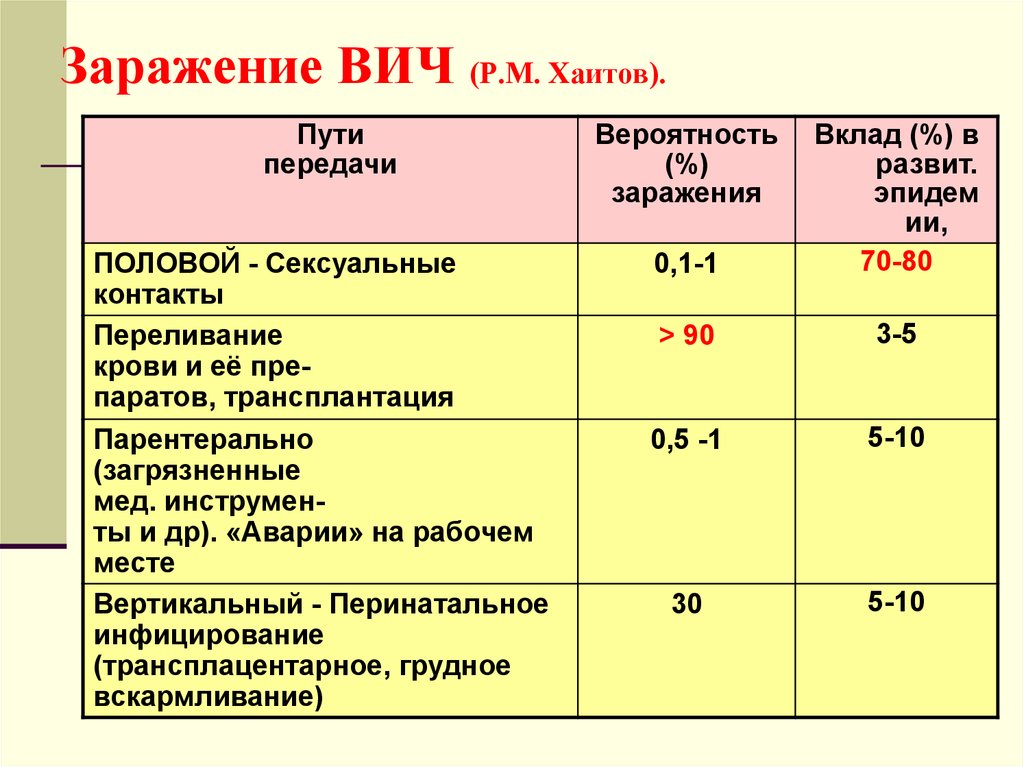 Тогда у ВИЧ-позитивного человека могут развивать заболевания, которые называют вторичными (первичным является ВИЧ-инфекция). Эти заболевания протекают вначале как бактериальные, грибковые и вирусные поражения слизистых оболочек и кожных покровов, позже развивается поражение внутренних органов. Одним из серьезных заболеваний для людей, живущих с ВИЧ является туберкулез. Если лечение так и не начинается, количество CD4 клеток становится менее 200, такое состояние угрожает жизни человека. Могут развиваться поражения нервной системы, онкологические заболевания, в т.ч. саркома Капоши - злокачественная опухоль кожи и сосудов.
Тогда у ВИЧ-позитивного человека могут развивать заболевания, которые называют вторичными (первичным является ВИЧ-инфекция). Эти заболевания протекают вначале как бактериальные, грибковые и вирусные поражения слизистых оболочек и кожных покровов, позже развивается поражение внутренних органов. Одним из серьезных заболеваний для людей, живущих с ВИЧ является туберкулез. Если лечение так и не начинается, количество CD4 клеток становится менее 200, такое состояние угрожает жизни человека. Могут развиваться поражения нервной системы, онкологические заболевания, в т.ч. саркома Капоши - злокачественная опухоль кожи и сосудов.
Заключительная стадия развития ВИЧ-инфекции - это СПИД или терминальная стадия. Эта стадия была введена в клиническую классификацию ВИЧ-инфекции в 1989г., когда высокоактивной АРТ ещё не существовало и, несмотря на адекватную (по тем временам) терапию, имеющиеся у болеющих вторичные заболевания приобретали необратимый характер, и пациент погибал в течение нескольких месяцев после их развития. В настоящее время даже у пациентов с уровнем CD4, близким к нулю, и тяжёлыми вторичными заболеваниями, лечение ВИЧ-инфекции не является бесперспективным.
В настоящее время даже у пациентов с уровнем CD4, близким к нулю, и тяжёлыми вторичными заболеваниями, лечение ВИЧ-инфекции не является бесперспективным.
Российская клиническая классификация ВИЧ-инфекции
1. Стадия инкубации.
2. Стадия первичных проявлений.
Варианты течения:
А. Бессимптомное;
Б. Острая ВИЧ-инфекция без вторичных заболеваний;
В. Острая ВИЧ-инфекция с вторичными заболеваниями.
3. Субклиническая стадия.
4. Стадия вторичных заболеваний.
4А. Потеря массы тела менее 10%, грибковые, вирусные, бактериальные поражения кожи и слизистых, повторные фарингиты, синуситы, опоясывающий лишай.
Фазы:
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
4Б. Потеря массы тела более 10%, необъяснимая диарея или лихорадка более мес, повторные стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних
органов, локализованная саркома Капоши, повторный или диссеминированный опоясывающий лишай.
Фазы:
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
4В. Кахексия. Генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания, в том числе: кандидоз пищевода, бронхов, трахеи, лёгких; пневмоцистная пневмония; злокачественные опухоли; поражения центральной нервной системы.
Фазы:
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
5. Терминальная стадия.
1. ЮНЭЙДС. Доклад о глобальной эпидемии СПИДа. (2016). Доступно на: http://www.unaids.org
ЮНЭЙДС. Доклад о глобальной эпидемии СПИДа. (2016). Доступно на: http://www.unaids.org
2. Marlink R, Kanki P, Thior I, Travers K, Eisen G, Siby T, et al. Снижение скорости развития заболевания после инфицирования ВИЧ-2 по сравнению с ВИЧ-1. Наука (1994) 265 (5178): 1587–90. 10.1126/science.7915856 [PubMed] [CrossRef] [Google Scholar]
3. Марлинк Р. Уроки второго вируса СПИДа, ВИЧ-2. СПИД (1996) 10(7):689–99. 10.1097/00002030-199606001-00002 [PubMed] [CrossRef] [Google Scholar]
4. Jaffar S, Wilkins A, Ngom PT, Sabally S, Corrah T, Bangali JE, et al. Скорость снижения процента CD4+ клеток выше при ВИЧ-1, чем при ВИЧ-2. J Acquir Immune Defic Syndr Hum Retrovirol (1997) 16(5):327–32. 10.1097/00042560-199712150-00003 [PubMed] [CrossRef] [Google Scholar]
5. Popper SJ, Sarr AD, Travers KU, Gueye-Ndiaye A, Mboup S, Essex ME, et al. Более низкая вирусная нагрузка вируса иммунодефицита человека (ВИЧ) 2 типа отражает разницу в патогенности ВИЧ-1 и ВИЧ-2. J заразить Dis (1999) 180(4):1116–21. 10.1086/315010 [PubMed] [CrossRef] [Google Scholar]
10.1086/315010 [PubMed] [CrossRef] [Google Scholar]
6. Popper SJ, Sarr AD, Gueye-Ndiaye A, Mboup S, Essex ME, Kanki PJ. Низкая вирусная нагрузка вируса иммунодефицита человека типа 2 в плазме не зависит от провирусной нагрузки: низкая продукция вируса in vivo. Дж. Вирол (2000) 74(3):1554–7. 10.1128/JVI.74.3.1554-1557.2000 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Wei X, Ghosh SK, Taylor ME, Johnson VA, Emini EA, Deutsch P, et al. Вирусная динамика при инфекции вирусом иммунодефицита человека 1 типа. Природа (1995) 373(6510):117–22. 10.1038/373117a0 [PubMed] [CrossRef] [Google Scholar]
8. Small CB, Klein RS, Friedland GH, Moll B, Emeson EE, Spigland I. Внебольничные оппортунистические инфекции и дефекты клеточного иммунитета у гетеросексуальных наркоманов и гомосексуалистов люди. Am J Med (1983) 74(3):433–41. 10.1016/0002-9343(83)90970-1 [PubMed] [CrossRef] [Google Scholar]
9. Chun TW, Stuyver L, Mizell SB, Ehler LA, Mican JA, Baseler M, et al.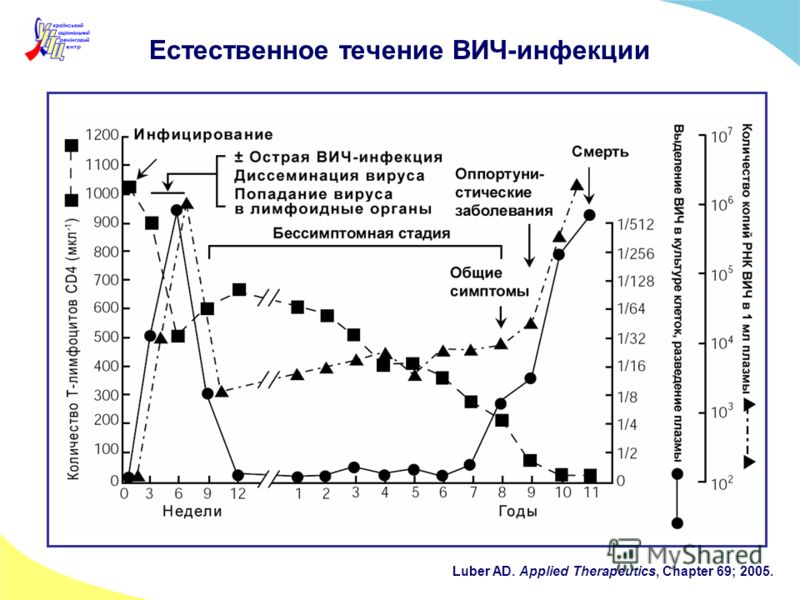 Наличие индуцибельного латентного резервуара ВИЧ-1 во время высокоактивной антиретровирусной терапии. Proc Natl Acad Sci U S A (1997) 94(24):13193–7. 10.1073/pnas.94.24.13193 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Наличие индуцибельного латентного резервуара ВИЧ-1 во время высокоактивной антиретровирусной терапии. Proc Natl Acad Sci U S A (1997) 94(24):13193–7. 10.1073/pnas.94.24.13193 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Nishimura Y, Brown CR, Mattapallil JJ, Igarashi T, Buckler-White A, Lafont BA, et al. Покоящиеся наивные CD4+ Т-клетки массово инфицируются и элиминируются X4-тропными обезьяно-человеческими вирусами иммунодефицита у макак. Proc Natl Acad Sci U S A (2005) 102(22):8000–5. 10.1073/pnas.0503233102 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Reimann KA, Li JT, Veazey R, Halloran M, Park IW, Karlsson GB, et al. Химерный вирус иммунодефицита обезьян/человека, экспрессирующий изолят env вируса иммунодефицита человека типа 1 первичного пациента, вызывает СПИД-подобное заболевание после пассажа in vivo у макак-резусов. Джей Вирол (1996) 70(10):6922–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Nowak MA, Lloyd AL, Vasquez GM, Wiltrout TA, Wahl LM, Bischofberger N, et al. Вирусная динамика первичной виремии и антиретровирусная терапия при инфицировании вирусом иммунодефицита обезьян. Дж. Вирол (1997) 71(10):7518–25. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Вирусная динамика первичной виремии и антиретровирусная терапия при инфицировании вирусом иммунодефицита обезьян. Дж. Вирол (1997) 71(10):7518–25. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Brenchley JM, Schacker TW, Ruff LE, Price DA, Taylor JH, Beilman GJ, et al. Истощение CD4+ Т-клеток на всех стадиях ВИЧ-инфекции происходит преимущественно в желудочно-кишечном тракте. J Exp Med (2004) 200 (6): 749–59. 10.1084/jem.20040874 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Haase AT. Популяционная биология ВИЧ-1-инфекции: вирусная и CD4+ Т-клеточная демография и динамика в лимфатических тканях. Annu Rev Immunol (1999) 17:625–56. 10.1146/annurev.immunol.17.1.625 [PubMed] [CrossRef] [Google Scholar]
15. Rosok BI, Bostad L, Voltersvik P, Bjerknes R, Olofsson J, Asjo B, et al. Снижение количества клеток CD4 в крови не отражает истощение клеток CD4 в ткани миндалин при бессимптомной инфекции ВИЧ-1. СПИД (1996) 10(10):F35–8. [PubMed] [Google Scholar]
16./51/51.jpg) Окойе А.А., Пикер Л.Дж. Истощение CD4(+) Т-клеток при ВИЧ-инфекции: механизмы иммунологической недостаточности. Immunol Rev (2013) 254(1):54–64. 10.1111/imr.12066 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Окойе А.А., Пикер Л.Дж. Истощение CD4(+) Т-клеток при ВИЧ-инфекции: механизмы иммунологической недостаточности. Immunol Rev (2013) 254(1):54–64. 10.1111/imr.12066 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Martin D, Sim J. Лабораторная диагностика ВИЧ-инфекции. S Afr Med J (2000) 90 (2): 105–9. [PubMed] [Google Scholar]
18. McCune JM. Динамика истощения CD4+ Т-клеток при ВИЧ-инфекции. Природа (2001) 410 (6831): 974–9. 10.1038/35073648 [PubMed] [CrossRef] [Google Scholar]
19. De Boer RJ. Временные шкалы истощения CD4+ Т-клеток при ВИЧ-инфекции. PLoS Med (2007) 4(5):e193. 10.1371/journal.pmed.0040193 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Ho DD, Neumann AU, Perelson AS, Chen W, Leonard JM, Markowitz M. Быстрый оборот вирионов плазмы и CD4-лимфоциты при ВИЧ-1-инфекции. Природа (1995) 373 (6510): 123–6. 10.1038/373123a0 [PubMed] [CrossRef] [Google Scholar]
21. Hazenberg MD, Hamann D, Schuitemaker H, Miedema F.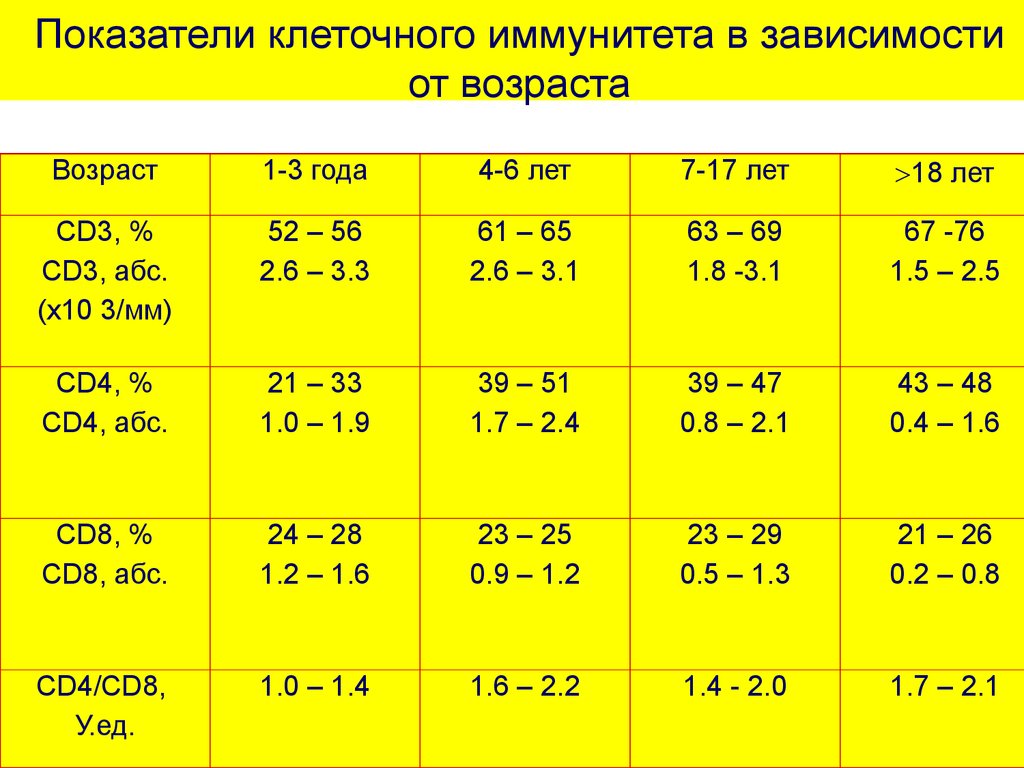 Истощение Т-клеток при ВИЧ-1-инфекции: как CD4+ Т-клетки исчезают. Nat Immunol (2000) 1(4):285–9. 10.1038/79724 [PubMed] [CrossRef] [Google Scholar]
Истощение Т-клеток при ВИЧ-1-инфекции: как CD4+ Т-клетки исчезают. Nat Immunol (2000) 1(4):285–9. 10.1038/79724 [PubMed] [CrossRef] [Google Scholar]
22. Cooper A, García M, Petrovas C, Yamamoto T, Koup RA, Nabel GJ. ВИЧ-1 вызывает гибель клеток CD4 через ДНК-зависимую протеинкиназу во время интеграции вируса. Природа (2013) 498: 376–9. 10.1038/nature12274 [PubMed] [CrossRef] [Google Scholar]
23. Отран Б., Катлама К. В контексте ВААРТ возможно достаточное восстановление иммунитета: за и против. Программа и тезисы XIII международных конференций по СПИДу; 2000 9 июля–14; Дурбан, Южная Африка: (2000). [Google Scholar]
24. Fleury S, Rizzardi GP, Chapuis A, Tambussi G, Knabenhans C, Simeoni E, et al. Долгосрочная кинетика продукции Т-клеток у ВИЧ-инфицированных, получавших высокоактивную антиретровирусную терапию. Proc Natl Acad Sci U S A (2000) 97(10):5393–8. 10.1073/pnas.97.10.5393 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Hellerstein M, Hanley MB, Cesar D, Siler S, Papageorgopoulos C, Wieder E, et al. Непосредственное измерение кинетики циркулирующих Т-лимфоцитов у нормальных и инфицированных ВИЧ-1 людей. Нат Мед (1999) 5(1):83–9. 10.1038/4772 [PubMed] [CrossRef] [Google Scholar]
Непосредственное измерение кинетики циркулирующих Т-лимфоцитов у нормальных и инфицированных ВИЧ-1 людей. Нат Мед (1999) 5(1):83–9. 10.1038/4772 [PubMed] [CrossRef] [Google Scholar]
26. Горохов Г., Нойманн А.Ю., Керевер А., Паризо С., Ли Т., Катлама С. и соавт. Нарушение репертуара CD4+ и CD8+ Т-клеток при прогрессировании СПИДа и регуляция репертуара CD4+ во время противовирусной терапии. Nat Med (1998) 4(2):215–21. 10.1038/nm0298-215 [PubMed] [CrossRef] [Google Scholar]
27. Fevrier M, Dorgham K, Rebollo A. Истощение CD4+ Т-клеток при инфицировании вирусом иммунодефицита человека (ВИЧ): роль апоптоза. Вирусы (2011) 3(5):586–612. 10.3390/v3050586 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Deeks SG, Kitchen CM, Liu L, Guo H, Gascon R, Narvaez AB, et al. Установленная точка активации иммунитета на ранней стадии ВИЧ-инфекции позволяет предсказать последующие изменения CD4+ Т-клеток независимо от вирусной нагрузки. Кровь (2004) 104 (4): 942–7. 10.1182/blood-2003-09-3333 [PubMed] [CrossRef] [Google Scholar]
10.1182/blood-2003-09-3333 [PubMed] [CrossRef] [Google Scholar]
29. Rodriguez B, Sethi AK, Cheruvu VK, Mackay W, Bosch RJ, Kitahata M, et al. Прогностическое значение уровня РНК ВИЧ в плазме по скорости снижения CD4 Т-клеток при нелеченой ВИЧ-инфекции. ДЖАМА (2006) 296 (12): 1498–506. 10.1001/jama.296.12.1498 [PubMed] [CrossRef] [Google Scholar]
30. Йейтс А., Старк Дж., Кляйн Н., Антиа Р., Каллард Р. Понимание медленного истощения CD4+ Т-клеток памяти при ВИЧ-инфекции. PLoS Med (2007) 4(5):e177. 10.1371/journal.pmed.0040177 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. De Boer RJ. Оценка роли продукции тимуса при ВИЧ-инфекции. Curr Opin HIV AIDS (2006) 1(1):16–21. 10.1097/01.COH.0000194105.12816.6a [PubMed] [CrossRef] [Google Scholar]
32. Дикс С.Г., Уокер Б.Д. Иммунный ответ на заражение вирусом СПИДа: хороший, плохой или и то, и другое? J Clin Invest (2004) 113 (6): 808–10. 10.1172/JCI21318 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Hazenberg MD, Otto SA, van Benthem BH, Roos MT, Coutinho RA, Lange JM, et al. Стойкая иммунная активация при ВИЧ-1-инфекции связана с прогрессированием заболевания до СПИДа. СПИД (2003) 17(13):1881–8. 10.1097/01.aids.0000076311.76477.6e [PubMed] [CrossRef] [Google Scholar]
Hazenberg MD, Otto SA, van Benthem BH, Roos MT, Coutinho RA, Lange JM, et al. Стойкая иммунная активация при ВИЧ-1-инфекции связана с прогрессированием заболевания до СПИДа. СПИД (2003) 17(13):1881–8. 10.1097/01.aids.0000076311.76477.6e [PubMed] [CrossRef] [Google Scholar]
34. Giorgi JV, Hultin LE, McKeating JA, Johnson TD, Owens B, Jacobson LP, et al. Более короткая выживаемость при запущенной инфекции вируса иммунодефицита человека типа 1 более тесно связана с активацией Т-лимфоцитов, чем с вирусной нагрузкой в плазме или использованием вирусных хемокиновых корецепторов. J Infect Dis (1999) 179(4):859–70. 10.1086/314660 [PubMed] [CrossRef] [Google Scholar]
35. Содора Д.Л., Сильвестри Г. Иммунная активация и патогенез СПИДа. СПИД (2008) 22(4):439–46. 10.1097/QAD.0b013e3282f2dbe7 [PubMed] [CrossRef] [Google Scholar]
36. Swingler S, Mann A, Jacque J, Brichacek B, Sasseville VG, Williams K, et al. ВИЧ-1 Nef опосредует хемотаксис лимфоцитов и активацию инфицированными макрофагами. Nat Med (1999) 5(9):997–1003. 10.1038/12433 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Nat Med (1999) 5(9):997–1003. 10.1038/12433 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Unutmaz D, Pileri P, Abrignani S. Независимая от антигена активация наивных Т-клеток и покоящихся в памяти Т-клеток комбинацией цитокинов. J Exp Med (1994) 180(3):1159–64. 10.1084/jem.180.3.1159 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. O’Brien M, Manches O, Bhardwaj N. Плазмацитоидные дендритные клетки при ВИЧ-инфекции. Adv Exp Med Biol (2013) 762:71–107. 10.1007/978-1-4614-4433-6_3 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
39. Valdez H, Lederman MM. Цитокины и цитокиновая терапия при ВИЧ-инфекции. AIDS Clin Rev (1997): 187–228. [PubMed] [Google Scholar]
40. Аппай В., Соус Д. Иммунная активация и воспаление при ВИЧ-1-инфекции: причины и последствия. Дж. Патол (2008) 214: 231–41. 10.1002/path.2276 [PubMed] [CrossRef] [Google Scholar]
41. Liu Z, Cumberland WG, Hultin LE, Kaplan AH, Detels R, Giorgi JV. Активация CD8+ Т-лимфоцитов при заболевании ВИЧ-1 отражает аспект патогенеза, отличный от вирусной нагрузки и иммунодефицита. J Acquir Immune Defic Syndr Hum Retrovirol (1998) 18(4):332–40. 10.1097/00042560-199808010-00004 [PubMed] [CrossRef] [Google Scholar]
Активация CD8+ Т-лимфоцитов при заболевании ВИЧ-1 отражает аспект патогенеза, отличный от вирусной нагрузки и иммунодефицита. J Acquir Immune Defic Syndr Hum Retrovirol (1998) 18(4):332–40. 10.1097/00042560-199808010-00004 [PubMed] [CrossRef] [Google Scholar]
42. Younes SA, Yassine-Diab B, Dumont AR, Boulassel MR, Grossman Z, Routy JP, et al. Виремия ВИЧ-1 предотвращает образование интерлейкина-2, продуцирующих ВИЧ-специфические CD4+ Т-клетки памяти, обладающие пролиферативной способностью. J Exp Med (2003) 198 (12): 1909–22. 10.1084/jem.20031598 [PMC free article] [PubMed] [CrossRef] [Google Scholar]
43. Харари А., Валлелиан Ф., Панталео Г. Фенотипическая гетерогенность антиген-специфических CD4 Т-клеток при различных условиях персистенции антигена и антигена нагрузка. Eur J Immunol (2004) 34(12):3525–33. 10.1002/eji.200425324 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
44. Birx DL, Redfield RR, Tencer K, Fowler A, Burke DS, Tosato G. Индукция интерлейкина-6 при иммунодефиците человека вирусная инфекция. Кровь (1990) 76(11):2303–10. [PubMed] [Google Scholar]
Кровь (1990) 76(11):2303–10. [PubMed] [Google Scholar]
45. Molina JM, Scadden DT, Byrn R, Dinarello CA, Groopman JE. Продукция фактора некроза опухоли альфа и интерлейкина 1 бета моноцитарными клетками, инфицированными вирусом иммунодефицита человека. J Clin Invest (1989) 84 (3): 733–7. 10.1172/JCI114230 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Emilie D, Peuchmaur M, Maillot MC, Crevon MC, Brousse N, Delfraissy JF, et al. Продукция интерлейкинов в лимфатических узлах, реплицирующих вирус иммунодефицита человека-1. Джей Клин Инвест (1990) 86(1):148–59. 10.1172/JCI114678 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. van Wijk F, Cheroutre H. Т-клетки слизистой оболочки в гомеостазе кишечника и воспалении. Expert Rev Clin Immunol (2010) 6(4):559–66. 10.1586/eci.10.34 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
48. Маттапаллил Дж. Дж., Доуек Д. С., Хилл Б., Нисимура Ю., Мартин М., Рёдерер М. Массивная инфекция и потеря памяти CD4+ T клеток во многих тканях во время острой SIV-инфекции. Природа (2005) 434 (7037): 1093–7. 10.1038/nature03501 [PubMed] [CrossRef] [Google Scholar]
Природа (2005) 434 (7037): 1093–7. 10.1038/nature03501 [PubMed] [CrossRef] [Google Scholar]
49. Ruemmele FM, Beaulieu JF, Dionne S, Levy E, Seidman EG, Cerf-Bensussan N, et al. Липополисахаридная модуляция нормального оборота энтероцитов с помощью толл-подобных рецепторов опосредуется эндогенно продуцируемым фактором некроза опухоли альфа. Гут (2002) 51 (6): 842–8. 10.1136/gut.51.6.842 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Sandler NG, Douek DC. Микробная транслокация при ВИЧ-инфекции: причины, последствия и возможности лечения. Nat Rev Microbiol (2012) 10 (9)): 655–66. 10.1038/nrmicro2848 [PubMed] [CrossRef] [Google Scholar]
51. Doitsh G, Cavrois M, Lassen KG, Zepeda O, Yang Z, Santiago ML, et al. Абортивная ВИЧ-инфекция опосредует истощение CD4 Т-клеток и воспаление в лимфоидной ткани человека. Сотовый (2010) 143 (5): 789–801. 10.1016/j.cell.2010.11.001 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Doitsh G, Galloway NL, Geng X, Yang Z, Monroe KM, Zepeda O, et al.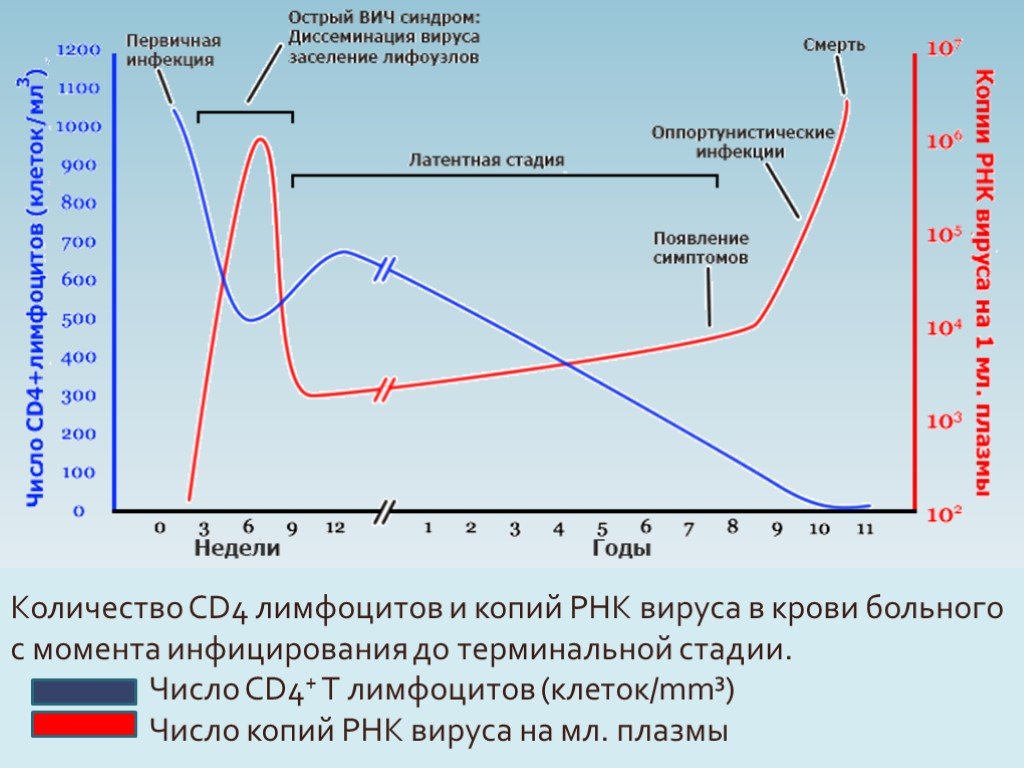 Гибель клеток в результате пироптоза приводит к истощению CD4 Т-клеток при ВИЧ-1-инфекции. Природа (2014) 505 (7484): 509–14. 10.1038/nature12940 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Гибель клеток в результате пироптоза приводит к истощению CD4 Т-клеток при ВИЧ-1-инфекции. Природа (2014) 505 (7484): 509–14. 10.1038/nature12940 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Sakaguchi S. Контроль иммунных ответов естественным образом возникающими регуляторными Т-клетками CD4+, которые экспрессируют толл-подобные рецепторы. J Exp Med (2003) 197(4):397–401. 10.1084/jem.20030012 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
54. Foxall RB, Albuquerque AS, Soares RS, Baptista AP, Cavaleiro R, Tendeiro R, et al. Память и наивно-подобные регуляторные CD4+ Т-клетки увеличиваются во время инфекции ВИЧ-2 в прямой связи с истощением CD4+ Т-клеток независимо от виремии. СПИД (2011) 25(16):1961–70. 10.1097/QAD.0b013e32834b3554 [PubMed] [CrossRef] [Google Scholar]
55. Eggena MP, Barugahare B, Jones N, Okello M, Mutalya S, Kityo C, et al. Истощение регуляторных Т-клеток при ВИЧ-инфекции связано с активацией иммунитета. J Immunol (2005) 174(7):4407–14. 10.4049/jimmunol.174.7.4407 [PubMed] [CrossRef] [Google Scholar]
10.4049/jimmunol.174.7.4407 [PubMed] [CrossRef] [Google Scholar]
56. Cavaleiro R, Brunn GJ, Albuquerque AS, Victorino RM, Platt JL, Sousa AE. Опосредованное моноцитами подавление Т-клеток белками оболочки ВИЧ-2. Eur J Immunol (2007) 37(12):3435–44. 10.1002/eji.200737511 [PubMed] [CrossRef] [Google Scholar]
57. Clavel F, Mansinho K, Chamaret S, Guetard D, Favier V, Nina J, et al. Инфекция вируса иммунодефицита человека типа 2, связанная со СПИДом в Западной Африке. N Engl J Med (1987) 316 (19): 1180–5. 10.1056/NEJM198705073161903 [PubMed] [CrossRef] [Google Scholar]
58. Bock PJ, Markovitz DM. Заражение ВИЧ-2. СПИД (2001) 15 (Приложение 5): S35–45. 10.1097/00002030-200100005-00006 [PubMed] [CrossRef] [Google Scholar]
59. Sousa AE, Carneiro J, Meier-Schellersheim M, Grossman Z, Victorino RM. Истощение CD4 Т-клеток напрямую связано с иммунной активацией в патогенезе ВИЧ-1 и ВИЧ-2, но только косвенно с вирусной нагрузкой. Дж Иммунол (2002) 169(6): 3400–6. 10.4049/jimmunol.169.6.3400 [PubMed] [CrossRef] [Google Scholar]
10.4049/jimmunol.169.6.3400 [PubMed] [CrossRef] [Google Scholar]
60. Miedema F, Hazenberg MD, Tesselaar K, van Baarle D, de Boer RJ, Borghans JA. Иммунная активация и сопутствующие повреждения в патогенезе СПИДа. Фронт Иммунол (2013) 4:298. 10.3389/fimmu.2013.00298 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
61. Funderburg N, Luciano AA, Jiang W, Rodriguez B, Sieg SF, Lederman MM. Лиганды Toll-подобных рецепторов индуцируют активацию и гибель Т-клеток человека, что является моделью патогенеза ВИЧ. PLoS One (2008) 3 (4): e1915. 10.1371/journal.pone.0001915 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
62. Mogensen TH, Melchjorsen J, Larsen CS, Paludan SR. Распознавание и активация врожденного иммунитета при ВИЧ-инфекции. Ретровирусология (2010) 7:54. 10.1186/1742-4690-7-54 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. Nowroozalizadeh S, Mansson F, da Silva Z, Repits J, Dabo B, Pereira C, et al. Микробная транслокация коррелирует с тяжестью ВИЧ-1 и ВИЧ-2 инфекций. J Infect Dis (2010) 201(8):1150–4. 10.1086/651430 [PubMed] [CrossRef] [Google Scholar]
J Infect Dis (2010) 201(8):1150–4. 10.1086/651430 [PubMed] [CrossRef] [Google Scholar]
64. Джонсон В.Е., Desrosiers RC. Вирусная персистенция: стратегии уклонения ВИЧ от иммунной системы. Annu Rev Med (2002) 53: 499–518. 10.1146/annurev.med.53.082901.104053 [PubMed] [CrossRef] [Google Scholar]
65. Michael NL, Morrow P, Mosca J, Vahey M, Burke DS, Redfield RR. Индукция экспрессии вируса иммунодефицита человека типа 1 в хронически инфицированных клетках связана в первую очередь со сдвигом в паттернах сплайсинга РНК. Дж. Вирол (1991) 65(3):1291–303. [Бесплатная статья PMC] [PubMed] [Google Scholar]
66. Soares RS, Tendeiro R, Foxall RB, Baptista AP, Cavaleiro R, Gomes P, et al. Ассоциированная с клетками вирусная нагрузка свидетельствует о продолжающейся репликации вируса у пациентов с авиремией, инфицированных ВИЧ-2. Дж. Вирол (2011) 85 (5): 2429–38. 10.1128/JVI.01921-10 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
67. Hanson A, Sarr AD, Shea A, Jones N, Mboup S, Kanki P, et al. Отдельный профиль активации Т-клеток при ВИЧ 2 типа по сравнению с ВИЧ 1 типа: дифференциальный механизм иммунозащиты. AIDS Res Hum Retroviruses (2005) 21 (9)): 791–8. 10.1089/aid.2005.21.791 [PubMed] [CrossRef] [Google Scholar]
Отдельный профиль активации Т-клеток при ВИЧ 2 типа по сравнению с ВИЧ 1 типа: дифференциальный механизм иммунозащиты. AIDS Res Hum Retroviruses (2005) 21 (9)): 791–8. 10.1089/aid.2005.21.791 [PubMed] [CrossRef] [Google Scholar]
68. Алатракчи Н., Дамонд Ф., Матерон С., Беретта-Темпельхофф С., Кампа П., Карселейн Г. и др. Пролиферативный ответ Т-клеток, продуцирующих IFNgamma и IL-2, на ВИЧ-2 при нелеченной инфекции ВИЧ-2. СПИД (2006) 20(1):29–34. 10.1097/01.aids.0000198077.30421.bf [PubMed] [CrossRef] [Google Scholar]
69. Hamann D, Baars PA, Rep MH, Hooibrink B, Kerkhof-Garde SR, Klein MR, et al. Фенотипическое и функциональное разделение памяти и эффекторных CD8+ Т-клеток человека. Джей Опыт Мед (1997) 186(9):1407–18. 10.1084/jem.186.9.1407 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
70. Adachi Y, Oyaizu N, Than S, McCloskey TW, Pahwa S. IL-2 спасает in vitro апоптоз лимфоцитов в пациенты с ВИЧ-инфекцией: корреляция с его способностью блокировать индуцированную культурой понижающую модуляцию Bcl-2. J Immunol (1996) 157(9):4184–93. [PubMed] [Google Scholar]
J Immunol (1996) 157(9):4184–93. [PubMed] [Google Scholar]
71. Sousa AE, Chaves AF, Loureiro A, Victorino RM. Сравнение частоты Т-клеток, продуцирующих интерлейкин (ИЛ)-2, интерферон-гамма и ИЛ-4, при 2 заболеваниях, вирусе иммунодефицита человека типов 1 и 2, с различными клиническими исходами. J Infect Dis (2001) 184 (5): 552–9. 10.1086/322804 [PubMed] [CrossRef] [Google Scholar]
72. Jaleco AC, Covas MJ, Victorino RM. Анализ гибели клеток лимфоцитов и апоптоза у ВИЧ-2-инфицированных пациентов. Clin Exp Immunol (1994) 98(2):185–9. 10.1111/j.1365-2249.1994.tb06123.x [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Michel P, Balde AT, Roussilhon C, Aribot G, Sarthou JL, Gougeon ML. Снижение иммунной активации и апоптоза Т-клеток при вирусе иммунодефицита человека типа 2 по сравнению с типом 1: корреляция апоптоза Т-клеток с концентрацией бета2-микроглобулина и развитием заболевания. J Infect Dis (2000) 181 (1): 64–75. 10.1086/315170 [PubMed] [CrossRef] [Google Scholar]
74. Дюваль М.Г., Джей А., Донг Т., Бренчли Дж.М., Алаби А.С., Джеффрис Д.Дж. и др. Поддержание ВИЧ-специфических CD4+ Т-клеток помогает отличить ВИЧ-2 от ВИЧ-1. J Immunol (2006) 176(11):6973–81. 10.4049/jimmunol.176.11.6973 [PubMed] [CrossRef] [Google Scholar]
Дюваль М.Г., Джей А., Донг Т., Бренчли Дж.М., Алаби А.С., Джеффрис Д.Дж. и др. Поддержание ВИЧ-специфических CD4+ Т-клеток помогает отличить ВИЧ-2 от ВИЧ-1. J Immunol (2006) 176(11):6973–81. 10.4049/jimmunol.176.11.6973 [PubMed] [CrossRef] [Google Scholar]
75. Kovacs JA, Lempicki RA, Sidorov IA, Adelsberger JW, Sereti I, Sachau W, et al. Индукция пролонгированного выживания CD4+ Т-лимфоцитов при прерывистой терапии IL-2 у ВИЧ-инфицированных пациентов. Дж. Клин Инвест (2005) 115 (8): 2139–48. 10.1172/JCI23196 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
76. Goldstone DC, Ennis-Adeniran V, Hedden JJ, Groom HC, Rice GI, Christodoulou E, et al. Фактор рестрикции ВИЧ-1 SAMHD1 представляет собой дезоксинуклеозидтрифосфаттрифосфогидролазу. Природа (2011) 480 (7377): 379–82. 10.1038/nature10623 [PubMed] [CrossRef] [Google Scholar]
77. Lahaye X, Satoh T, Gentili M, Cerboni S, Conrad C, Hurbain I, et al. Капсиды ВИЧ-1 и ВИЧ-2 определяют иммунное обнаружение вирусной кДНК с помощью врожденного сенсора cGAS в дендритных клетках. Иммунитет (2013) 39(6): 1132–42. 10.1016/j.immuni.2013.11.002 [PubMed] [CrossRef] [Google Scholar]
Иммунитет (2013) 39(6): 1132–42. 10.1016/j.immuni.2013.11.002 [PubMed] [CrossRef] [Google Scholar]
78. Granelli-Piperno A, Golebiowska A, Trumpfheller C, Siegal FP, Steinman RM. ВИЧ-1-инфицированные дендритные клетки, происходящие из моноцитов, не подвергаются созреванию, но могут вызывать продукцию IL-10 и регуляцию Т-клеток. Proc Natl Acad Sci U S A (2004) 101:7669–74. 10.1073/pnas.0402431101 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
79. Manel N, Hogstad B, Wang Y, Levy DE, Unutmaz D, Littman DR. Скрытый сенсор для ВИЧ-1 активирует противовирусный врожденный иммунитет в дендритных клетках. Природа (2010) 467 (7312): 214–7. 10.1038/природа09337 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
80. Mandl JN, Barry AP, Vanderford TH, Kozyr N, Chavan R, Klucking S, et al. Различная передача сигналов TLR7 и TLR9 и продукция интерферона типа I отличают патогенные и непатогенные вирусные инфекции СПИДа. Nat Med (2008) 14 (10): 1077–87.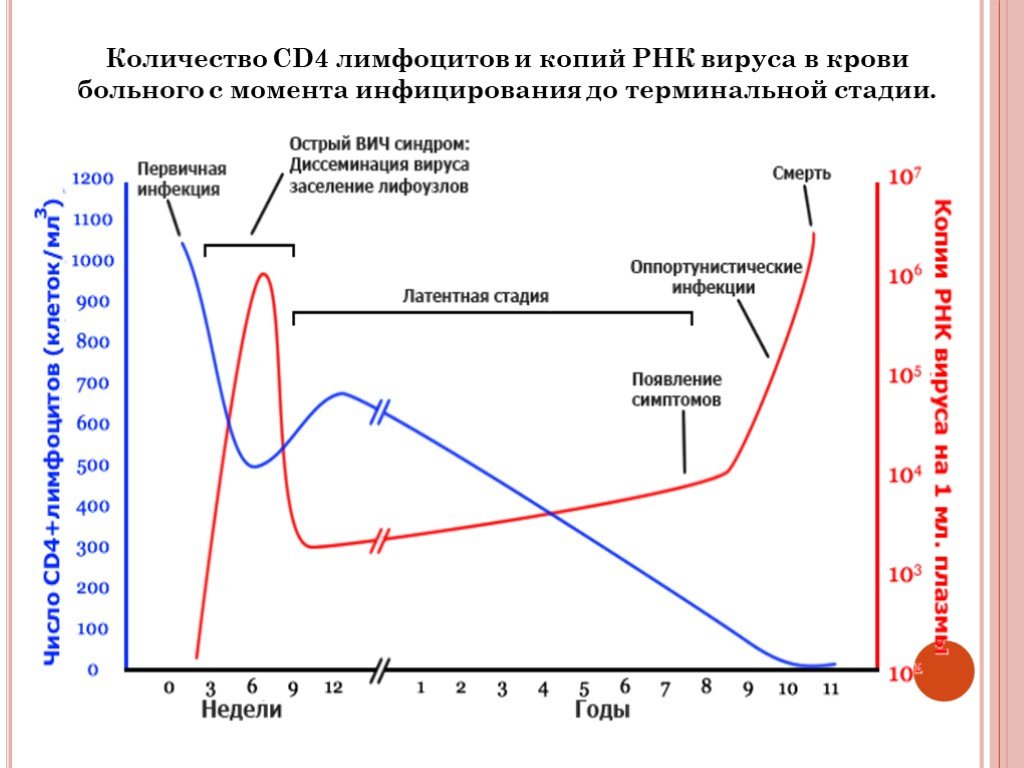 10.1038/nm.1871 [PubMed] [CrossRef] [Google Scholar]
10.1038/nm.1871 [PubMed] [CrossRef] [Google Scholar]
81. Cavaleiro R, Baptista AP, Soares RS, Tendeiro R, Foxall RB, Gomes P, et al. Большое истощение плазмацитоидных дендритных клеток при ВИЧ-2-инфекции, ослабленной форме ВИЧ-инфекции. Плос Патог (2009 г.)) 5(11):e1000667. 10.1371/journal.ppat.1000667 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
82. Chun TW, Davey RT, Jr, Engel D, Lane HC, Fauci AS. Повторное появление ВИЧ после прекращения терапии. Природа (1999) 401 (6756): 874–5. 10.1038/44755 [PubMed] [CrossRef] [Google Scholar]
83. Ramratnam B, Mittler JE, Zhang L, Boden D, Hurley A, Fang F, et al. Распад латентного резервуара способного к репликации ВИЧ-1 обратно пропорционален степени остаточной репликации вируса во время длительной антиретровирусной терапии. Nat Med (2000) 6 (1): 82–5. 10.1038/71577 [PubMed] [CrossRef] [Google Scholar]
84. Nunes-Cabaco H, Matoso P, Foxall RB, Tendeiro R, Pires AR, Carvalho T, et al. Тимусная инфекция ВИЧ-2 раскрывает посттранскрипционный контроль репликации вируса в тимоцитах человека.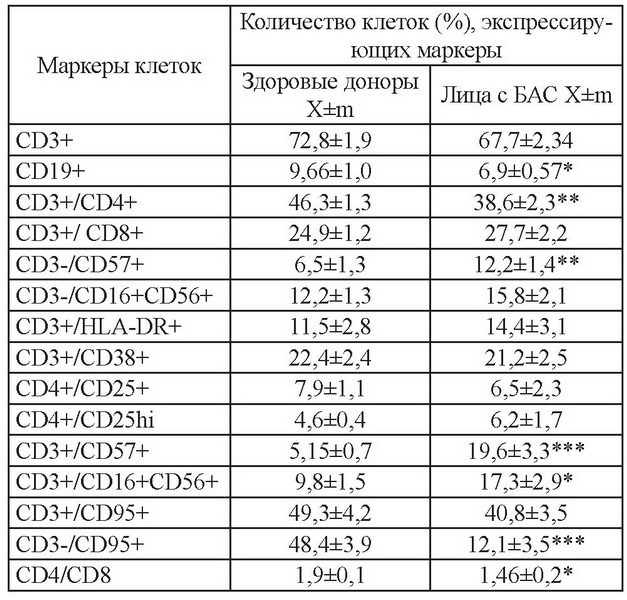 Дж. Вирол (2015) 89 (4): 2201–8. 10.1128/JVI.03047-14 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Дж. Вирол (2015) 89 (4): 2201–8. 10.1128/JVI.03047-14 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
София А. Баттистини Гарсия; Нилмари Гусман.
Информация об авторе
Последнее обновление: 8 августа 2022 г.
В течение десятилетий измерение количества клеток CD4 использовалось для понимания прогрессирования болезни, вызванной вирусом иммунодефицита человека (ВИЧ). ВИЧ представляет собой смертельную инфекцию, характеризующуюся нацеливанием и разрушением CD4 Т-лимфоцитов в периферической крови. CD4 Т-лимфоциты являются частью клеток Т-лимфоцитов человека, которые продуцируются в костном мозге и в конечном итоге созревают в тимусе. Они циркулируют в организме для борьбы с бактериями, вирусами и другими организмами. Если ВИЧ не лечить, вирус проникает в клетку и размножается, что в конечном итоге приводит к гибели клеток CD4. Оставшиеся инфицированные клетки выделяют вирионы, которые заражают другие клетки, что приводит к прогрессированию заболевания. Потеря CD4 Т-лимфоцитов приведет к неспособности иметь надлежащий иммунный ответ.[1][2] 93. Снижение количества CD4 Т-клеток может привести к оппортунистическим инфекциям и увеличить смертность.
Оставшиеся инфицированные клетки выделяют вирионы, которые заражают другие клетки, что приводит к прогрессированию заболевания. Потеря CD4 Т-лимфоцитов приведет к неспособности иметь надлежащий иммунный ответ.[1][2] 93. Снижение количества CD4 Т-клеток может привести к оппортунистическим инфекциям и увеличить смертность.
Образец крови, необходимый для подсчета CD4, берется путем взятия стандартной крови. Образцы крови должны пройти обработку в течение 18 часов. Проточная цитометрия обычно дает результаты.
Для подсчета абсолютного числа Т-лимфоцитов CD4 могут быть полезны несколько методов. Золотым стандартом является иммунофлуоресцентный анализ методом проточной цитометрии. В проточной цитометрии используются зонды с флуорохромными метками, которые связываются с определенными компонентами клеток. Для подсчета клеток CD4 Т-лимфоциты CD4 окрашивают флуоресцентными метками, которые обнаруживаются в проточном цитометре. Моноклональные антитела связываются с рецептором CD4 на поверхности Т-клеток. Относительный процент клеток, экспрессирующих рецептор на своей поверхности, получают из проточного цитометра. Другими словами, результаты представляются в виде процентного содержания CD4, а абсолютное число получается путем умножения процентного содержания и общего количества лейкоцитов. Например, процент CD4 выше 293.[3][4]
Моноклональные антитела связываются с рецептором CD4 на поверхности Т-клеток. Относительный процент клеток, экспрессирующих рецептор на своей поверхности, получают из проточного цитометра. Другими словами, результаты представляются в виде процентного содержания CD4, а абсолютное число получается путем умножения процентного содержания и общего количества лейкоцитов. Например, процент CD4 выше 293.[3][4]
Существуют альтернативные системы производства различных компаний, которые являются опциями. Важно знать, какой метод используется, потому что абсолютные числа подсчета могут отличаться. При использовании разных методов анализ результатов требует осторожности.
Врачи и пациенты должны знать, что определенные факторы могут вызывать изменение числа клеток CD4. Любые изменения общего количества лейкоцитов (лейкоцитов) могут привести к изменению абсолютного значения. Многие факторы, в том числе циркадные колебания, влияют на абсолютное количество лимфоцитов. Исследования показали, что количество CD4 обычно ниже утром и увеличивается в течение дня. Острая инфекция, например грипп, пневмония, гепатит В, цитомегаловирус и химиотерапия, могут привести к снижению количества клеток CD4. Стресс и усталость также могут повлиять на результаты. Интересно, что кортикостероиды могут как повышать, так и снижать уровни клеток CD4. Разовые дозы стероидов могут привести к снижению абсолютного значения. С другой стороны, хроническое употребление стероидов может привести к повышенному показателю. Другими факторами, которые следует учитывать, являются алкоголь, никотин и беременность, поскольку они также могут изменить абсолютное количество CD4. 93, что является одним из показаний для диагностики СПИДа. Широкий диапазон нормального значения является произведением трех переменных: количества лейкоцитов, процента лимфоцитов и процента лимфоцитов, несущих рецептор CD4.
Исследования показали, что количество CD4 обычно ниже утром и увеличивается в течение дня. Острая инфекция, например грипп, пневмония, гепатит В, цитомегаловирус и химиотерапия, могут привести к снижению количества клеток CD4. Стресс и усталость также могут повлиять на результаты. Интересно, что кортикостероиды могут как повышать, так и снижать уровни клеток CD4. Разовые дозы стероидов могут привести к снижению абсолютного значения. С другой стороны, хроническое употребление стероидов может привести к повышенному показателю. Другими факторами, которые следует учитывать, являются алкоголь, никотин и беременность, поскольку они также могут изменить абсолютное количество CD4. 93, что является одним из показаний для диагностики СПИДа. Широкий диапазон нормального значения является произведением трех переменных: количества лейкоцитов, процента лимфоцитов и процента лимфоцитов, несущих рецептор CD4.
Как уже упоминалось, количество CD4 используется для оценки прогрессирования ВИЧ. 3, поскольку в этой популяции пациентов чаще возникают осложнения. Уровни следует контролировать каждые 3–6 месяцев после начала АРТ, чтобы проверить реакцию на терапию. Если ответ адекватный, количество CD4 можно перепроверять каждые 6–12 месяцев. Успешное лечение связано с увеличением количества CD4 и соблюдением режима терапии. При использовании АРТ уровни могут увеличиться на 100–150 клеток/мм3 через год.[5][6]
3, поскольку в этой популяции пациентов чаще возникают осложнения. Уровни следует контролировать каждые 3–6 месяцев после начала АРТ, чтобы проверить реакцию на терапию. Если ответ адекватный, количество CD4 можно перепроверять каждые 6–12 месяцев. Успешное лечение связано с увеличением количества CD4 и соблюдением режима терапии. При использовании АРТ уровни могут увеличиться на 100–150 клеток/мм3 через год.[5][6]
Для измерения числа CD4+ требуется образец крови и лабораторный анализ. Необходимы надлежащие меры предосторожности при сборе образца крови и обращении с ним. Во-первых, пробирка должна быть соответствующим образом маркирована с указанием даты и времени сбора и идентификатора пациента. Должны быть указаны возраст и пол, а также имя и инициалы коллекционера. Затем образец крови берется путем венепункции в соответствии со стандартной процедурой. Закон о перевозке опасных грузов и правила перевозки опасных грузов Международной ассоциации воздушного транспорта (ИАТА) регулируют перевозку содержащих инфицированных агентов, включая кровь, зараженную ВИЧ. Пациенту не требуется голодать для проведения теста. Очень важно перед проведением теста обсудить с пациентом возможные опасения относительно результатов, которые могут быть получены в результате теста. Пациент должен быть эмоционально готов к получению информации, которую дают результаты теста.
Пациенту не требуется голодать для проведения теста. Очень важно перед проведением теста обсудить с пациентом возможные опасения относительно результатов, которые могут быть получены в результате теста. Пациент должен быть эмоционально готов к получению информации, которую дают результаты теста.
Количество CD4 — очень полезный лабораторный параметр при оценке пациентов с иммуносупрессией, особенно ВИЧ-инфицированных. Практикующие медсестры, поставщики первичной медико-санитарной помощи и другие врачи должны иметь некоторое представление о нормальных уровнях CD4. Подсчет CD4 следует проводить у всех пациентов, у которых впервые диагностировано заболевание ВИЧ. Служба общественного здравоохранения рекомендует всем ВИЧ-позитивным пациентам проходить тестирование каждые 3–6 месяцев. Результаты могут дать представление о возможном диагнозе СПИДа и риске оппортунистических инфекций. Также тест может быть индикатором неэффективности лечения.
Получите бесплатный доступ к вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Nacher M, Huber F, Adriouch L, Djossou F, Adenis A, Couppié P. Временная тенденция доли пациентов с поздними стадиями ВИЧ во Французской Гвиане: застрял на асимптоте ? Примечания BMC Res. 2018 26 ноября; 11 (1): 831. [Бесплатная статья PMC: PMC6258272] [PubMed: 30477588]
Карр А., Ричардсон Р., Лю З. Успех и неудача начальной антиретровирусной терапии у взрослых: обновленный систематический обзор. СПИД. 2019 01 марта; 33 (3): 443-453. [PubMed: 30475265]
Vogler IH, Alfieri DF, Gianjacomo HDB, Almeida ERD, Reiche EMV. Безопасность мониторинга ответа на антиретровирусную терапию при ВИЧ-1-инфекции с использованием количества CD4+ Т-клеток с длительными интервалами. Кэд Сауд Публика.